弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
(1)已知H2A在水中存在以下平衡:H2A=H++HA-,HA- H++A2-。
H++A2-。
①NaHA溶液的pH__ (填“大于”“小于”或“等于”)Na2A溶液的pH。
②某温度下,若向0.1mol•L-1的NaHA溶液中逐滴滴加0.1mol•L-1KOH溶液至溶液呈中性。此时该混合溶液中,下列关系一定正确的是__ 。
A.c(H+)•c(OH-)=1×10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05mol•L-1
③已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s) Ca2+(aq)+A2-(aq)△H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有
Ca2+(aq)+A2-(aq)△H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有__ 。
A.升高温度 B.降低温度
C.加入NH4Cl晶体 D.加入Na2A固体
(2)0.2mol•L-1HR溶液与0.1mol•L-1NaOH溶液等体积混合,测得混合溶液pH>7,则说明在相同条件下HR的电离程度__ (填“>”“<”或“=”)NaR的水解程度,混合溶液中各离子浓度的大小顺序为__ 。
(3)常温下,若在0.10mol•L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=___ mol•L-1(Ksp[Cu(OH)2]=2.2×10-20)。
(1)已知H2A在水中存在以下平衡:H2A=H++HA-,HA-
 H++A2-。
H++A2-。①NaHA溶液的pH
②某温度下,若向0.1mol•L-1的NaHA溶液中逐滴滴加0.1mol•L-1KOH溶液至溶液呈中性。此时该混合溶液中,下列关系一定正确的是
A.c(H+)•c(OH-)=1×10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05mol•L-1
③已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)
 Ca2+(aq)+A2-(aq)△H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有
Ca2+(aq)+A2-(aq)△H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有A.升高温度 B.降低温度
C.加入NH4Cl晶体 D.加入Na2A固体
(2)0.2mol•L-1HR溶液与0.1mol•L-1NaOH溶液等体积混合,测得混合溶液pH>7,则说明在相同条件下HR的电离程度
(3)常温下,若在0.10mol•L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=
更新时间:2021-01-02 20:30:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】以下是制备FeC2O4·2H2O的流程:
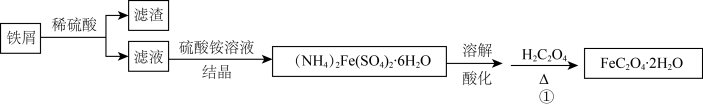
实验I:制备(NH4)2Fe(SO4)2·6H2O
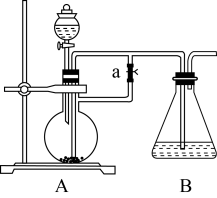
(1)B中盛有一定量的(NH4)2SO4溶液,A中分液漏斗中的药品是_______ 。
(2)实验开始时先将止水夹a_______ (填“打开”或“关闭”)。
(3)简述B中生成(NH4)2Fe(SO4)2的操作过程_______ 。
实验II:制备FeC2O4·2H2O
已知:25℃时,当pH>4,Fe2+易被氧化。
(4)步骤①生成FeC2O4·2H2O的化学方程式为_______ ,该步加入H2C2O4而不是Na2C2O4溶液的原因是_______ 。
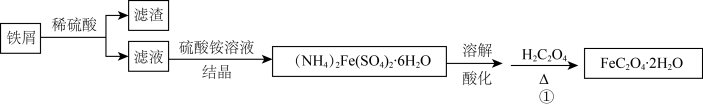
实验I:制备(NH4)2Fe(SO4)2·6H2O

(1)B中盛有一定量的(NH4)2SO4溶液,A中分液漏斗中的药品是
(2)实验开始时先将止水夹a
(3)简述B中生成(NH4)2Fe(SO4)2的操作过程
实验II:制备FeC2O4·2H2O
已知:25℃时,当pH>4,Fe2+易被氧化。
(4)步骤①生成FeC2O4·2H2O的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】完成下列填空
(1)已知常温下A-的水解常数Kh=1.61×10-5,常温下,含等物质的量浓度的HA与NaA的混合溶液显___________ (填“酸”、“碱”、“中”)性,c(A-)___________ (填“>”、“<”或“=”)c(HA),该溶液中各离子浓度由大到小的顺序为___________ 。
(2)25℃时,将xmolCH3COONa溶于水,溶液显碱性,向该溶液滴加yL醋酸溶液后溶液呈中性(体积变化忽略不计),则所滴加醋酸溶液的浓度为___________ mol/L(CH3COOH的电离平衡常数取Ka=2×10-5)
(1)已知常温下A-的水解常数Kh=1.61×10-5,常温下,含等物质的量浓度的HA与NaA的混合溶液显
(2)25℃时,将xmolCH3COONa溶于水,溶液显碱性,向该溶液滴加yL醋酸溶液后溶液呈中性(体积变化忽略不计),则所滴加醋酸溶液的浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】已知常温下部分弱电解质的电离平衡常数如表:
(1)25℃时,用离子方程式说明 溶液呈酸性的原因:
溶液呈酸性的原因:_____ , 的
的 溶液中各离子浓度的大小关系为
溶液中各离子浓度的大小关系为_____ 。
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式_____ 。
(3)室温下,经测定0.1mol⋅L
 溶液
溶液 ,则
,则
_____  (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。
(4)25℃时,若氨水的浓度为2.0mol⋅L ,将
,将 通入该氨水中,当
通入该氨水中,当 降至
降至 mol⋅L
mol⋅L 时,溶液中
时,溶液中
_____ 。
| 化学式 | HF | HClO |  |  |  |
| 电离常数 | 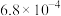 | 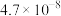 | 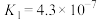 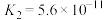 |   | 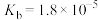 |
 溶液呈酸性的原因:
溶液呈酸性的原因: 的
的 溶液中各离子浓度的大小关系为
溶液中各离子浓度的大小关系为(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式
(3)室温下,经测定0.1mol⋅L

 溶液
溶液 ,则
,则
 (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。(4)25℃时,若氨水的浓度为2.0mol⋅L
 ,将
,将 通入该氨水中,当
通入该氨水中,当 降至
降至 mol⋅L
mol⋅L 时,溶液中
时,溶液中
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】工业上除去SO2尾气有多种方法.
I:烟道气中除去SO2的方法:2CO(g) + SO2(g) ⇌ 2CO2(g)+ S(l)+Q (Q>0)
(1)该反应的平衡常数表达式为________ 。若保持其他条件不变,缩小反应容器的体积,平衡常数将会________ (选填“变大”、 “变小”或“不变”) 。
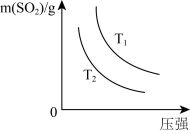
(2)下图是平衡时SO2的质量在不同温度下随压强的变化曲线,判断: T1________ T2 (选填“>”、“<”或“=”)。
(3)若在2L的密闭容器中进行上述反应,经测定在5 min内气体的质量减小了1.6g。则0~5 min的平均反应速率v(CO2)=_________________________________ 。
II:硫酸工业中用氢氧化钠溶液吸收SO2:2NaOH + SO2 → Na2SO3 + H2O, Na2SO3 + SO2 + H2O → 2NaHSO3已知: Na2SO3溶液显碱性,NaHSO3溶液显酸性,两者均易被氧化。
(1)用离子方程式解释Na2SO3溶液显碱性的原因。________________________
(2)若测得某次吸收SO2后的溶液的pH=7 (常温),则该溶液中c(H+)________ c(OH-) (选填“>”、“<”或“=”,下同),c(Na+)________ c(SO32-)+c(HSO3-)。上述溶液在空气中放置一段时间后,溶液的pH________ 7;原因是________________________________________ 。
I:烟道气中除去SO2的方法:2CO(g) + SO2(g) ⇌ 2CO2(g)+ S(l)+Q (Q>0)
(1)该反应的平衡常数表达式为
(2)下图是平衡时SO2的质量在不同温度下随压强的变化曲线,判断: T1

(3)若在2L的密闭容器中进行上述反应,经测定在5 min内气体的质量减小了1.6g。则0~5 min的平均反应速率v(CO2)=
II:硫酸工业中用氢氧化钠溶液吸收SO2:2NaOH + SO2 → Na2SO3 + H2O, Na2SO3 + SO2 + H2O → 2NaHSO3已知: Na2SO3溶液显碱性,NaHSO3溶液显酸性,两者均易被氧化。
(1)用离子方程式解释Na2SO3溶液显碱性的原因。
(2)若测得某次吸收SO2后的溶液的pH=7 (常温),则该溶液中c(H+)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】捕碳技术是指从空气中捕获二氧化碳的各种科学技术的统称。许多科学家认为从空气中捕获二氧化碳不仅在理论上可行,很快还会成为一个对付全球变暖的实用武器;目前NH3和(NH4)2CO3等物质已经被用作工业捕碳剂。
(1)下列物质中不可能作为CO2捕获剂的是___________ 。
A.Na2CO3 B.HOCH2CH2NH2 C.CH3CH2OH D.NH4Cl
(2)工业上用NH3捕碳可合成CO (NH2)2:
已知:①标准状况下,11.2L NH3与足量CO2完全反应生成NH2CO2 NH4 (s)时放出39.8kJ的热量;②NH2CO2 NH4 (s)= CO(NH2)2(s)+ H2O(g) =+72.5 kJ·mol-1。
=+72.5 kJ·mol-1。
则2NH3(g)+CO2(g)=CO(NH2)2(s)+ H2O(g) 的 =
=_____________ kJ·mol-1。
(3)用(NH4)2CO3捕碳的反应如下:
(NH4)2CO3(aq)+H2O(l)+CO2(g) 2(NH4)2HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
2(NH4)2HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:

①c点的逆反应速率和d点的正反应速率的大小关系为V逆c_____ V正d。(填“>”、“=”或“<”)
②b、c、d三点的平衡常数K b、K c、 Kd 从大到小的顺序为_____________ 。(填“>”、“=”或“<”)
③在T2~T4温度区间,容器内CO2气体浓度呈现先减小后增大的变化趋势,其原因是________ 。
(4)用碱性溶液也可捕碳:在常温下,将0.04mol CO2通入200mL 0.2mol/L的Na2S溶液中,已知: H2CO3的电离平衡常数:K1=4.3×10-7、K2=5.6×10-11;H2S的电离平衡常数:K1=5.0×10-8、K2=1.1×10-12。回答下列问题:
①发生反应的离子方程式为________ ;
②充分反应后下列关系式中正确的是_____________________ ;
A.(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-)
B. c(CO32-)+ c(HCO3-)+ c(H2CO3)>c(H2S)+c(HS-)+c(S2-)
C.c(Na+)>c(HCO3-)>c(HS-)>c(OH-)
③计算反应后的溶液中 的值为
的值为______ 。
(1)下列物质中不可能作为CO2捕获剂的是
A.Na2CO3 B.HOCH2CH2NH2 C.CH3CH2OH D.NH4Cl
(2)工业上用NH3捕碳可合成CO (NH2)2:
已知:①标准状况下,11.2L NH3与足量CO2完全反应生成NH2CO2 NH4 (s)时放出39.8kJ的热量;②NH2CO2 NH4 (s)= CO(NH2)2(s)+ H2O(g)
 =+72.5 kJ·mol-1。
=+72.5 kJ·mol-1。则2NH3(g)+CO2(g)=CO(NH2)2(s)+ H2O(g) 的
 =
=(3)用(NH4)2CO3捕碳的反应如下:
(NH4)2CO3(aq)+H2O(l)+CO2(g)
 2(NH4)2HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
2(NH4)2HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
①c点的逆反应速率和d点的正反应速率的大小关系为V逆c
②b、c、d三点的平衡常数K b、K c、 Kd 从大到小的顺序为
③在T2~T4温度区间,容器内CO2气体浓度呈现先减小后增大的变化趋势,其原因是
(4)用碱性溶液也可捕碳:在常温下,将0.04mol CO2通入200mL 0.2mol/L的Na2S溶液中,已知: H2CO3的电离平衡常数:K1=4.3×10-7、K2=5.6×10-11;H2S的电离平衡常数:K1=5.0×10-8、K2=1.1×10-12。回答下列问题:
①发生反应的离子方程式为
②充分反应后下列关系式中正确的是
A.(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-)
B. c(CO32-)+ c(HCO3-)+ c(H2CO3)>c(H2S)+c(HS-)+c(S2-)
C.c(Na+)>c(HCO3-)>c(HS-)>c(OH-)
③计算反应后的溶液中
 的值为
的值为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为________ 。
利用反应6NO2+8NH3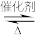 7N2+12H2O也可处理NO2。当转移0.4mol电子时,消耗的NO2在标准状况下的体积是
7N2+12H2O也可处理NO2。当转移0.4mol电子时,消耗的NO2在标准状况下的体积是______ L。
(2)SO2可用足量的NaOH溶液吸收,该反应的离子方程式为______ ;若继续通入SO2,当n (SO2): n(NaOH)=1:1时所得溶液呈酸性,下列关系正确的是_____ (填字母编号)。
a. c(Na+)> c(HSO3-)> c(SO32-)
b. c(Na+)+ c(H+)= c(SO32-)+ c(HSO3-)+ c(OH-)
c. c(Na+)= c(SO32-)+ c(HSO3-)
SO2也可用O2氧化生成SO3
已知:①NO2(g)+SO2(g) SO3(g)+NO(g) ΔH =" -41.8" kJ/mol ;
SO3(g)+NO(g) ΔH =" -41.8" kJ/mol ;
②2NO(g)+O2(g) 2NO2(g) ΔH =" -113.0" kJ/mol ;
2NO2(g) ΔH =" -113.0" kJ/mol ;
则反应2SO2(g)+O2(g) 2SO3(g) ΔH=
2SO3(g) ΔH=______ kJ/mol。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示。
CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示。
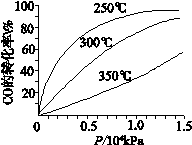
①该反应ΔH______ 0(填“>”或“<”)。
②若容器容积不变,下列措施可提高CO转化率的是_____ 。
a.升高温度 b.将CH3OH(g)从体系中分离
c.充入氦气,使体系总压强增大 d.再充入一定量的 CO气体
(1)NO2可用水吸收,相应的化学反应方程式为
利用反应6NO2+8NH3
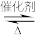 7N2+12H2O也可处理NO2。当转移0.4mol电子时,消耗的NO2在标准状况下的体积是
7N2+12H2O也可处理NO2。当转移0.4mol电子时,消耗的NO2在标准状况下的体积是(2)SO2可用足量的NaOH溶液吸收,该反应的离子方程式为
a. c(Na+)> c(HSO3-)> c(SO32-)
b. c(Na+)+ c(H+)= c(SO32-)+ c(HSO3-)+ c(OH-)
c. c(Na+)= c(SO32-)+ c(HSO3-)
SO2也可用O2氧化生成SO3
已知:①NO2(g)+SO2(g)
 SO3(g)+NO(g) ΔH =" -41.8" kJ/mol ;
SO3(g)+NO(g) ΔH =" -41.8" kJ/mol ;②2NO(g)+O2(g)
 2NO2(g) ΔH =" -113.0" kJ/mol ;
2NO2(g) ΔH =" -113.0" kJ/mol ;则反应2SO2(g)+O2(g)
 2SO3(g) ΔH=
2SO3(g) ΔH=(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)
 CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示。
CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示。
①该反应ΔH
②若容器容积不变,下列措施可提高CO转化率的是
a.升高温度 b.将CH3OH(g)从体系中分离
c.充入氦气,使体系总压强增大 d.再充入一定量的 CO气体
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。
(1)室温下,测得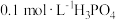 溶液的
溶液的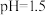 ,用电离方程式解释原因:
,用电离方程式解释原因:___________ 。
(2)羟基磷灰石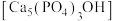 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: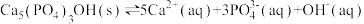 。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:___________ 。
(3)常温下,向磷酸溶液中滴加NaOH溶液,含磷微粒的分布比例与pH的关系如图所示。
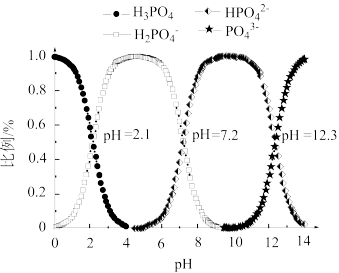
① 溶液显酸性。下列有关分析正确的是
溶液显酸性。下列有关分析正确的是___________ 。
a.溶液中
b. 的电离程度大于其水解程度
的电离程度大于其水解程度
c.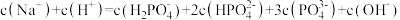
d.溶液中水的电离程度比纯水大
②当溶液的pH由4到10时,所发生反应的离子方程式是:___________ 。
(4)小组同学在实验室测定某可乐中磷酸的含量(不考虑白砂糖、咖啡因的影响)。
i.将可乐样品注入圆底烧瓶,加入活性炭,吸附色素。
ii.将可乐回流加热10 min,冷却至室温,过滤。
iii.取50.00 mL滤液,用百里香酚酞作指示剂,用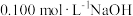 溶液滴定至终点时生成
溶液滴定至终点时生成 ,消耗NaOH溶液5.00 mL。
,消耗NaOH溶液5.00 mL。
①加热的目的是___________ 。
②该可乐样品中磷酸的含量为___________ g/L。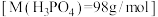
 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。(1)室温下,测得
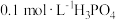 溶液的
溶液的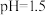 ,用电离方程式解释原因:
,用电离方程式解释原因:(2)羟基磷灰石
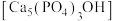 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: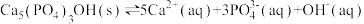 。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:(3)常温下,向磷酸溶液中滴加NaOH溶液,含磷微粒的分布比例与pH的关系如图所示。

①
 溶液显酸性。下列有关分析正确的是
溶液显酸性。下列有关分析正确的是a.溶液中

b.
 的电离程度大于其水解程度
的电离程度大于其水解程度c.
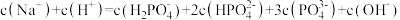
d.溶液中水的电离程度比纯水大
②当溶液的pH由4到10时,所发生反应的离子方程式是:
(4)小组同学在实验室测定某可乐中磷酸的含量(不考虑白砂糖、咖啡因的影响)。
i.将可乐样品注入圆底烧瓶,加入活性炭,吸附色素。
ii.将可乐回流加热10 min,冷却至室温,过滤。
iii.取50.00 mL滤液,用百里香酚酞作指示剂,用
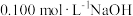 溶液滴定至终点时生成
溶液滴定至终点时生成 ,消耗NaOH溶液5.00 mL。
,消耗NaOH溶液5.00 mL。①加热的目的是
②该可乐样品中磷酸的含量为
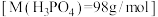
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】捕集CO2的技术对解决全球温室效应意义重大。目前国际空间站处理CO2的一个重要方法是将CO2还原,涉及的化学反应如下:CO2(g)+4H2(g)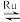 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)
完成下列填空:
(1)该反应的平衡常数表达式为________________________________ 。如果改变某种条件,平衡向正反应方向移动,则平衡常数________ (填写编号)。
a、一定增大 b、一定减小 c、可能增大 d、可能减小 e、可能不变
(2)为了提高CO2的捕获百分率,可采取的措施是____________________ 。(任写一条)
(3)向2L某密闭容器充入1mol CO2和4mol H2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为_______________ 。CO2还可应用于纯碱工业。工业生产纯碱的过程中,向饱和的氨化食盐水中通入足量CO2的生产环节又被称为“碳酸化”。
(4)碳酸化时产生的现象是____________________________ 。碳酸化过程中,溶液中c(CO32-)的变化情况为____________________ 。
(5)碳酸化后过滤,留在滤液中的阳离子主要有_______________ (填写化学式)。简述检验滤液中Cl- 离子的实验操作。________________________________
 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)完成下列填空:
(1)该反应的平衡常数表达式为
a、一定增大 b、一定减小 c、可能增大 d、可能减小 e、可能不变
(2)为了提高CO2的捕获百分率,可采取的措施是
(3)向2L某密闭容器充入1mol CO2和4mol H2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为
(4)碳酸化时产生的现象是
(5)碳酸化后过滤,留在滤液中的阳离子主要有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上用含三价钒( )为主的某石煤为原料(含有
)为主的某石煤为原料(含有 、CaO等杂质),钙化法焙烧制备
、CaO等杂质),钙化法焙烧制备 ,其流程如下:
,其流程如下:

【资料】:+5价钒在溶液中的主要存在形式与溶液pH的关系:
(1)焙烧:向石煤中加生石灰焙烧,将 转化为
转化为 的化学方程式是
的化学方程式是_______ 。
(2)酸浸:
① 难溶于水,可溶于盐酸。若焙砂酸浸时溶液的
难溶于水,可溶于盐酸。若焙砂酸浸时溶液的 ,
, 溶于盐酸的离子方程式是
溶于盐酸的离子方程式是_______ 。
②酸度对钒和铝的溶解量的影响如图所示:
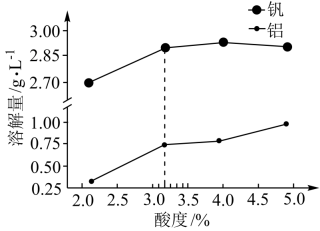
酸浸时溶液的酸度控制在大约3.2%,根据图推测,酸浸时不选择更高酸度的原因是_______ 。
(3)转沉:将浸出液中的钒转化为 固体,其流程如下:
固体,其流程如下:

①浸出液中加入石灰乳的作用是_______ 。
②已知 的溶解度小于
的溶解度小于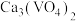 。向
。向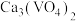 沉淀中加入
沉淀中加入 溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:
溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:_______ 。
③向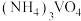 溶液中加入
溶液中加入 溶液,控制溶液的
溶液,控制溶液的 。当
。当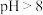 时,
时, 的产量明显降低,原因是
的产量明显降低,原因是_______ 。
(4)测定产品中 的纯度:称取ag产品,先用硫酸溶解,得到
的纯度:称取ag产品,先用硫酸溶解,得到 溶液。再加入
溶液。再加入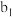 mL
mL 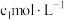
 溶液(
溶液(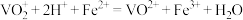 )。最后用
)。最后用 溶液滴定过量的
溶液滴定过量的 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 mL。已知
mL。已知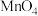 被还原为
被还原为 ,假设杂质不参与反应。则产品中
,假设杂质不参与反应。则产品中 的质量分数是
的质量分数是_______ 。( 的摩尔质量:
的摩尔质量: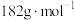 )
)
(5)全钒液流电池是具有发展前景的、用作储能系统的蓄电池,已知放电时 发生氧化反应,电池原理(电解液中含
发生氧化反应,电池原理(电解液中含 )如图:
)如图:
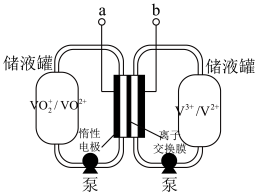
①a是_______ (填“正极”或“负极”)。
②该蓄电池反应方程式为_______ (标出“充电”“放电”方向)。
 )为主的某石煤为原料(含有
)为主的某石煤为原料(含有 、CaO等杂质),钙化法焙烧制备
、CaO等杂质),钙化法焙烧制备 ,其流程如下:
,其流程如下:
【资料】:+5价钒在溶液中的主要存在形式与溶液pH的关系:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |
 转化为
转化为 的化学方程式是
的化学方程式是(2)酸浸:
①
 难溶于水,可溶于盐酸。若焙砂酸浸时溶液的
难溶于水,可溶于盐酸。若焙砂酸浸时溶液的 ,
, 溶于盐酸的离子方程式是
溶于盐酸的离子方程式是②酸度对钒和铝的溶解量的影响如图所示:

酸浸时溶液的酸度控制在大约3.2%,根据图推测,酸浸时不选择更高酸度的原因是
(3)转沉:将浸出液中的钒转化为
 固体,其流程如下:
固体,其流程如下:
①浸出液中加入石灰乳的作用是
②已知
 的溶解度小于
的溶解度小于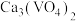 。向
。向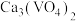 沉淀中加入
沉淀中加入 溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:
溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:③向
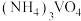 溶液中加入
溶液中加入 溶液,控制溶液的
溶液,控制溶液的 。当
。当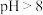 时,
时, 的产量明显降低,原因是
的产量明显降低,原因是(4)测定产品中
 的纯度:称取ag产品,先用硫酸溶解,得到
的纯度:称取ag产品,先用硫酸溶解,得到 溶液。再加入
溶液。再加入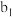 mL
mL 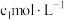
 溶液(
溶液(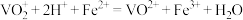 )。最后用
)。最后用 溶液滴定过量的
溶液滴定过量的 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 mL。已知
mL。已知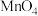 被还原为
被还原为 ,假设杂质不参与反应。则产品中
,假设杂质不参与反应。则产品中 的质量分数是
的质量分数是 的摩尔质量:
的摩尔质量: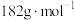 )
)(5)全钒液流电池是具有发展前景的、用作储能系统的蓄电池,已知放电时
 发生氧化反应,电池原理(电解液中含
发生氧化反应,电池原理(电解液中含 )如图:
)如图:
①a是
②该蓄电池反应方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】工业上以软锰矿(主要成分为MnO2,另含有少量铁、铝等金属化合物)为原料制得高纯MnO2,然后再继续制取KMnO4,其流程如下:
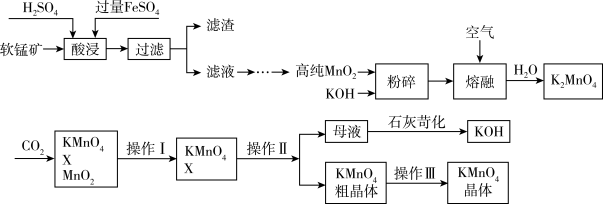
(1)实验室配制FeSO4往往会加入稀硫酸,原因是:_______ 。(结合离子方程式进行解释)
(2)由滤液制取高纯MnO2的过程中,有一步是加入氨水调节溶液pH,除去MnSO4溶液中的Al3+、Fe3+(使其浓度小于1×10-5mol/L),pH范围为_______ 。(已知:Ksp[Al(OH)3]=1×10-32,Ksp[Fe(OH)3]=1×10-38,pH=7时Mn(OH)2开始沉淀)
(3)由高纯MnO2生产K2MnO4的化学方程式为_______ 。
(4)在K2MnO4溶液中通入过量CO2气体,则X是_______ (填化学式),此时K2MnO4的理论利用率为_______ 。(保留1位小数)
(5)操作Ⅱ的名称为_______ 。
(6)上述流程中可循环使用的物质有_______ 。

(1)实验室配制FeSO4往往会加入稀硫酸,原因是:
(2)由滤液制取高纯MnO2的过程中,有一步是加入氨水调节溶液pH,除去MnSO4溶液中的Al3+、Fe3+(使其浓度小于1×10-5mol/L),pH范围为
(3)由高纯MnO2生产K2MnO4的化学方程式为
(4)在K2MnO4溶液中通入过量CO2气体,则X是
(5)操作Ⅱ的名称为
(6)上述流程中可循环使用的物质有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】Mg(OH)2具有广泛的用途。以菱镁矿(主要成分是MgCO3,含少量Al2O3、FeO等)为原科制备Mg(OH)2的工艺流程如下:
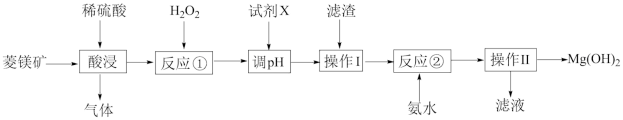
已知:常温下,部分氢氧化物开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“气体”的电子式是_______ 。
(2)下列操作不能显著增大“酸浸”速率的是_______ (填标号)。
a.适当增大稀硫酸的浓度
b.适当升高浸取液的温度
c.增大压强
d.将菱镁矿粉碎
(3)写出反应①的离子方程式:_______ 。
(4)“试剂X”较合理的是_______ (填化学式)。“调pH”时,合适的pH是_______ (填标号)。
a.1.9 b.3.4 c.7.6 d.9.6
(5)“操作I”和“操作II”为同一种操作,该操作名称是_______ ,“操作I”得到“滤渣”的主要成分是_______ (填化学式)。
(6)常温下,滴加氨水时,Mg2+的浓度为 时被认为完全沉淀,这时的pH为x,x=
时被认为完全沉淀,这时的pH为x,x=_______ (已知:常温下,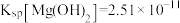 ,
, )。
)。

已知:常温下,部分氢氧化物开始沉淀和完全沉淀的pH如下表所示:
| 物质 |  |  |  |  |
| 开始沉淀的pH | 7.6 | 1.9 | 3.4 | 9.1 |
| 完全沉淀的pH | 9.6 | 3.2 | 4.8 | x |
回答下列问题:
(1)“气体”的电子式是
(2)下列操作不能显著增大“酸浸”速率的是
a.适当增大稀硫酸的浓度
b.适当升高浸取液的温度
c.增大压强
d.将菱镁矿粉碎
(3)写出反应①的离子方程式:
(4)“试剂X”较合理的是
a.1.9 b.3.4 c.7.6 d.9.6
(5)“操作I”和“操作II”为同一种操作,该操作名称是
(6)常温下,滴加氨水时,Mg2+的浓度为
 时被认为完全沉淀,这时的pH为x,x=
时被认为完全沉淀,这时的pH为x,x=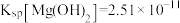 ,
, )。
)。
您最近一年使用:0次
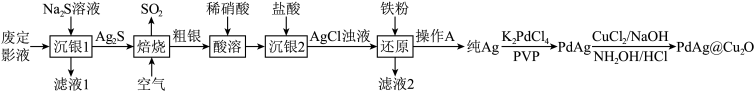
【推荐3】在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na2S2O3)溶解。从废定影液{主要含有[Ag(S2O3)2]3-、Br-等}中回收Ag并制取催化剂PdAg@Cu2O的流程如图所示:
已知:① 的结构如图所示:
的结构如图所示: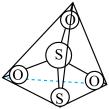 ;
;
②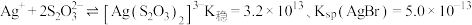 。
。
请回答下列问题:
(1)写出Na2S2O3溶液溶解AgBr生成 的离子方程式:
的离子方程式:___________ ,该反应的化学平衡常数为___________ 。
(2)在 配合反应中,作配位原子的不可能是
配合反应中,作配位原子的不可能是___________ (填字母)。
a. 中的中心S原子 b.
中的中心S原子 b. 中的端基S原子
中的端基S原子
(3)向滤液1中通入足量氯气后,通过一系列操作可分离出Br2。通入足量氯气后,Cl2发生的氧化还原反应主要有 、
、 、
、___________ 。
(4)“酸溶”过程中产生的有害气体是___________ (填化学式),实验室消除该有害气体的方法为___________ 。
(5)操作 的目的是
的目的是___________ 。
(6)在制备PdAg@Cu2O的反应中,NH2OH被氧化成无污染物(N2),若获得0.5molPdAg@Cu2O,理论上至少需要NH2OH___________ g。

已知:①
 的结构如图所示:
的结构如图所示: ;
;②
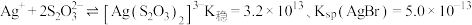 。
。请回答下列问题:
(1)写出Na2S2O3溶液溶解AgBr生成
 的离子方程式:
的离子方程式:(2)在
 配合反应中,作配位原子的不可能是
配合反应中,作配位原子的不可能是a.
 中的中心S原子 b.
中的中心S原子 b. 中的端基S原子
中的端基S原子(3)向滤液1中通入足量氯气后,通过一系列操作可分离出Br2。通入足量氯气后,Cl2发生的氧化还原反应主要有
 、
、 、
、(4)“酸溶”过程中产生的有害气体是
(5)操作
 的目的是
的目的是(6)在制备PdAg@Cu2O的反应中,NH2OH被氧化成无污染物(N2),若获得0.5molPdAg@Cu2O,理论上至少需要NH2OH
您最近一年使用:0次



