常温下,二元弱酸 溶液中含磷元素粒子的浓度之和为0.1
溶液中含磷元素粒子的浓度之和为0.1 ,溶液中各含磷粒子的pc-pOH关系如图所示。图中pc表示各含磷粒子的浓度负对数(
,溶液中各含磷粒子的pc-pOH关系如图所示。图中pc表示各含磷粒子的浓度负对数( ),pOH表示OH的浓度的负对数[
),pOH表示OH的浓度的负对数[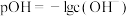 ]。下列有关说法不正确的是
]。下列有关说法不正确的是
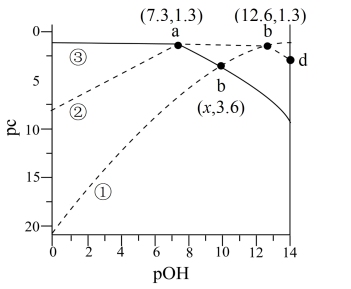
 溶液中含磷元素粒子的浓度之和为0.1
溶液中含磷元素粒子的浓度之和为0.1 ,溶液中各含磷粒子的pc-pOH关系如图所示。图中pc表示各含磷粒子的浓度负对数(
,溶液中各含磷粒子的pc-pOH关系如图所示。图中pc表示各含磷粒子的浓度负对数( ),pOH表示OH的浓度的负对数[
),pOH表示OH的浓度的负对数[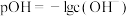 ]。下列有关说法不正确的是
]。下列有关说法不正确的是
A. 为酸式盐 为酸式盐 |
B.b点时, |
C.曲线③表示pc( )随pOH的变化 )随pOH的变化 |
D.d点溶液中: |
更新时间:2022-01-17 08:04:48
|
相似题推荐
多选题
|
较难
(0.4)
名校
【推荐1】化学上把由浓度相对较大的弱酸(弱碱)及其相应的盐组成的溶液,外加少量酸、碱而pH基本不变,称为缓冲溶液。弱酸及其盐组成的缓冲溶液的 。现有25℃时,浓度均为0.10mol·L-1的CH3COOH和CH3COONa的缓冲溶液
。现有25℃时,浓度均为0.10mol·L-1的CH3COOH和CH3COONa的缓冲溶液 。下列有关说法正确的是
。下列有关说法正确的是
 。现有25℃时,浓度均为0.10mol·L-1的CH3COOH和CH3COONa的缓冲溶液
。现有25℃时,浓度均为0.10mol·L-1的CH3COOH和CH3COONa的缓冲溶液 。下列有关说法正确的是
。下列有关说法正确的是| A.将该缓冲溶液加水稀释100倍,溶液的pH基本不变 |
| B.该缓冲溶液的pH=4.76 |
C.该缓冲溶液中离子浓度大小顺序是: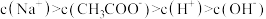 |
| D.人体血液存在H2CO3(CO2)和NaHCO3的缓冲溶液,可除掉人体代谢产生的酸、碱,保持pH基本不变 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】电解质溶液的导电能力越强,电导率越大。常温下用0.1000 mol∙L-1盐酸分别滴定10.00 mL浓度均为0.1000 mol·L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,已知在常温下Kb[(CH3)2NH∙H2O]=1.6×10-4),利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
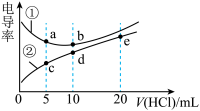

| A.曲线②代表滴定二甲胺溶液的曲线 |
B.d点溶液中:c(H+)>c(OH-)+c[(CH3)2NH ] ] |
| C.b、c、d三点的溶液中,b点水的电离程度最大 |
| D.a点溶液与d点的溶液混合后的溶液中:c[(CH3)2NH2+]>c[(CH3)2NH∙H2O] |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐3】常温下,向某浓度H2A溶液中加入NaOH(s),保持溶液体积和温度不变,测得pH与-lgc(M)[-lgc(H2A)、-lgc(A2-)、-lg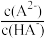 ]变化如图所示。下列说法错误的是
]变化如图所示。下列说法错误的是
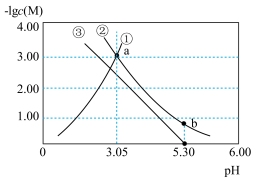
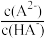 ]变化如图所示。下列说法错误的是
]变化如图所示。下列说法错误的是
| A.常温下,H2A电离平衡常数Ka1为10-1.08 |
| B.曲线②表示 -lg c(A2-)与pH变化关系 |
| C.NaHA溶液中c(Na+)>c(HA-)>c(A2-)>c(H2A) |
| D.b点时,满足c(Na+)>3c(A2-) |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】常温下,某浓度的H2A溶液中滴加NaOH溶液,若定义pc=-lgc,则测得pc(H2A)、pc(HA-)、pc(A2-)变化如图所示。下列说法错误的是( )
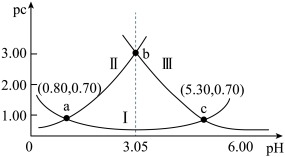
| A.pH=3时溶液中c(A2-)>c(H2A)>c(HA-) |
| B.常温下,H2A的Ka1=10-0.80,Ka2=10-5.30 |
| C.NaHA溶液中c(H+)>c(OH-) |
D.从a点到c点,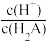 先增大后减小 先增大后减小 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】已知:p= 。室温下,向0.10mol·L-1的HX溶液中滴加0.1 mol·L-1的NaOH溶液,溶液pH随p的变化关系如图。下列说法正确的是
。室温下,向0.10mol·L-1的HX溶液中滴加0.1 mol·L-1的NaOH溶液,溶液pH随p的变化关系如图。下列说法正确的是

 。室温下,向0.10mol·L-1的HX溶液中滴加0.1 mol·L-1的NaOH溶液,溶液pH随p的变化关系如图。下列说法正确的是
。室温下,向0.10mol·L-1的HX溶液中滴加0.1 mol·L-1的NaOH溶液,溶液pH随p的变化关系如图。下列说法正确的是
| A.a点溶液中:c(HX)+ c(X—)=0.10mol·L-1 |
| B.b点坐标为(0,4.75) |
| C.c点溶液中:c(Na+)<10c(HX) |
| D.溶液中水的电离程度:c<b<a |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐3】改变0.1 mol·L-1二元弱酸H2A溶液的PH,溶液中H2A、HA-、A2-的物质的量分数 (X)随PH的变化如图所示[已知
(X)随PH的变化如图所示[已知 (X)=
(X)=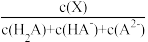 ,X表示含A微粒]。
,X表示含A微粒]。
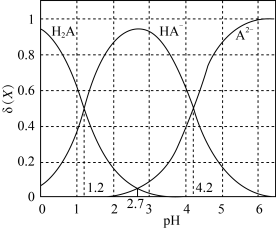
下列叙述错误的是
 (X)随PH的变化如图所示[已知
(X)随PH的变化如图所示[已知 (X)=
(X)=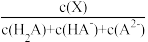 ,X表示含A微粒]。
,X表示含A微粒]。
下列叙述错误的是
A.H2A H+ +HA-,Kal = 1.0 H+ +HA-,Kal = 1.0 10-1.2 10-1.2 |
| B.pH =2.7 时,c(HA- ) >c(H2A) =c(A2-) |
| C.0.1 mol • L1 NaHA 溶液中存在 c(H+ ) + c(H2 A)= c(OH-) +2c(A2-) |
D.相同条件下,HF的Ka=1.0 10 -3.4,在NaF溶液中加入少量H2A,发生反应: H2A+2F- = 2HF+A2- 10 -3.4,在NaF溶液中加入少量H2A,发生反应: H2A+2F- = 2HF+A2- |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】25℃时,Ka1(H2C2O4)=10-1.3,Ka2(H2C2O4)=10-4.2。用0.050 mol/LH2C2O4溶液滴定25.00 mL0.100 mol/LNaOH溶液所得滴定曲线如图。下列说法正确的是( )
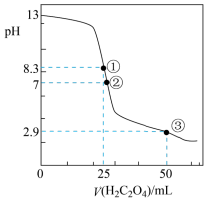

A.点①所示溶液中:c(H+)+c(H2C2O4)+c(HC2O )=c(OH-) )=c(OH-) |
B.点②所示溶液中:c(HC2O )+c(C2O )+c(C2O )<c(Na+) )<c(Na+) |
C.点③所示溶液中:c(Na+)>c(HC2O )>c(H2C2O4)>c(C2O )>c(H2C2O4)>c(C2O ) ) |
D.滴定过程中可能出现:c(Na+)>c(C2O )=c(HC2O )=c(HC2O )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】PT(KHC2O4·H2C2O4·2H2O,名称:四草酸钾)是一种分析试剂。室温时,H2C2O4的pKa1、pKa2分别为1.23、4.19(pKa=-lgKa)。下列说法不正确的是( )
A.0.1mol·L-1PT溶液中:c(HC2O )>c(K+)>c(H2C2O4) )>c(K+)>c(H2C2O4) |
B.0.1mol·L-1PT中滴加NaOH至溶液pH=4.19:c(C2O )=c(HC2O )=c(HC2O ) ) |
C.0.1mol·L-1PT中滴加NaOH至溶液呈中性:c(K+)>c(Na+)>c(HC2O )>c(C2O )>c(C2O ) ) |
| D.0.1mol·L-1PT与0.1mol·L-1KOH溶液等体积混合,溶液中水的电离程度比纯水的大 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】25℃时,某酸(结构简式为 )溶液中含元素X物种的浓度之和为
)溶液中含元素X物种的浓度之和为 ,溶液中各含元素X物种的pX随pOH变化关系如图所示。图中
,溶液中各含元素X物种的pX随pOH变化关系如图所示。图中 ,
,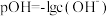 ;x、y两点的坐标:
;x、y两点的坐标: ;
; 、
、 分别表示
分别表示 的一级、二级电离常数。下列说法错误的是
的一级、二级电离常数。下列说法错误的是

 )溶液中含元素X物种的浓度之和为
)溶液中含元素X物种的浓度之和为 ,溶液中各含元素X物种的pX随pOH变化关系如图所示。图中
,溶液中各含元素X物种的pX随pOH变化关系如图所示。图中 ,
,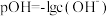 ;x、y两点的坐标:
;x、y两点的坐标: ;
; 、
、 分别表示
分别表示 的一级、二级电离常数。下列说法错误的是
的一级、二级电离常数。下列说法错误的是
A. 溶液显碱性,是因为 溶液显碱性,是因为 的水解程度大于电离程度 的水解程度大于电离程度 |
B. 溶液中, 溶液中, |
C.该体系中, |
D.z点时, |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】已知CaF2是难溶于水、可溶于酸的盐。常温下,用盐酸调节CaF2浊液的pH,测得在不同pH条件下,体系中 与-lgc(X)(X为Ca2+或F- )的关系如图所示。
与-lgc(X)(X为Ca2+或F- )的关系如图所示。
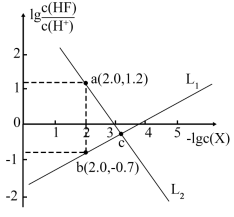
下列说法错误的是
 与-lgc(X)(X为Ca2+或F- )的关系如图所示。
与-lgc(X)(X为Ca2+或F- )的关系如图所示。
下列说法错误的是
A.L1表示-lgc(F- )与 的变化曲线 的变化曲线 |
| B.K sp(CaF2 )的数量级为10-10 |
| C.c点的溶液中: c(Cl-)<c(Ca2+) |
| D.a、b、c三点的溶液中: 2c(Ca2+)=c(F- )+c(HF) |
您最近一年使用:0次

 随H2A被滴定分数
随H2A被滴定分数 的变化关系如图所示。
的变化关系如图所示。
 =0.5的溶液中:2c(H+)+c(H2A)=c(HA-)+3c(A2-)+2c(OH-)
=0.5的溶液中:2c(H+)+c(H2A)=c(HA-)+3c(A2-)+2c(OH-) 溶液滴加到某二元弱酸
溶液滴加到某二元弱酸 溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是
溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是
 溶液中
溶液中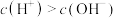
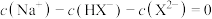 时,
时,
 上的点大于
上的点大于 上的点
上的点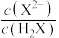 的数量级为
的数量级为


