由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见下图)中的重要反应之一。
人工合成淀粉(节选途径见下图)中的重要反应之一。
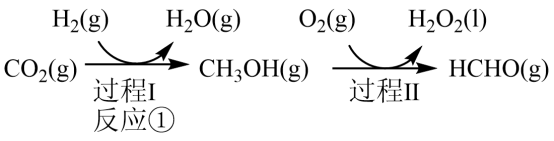
已知:
反应②:
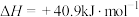 ;
;
反应③:
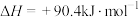 。
。
(1)反应①的热化学方程式为_______ ;若过程II中 得到4mol电子,则理论上可生成
得到4mol电子,则理论上可生成_______ mol HCHO。
(2)反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。
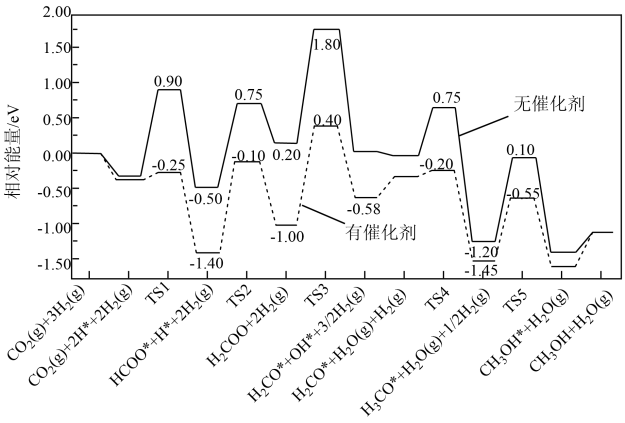
该反应历程中决速步骤的化学方程式为_______ ,催化剂使该步骤的活化能降低_______ eV。
(3)某研究小组采用上述催化剂,向密闭容器中通入 和
和 ,只发生反应①和反应②,在不同条件下达到平衡,在T=300℃下甲醇的体积分数
,只发生反应①和反应②,在不同条件下达到平衡,在T=300℃下甲醇的体积分数 随压强p的变化、在p=600kPa下
随压强p的变化、在p=600kPa下 随温度T的变化,如下图所示。
随温度T的变化,如下图所示。

i.下列说法正确的是_______ (填标号)。
A.曲线a为等压线,曲线b为等温线
B.增大 与
与 的浓度,反应①和反应②的正反应速率都增大
的浓度,反应①和反应②的正反应速率都增大
C.反应①的平衡常数:K(X)=K(Y)
D.反应②的正反应速率:v(X)<v(M)
ii.已知M点:容器中 为
为 ,CO为
,CO为 ,则此时
,则此时 的分压为
的分压为_______ kPa,反应①的压强平衡常数
_______  (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
iii.图中M点的 高于N点的原因是
高于N点的原因是_______ 。
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见下图)中的重要反应之一。
人工合成淀粉(节选途径见下图)中的重要反应之一。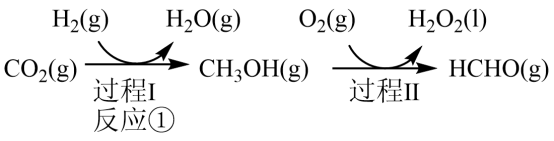
已知:
反应②:

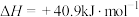 ;
;反应③:

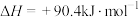 。
。(1)反应①的热化学方程式为
 得到4mol电子,则理论上可生成
得到4mol电子,则理论上可生成(2)反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。

该反应历程中决速步骤的化学方程式为
(3)某研究小组采用上述催化剂,向密闭容器中通入
 和
和 ,只发生反应①和反应②,在不同条件下达到平衡,在T=300℃下甲醇的体积分数
,只发生反应①和反应②,在不同条件下达到平衡,在T=300℃下甲醇的体积分数 随压强p的变化、在p=600kPa下
随压强p的变化、在p=600kPa下 随温度T的变化,如下图所示。
随温度T的变化,如下图所示。
i.下列说法正确的是
A.曲线a为等压线,曲线b为等温线
B.增大
 与
与 的浓度,反应①和反应②的正反应速率都增大
的浓度,反应①和反应②的正反应速率都增大C.反应①的平衡常数:K(X)=K(Y)
D.反应②的正反应速率:v(X)<v(M)
ii.已知M点:容器中
 为
为 ,CO为
,CO为 ,则此时
,则此时 的分压为
的分压为
 (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。iii.图中M点的
 高于N点的原因是
高于N点的原因是
2022·广东·一模 查看更多[4]
福建省永春第一中学2023届高三下学期期初考试化学试题(已下线)押广东卷化学第19题 化学反应原理综合题-备战2022年高考化学临考题号押题(广东卷)广东省普通高中2022届高三学业水平选择考化学模拟测试(一)广东省2021-2022学年高三下学期一模化学试题
更新时间:2022-03-31 16:12:52
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】Ⅰ.CH4—CO2催化重整是减少温室气体排放的重要途径。
已知以下的热化学反应方程式:
C(s)+2H2(g)=CH4(g)ΔH1= -75kJ·mol-1
C(s)+O2(g)=CO2(g)ΔH2= -394kJ·mol-1
C(s)+ O2(g)=CO(g)ΔH3= -111kJ·mol-1
O2(g)=CO(g)ΔH3= -111kJ·mol-1
写出催化重整反应CH4(g)和CO2(g)生成CO(g)和H2(g)的热化学方程式:____ 。
Ⅱ.CO是煤气的主要成分,可与水蒸气反应生成氢气:CO(g)+H2O(g) CO2(g)+H2(g)ΔH。 查阅资料得出相关数据如下:
CO2(g)+H2(g)ΔH。 查阅资料得出相关数据如下:
(1)通过表格中的数值可以推断:反应ΔH______ 0(填“>”或“<”)。该反应升高到一定温度时,反应将不能正向进行,由此判断该反应的ΔS_______ 0(填“>”或“<”)。
(2)在容积为10L的密闭容器中通入0.1molCO(g)和0.1molH2O(g)发生反应,在400℃时反应达到平衡,此时CO(g)的转化率为_____ 。
(3)在绝热恒容条件下,反应物物质的量均为1mol发生反应,下列不能说明反应达到平衡状态的有______ (填字母)。
a.体系的压强不再发生变化b.混合气体的密度不变c.混合气体的平均相对分子质量不变
d.各组分的物质的量浓度不再改变e.体系的温度不再发生变化f.v正(CO)=v逆(H2O)
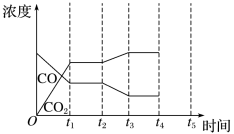
(4)如图是反应在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:则t2时刻改变的条件可能是____ (写出1种即可)。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称___ (假设各物质状态均保持不变)。
已知以下的热化学反应方程式:
C(s)+2H2(g)=CH4(g)ΔH1= -75kJ·mol-1
C(s)+O2(g)=CO2(g)ΔH2= -394kJ·mol-1
C(s)+
 O2(g)=CO(g)ΔH3= -111kJ·mol-1
O2(g)=CO(g)ΔH3= -111kJ·mol-1写出催化重整反应CH4(g)和CO2(g)生成CO(g)和H2(g)的热化学方程式:
Ⅱ.CO是煤气的主要成分,可与水蒸气反应生成氢气:CO(g)+H2O(g)
 CO2(g)+H2(g)ΔH。 查阅资料得出相关数据如下:
CO2(g)+H2(g)ΔH。 查阅资料得出相关数据如下:温度/℃ | 400 | 500 |
平衡常数K | 9 | 5.3 |
(2)在容积为10L的密闭容器中通入0.1molCO(g)和0.1molH2O(g)发生反应,在400℃时反应达到平衡,此时CO(g)的转化率为
(3)在绝热恒容条件下,反应物物质的量均为1mol发生反应,下列不能说明反应达到平衡状态的有
a.体系的压强不再发生变化b.混合气体的密度不变c.混合气体的平均相对分子质量不变
d.各组分的物质的量浓度不再改变e.体系的温度不再发生变化f.v正(CO)=v逆(H2O)
(4)如图是反应在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:则t2时刻改变的条件可能是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】研究氮氧化物污染的治理是环保的一项重要工作.合理应用和处理氨氧化物,在生产生活中有重要意义.
(1)已知:①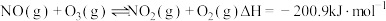 ;
;
② .
.
则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为_______________________ .
(2)利用测压法在恒容刚性反应器中研究反应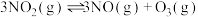 ,充入一定量
,充入一定量 ,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
① 时,反应物的转化率
时,反应物的转化率
_____________ .若降低反应温度,则平衡后体系总压强小于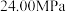 ,主要原因是
,主要原因是________________________ .
②T℃时反应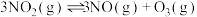 的平衡常数
的平衡常数
______ ( 为以分压表示的平衡常数).
为以分压表示的平衡常数).
(3)一定条件下,在体积为2L的密闭容器中充入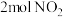 发生反应:
发生反应: 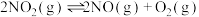 .实验测得
.实验测得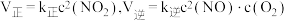 ,
, 是为速率常数,受温度影响.在温度为T℃时
是为速率常数,受温度影响.在温度为T℃时 的转化率随时间变化的情况如图所示.
的转化率随时间变化的情况如图所示.
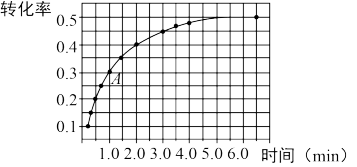
①要提高 的转化率,可采取的措施是
的转化率,可采取的措施是_____________ 、____________ (写两条).
②计算A点处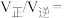
_____________ (保留一位小数).
(1)已知:①
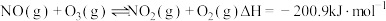 ;
;②
 .
.则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为
(2)利用测压法在恒容刚性反应器中研究反应
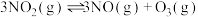 ,充入一定量
,充入一定量 ,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
,T℃时,测得体系的总压强p随反应时间t的变化如表所示:| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| p/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
 时,反应物的转化率
时,反应物的转化率
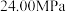 ,主要原因是
,主要原因是②T℃时反应
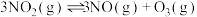 的平衡常数
的平衡常数
 为以分压表示的平衡常数).
为以分压表示的平衡常数).(3)一定条件下,在体积为2L的密闭容器中充入
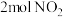 发生反应:
发生反应: 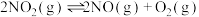 .实验测得
.实验测得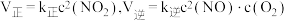 ,
, 是为速率常数,受温度影响.在温度为T℃时
是为速率常数,受温度影响.在温度为T℃时 的转化率随时间变化的情况如图所示.
的转化率随时间变化的情况如图所示.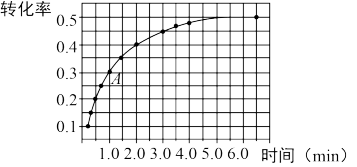
①要提高
 的转化率,可采取的措施是
的转化率,可采取的措施是②计算A点处
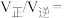
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】NOx是造成大气污染的主要物质,用还原法将其转化为无污染的物质,对于消除环境污染有重要意义。
(1)已知:2C(s)+O2(g) 2CO(g)△H=-221.0kJ/mol
2CO(g)△H=-221.0kJ/mol
N2(g)+O2(g) 2NO(g)△H=+180.5kJ/mol
2NO(g)△H=+180.5kJ/mol
2NO(g)+2CO(g) 2CO2(g)+N2(g)△H=-746.0kJ/mol
2CO2(g)+N2(g)△H=-746.0kJ/mol
则用焦炭还原NO生成无污染气体的热化学方程式为____ 。该反应的平衡常数Kp=___ (写表达式)。
(2)用NR催化还原NOx也可以消除氮氧化物的污染。
已知:8NH3(g)+6NO2(g)=7N2(g)+12H2O(l)△H<0,相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间变化如图所示。
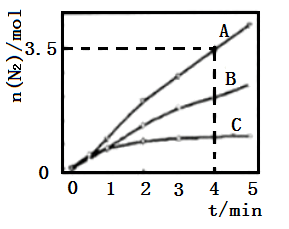
①在催化剂A的作用下,0~4min的v(NH3)=__________ 。
②该反应活化能Ea(A)、Ea(B)、Ea(C)由大到小的顺序是______ ,理由是____________ 。
③下列说法正确的是_____ (填标号)。
a使用催化剂A达平衡时,△H值更大
b升高温度可使容器内气体颜色加深
c单位时间内形成N-H键与O-H键的数目相等时,说明反应已经达到平衡
d若在恒容绝热的密闭容器中反应,当平衡常数不变时,说明反应已经达到平衡
(1)已知:2C(s)+O2(g)
 2CO(g)△H=-221.0kJ/mol
2CO(g)△H=-221.0kJ/molN2(g)+O2(g)
 2NO(g)△H=+180.5kJ/mol
2NO(g)△H=+180.5kJ/mol2NO(g)+2CO(g)
 2CO2(g)+N2(g)△H=-746.0kJ/mol
2CO2(g)+N2(g)△H=-746.0kJ/mol则用焦炭还原NO生成无污染气体的热化学方程式为
(2)用NR催化还原NOx也可以消除氮氧化物的污染。
已知:8NH3(g)+6NO2(g)=7N2(g)+12H2O(l)△H<0,相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间变化如图所示。

①在催化剂A的作用下,0~4min的v(NH3)=
②该反应活化能Ea(A)、Ea(B)、Ea(C)由大到小的顺序是
③下列说法正确的是
a使用催化剂A达平衡时,△H值更大
b升高温度可使容器内气体颜色加深
c单位时间内形成N-H键与O-H键的数目相等时,说明反应已经达到平衡
d若在恒容绝热的密闭容器中反应,当平衡常数不变时,说明反应已经达到平衡
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】碳酸二甲酯(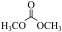 )是一种绿色化工原料。用于汽车、医疗器械等领域。以甲醇为原料生产碳酸二甲酯的反应过程如下。
)是一种绿色化工原料。用于汽车、医疗器械等领域。以甲醇为原料生产碳酸二甲酯的反应过程如下。
i.
ii.
(1)碳酸二甲酯分子中碳原子的杂化类型是___________ 。
(2)CuCl中,基态 的价电子排布式为
的价电子排布式为___________ ,CuCl在生产碳酸二甲酯的反应过程中所起的作用是___________ 。
(3)上述方法中,甲醇单位时间内的转化率较低。为分析原因,查阅如下资料。
i.甲醇单位时间内的转化率主要受 (+1价铜元素)浓度的影响。
(+1价铜元素)浓度的影响。
ii.CuCl在甲醇中溶解度较小,且其中的 易被氧化为难溶的CuO。
易被氧化为难溶的CuO。
iii.加入4-甲基咪唑(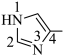 )可与
)可与 形成配合物, 可提高甲醇的转化率。4-甲基咪唑中,1号N原子的孤电子对因参与形成大π键,电子云密度降低。
形成配合物, 可提高甲醇的转化率。4-甲基咪唑中,1号N原子的孤电子对因参与形成大π键,电子云密度降低。
请结合信息回答以下问题。
①4-甲基咪唑中,1~4号原子___________ (填“在”或“不在”)同一平面上,___________ (填“1”或“3”)号N原子更容易与 形成配位键。
形成配位键。
②加入4-甲基咪唑后,甲醇转化率提高,可能的原因是___________ (填序号)。
a. 配合物中的-NH结构可增大其在甲醇中的溶解度
配合物中的-NH结构可增大其在甲醇中的溶解度
b.通过形成配合物,避免 被氧化为难溶的CuO
被氧化为难溶的CuO
c.形成的 配合物能增大反应的限度
配合物能增大反应的限度
(4)配位原子提供孤电子对的能力是影响配体与 之间配位键强度的一个重要因素。若用某结构相似的含O配体与
之间配位键强度的一个重要因素。若用某结构相似的含O配体与 配位,所得配合物的稳定性比含N配体低,可能的原因是
配位,所得配合物的稳定性比含N配体低,可能的原因是___________ 。
 )是一种绿色化工原料。用于汽车、医疗器械等领域。以甲醇为原料生产碳酸二甲酯的反应过程如下。
)是一种绿色化工原料。用于汽车、医疗器械等领域。以甲醇为原料生产碳酸二甲酯的反应过程如下。i.

ii.

(1)碳酸二甲酯分子中碳原子的杂化类型是
(2)CuCl中,基态
 的价电子排布式为
的价电子排布式为(3)上述方法中,甲醇单位时间内的转化率较低。为分析原因,查阅如下资料。
i.甲醇单位时间内的转化率主要受
 (+1价铜元素)浓度的影响。
(+1价铜元素)浓度的影响。ii.CuCl在甲醇中溶解度较小,且其中的
 易被氧化为难溶的CuO。
易被氧化为难溶的CuO。iii.加入4-甲基咪唑(
 )可与
)可与 形成配合物, 可提高甲醇的转化率。4-甲基咪唑中,1号N原子的孤电子对因参与形成大π键,电子云密度降低。
形成配合物, 可提高甲醇的转化率。4-甲基咪唑中,1号N原子的孤电子对因参与形成大π键,电子云密度降低。请结合信息回答以下问题。
①4-甲基咪唑中,1~4号原子
 形成配位键。
形成配位键。②加入4-甲基咪唑后,甲醇转化率提高,可能的原因是
a.
 配合物中的-NH结构可增大其在甲醇中的溶解度
配合物中的-NH结构可增大其在甲醇中的溶解度b.通过形成配合物,避免
 被氧化为难溶的CuO
被氧化为难溶的CuOc.形成的
 配合物能增大反应的限度
配合物能增大反应的限度(4)配位原子提供孤电子对的能力是影响配体与
 之间配位键强度的一个重要因素。若用某结构相似的含O配体与
之间配位键强度的一个重要因素。若用某结构相似的含O配体与 配位,所得配合物的稳定性比含N配体低,可能的原因是
配位,所得配合物的稳定性比含N配体低,可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】草酸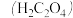 溶液与酸性
溶液与酸性 溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
【查阅资料】 溶液氧化
溶液氧化 的反应历程为:
的反应历程为:
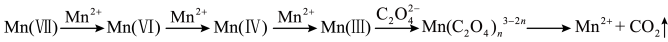
【提出假设】假设1:该反应为放热
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是______ 。
【设计、完成实验】
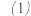 称取
称取______ g草酸晶体 ,配置500mL
,配置500mL
 溶液。
溶液。
①在上述过程中必须用到的2种定量仪器是托盘天平和______ 。
②下列操作会使所配溶液浓度偏低的是______ 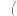 填下列选项的字母序号
填下列选项的字母序号 。
。
A 称取草酸晶体时,将草酸晶体放在托盘天平右盘
B 定容时俯视刻度线
C 将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D 摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
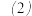 完成探究,记录数据
完成探究,记录数据
则
______ ,假设______ 成立。
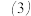 由于
由于 能氧化水中有机物等因素,配置好稳定的
能氧化水中有机物等因素,配置好稳定的 溶液,其浓度需标定.取
溶液,其浓度需标定.取

 溶液于锥形瓶中,加入10mL
溶液于锥形瓶中,加入10mL 稀硫酸,用
稀硫酸,用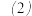 中
中 溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗
溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗 溶液
溶液 ,则草酸溶液与酸性
,则草酸溶液与酸性 溶液反应的离子方程式为:
溶液反应的离子方程式为:______ ,上述实验中 溶液的物质的量浓度为
溶液的物质的量浓度为______ 。
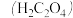 溶液与酸性
溶液与酸性 溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:【查阅资料】
 溶液氧化
溶液氧化 的反应历程为:
的反应历程为: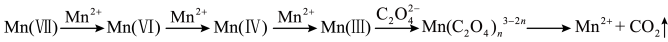
【提出假设】假设1:该反应为放热
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是
【设计、完成实验】
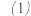 称取
称取 ,配置500mL
,配置500mL
 溶液。
溶液。①在上述过程中必须用到的2种定量仪器是托盘天平和
②下列操作会使所配溶液浓度偏低的是
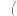 填下列选项的字母序号
填下列选项的字母序号 。
。A 称取草酸晶体时,将草酸晶体放在托盘天平右盘
B 定容时俯视刻度线
C 将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D 摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
 完成探究,记录数据
完成探究,记录数据| 实验 编号 | 烧杯中所加试剂及用量 | 控制条件 | 溶液褪 色时间  | |||
  溶液 溶液 | 等浓度 溶液 溶液 |  |  稀硫酸 | |||
| 1 | 30 | 20 | 30 | 20 | 18 | |
| 2 | 30 | 20 | 30 | 20 | 水浴控制温度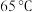 | 15 |
| 3 | 30 | 20 | 30 | 20 | 加入少量 固体 固体 |  |
| 4 | 30 | 20 | x | 20 | 加入5mL  溶液 溶液 | 18 |

 由于
由于 能氧化水中有机物等因素,配置好稳定的
能氧化水中有机物等因素,配置好稳定的 溶液,其浓度需标定.取
溶液,其浓度需标定.取

 溶液于锥形瓶中,加入10mL
溶液于锥形瓶中,加入10mL 稀硫酸,用
稀硫酸,用 中
中 溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗
溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗 溶液
溶液 ,则草酸溶液与酸性
,则草酸溶液与酸性 溶液反应的离子方程式为:
溶液反应的离子方程式为: 溶液的物质的量浓度为
溶液的物质的量浓度为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】“氢经济”是“双碳”转型中非常关键的一环。大量安全制氢是关键技术之一。
方法一:工业上常用甲烷、水蒸气重整制备氢气,体系中发生如下反应:
反应①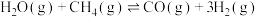
反应②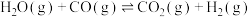
(1)下列操作中,能提高 平衡转化率的是_____。(双选)
平衡转化率的是_____。(双选)
(2)恒温条件下,1L密闭容器中, 和
和 反应达平衡时,
反应达平衡时, 的转化率为
的转化率为 ,
, 的物质的量为
的物质的量为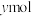 ,则反应①的平衡常数
,则反应①的平衡常数
_____ 。(用 、
、 表示)
表示)
方法二:用与 制备
制备 可以同时实现资源化利用,其反应历程如下:
可以同时实现资源化利用,其反应历程如下:
反应①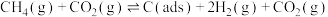
反应②
已知: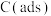 为吸附型活性炭。
为吸附型活性炭。
(3)使用不同催化剂时,相同时间内测得 的转化率随温度的变化如下图所示:
的转化率随温度的变化如下图所示:

催化效果最佳的是催化剂_____ (选填“Ⅰ”、“Ⅱ”或“Ⅲ”),b点的
_____  (选填“>”、“<”或“=”),c点转化率比a点低的可能原因是
(选填“>”、“<”或“=”),c点转化率比a点低的可能原因是_____ 。(任写一点)
方法一:工业上常用甲烷、水蒸气重整制备氢气,体系中发生如下反应:
反应①
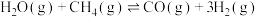
反应②
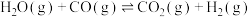
(1)下列操作中,能提高
 平衡转化率的是_____。(双选)
平衡转化率的是_____。(双选)A.增大 的浓度 的浓度 | B.分离出 |
| C.恒温恒压下通入惰性气体 | D.加入催化剂 |
(2)恒温条件下,1L密闭容器中,
 和
和 反应达平衡时,
反应达平衡时, 的转化率为
的转化率为 ,
, 的物质的量为
的物质的量为 ,则反应①的平衡常数
,则反应①的平衡常数
 、
、 表示)
表示)方法二:用与
 制备
制备 可以同时实现资源化利用,其反应历程如下:
可以同时实现资源化利用,其反应历程如下:反应①
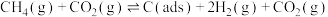
反应②

已知:
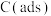 为吸附型活性炭。
为吸附型活性炭。(3)使用不同催化剂时,相同时间内测得
 的转化率随温度的变化如下图所示:
的转化率随温度的变化如下图所示:
催化效果最佳的是催化剂

 (选填“>”、“<”或“=”),c点转化率比a点低的可能原因是
(选填“>”、“<”或“=”),c点转化率比a点低的可能原因是
您最近一年使用:0次
【推荐1】NOx是污染大气的主要成分之一,它主要来源于汽车尾气的排放和化石燃料的燃烧。回答下列问题:
(1)已知:①2C(s)+O2(g) 2CO(g)
2CO(g)  H1=-221kJ/mol
H1=-221kJ/mol
②2NO(g) N2(g)+O2(g)
N2(g)+O2(g)  H2=-180kJ/mol
H2=-180kJ/mol
③2NO(g)+C(s) CO2(g)+N2(g)
CO2(g)+N2(g)  H3=-573kJ/mol
H3=-573kJ/mol
则2NO(g)+2CO(g) 2CO2(g)+N2(g)的反应热
2CO2(g)+N2(g)的反应热 H=
H=___________ 。
(2)燃煤烟气脱硝的反应之一为2NO2(g)+4CO(g) N2(g)+4CO2(g),在一定温度下,向1L恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:
N2(g)+4CO2(g),在一定温度下,向1L恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:
①c值可能为___________ (填字母),其他条件不变,若不使用催化剂,则0~2min内NO2的转化率将___________ (填“变大”“变小”或“不变”)。
A.1.68 B.1.65 C.1.6 D.1.55
②维持其他条件不变,第9min时向容器中再充入1.0molNO2和1.0molN2,则v(正)___________ (填“>”或“<”)v(逆)。
(3)烟气脱硝的另一个反应为2C(s)+2NO2(g) N2(g)+2CO2(g)。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强下,相同时间内NO2的转化率与压强的关系如图所示。
N2(g)+2CO2(g)。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强下,相同时间内NO2的转化率与压强的关系如图所示。___________ ,在T℃时,用此反应脱硝适宜的压强是___________ ,1100kPa时,该反应的化学平衡常数Kp=___________ kPa(用平衡分压代替平衡浓度,气体分压=气体总压×体积分数,结果保留两位小数)。
(4)利用电化学原理脱硝可获得电能,其工作原理如图所示:___________ 。
(1)已知:①2C(s)+O2(g)
 2CO(g)
2CO(g)  H1=-221kJ/mol
H1=-221kJ/mol②2NO(g)
 N2(g)+O2(g)
N2(g)+O2(g)  H2=-180kJ/mol
H2=-180kJ/mol③2NO(g)+C(s)
 CO2(g)+N2(g)
CO2(g)+N2(g)  H3=-573kJ/mol
H3=-573kJ/mol则2NO(g)+2CO(g)
 2CO2(g)+N2(g)的反应热
2CO2(g)+N2(g)的反应热 H=
H=(2)燃煤烟气脱硝的反应之一为2NO2(g)+4CO(g)
 N2(g)+4CO2(g),在一定温度下,向1L恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:
N2(g)+4CO2(g),在一定温度下,向1L恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:| 时间 | 0min | 2min | 4min | 6min | 8min | 10min |
| c(NO2)/mol·L-1 | 2.00 | 1.80 | c | 1.55 | 1.50 | 1.50 |
A.1.68 B.1.65 C.1.6 D.1.55
②维持其他条件不变,第9min时向容器中再充入1.0molNO2和1.0molN2,则v(正)
(3)烟气脱硝的另一个反应为2C(s)+2NO2(g)
 N2(g)+2CO2(g)。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强下,相同时间内NO2的转化率与压强的关系如图所示。
N2(g)+2CO2(g)。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强下,相同时间内NO2的转化率与压强的关系如图所示。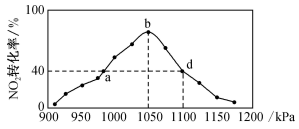
(4)利用电化学原理脱硝可获得电能,其工作原理如图所示:
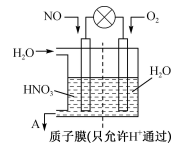
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】某小组研究发现某条件下可实现乙醛的分解,其热化学方程式为CH3CHO(g) CH4(g)+CO(g) △H。回答下列问题:
CH4(g)+CO(g) △H。回答下列问题:
(1)已知几种共价键的键能如表:
上述反应的△H=____ kJ•mol-1。
(2)上述正反应速率方程为v=kcn(CH3CHO)(k为速率常数,与温度、催化剂有关)。实验测得CH3CHO的反应速率与浓度关系如表所示:
①上述速率方程中,n=____ (n为整数)。
②c(CH3CHO)=0.15mol•L-1时,正反应速率为____ 。
③下列有关说法正确的是____ (填字母)。
A.升高温度,k增大;加催化剂,k减小 B.升高温度,k减小;加催化剂,k增大
C.降低温度,k减小;加催化剂,k增大 D.降低温度,k增大;加催化剂,k减小
(3)在一定温度下,向恒容密闭容器中充入1molCH3CHO(g),在一定条件下达到平衡。
①下列情况表明上述反应达到平衡状态的是___ (填字母)。
A.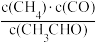 保持不变 B.混合气体密度保持不变
保持不变 B.混合气体密度保持不变
C.气体压强保持不变 D. 消耗速率等于CH3CHO生成速率
消耗速率等于CH3CHO生成速率
②平衡后再充入少量乙醛,平衡____ (填“向左”“向右”或“不”)移动,达到新平衡时乙醛的平衡转化率____ (填“增大”“减小”或“不变”)。
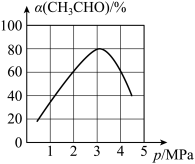
(4)一定温度下,向某密闭容器中充入适量CH3CHO(g),测得CH3CHO的转化率与压强的关系如图所示。当压强为4MPa时,该反应的平衡常数Kp=____ (结果保留三位有效数字且带单位)。(提示:用各物质分压计算的平衡常数为Kp,分压=总压×物质的量分数)。
 CH4(g)+CO(g) △H。回答下列问题:
CH4(g)+CO(g) △H。回答下列问题:(1)已知几种共价键的键能如表:
| 共价键 | C-H | C-C | C-O | C≡O |
| 键能/(kJ•mol-1) | 413 | 347 | 745 | 958.5 |
(2)上述正反应速率方程为v=kcn(CH3CHO)(k为速率常数,与温度、催化剂有关)。实验测得CH3CHO的反应速率与浓度关系如表所示:
| c(CH3CHO)/(mol•L-1) | 0.1 | 0.2 | 0.3 | 0.4 |
| v/( mol•L-1•s-1) | 0.020 | 0.081 | 0.182 | 0.318 |
②c(CH3CHO)=0.15mol•L-1时,正反应速率为
③下列有关说法正确的是
A.升高温度,k增大;加催化剂,k减小 B.升高温度,k减小;加催化剂,k增大
C.降低温度,k减小;加催化剂,k增大 D.降低温度,k增大;加催化剂,k减小
(3)在一定温度下,向恒容密闭容器中充入1molCH3CHO(g),在一定条件下达到平衡。
①下列情况表明上述反应达到平衡状态的是
A.
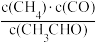 保持不变 B.混合气体密度保持不变
保持不变 B.混合气体密度保持不变C.气体压强保持不变 D.
 消耗速率等于CH3CHO生成速率
消耗速率等于CH3CHO生成速率②平衡后再充入少量乙醛,平衡
(4)一定温度下,向某密闭容器中充入适量CH3CHO(g),测得CH3CHO的转化率与压强的关系如图所示。当压强为4MPa时,该反应的平衡常数Kp=

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】完成下列问题。
(1)化学键的键能是形成(或断裂)1 mol化学键时释放(或吸收)的能量。以下是部分共价键键能的数据:H-S:364 kJ·mol-1,S-S:266 kJ·mol-1,S=O:522 kJ·mol-1,H-O:463 kJ·mol-1,试根据这些数据计算下列反应的反应热:2H2S(g)+SO2(g)= 3S(s)+2H2O(l) ΔH=-Q kJ·mol-1,反应产物中的S实为S8,实际分子是一个八元环状分子( ),则Q=
),则Q=______ 。
(2)已知反应aA(g)+bB(g) cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。_____ 。
②经测定,前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为______ 。
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1,乙:v(B)=0.12 mol·L-1·s-1,丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为_______ 。
(3)向某容积不变的密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。
N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。
(4)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应:
Ⅰ.CH4(g)+H2O(g) CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)
CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
①下列操作中,能提高CH4(g)平衡转化率的是____ (填标号)。
A.增加CH4 (g)用量 B.恒温恒压下通入惰性气体
C.移除CO(g) D.加入催化剂
②恒温恒压条件下,1 mol CH4 (g)和1 mol H2O(g)反应达平衡时,CH4 (g)的转化率为α,CO2(g)的物质的量为b mol,则反应Ⅰ的平衡常数Kx=____ [写出含有α、b的计算式;对于反应mA(g)+nB(g) pC(g)+qD(g),Kx=
pC(g)+qD(g),Kx=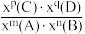 ,x为物质的量分数]。
,x为物质的量分数]。
(1)化学键的键能是形成(或断裂)1 mol化学键时释放(或吸收)的能量。以下是部分共价键键能的数据:H-S:364 kJ·mol-1,S-S:266 kJ·mol-1,S=O:522 kJ·mol-1,H-O:463 kJ·mol-1,试根据这些数据计算下列反应的反应热:2H2S(g)+SO2(g)= 3S(s)+2H2O(l) ΔH=-Q kJ·mol-1,反应产物中的S实为S8,实际分子是一个八元环状分子(
 ),则Q=
),则Q=(2)已知反应aA(g)+bB(g)
 cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。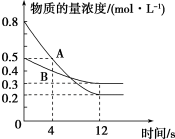
②经测定,前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1,乙:v(B)=0.12 mol·L-1·s-1,丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
(3)向某容积不变的密闭容器中充入一定量的NO2,发生反应2NO2(g)
 N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。
N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。| A.升高温度,混合气体的颜色变浅 |
| B.通入NO2,化学平衡常数增大 |
| C.通入NO2,重新达到平衡后混合气体的平均相对分子质量增大 |
| D.增大压强,平衡向正反应方向移动,混合气体的颜色变浅 |
Ⅰ.CH4(g)+H2O(g)
 CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)
CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)①下列操作中,能提高CH4(g)平衡转化率的是
A.增加CH4 (g)用量 B.恒温恒压下通入惰性气体
C.移除CO(g) D.加入催化剂
②恒温恒压条件下,1 mol CH4 (g)和1 mol H2O(g)反应达平衡时,CH4 (g)的转化率为α,CO2(g)的物质的量为b mol,则反应Ⅰ的平衡常数Kx=
 pC(g)+qD(g),Kx=
pC(g)+qD(g),Kx=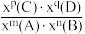 ,x为物质的量分数]。
,x为物质的量分数]。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】甲烷和水蒸气催化制氢主要有如下两个反应:
①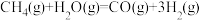 ΔH=+206kJ/mol
ΔH=+206kJ/mol
②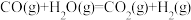 ΔH=-41kJ/mol
ΔH=-41kJ/mol
恒定压强为 时,将n(CH4)∶n(H2O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
时,将n(CH4)∶n(H2O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
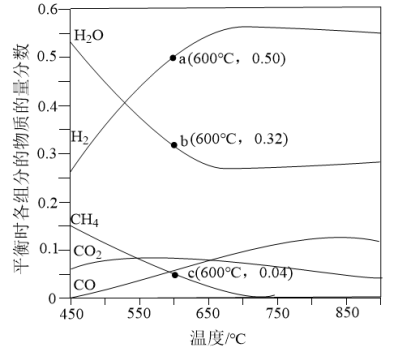
回答下列问题:
(1)写出 与
与 生成
生成 和
和 的热化学方程式:
的热化学方程式:_______ 。
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是_______ (填标号)。
A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快
D.加入合适的催化剂,降低反应温度也能实现平衡转化率不变
(3)系统中 的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
①低于700℃,_______ ;
②高于700℃,_______ 。
(4)已知投料比为n(CH4)∶n(H2O)=1∶3的混合气体,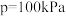 。600℃时,
。600℃时, 的平衡转化率为
的平衡转化率为_______ ,反应①的平衡常数的计算式为
_______ ( 是以分压表示的平衡常数,分压=总压×物质的量分数)。
是以分压表示的平衡常数,分压=总压×物质的量分数)。
①
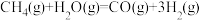 ΔH=+206kJ/mol
ΔH=+206kJ/mol②
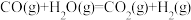 ΔH=-41kJ/mol
ΔH=-41kJ/mol恒定压强为
 时,将n(CH4)∶n(H2O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
时,将n(CH4)∶n(H2O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
回答下列问题:
(1)写出
 与
与 生成
生成 和
和 的热化学方程式:
的热化学方程式:(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是
A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快
D.加入合适的催化剂,降低反应温度也能实现平衡转化率不变
(3)系统中
 的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:①低于700℃,
②高于700℃,
(4)已知投料比为n(CH4)∶n(H2O)=1∶3的混合气体,
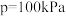 。600℃时,
。600℃时, 的平衡转化率为
的平衡转化率为
 是以分压表示的平衡常数,分压=总压×物质的量分数)。
是以分压表示的平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】利用 可消除CO污染或定量测定CO,反应为:
可消除CO污染或定量测定CO,反应为:
完成下列填空:
(1)该反应的平衡常数表达式
___________ 。在2L恒容密闭容器中反应25min后,固体质量减少了6.4g,则0~25min  的平均反应速率为
的平均反应速率为___________ 。
(2)取一定量的 和CO于某密闭容器中,分别在80
和CO于某密闭容器中,分别在80 和100
和100 下进行实验,测得
下进行实验,测得 如下:
如下:
上表中
___________ ,理由是___________ 。根据上表数据可以得出的结论是___________ 。
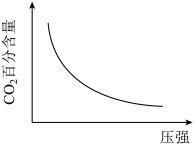
(3)如图所示,300 时
时 的百分含量随着压强的增大而减小,请解释其原因
的百分含量随着压强的增大而减小,请解释其原因___________ 。
(4) 可用高浓度NaOH溶液吸收。
可用高浓度NaOH溶液吸收。
①若4.48L (标准状况)和0.35mol NaOH溶液完全反应,生成的碳酸钠和碳酸氢钠的物质的量之比为
(标准状况)和0.35mol NaOH溶液完全反应,生成的碳酸钠和碳酸氢钠的物质的量之比为___________ 。
②继续通入二氧化碳至溶液中碳酸钠和碳酸氢钠(碳酸氢钠溶液呈碱性)的物质的量之比1∶1,则溶液中各离子浓度大小顺序为___________ 。
③若使碳酸氢钠溶液中 的比值变小,可加入的物质是
的比值变小,可加入的物质是___________ 。
a.通入HCl b.NaOH固体 c.通入 d.
d. 固体
固体
 可消除CO污染或定量测定CO,反应为:
可消除CO污染或定量测定CO,反应为:
完成下列填空:
(1)该反应的平衡常数表达式

 的平均反应速率为
的平均反应速率为(2)取一定量的
 和CO于某密闭容器中,分别在80
和CO于某密闭容器中,分别在80 和100
和100 下进行实验,测得
下进行实验,测得 如下:
如下:| 时间/min 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
80 | 0.50 | 0.37 | 0.26 | 0.18 | 0.12 | 0.12 |
100 | 0.50 | 0.35 | 0.24 | 0.17 | x | 0.15 |
上表中

(3)如图所示,300
 时
时 的百分含量随着压强的增大而减小,请解释其原因
的百分含量随着压强的增大而减小,请解释其原因
(4)
 可用高浓度NaOH溶液吸收。
可用高浓度NaOH溶液吸收。①若4.48L
 (标准状况)和0.35mol NaOH溶液完全反应,生成的碳酸钠和碳酸氢钠的物质的量之比为
(标准状况)和0.35mol NaOH溶液完全反应,生成的碳酸钠和碳酸氢钠的物质的量之比为②继续通入二氧化碳至溶液中碳酸钠和碳酸氢钠(碳酸氢钠溶液呈碱性)的物质的量之比1∶1,则溶液中各离子浓度大小顺序为
③若使碳酸氢钠溶液中
 的比值变小,可加入的物质是
的比值变小,可加入的物质是a.通入HCl b.NaOH固体 c.通入
 d.
d. 固体
固体
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】铁及其化合物在工农业生产中有重要的作用。
(1)已知:①C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol;
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
③4Fe(s)+3O2(g)=2Fe2O3(s) △H3=-1651.0kJ/mol
CO还原Fe2O3的热化学方程式为__________________________________________ 。
(2)高炉炼铁产生的高炉气中含有CO、H2、CO2等气体,用CO和H2在催化剂作用下合成甲醇,是减少污染、节约能源的新举措,反应原理:CO(g)+2H2(g) CH3OH(g) △H。在体积不同的两个恒容密闭容器中分别充入1molCO和2mol H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图。
CH3OH(g) △H。在体积不同的两个恒容密闭容器中分别充入1molCO和2mol H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图。
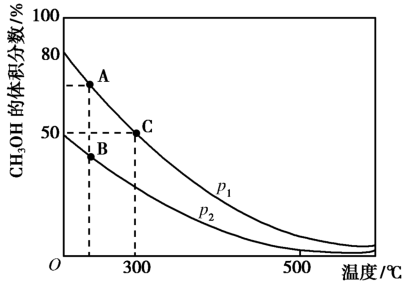
①在上图A、B、C三点中,选出对应下表物理量最小的点。
②在300℃时,向C点平衡体系中再充入0. 5molCO、1.0molH2和0.5mol的CH3OH,该反应向_________ 方向进行(填“正反应”、‘逆反应”或“不移动”)。
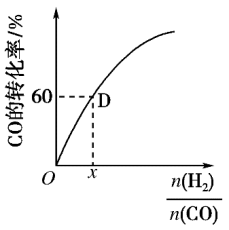
③一定温度下,CO的转化率与起始投料比[n(H2)/n(CO)]的变化关系图所示,测得D点氢气的转化率为40%,则x=_____________ 。
(3)三氯化铁是一种重要的化合物,可以用来腐蚀电路板。某腐蚀废液中含有0.5mol·L-1Fe3+和0.26mol·L-1的Cu2+,欲使Fe3+完全沉淀[c(Fe3+)≤4×l0-5]而Cu2+不沉淀,则需控制溶液pH的范围为_________ 。[KspCu(OH)2=2.6×l0-19;KspFe(OH)3=4×l0-38]
(4)莫尔盐,即六水合硫酸亚铁铵晶体,是一种重要的化工原料,在空气中缓慢风化及氧化,欲证明一瓶久置的莫尔盐已经部分氧化,需要进行实验操作是:取少量样品,加无氧水溶解,将溶液分成两份,______________________________________ ,则证明该样品已部分氧化。
(1)已知:①C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol;
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
③4Fe(s)+3O2(g)=2Fe2O3(s) △H3=-1651.0kJ/mol
CO还原Fe2O3的热化学方程式为
(2)高炉炼铁产生的高炉气中含有CO、H2、CO2等气体,用CO和H2在催化剂作用下合成甲醇,是减少污染、节约能源的新举措,反应原理:CO(g)+2H2(g)
 CH3OH(g) △H。在体积不同的两个恒容密闭容器中分别充入1molCO和2mol H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图。
CH3OH(g) △H。在体积不同的两个恒容密闭容器中分别充入1molCO和2mol H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图。
①在上图A、B、C三点中,选出对应下表物理量最小的点。
| 反应速率 | 平衡常数K | 平衡转化率α |
③一定温度下,CO的转化率与起始投料比[n(H2)/n(CO)]的变化关系图所示,测得D点氢气的转化率为40%,则x=

(3)三氯化铁是一种重要的化合物,可以用来腐蚀电路板。某腐蚀废液中含有0.5mol·L-1Fe3+和0.26mol·L-1的Cu2+,欲使Fe3+完全沉淀[c(Fe3+)≤4×l0-5]而Cu2+不沉淀,则需控制溶液pH的范围为
(4)莫尔盐,即六水合硫酸亚铁铵晶体,是一种重要的化工原料,在空气中缓慢风化及氧化,欲证明一瓶久置的莫尔盐已经部分氧化,需要进行实验操作是:取少量样品,加无氧水溶解,将溶液分成两份,
您最近一年使用:0次



