对于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.该反应的 |
B.该反应的平衡常数表达式为 |
| C.升高温度,该反应的正反应速率减小,逆反应速率增大 |
| D.将反应器容积压缩为原来的一半,气体颜色比压缩前深 |
更新时间:2022-05-24 17:52:24
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】偏二甲肼[(CH3)2N—NH2]与N2O4是常用的火箭推进剂,火箭发射时常出现红棕色气体,发生的化学反应如下:
① (CH3)2N—NH2(l) + 2N2O4(l) = 2CO2(g) + 3N2(g) + 4H2O(g) ∆H1<0
② N2O4(l) 2NO2(g) ∆H2 >0
2NO2(g) ∆H2 >0
下列说法不正确 的是
① (CH3)2N—NH2(l) + 2N2O4(l) = 2CO2(g) + 3N2(g) + 4H2O(g) ∆H1<0
② N2O4(l)
 2NO2(g) ∆H2 >0
2NO2(g) ∆H2 >0下列说法
| A.反应①中,N2O4为氧化剂 |
| B.反应①中,生成1mol CO2时,转移8 mol e- |
| C.由反应②推断:加压、降温是获得液态N2O4的条件 |
| D.温度升高,反应①的化学反应速率减小、反应②的化学反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】反应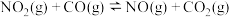 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
| A.图中X→Z为吸热过程 |
| B.理论上该反应不可以设计成原电池 |
| C.升高温度,正反应速率加快,逆反应速率减慢 |
| D.图中X→Y表示反应物断键时吸收能量的过程 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】{Ti12O18}团簇是比较罕见的一个穴醚无机类似物,我国科学家通过将{Rb@Ti12O18}和Cs+反应,测定笼内Cs+的浓度,计算Cs+取代Rb+反应的平衡常数(Keq),反应示意图和所测数据如下,有关说法不正确 的是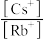 表示平衡时铯离子浓度和铷离子浓度之比,其它类似
表示平衡时铯离子浓度和铷离子浓度之比,其它类似

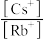 表示平衡时铯离子浓度和铷离子浓度之比,其它类似
表示平衡时铯离子浓度和铷离子浓度之比,其它类似| A.离子半径:r(Cs+)>r(Rb+) |
| B.已知冠醚18−冠−6能识别Rb+而不能识别Cs+,则往体系中加18−冠−6时,上述平衡会正向移动 |
| C.Keq≈0.1 |
| D.{Ti12O18}团簇对于Cs+具有比Rb+大的亲和力 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验不能 达到实验目的的是
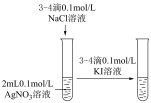 | 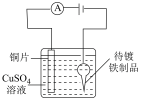 | 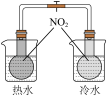 |  |
| A.验证AgCl溶解度大于AgI | B.电镀铜 | C.证明温度对平衡的影响 | D.验证Fe与水的反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验方案的设计能达到目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 探究增大压强,平衡逆向移动 | 其他条件不变,缩小H2(g)+I2(g) 2HI(g)的平衡体系的容器容积,气体颜色变深 2HI(g)的平衡体系的容器容积,气体颜色变深 |
| B | 取20.00mL盐酸 | 在50mL酸式滴定管中装入盐酸,调整初始读数为30.00mL后,将剩余盐酸放入锥形瓶 |
| C | 探究温度对化学平衡的影响 | 把装有颜色相同的NO2和N2O4混合气的两支试管(密封)分别浸入冷水和热水中 |
| D | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液直接加热蒸干 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氨气是一种重要的化工原料,以氨为原料可以生产化肥和硝酸,在催化剂条件下,氨催化氧化生成NO,进而继续被氧化为NO2,再与水反应生成硝酸,氨气与硝酸反应可得氮肥硝酸铵。4NH3(g) +5O2(g) 4NO(g)+6H2O(g) ΔH= -905.8kJ·mol-1。工业上将含NO2,废气通入氢氧化钠溶液中可获得NaNO3 和NaNO2,也可向废气中通入NH3在催化剂的条件转化为无毒无害的气体排放。对于反应来说下列说法正确的是
4NO(g)+6H2O(g) ΔH= -905.8kJ·mol-1。工业上将含NO2,废气通入氢氧化钠溶液中可获得NaNO3 和NaNO2,也可向废气中通入NH3在催化剂的条件转化为无毒无害的气体排放。对于反应来说下列说法正确的是
 4NO(g)+6H2O(g) ΔH= -905.8kJ·mol-1。工业上将含NO2,废气通入氢氧化钠溶液中可获得NaNO3 和NaNO2,也可向废气中通入NH3在催化剂的条件转化为无毒无害的气体排放。对于反应来说下列说法正确的是
4NO(g)+6H2O(g) ΔH= -905.8kJ·mol-1。工业上将含NO2,废气通入氢氧化钠溶液中可获得NaNO3 和NaNO2,也可向废气中通入NH3在催化剂的条件转化为无毒无害的气体排放。对于反应来说下列说法正确的是| A.该反应须在高温下才能自发进行 |
| B.升高温度、增大压强都有利于提高NH3的平衡转化率 |
| C.0.4mol NH3与0.5mol O2充分反应可释放90.58kJ的能量 |
| D.及时分离出混合体系中的水可以促使平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
【推荐1】N2是合成氨工业的重要原料,NH3不仅可制造化肥,还能通过催化氧化生产HNO3;HNO3能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N2与O2反应生成NO,NO进一步氧化生成NO2。2NO(g)+O2(g)=2NO2(g) ΔH=-116.4kJ·mol-1。大气中过量的NOx和水体中过量的NH 、NO
、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3-转化为N2。对于反应2NO(g)+O2(g)
均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3-转化为N2。对于反应2NO(g)+O2(g) 2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是
 、NO
、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3-转化为N2。对于反应2NO(g)+O2(g)
均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3-转化为N2。对于反应2NO(g)+O2(g) 2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是| A.该反应的ΔH<0,ΔS<0 |
B.反应的平衡常数可表示为K= |
| C.使用高效催化剂能降低反应的焓变 |
D.其他条件相同,增大 ,NO的转化率下降 ,NO的转化率下降 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】工业制备四氯化钛( ,熔点为
,熔点为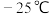 ,沸点为136.4℃)有以下两种方法:
,沸点为136.4℃)有以下两种方法:
①直接氯化法: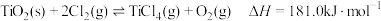
②加碳氯化法:
下列说法
| A.固态四氯化钛属于分子晶体 |
B.加碳氯化反应的化学平衡常数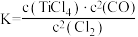 |
| C.增加加碳氯化法中原料C的投入量,既可加快反应速率,又能提高平衡产率 |
| D.与直接氯化法相比,加碳氯化法既利于反应正向进行,又为氯化提供了能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列关于化学平衡常数(K),电离平衡常数(Ka或Kb),水解平衡常数(Kh),沉淀溶解平衡常数(Ksp),水的离子积常数(Kw)的叙述中错误的是( )
| A.K、Ka或Kb、Kh、Ksp、Kw都与温度有关,温度越高,常数值越大 |
| B.比较Ksp与离子积Qc的相对大小,可判断难溶解电解质在给定条件下沉淀能否生成或溶解 |
| C.K值越大,正反应进行的程度越大,一般地说,K>105时,该反应进行得就基本完全了 |
| D.弱酸HA的Ka与NaA的Kh、水的离子积常数Kw三者间的关系可表示为:Kw=Ka·Kh |
您最近一年使用:0次

 与
与 的反应分两步完成,其能量曲线如下图所示。
的反应分两步完成,其能量曲线如下图所示。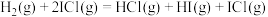




 ,图中的曲线是表示其他条件一定时,反应中NO的平衡转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)<v(逆)的是
,图中的曲线是表示其他条件一定时,反应中NO的平衡转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)<v(逆)的是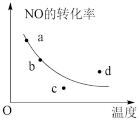
 和
和 混合气体,发生反应:
混合气体,发生反应: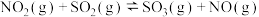 。起始浓度如下表所示,其中甲经5min达到平衡,平衡时
。起始浓度如下表所示,其中甲经5min达到平衡,平衡时
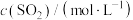
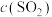 是甲中的2倍
是甲中的2倍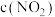 为
为 ,
, 为
为 ,则达到平衡时
,则达到平衡时 与乙的原平衡相同
与乙的原平衡相同

