VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)基态氧原子的价层电子排布图为___________ ,基态硒原子的核外电子排布式为___________ 。单质硒的熔点为221℃,其晶体类型是___________ 。
(2)H2O、H2S、H2Se的稳定性由强到弱的顺序是___________ ,H2O的沸点高于H2Se的沸点(-42℃),其原因是___________ 。
(3)H+可与H2O形成 ,
, 中H-O-H键角比H2O中H-O-H键角大,原因是
中H-O-H键角比H2O中H-O-H键角大,原因是___ 。
(4)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物II。

①下列说法正确的有___ (填字母序号)。
A.在1中C-C-C键角接近109°28' B.在II中O元素的电负性最大
C.在III中S原子均采取sp2杂化 D.在IV中硫氧键的键能均相等
②化合物III也是一种汞解毒剂,汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。比较水溶性的大小关系;化合物I___ 化合物III(填“<、>或=”)。
③化合物IV(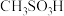 )是一种强酸,写出其电离方程式
)是一种强酸,写出其电离方程式___ 。
(1)基态氧原子的价层电子排布图为
(2)H2O、H2S、H2Se的稳定性由强到弱的顺序是
(3)H+可与H2O形成
 ,
, 中H-O-H键角比H2O中H-O-H键角大,原因是
中H-O-H键角比H2O中H-O-H键角大,原因是(4)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物II。

①下列说法正确的有
A.在1中C-C-C键角接近109°28' B.在II中O元素的电负性最大
C.在III中S原子均采取sp2杂化 D.在IV中硫氧键的键能均相等
②化合物III也是一种汞解毒剂,汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。比较水溶性的大小关系;化合物I
③化合物IV(
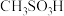 )是一种强酸,写出其电离方程式
)是一种强酸,写出其电离方程式
更新时间:2022-07-05 17:09:15
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】几种主族元素在周期表中的位置如图。
周期根据上表回答下列问题:
(1)⑤元素的氢化物的结构式______________ ,①和②形成化合物属于________________ 化合物(填“离子化合物”或“共价化合物”)
(2)⑥③⑦三种元素离子半径由大到小的顺序是_________ (用元素符号表示)
(3)⑤和⑥简单气态氢化物的沸点由高到低的顺序是:_______________________ (用化学式表示)
(4)这些元素中最高价氧化物对应水化物碱性最强的___________________________ (填电子式),这些元素中最高价氧化物对应水化物酸性最强的是______________ (填化学式)。
(5)②与水反应的离子方程式_________________ 。
②和③的最高价氧化物对应水化物相互反应的化学方程式_______________________ 。
(6)⑦的非金属性强于⑧,下 列表述中能证明这一事实的是_____________ (填字母)。
a.⑦的氢化物比⑧ 的氢化物稳定
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性强于⑧的氢化物酸性
族 周期 | I A | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ④ | ⑤ | ⑥ | |||||
3 | ② | ③ | ⑦ | |||||
4 |
| ⑧ |
(1)⑤元素的氢化物的结构式
(2)⑥③⑦三种元素离子半径由大到小的顺序是
(3)⑤和⑥简单气态氢化物的沸点由高到低的顺序是:
(4)这些元素中最高价氧化物对应水化物碱性最强的
(5)②与水反应的离子方程式
②和③的最高价氧化物对应水化物相互反应的化学方程式
(6)⑦的非金属性强于⑧,下 列表述中能证明这一事实的是
a.⑦的氢化物比⑧ 的氢化物稳定
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性强于⑧的氢化物酸性
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】下表为四种短周期元素的相关信息
回答下列问题(注:涉及元素的均要用对应元素的元素符号书写作答)
(1)Y元素的最简单氢化物的空间构型是___________ 。
(2)最高价的R与Z元素组成的化合物中R原子的杂化方式为___________ ,其中R在周期表中的位置是___________ ,R的基态原子电子排布式为___________ 。
(3)Z、Q、R相比,其原子半径由大到小的顺序是___________ 。
(4)与O3分子互为等电子体的一种分子为___________ ,阴离子为___________ 。
(5)Y与R相比,非金属性较强的是___________ ,能证明这一结论的事实是___________ 。(用化学方程式表示)
| 元素 | 元素的相关信息 |
| Y | 原子最外层电子数是次外层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| Q | 短周期中金属性最强 |
| R | 常温下,R的单质是淡黄色固体,常在火山喷口附近沉积 |
回答下列问题(注:涉及元素的均要用对应元素的元素符号书写作答)
(1)Y元素的最简单氢化物的空间构型是
(2)最高价的R与Z元素组成的化合物中R原子的杂化方式为
(3)Z、Q、R相比,其原子半径由大到小的顺序是
(4)与O3分子互为等电子体的一种分子为
(5)Y与R相比,非金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E为原子序数依次增大的五种短周期主族元素,其中仅含有一种金属元素,A单质是自然界中密度最小的气体,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成A2C和A2C2两种常见的液态化合物.请回答下列问题:
(1)D在周期表中的位置______ ,E的简单阴离子结构示意图_______ ,A2C2的结构式:
(2)C、D、E三种元素简单离子的离子半径由大到小的顺序是_____________________ 。
(3)请举一个事实说明C和E的非金属性强弱______________ .
(4)用含A元素最简单的有机化合物与炽热的氧化铜反应生成一种单质、液态氧化物和一种可以使澄清石灰水变浑浊的气体,其化学方程式为_____________________________ .
(1)D在周期表中的位置
(2)C、D、E三种元素简单离子的离子半径由大到小的顺序是
(3)请举一个事实说明C和E的非金属性强弱
(4)用含A元素最简单的有机化合物与炽热的氧化铜反应生成一种单质、液态氧化物和一种可以使澄清石灰水变浑浊的气体,其化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
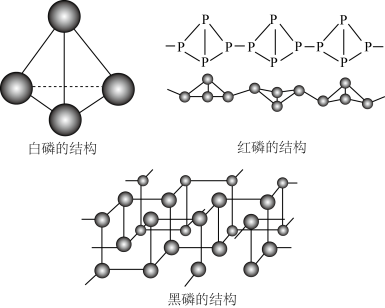
【推荐1】磷是维持人体骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。磷的几种单质结构如下图所示,回答下列相关问题。
(1)基态P原子的价电子排布图为_______ 。
(2)P的第一电离能大于S的第一电离能的原因是_______ 。
(3)NH3、PH3、AsH3的沸点由高到低的顺序为_______ (填化学式,下同),键角由大到小的顺序为_______ 。
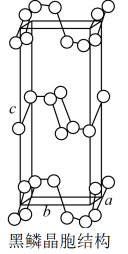
(4)三种磷的单质中P原子的杂化方式均为_______ 杂化,其中白磷的键角为_______ ,黑磷属于类似石墨的多层结构,其中层和层之间的作用力为_______ ,同层P原子之间的作用力为_______ 。
(5)黑磷晶胞结构如图所示,若已知黑磷晶胞参数为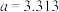 Å,
Å,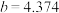 Å,
Å,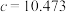 Å,且知道一个晶胞中含有8个P原子,晶胞密度为Ng/cm3,则阿伏加德罗常数可以表示为
Å,且知道一个晶胞中含有8个P原子,晶胞密度为Ng/cm3,则阿伏加德罗常数可以表示为_______ (已知:1Å=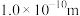 )(列出计算式即可)。
)(列出计算式即可)。

(1)基态P原子的价电子排布图为
(2)P的第一电离能大于S的第一电离能的原因是
(3)NH3、PH3、AsH3的沸点由高到低的顺序为
(4)三种磷的单质中P原子的杂化方式均为
(5)黑磷晶胞结构如图所示,若已知黑磷晶胞参数为
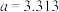 Å,
Å,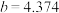 Å,
Å,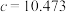 Å,且知道一个晶胞中含有8个P原子,晶胞密度为Ng/cm3,则阿伏加德罗常数可以表示为
Å,且知道一个晶胞中含有8个P原子,晶胞密度为Ng/cm3,则阿伏加德罗常数可以表示为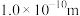 )(列出计算式即可)。
)(列出计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】某配位化合物为深蓝色晶体,由原子序数由小到大的A,B,C,D,E五种元素组成,其原子个数比为14∶4∶5∶1∶1。其中C,D同主族且原子序数D为C的2倍,E元素的外围电子排布式为(n-1)dn+6ns1,试回答下列问题:
(1)元素B,C,D的第一电离能由大到小排列顺序为________ (用元素符号表示)。
(2)D元素基态原子的最外层电子排布图为________ 。
(3)该配位化合物的化学式为________ ,配体的中心原子的杂化方式为________ 。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可以任意比互溶,解释其主要原因为_______________ 。
(5)A元素与B元素可形成分子式为B2A2的某化合物,该化合物的分子具有平面结构,则其结构式为________ ,分子中含有________ 个σ键,________ 个π键。
(1)元素B,C,D的第一电离能由大到小排列顺序为
(2)D元素基态原子的最外层电子排布图为
(3)该配位化合物的化学式为
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可以任意比互溶,解释其主要原因为
(5)A元素与B元素可形成分子式为B2A2的某化合物,该化合物的分子具有平面结构,则其结构式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为:
①ZnSO4+2FeSO4+3Na2C2O4+6H2O ZnFe2(C2O4)3·6H2O↓+3Na2SO4
ZnFe2(C2O4)3·6H2O↓+3Na2SO4
②ZnFe2(C2O4)3·6H2O ZnFe2O4+2CO2 ↑+4CO↑+6H2O
ZnFe2O4+2CO2 ↑+4CO↑+6H2O
回答下列问题:
(1)基态 Fe2+的价层电子排布图为___________ .
(2)电离能大小比较:I1(Zn)___________ I1(Cu),I2(Zn)___________ I2 (Cu) (填“>”“<”或“=”)。
(3)Na2SO4中阴离子的空间构型是___________ ,该离子中 S 的杂化类型是_____ 。
(4)CO和N2的分子结构相似,标准状况下,VLCO2和CO的混合气体中含键的物质的量为___________ 。与CO2互为等电子体的离子有____________ (写一种即可)。
(5)ZnCl2、ZnBr2、ZnI2 的熔点依次为283℃、394℃、446℃,其主要原因是___________ 。
(6)铁和碳组成的某种晶体的晶胞如图所示。面心上铁原子相连构成正八面体。
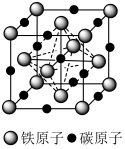
已知该晶体的密度为 dg·cm-3,NA是阿伏加 德罗常数的值。
①该晶体中Fe、C原子的最简比为___________ 。
②该晶胞中相邻两个面心上铁原子最近的核间距离 D=___________ nm(只列计算式)。
①ZnSO4+2FeSO4+3Na2C2O4+6H2O
 ZnFe2(C2O4)3·6H2O↓+3Na2SO4
ZnFe2(C2O4)3·6H2O↓+3Na2SO4②ZnFe2(C2O4)3·6H2O
 ZnFe2O4+2CO2 ↑+4CO↑+6H2O
ZnFe2O4+2CO2 ↑+4CO↑+6H2O回答下列问题:
(1)基态 Fe2+的价层电子排布图为
(2)电离能大小比较:I1(Zn)
(3)Na2SO4中阴离子的空间构型是
(4)CO和N2的分子结构相似,标准状况下,VLCO2和CO的混合气体中含键的物质的量为
(5)ZnCl2、ZnBr2、ZnI2 的熔点依次为283℃、394℃、446℃,其主要原因是
(6)铁和碳组成的某种晶体的晶胞如图所示。面心上铁原子相连构成正八面体。

已知该晶体的密度为 dg·cm-3,NA是阿伏加 德罗常数的值。
①该晶体中Fe、C原子的最简比为
②该晶胞中相邻两个面心上铁原子最近的核间距离 D=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】CuO、Cu2S等含铜化合物可以催化合成HCOOH.回答下列问题:
(1)基态铜原子的价电子排布式为___________ 。
(2)HCOOH中碳原子的轨道杂化类型为___________ ,元素电负性从大到小的顺序为___________ 。
(3)催化过程中可能产生 ,
, 的空间构型为
的空间构型为___________ ,碳氧键的平均键长 比CH3OH要
比CH3OH要___________ (填“长”或“短”)。
(4)在有机溶剂中,H2SO4的电离平衡常数Ka1(H2SO4)比H2CO3的电离平衡常数Ka1(H2CO3)大,除S的非金属性比C强外,在分子结构上还存在的原因是___________ 。
(5)已知Cu2S晶胞中S2-的位置如图所示,Cu+位于S2-所构成的正四面体中心。
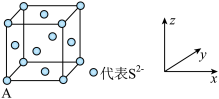
S2-配位数为______________________ ;已知图中A处(S2-)的原子分数坐标为(0,0,0),则晶胞中与A距离最近的为Cu+原子分数坐标为___________ ;若晶胞参数anm,晶体的密度为dg·cm-3),则阿伏加德罗常数的值为___________ (用含a和d的式子表示)。
(1)基态铜原子的价电子排布式为
(2)HCOOH中碳原子的轨道杂化类型为
(3)催化过程中可能产生
 ,
, 的空间构型为
的空间构型为 比CH3OH要
比CH3OH要(4)在有机溶剂中,H2SO4的电离平衡常数Ka1(H2SO4)比H2CO3的电离平衡常数Ka1(H2CO3)大,除S的非金属性比C强外,在分子结构上还存在的原因是
(5)已知Cu2S晶胞中S2-的位置如图所示,Cu+位于S2-所构成的正四面体中心。

S2-配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)基态硅原子最外层的电子排布图为___________ ,晶体硅和碳化硅熔点较高的是___________ (填化学式);
(2)硅和卤素单质反应可以得到SiX4,SiX4的熔沸点如下表:
①SiF4、SiCl4、SiBr4、SiI4沸点依次升高的原因___________ ,气态SiF4分子的空间构型是___________ ;
②SiCl4与N-甲基咪唑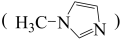 反应可以得到M2+,其结构如图所示:
反应可以得到M2+,其结构如图所示:

N-甲基咪唑分子中碳原子的杂化轨道类型为___________ ,H、C、N的电负性由大到小的顺序为___________ ,1个M2+中含有___________ 个σ键。
(3)下图是Mg、Ge、O三种元素形成的某化合物的晶胞示意图。
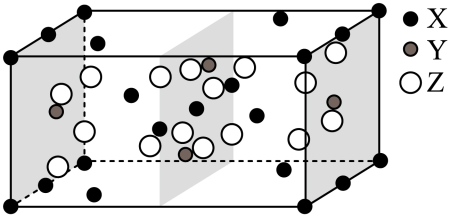
①已知化合物中Ge和O的原子个数比为1:4,图中Z表示___________ 原子(填元素符号),该化合物的化学式为___________ ;
②已知该晶胞的晶胞参数分别为anm、bnm、cnm,α=β=γ=90°,则该晶体的密度ρ=___________ 。
(1)基态硅原子最外层的电子排布图为
(2)硅和卤素单质反应可以得到SiX4,SiX4的熔沸点如下表:
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
②SiCl4与N-甲基咪唑
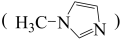 反应可以得到M2+,其结构如图所示:
反应可以得到M2+,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为
(3)下图是Mg、Ge、O三种元素形成的某化合物的晶胞示意图。

①已知化合物中Ge和O的原子个数比为1:4,图中Z表示
②已知该晶胞的晶胞参数分别为anm、bnm、cnm,α=β=γ=90°,则该晶体的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】过渡金属及其化合物在生产、生活中有重要的应用。回答下列问题:
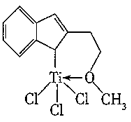
(1)一种含Ti的催化剂X能催化乙烯、丙烯等的聚合,其结构如图所示。X中C原子的杂化类型有________ ,含有的作用力类型有________ (填字母),非金属元素电负性由大到小的顺序为________ 。
A.π键 B.氢键 C.配位键 D.σ键 E.离子键
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_______ (填晶体类型)。Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_______ 。
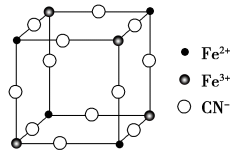
(3)有一种蓝色晶体可表示为MxFey(CN)6,经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上。其晶体中阴离子的最小结构单元如图所示,通过计算x和y的数值,可进一步确定该晶体的化学式为_______ ,该晶体属于_______ 晶体,M呈_______ 价。
(1)一种含Ti的催化剂X能催化乙烯、丙烯等的聚合,其结构如图所示。X中C原子的杂化类型有

A.π键 B.氢键 C.配位键 D.σ键 E.离子键
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于
(3)有一种蓝色晶体可表示为MxFey(CN)6,经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上。其晶体中阴离子的最小结构单元如图所示,通过计算x和y的数值,可进一步确定该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)已知H2O2的结构如图:
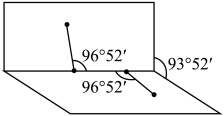
H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′。根据该结构写出H2O2分子的电子式______ 。估计它难溶于CS2,简要说明原因:________________ 。
(2)O、S、Se原子的第一电离能由大到小的顺序为____________________ 。
(3)H2Se的酸性比H2S_____ (填“强”或“弱”)。气态SeO3分子的立体构型为______ ,SeO32-离子中Se的杂化方式为______ 。
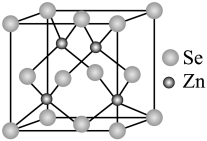
(4)硒化锌的晶胞结构如图所示,硒离子的配位数是____ ,若晶胞参数为d pm,则硒化锌的密度为______ g·cm-3。(不需要化简,1 m=109 nm=1012 pm)。
(1)已知H2O2的结构如图:

H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′。根据该结构写出H2O2分子的电子式
(2)O、S、Se原子的第一电离能由大到小的顺序为
(3)H2Se的酸性比H2S
(4)硒化锌的晶胞结构如图所示,硒离子的配位数是

您最近一年使用:0次
【推荐2】太阳能电池可分为:硅太阳能电池,化合物太阳能电池,如砷化镓 、铜铟镓硒
、铜铟镓硒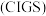 、硫化镉
、硫化镉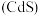 ,功能高分子太阳能电池等,
,功能高分子太阳能电池等, 常作电极。据此回答问题:
常作电极。据此回答问题:
(1)S原子的价电子排布式为_______ ;元素Ga、As和 的第一电离能由大到小的顺序是
的第一电离能由大到小的顺序是_______ 。
(2) 中As原子的杂化方式为
中As原子的杂化方式为_______ ; 的空间构型为
的空间构型为_______ 。
(3)GaAs熔点为 熔点约为
熔点约为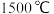 ,
, 熔点低于GaN的原因为
熔点低于GaN的原因为_______ 。
(4)写出一种与 互为等电子体的分子
互为等电子体的分子_______ 。
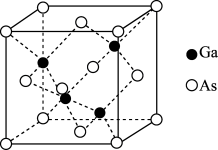
(5) 的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为
的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为_______ 。已知 的密度为
的密度为 ,Ga和As的摩尔质量分别为
,Ga和As的摩尔质量分别为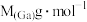 和
和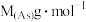 ,则
,则 晶胞中Ga之间的最短距离为
晶胞中Ga之间的最短距离为_______  。
。
 、铜铟镓硒
、铜铟镓硒 、硫化镉
、硫化镉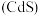 ,功能高分子太阳能电池等,
,功能高分子太阳能电池等, 常作电极。据此回答问题:
常作电极。据此回答问题:(1)S原子的价电子排布式为
 的第一电离能由大到小的顺序是
的第一电离能由大到小的顺序是(2)
 中As原子的杂化方式为
中As原子的杂化方式为 的空间构型为
的空间构型为(3)GaAs熔点为
 熔点约为
熔点约为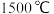 ,
, 熔点低于GaN的原因为
熔点低于GaN的原因为(4)写出一种与
 互为等电子体的分子
互为等电子体的分子(5)
 的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为
的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为 的密度为
的密度为 ,Ga和As的摩尔质量分别为
,Ga和As的摩尔质量分别为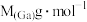 和
和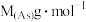 ,则
,则 晶胞中Ga之间的最短距离为
晶胞中Ga之间的最短距离为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】二氟草酸硼酸锂[LiBF2(C2O4)]是新型锂离子电池电解质,乙酸锰(CH3COO)3Mn]可用于制造离子电池的负极材料。合成方程式如下:
2H2C2O4+SiC14+2LiBF4==2LiBF2(C2O4)+SiF4+4HCl
4Mn(NO3)2·6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40 CH3COOH
(1)基态Mn原子的核外电子排布式为_________ 。
(2)草酸(HOOCCOOH)分子中碳原子轨道的杂化类型是___________ ,1mol草酸分子中含有 键的数目为
键的数目为_______________ 。
(3)与SiF4互为等电子体的两种阴离子的化学式为_________________ 。
(4)CH3COOH易溶于水,除了它是极性分子外,还因为___________________ 。
(5)向硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子的原因是_______________ 。

(6)硼氢化钠的晶胞结构如图所示,该晶胞中Na+的配位数为___________ ,若硼氢化钠晶体的密度为d g/cm3,NA表示阿伏伽德罗常数的值,则a=______ (用含d、NA的代数式表示);若硼氢化钠晶胞上、下底心处的Na+被Li+取代,则得到晶体的化学式为___________________ 。
2H2C2O4+SiC14+2LiBF4==2LiBF2(C2O4)+SiF4+4HCl
4Mn(NO3)2·6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40 CH3COOH
(1)基态Mn原子的核外电子排布式为
(2)草酸(HOOCCOOH)分子中碳原子轨道的杂化类型是
 键的数目为
键的数目为(3)与SiF4互为等电子体的两种阴离子的化学式为
(4)CH3COOH易溶于水,除了它是极性分子外,还因为
(5)向硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子的原因是

(6)硼氢化钠的晶胞结构如图所示,该晶胞中Na+的配位数为
您最近一年使用:0次



