盐溶液有的显中性,有的显酸性,有的显碱性。根据要求回答下列问题:
(1)将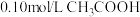 溶液与
溶液与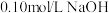 溶液等体积混合后,溶液中存在的离子浓度由大到小的顺序是
溶液等体积混合后,溶液中存在的离子浓度由大到小的顺序是_______ 。
(2)25℃时,将amol/L氨水与0.01mol/L盐酸等体积混合,反应平衡时溶液中c( )=c(Cl﹣),则溶液显
)=c(Cl﹣),则溶液显_______ (填“酸”“碱”或“中”)性。
(3)甲酸钠(HCOONa)溶液呈碱性的原因是_______ (用离子方程式表示)。0.02mol/L的HCOONa溶液中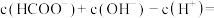
_______ mol/L。
(4)常温下,浓度均为0.1mol/L的7种溶液pH如表:
根据表中的数据分析,物质的量浓度均为0.1mol/L的Na2CO3、NaHSO3、NaHCO3、Na2SiO3,溶液中水的电离程度由小到大的顺序是:_______ (填化学式)。
(1)将
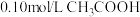 溶液与
溶液与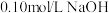 溶液等体积混合后,溶液中存在的离子浓度由大到小的顺序是
溶液等体积混合后,溶液中存在的离子浓度由大到小的顺序是(2)25℃时,将amol/L氨水与0.01mol/L盐酸等体积混合,反应平衡时溶液中c(
 )=c(Cl﹣),则溶液显
)=c(Cl﹣),则溶液显(3)甲酸钠(HCOONa)溶液呈碱性的原因是
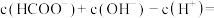
(4)常温下,浓度均为0.1mol/L的7种溶液pH如表:
| 溶质 | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaHSO4 | NaClO |
| pH | 12 | 9.7 | 12.3 | 10.0 | 6.0 | 1.0 | 10.3 |
更新时间:2022-12-02 18:32:10
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】请回答以下问题
(1)某温度时,测得pH=11的Ba(OH)2溶液浓度是0.005mol·L-1。
①该温度下水的离子积常数Kw=________ 。
②在此温度下,将pH=12的Ba(OH)2溶液Va L与pH=2的硫酸Vb L混合。若所得混合液为中性,则Va∶Vb=________ 。
(2)25 ℃时,部分物质的电离平衡常数如下表所示。请回答下列问题:
①下列说法正确的是__________
A.25 ℃时,向CH3COOH溶液中加入适量的NaOH溶液,CH3COOH的电离程度增大,电离平衡常数不变
B.0.1mol•L-1 CH3COOH溶液加水稀释,稀释后的溶液中水的电离程度减小
C.0.1mol•L-1 HClO溶液和0.1mol•L-1 NaClO溶液等体积混合呈溶液碱性
D.碳酸氢钠溶液中阴阳离子数目相等
② 同浓度的CH3COO-、HCO 、CO32-、ClO-结合H+的能力由强到弱的顺序为
、CO32-、ClO-结合H+的能力由强到弱的顺序为___
③ 25 ℃时,某CH3COOH和CH3COOK混合溶液呈中性,则该混合溶液中: =
=________
(3)煤燃烧排放的烟气含有SO2和NO,采用碱性的NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10−3mol·L−1。反应10min后溶液中离子浓度的分析结果如下表。
①写出NaClO2溶液脱硝过程中主要反应 的离子方程式______ 。
②如果采用Ca(ClO)2替代NaClO2,其脱硫效果会更好。试从化学平衡原理分析,Ca(ClO)2相比NaClO2具有的优点是________ 。
(1)某温度时,测得pH=11的Ba(OH)2溶液浓度是0.005mol·L-1。
①该温度下水的离子积常数Kw=
②在此温度下,将pH=12的Ba(OH)2溶液Va L与pH=2的硫酸Vb L混合。若所得混合液为中性,则Va∶Vb=
(2)25 ℃时,部分物质的电离平衡常数如下表所示。请回答下列问题:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10—5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
①下列说法正确的是
A.25 ℃时,向CH3COOH溶液中加入适量的NaOH溶液,CH3COOH的电离程度增大,电离平衡常数不变
B.0.1mol•L-1 CH3COOH溶液加水稀释,稀释后的溶液中水的电离程度减小
C.0.1mol•L-1 HClO溶液和0.1mol•L-1 NaClO溶液等体积混合呈溶液碱性
D.碳酸氢钠溶液中阴阳离子数目相等
② 同浓度的CH3COO-、HCO
 、CO32-、ClO-结合H+的能力由强到弱的顺序为
、CO32-、ClO-结合H+的能力由强到弱的顺序为③ 25 ℃时,某CH3COOH和CH3COOK混合溶液呈中性,则该混合溶液中:
 =
=(3)煤燃烧排放的烟气含有SO2和NO,采用碱性的NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10−3mol·L−1。反应10min后溶液中离子浓度的分析结果如下表。
| 离子 | SO42− | SO32− | NO3− | NO2− | Cl− |
| c/(mol·L−1) | 8.35×10−4 | 6.87×10−6 | 1.5×10−4 | 1.2×10−5 | 3.4×10−3 |
①写出NaClO2溶液脱硝过程中
②如果采用Ca(ClO)2替代NaClO2,其脱硫效果会更好。试从化学平衡原理分析,Ca(ClO)2相比NaClO2具有的优点是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】常温下,某同学向锥形瓶中加入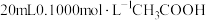 溶液,滴入几滴酚酞后,用碱式滴定管向其中滴加
溶液,滴入几滴酚酞后,用碱式滴定管向其中滴加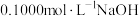 溶液,滴加
溶液,滴加 溶液过程中溶液的pH变化如图所示(忽略混合后溶液体积的变化):
溶液过程中溶液的pH变化如图所示(忽略混合后溶液体积的变化):

请问答下列问题:
(1)若A点的 ,该点溶液中由水电离出的
,该点溶液中由水电离出的
___________ ,滴加甲基橙溶液显___________ 色。
(2)从B点可以看出: 的电离程度
的电离程度___________ (填“大于”“小于”成“等于”) 的水解程度,该点溶液中离子浓度由大到小的顺序是
的水解程度,该点溶液中离子浓度由大到小的顺序是___________ 。
(3)若C点对应 溶液的体积为
溶液的体积为 ,则醋酸的电离平衡常数
,则醋酸的电离平衡常数
___________ (用含x的代数式表示)。
(4)达到滴定终点的现象为滴入最后一滴氢氧化钠溶液时,溶液呈红色,且半分钟内不褪出。苦D点的pH为10,则该点溶液中由水电离出的
___________ ;下列操作中两溶液恰好完全反应时,测得消耗的 溶液的体积可能超过
溶液的体积可能超过 的是
的是___________ (填字母)。
a.碱式滴定管用蒸馏水洗涤后未用 溶液润洗就直接注入
溶液润洗就直接注入 溶液
溶液
b.滴定前盛放醋酸溶液的锥形瓶用蒸馏水洗净后没有干燥
c.用滴定管量取醋酸溶液时,开始俯视读数,放完后仰视读数
d.碱式滴定管在滴定前有气泡,滴定后气泡消失
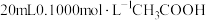 溶液,滴入几滴酚酞后,用碱式滴定管向其中滴加
溶液,滴入几滴酚酞后,用碱式滴定管向其中滴加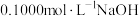 溶液,滴加
溶液,滴加 溶液过程中溶液的pH变化如图所示(忽略混合后溶液体积的变化):
溶液过程中溶液的pH变化如图所示(忽略混合后溶液体积的变化):
请问答下列问题:
(1)若A点的
 ,该点溶液中由水电离出的
,该点溶液中由水电离出的
(2)从B点可以看出:
 的电离程度
的电离程度 的水解程度,该点溶液中离子浓度由大到小的顺序是
的水解程度,该点溶液中离子浓度由大到小的顺序是(3)若C点对应
 溶液的体积为
溶液的体积为 ,则醋酸的电离平衡常数
,则醋酸的电离平衡常数
(4)达到滴定终点的现象为滴入最后一滴氢氧化钠溶液时,溶液呈红色,且半分钟内不褪出。苦D点的pH为10,则该点溶液中由水电离出的

 溶液的体积可能超过
溶液的体积可能超过 的是
的是a.碱式滴定管用蒸馏水洗涤后未用
 溶液润洗就直接注入
溶液润洗就直接注入 溶液
溶液b.滴定前盛放醋酸溶液的锥形瓶用蒸馏水洗净后没有干燥
c.用滴定管量取醋酸溶液时,开始俯视读数,放完后仰视读数
d.碱式滴定管在滴定前有气泡,滴定后气泡消失
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某学生用0.10 mol·L-1标准NaOH溶液滴定某浓度的盐酸。记录数据如下:
(1)盐酸的物质的量浓度为_____ 。
(2)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是_____ (填“偏高”或“偏低”或“无影响”)。
(3)下列有关实验的说法正确的是______ 。
A.在测定中和反应的反应热实验中,至少要读两次温度
B.可用pH试纸测定新制氯水中的pH
C.中和滴定实验中,洗净后的锥形瓶不需要干燥
D.向CH3COONa溶液中滴入石蕊试液,溶液变蓝
E.向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS)
(4)常温下,pH=5的盐酸和pH=9的氢氧化钠溶液以体积比9∶11混合,则混合液的pH=_________ 。
| 实验序号 | 待测液体积(mL) | 所消耗NaOH标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.54 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.36 |
(2)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是
(3)下列有关实验的说法正确的是
A.在测定中和反应的反应热实验中,至少要读两次温度
B.可用pH试纸测定新制氯水中的pH
C.中和滴定实验中,洗净后的锥形瓶不需要干燥
D.向CH3COONa溶液中滴入石蕊试液,溶液变蓝
E.向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS)
(4)常温下,pH=5的盐酸和pH=9的氢氧化钠溶液以体积比9∶11混合,则混合液的pH=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】浅绿色的硫酸亚铁铵晶体[又名莫尔盐,(NH4)2SO4·FeSO4·6H2O]比绿矾(FeSO4·7H2O)更稳定,常用于定量分析。莫尔盐的一种实验室制法如下:
废铁屑
 溶液A
溶液A

 莫尔盐
莫尔盐
(1)向废铁屑中加入稀硫酸后,不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是__ 。
(2)浓度均为0.10 mol·L-1的莫尔盐溶液和FeSO4溶液,c(Fe2+)前者_______ 后者。(填“大于”、“小于”、“等于”或“无法判断”)
(3)0.10 mol·L-1莫尔盐溶液中离子浓度由大到小的顺序为_______ 。
(4)常温下,(NH4)2SO4溶液呈酸性的原因_______ (用离子方程式表示)。
(5)用标准浓度的莫尔盐溶液定量分析某样品中KMnO4的含量。
①称量1.5800 g KMnO4样品于烧杯中,溶解后加稀H2SO4酸化,配成250 mL溶液。
②取0.1000 mol·L-1的莫尔盐标准溶液25.00mL于锥形瓶中,然后用KMnO4样品溶液滴定。滴定终点的现象是_______ 。平行滴定3次,样品溶液的平均用量为17.50 mL,则样品纯度为_______ 。(保留三位有效数字)
废铁屑
 溶液A
溶液A

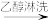 莫尔盐
莫尔盐(1)向废铁屑中加入稀硫酸后,不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是
(2)浓度均为0.10 mol·L-1的莫尔盐溶液和FeSO4溶液,c(Fe2+)前者
(3)0.10 mol·L-1莫尔盐溶液中离子浓度由大到小的顺序为
(4)常温下,(NH4)2SO4溶液呈酸性的原因
(5)用标准浓度的莫尔盐溶液定量分析某样品中KMnO4的含量。
①称量1.5800 g KMnO4样品于烧杯中,溶解后加稀H2SO4酸化,配成250 mL溶液。
②取0.1000 mol·L-1的莫尔盐标准溶液25.00mL于锥形瓶中,然后用KMnO4样品溶液滴定。滴定终点的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】请回答:
(1)室温下,使用pH计测定0.1mol/LNH4Cl溶液的pH=5.12(如图1)由此可以得到的结论是___ (填字母)。

a.NH3·H2O是弱碱
b.溶液中c(H+)>c(OH-)
c.NH4+水解是吸热反应
d.由H2O电离出的c(H+)<10-7mol/L
e.物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7
(2)室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的盐酸和醋酸,滴定曲线如图2所示。
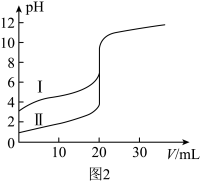
①表示滴定盐酸的曲线是____ (填序号)。若此实验选用酚酞为指示剂,则滴定到达终点的现象是____ 。若用标准NaOH溶液测定未知盐酸溶液的浓度,下列实验操作会使实验结果偏低的是____ 。
a.锥形瓶用待测液润洗后再注入待测液
b.碱式滴定管滴定前有气泡,滴定后无气泡
c.碱式滴定管滴定前仰视读数,滴定后平视读数
②在滴定醋酸溶液的过程中:
V(NaOH)=10.00mL时,溶液中离子浓度由大到小的顺序为____ 。当c(Na+)=c(CH3COO-)+c(CH3COOH)时,溶液pH____ 7(填“>”、“=”或“<”)。
(1)室温下,使用pH计测定0.1mol/LNH4Cl溶液的pH=5.12(如图1)由此可以得到的结论是

a.NH3·H2O是弱碱
b.溶液中c(H+)>c(OH-)
c.NH4+水解是吸热反应
d.由H2O电离出的c(H+)<10-7mol/L
e.物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7
(2)室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的盐酸和醋酸,滴定曲线如图2所示。

①表示滴定盐酸的曲线是
a.锥形瓶用待测液润洗后再注入待测液
b.碱式滴定管滴定前有气泡,滴定后无气泡
c.碱式滴定管滴定前仰视读数,滴定后平视读数
②在滴定醋酸溶液的过程中:
V(NaOH)=10.00mL时,溶液中离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学小组研究草酸(H2C2O4)及其盐的性质。
(1)已知: ,
, ,在等物质的量浓度、等体积的
,在等物质的量浓度、等体积的 溶液与KOH溶液混合后所得的酸性溶液中,下列关系正确的是
溶液与KOH溶液混合后所得的酸性溶液中,下列关系正确的是_______ (填字母)。
a.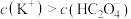
b.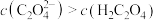
c.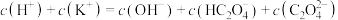
d.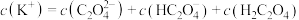
(2) 中碳元素的化合价是+3价,推测其有还原性。文献表明:相同条件下,
中碳元素的化合价是+3价,推测其有还原性。文献表明:相同条件下, 的还原性强于
的还原性强于 。为验证此结论,小组同学完成了如下实验:
。为验证此结论,小组同学完成了如下实验:
向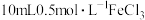 溶液中缓慢加入
溶液中缓慢加入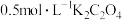 溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。
溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。
资料:三水三草酸合铁酸钾[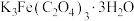 ]为翠绿色晶体
]为翠绿色晶体
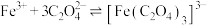
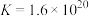
①取少量晶体洗净,配成溶液,滴加KSCN溶液,不变红,继续加入硫酸,溶液变红。用平衡移动原理解释溶液变红的原因是_______ 。
②经检验反应后的溶液中无 ,从反应原理的角度解释
,从反应原理的角度解释 和
和 未发生氧化还原反应的可能原因是
未发生氧化还原反应的可能原因是_______ 。
③某同学利用如图所示装置比较 和
和 的还原性强弱。
的还原性强弱。
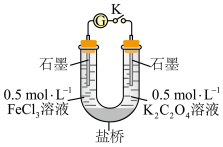
i.闭合K,电流计指针偏转,一段时间后,取左侧溶液,_______ (填操作和现象),证实 的还原性强于
的还原性强于 。
。
ii.该装置的优点是_______ 。
(3)可利用草酸盐测定某高锰酸钾产品的纯度,步骤如下:
已知: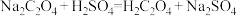
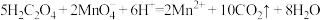
(摩尔质量: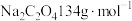 、
、
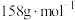 )
)
ⅰ.称取ag产品,配成50mL溶液。
ⅱ.称取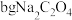 ,置于锥形瓶中,加蒸馏水使其溶解,再加入过量的硫酸。
,置于锥形瓶中,加蒸馏水使其溶解,再加入过量的硫酸。
ⅲ.将锥形瓶中溶液加热到75℃~80℃,恒温,用i中所配溶液滴定至终点,消耗溶液VmL(杂质不参与反应)。
产品中 的质量分数的表达式为
的质量分数的表达式为_______ 。
(1)已知:
 ,
, ,在等物质的量浓度、等体积的
,在等物质的量浓度、等体积的 溶液与KOH溶液混合后所得的酸性溶液中,下列关系正确的是
溶液与KOH溶液混合后所得的酸性溶液中,下列关系正确的是a.
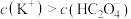
b.
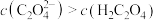
c.
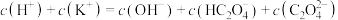
d.
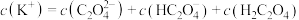
(2)
 中碳元素的化合价是+3价,推测其有还原性。文献表明:相同条件下,
中碳元素的化合价是+3价,推测其有还原性。文献表明:相同条件下, 的还原性强于
的还原性强于 。为验证此结论,小组同学完成了如下实验:
。为验证此结论,小组同学完成了如下实验:向
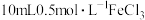 溶液中缓慢加入
溶液中缓慢加入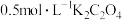 溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。
溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。资料:三水三草酸合铁酸钾[
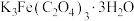 ]为翠绿色晶体
]为翠绿色晶体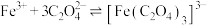
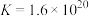
①取少量晶体洗净,配成溶液,滴加KSCN溶液,不变红,继续加入硫酸,溶液变红。用平衡移动原理解释溶液变红的原因是
②经检验反应后的溶液中无
 ,从反应原理的角度解释
,从反应原理的角度解释 和
和 未发生氧化还原反应的可能原因是
未发生氧化还原反应的可能原因是③某同学利用如图所示装置比较
 和
和 的还原性强弱。
的还原性强弱。
i.闭合K,电流计指针偏转,一段时间后,取左侧溶液,
 的还原性强于
的还原性强于 。
。ii.该装置的优点是
(3)可利用草酸盐测定某高锰酸钾产品的纯度,步骤如下:
已知:
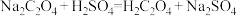
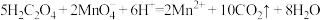
(摩尔质量:
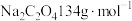 、
、
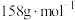 )
)ⅰ.称取ag产品,配成50mL溶液。
ⅱ.称取
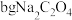 ,置于锥形瓶中,加蒸馏水使其溶解,再加入过量的硫酸。
,置于锥形瓶中,加蒸馏水使其溶解,再加入过量的硫酸。ⅲ.将锥形瓶中溶液加热到75℃~80℃,恒温,用i中所配溶液滴定至终点,消耗溶液VmL(杂质不参与反应)。
产品中
 的质量分数的表达式为
的质量分数的表达式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硫化钠是重要的化工原料,大多采用无水芒硝(Na2SO4)—炭粉还原法制备,原理为Na2SO4+2C Na2S+2CO2↑。其主要流程如下:
Na2S+2CO2↑。其主要流程如下:
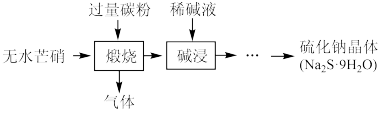
(1) Na2S溶液显碱性,写出相关反应的方程式(主要)______ ,上述流程中采用稀碱液比用热水更好,理由是___________ 。
(2)常温下,等体积、等物质的量浓度的NaHS溶液与Na2S溶液混合,混合溶液中c(S2-)_____ c(HS-) (填“大于”、“小于”或“等于”)。若混合溶液的pH=10,则c(HS-)+3c(H2S)-c(S2-)= ___________________
(3)已知:I2+2S2O32-=2I-+S4O62-。上述所制得的Na2S·9H2O晶体中含有Na2S2O3·5H2O等杂质。为测定产品的成分,进行下列实验,步骤如下:
a. 取试样10.00 g配成500.00 mL溶液。
b. 取所配溶液25.00 mL于碘量瓶中,加入过量ZnCO3悬浊液除去Na2S后,过滤,向滤液中滴入2~3滴淀粉溶液,用0.050 00 mol·L-1I2溶液滴定至终点,用去5.00mL I2溶液。
c. 再取所配溶液25.00 mL于碘量瓶中,加入50.00 mL 0.050 00 mol·L-1的I2溶液,并滴入2~3滴淀粉溶液,振荡。用标准Na2S2O3溶液滴定多余的I2,用去15.00 mL 0.100 0 mol·L-1 Na2S2O3溶液。
①步骤b中用ZnCO3除去Na2S的离子方程式为________ 。
②判断步骤c中滴定终点的方法为______________ 。
③计算试样中Na2S·9H2O和Na2S2O3·5H2O的质量分数_________ (写出计算过程)。
 Na2S+2CO2↑。其主要流程如下:
Na2S+2CO2↑。其主要流程如下:
(1) Na2S溶液显碱性,写出相关反应的方程式(主要)
(2)常温下,等体积、等物质的量浓度的NaHS溶液与Na2S溶液混合,混合溶液中c(S2-)
(3)已知:I2+2S2O32-=2I-+S4O62-。上述所制得的Na2S·9H2O晶体中含有Na2S2O3·5H2O等杂质。为测定产品的成分,进行下列实验,步骤如下:
a. 取试样10.00 g配成500.00 mL溶液。
b. 取所配溶液25.00 mL于碘量瓶中,加入过量ZnCO3悬浊液除去Na2S后,过滤,向滤液中滴入2~3滴淀粉溶液,用0.050 00 mol·L-1I2溶液滴定至终点,用去5.00mL I2溶液。
c. 再取所配溶液25.00 mL于碘量瓶中,加入50.00 mL 0.050 00 mol·L-1的I2溶液,并滴入2~3滴淀粉溶液,振荡。用标准Na2S2O3溶液滴定多余的I2,用去15.00 mL 0.100 0 mol·L-1 Na2S2O3溶液。
①步骤b中用ZnCO3除去Na2S的离子方程式为
②判断步骤c中滴定终点的方法为
③计算试样中Na2S·9H2O和Na2S2O3·5H2O的质量分数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】化学反应原理对于研究化学物质有十分重要的意义。
(1)已知次磷酸(H3PO2,一元中强酸)和亚磷酸(H3PO3,结构式为 ,二元中强酸)均是重要的精细化工产品。
,二元中强酸)均是重要的精细化工产品。
①写出次磷酸的结构式:_____________________________________ 。
②已知某温度下0.01 mol·L-1的NaOH溶液pH=10,将该NaOH溶液与等浓度等体积的次磷酸溶液混合,混合后溶液pH=7,则此时c(OH-)—c(H3PO2)=___________ 。(用具体数值表示)
(2)实验室配制FeCl3溶液时,需要将FeCl3固体溶解在较浓的盐酸中,其原因是_______________________________________________________ (用离子方程式和必要的文字说明)。
已知25℃时,Fe(OH)3的Ksp=4.0×10-38,配制100ml 5 mol·L-1的FeCl3溶液,至少需要加入_______ mL 2 mol·L-1的盐酸(忽略加入盐酸的体积)。
(3)工业废水中的Cr2O72-对生态系统有很大损害。常用的处理方法有两种。
①还原沉淀法:Cr2O72- Cr3+
Cr3+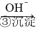 Cr(OH)3。常温下,要使Cr3+沉淀完全,溶液的pH应调至
Cr(OH)3。常温下,要使Cr3+沉淀完全,溶液的pH应调至________ 。(已知Cr(OH)3的Ksp=10-32)
②电解法:用铁和石墨做电极,电解产生的还原剂将Cr2O72-还原成Cr3+,最终产生Cr(OH)3沉淀。若有1mol Cr2O72-被还原,理论上导线中通过___________ mol电子。
(1)已知次磷酸(H3PO2,一元中强酸)和亚磷酸(H3PO3,结构式为
 ,二元中强酸)均是重要的精细化工产品。
,二元中强酸)均是重要的精细化工产品。①写出次磷酸的结构式:
②已知某温度下0.01 mol·L-1的NaOH溶液pH=10,将该NaOH溶液与等浓度等体积的次磷酸溶液混合,混合后溶液pH=7,则此时c(OH-)—c(H3PO2)=
(2)实验室配制FeCl3溶液时,需要将FeCl3固体溶解在较浓的盐酸中,其原因是
已知25℃时,Fe(OH)3的Ksp=4.0×10-38,配制100ml 5 mol·L-1的FeCl3溶液,至少需要加入
(3)工业废水中的Cr2O72-对生态系统有很大损害。常用的处理方法有两种。
①还原沉淀法:Cr2O72-
 Cr3+
Cr3+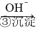 Cr(OH)3。常温下,要使Cr3+沉淀完全,溶液的pH应调至
Cr(OH)3。常温下,要使Cr3+沉淀完全,溶液的pH应调至②电解法:用铁和石墨做电极,电解产生的还原剂将Cr2O72-还原成Cr3+,最终产生Cr(OH)3沉淀。若有1mol Cr2O72-被还原,理论上导线中通过
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】Ⅰ.(1)已知t℃时, ,将
,将 的NaOH溶液aL与
的NaOH溶液aL与 的
的 溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的
溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的 ,则
,则
___________ 。
(2)已知 ,向
,向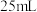

 溶液中加入相同体积的
溶液中加入相同体积的 盐酸,充分反应后,溶液中
盐酸,充分反应后,溶液中
___________ mol/L(忽略混合后溶液体积变化)。
(3)常温下,用 NaOH溶液分别滴定
NaOH溶液分别滴定 HCl溶液和
HCl溶液和
 溶液,滴定曲线如图所示:
溶液,滴定曲线如图所示:

①滴定HCl溶液的曲线是___________ (填“图甲”或“图乙”)。
② 的点是
的点是___________ 。
③E点对应离子浓度由大到小的顺序为___________ 。
Ⅱ.我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图所示:

(4)金属锂在电极___________ (填“A”或“B”)上生成。
(5)阳极能产生两种气体单质,电极反应是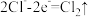 和
和___________ 。
(6)某种锂离子二次电池的总反应为 ,装置如图所示(a极材料为金属锂和石墨的复合材料),下列说法错误的有
,装置如图所示(a极材料为金属锂和石墨的复合材料),下列说法错误的有___________ 。

A.图中 及
及 移动方向说明该电池处于放电状态
移动方向说明该电池处于放电状态
B.该电池可选择含 的水溶液作离子导体
的水溶液作离子导体
C.充电时,a极连接外接电源的正极
D.充电时,b极电板反应为
 ,将
,将 的NaOH溶液aL与
的NaOH溶液aL与 的
的 溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的
溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的 ,则
,则
(2)已知
 ,向
,向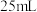

 溶液中加入相同体积的
溶液中加入相同体积的 盐酸,充分反应后,溶液中
盐酸,充分反应后,溶液中
(3)常温下,用
 NaOH溶液分别滴定
NaOH溶液分别滴定 HCl溶液和
HCl溶液和
 溶液,滴定曲线如图所示:
溶液,滴定曲线如图所示:
①滴定HCl溶液的曲线是
②
 的点是
的点是③E点对应离子浓度由大到小的顺序为
Ⅱ.我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图所示:

(4)金属锂在电极
(5)阳极能产生两种气体单质,电极反应是
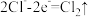 和
和(6)某种锂离子二次电池的总反应为
 ,装置如图所示(a极材料为金属锂和石墨的复合材料),下列说法错误的有
,装置如图所示(a极材料为金属锂和石墨的复合材料),下列说法错误的有
A.图中
 及
及 移动方向说明该电池处于放电状态
移动方向说明该电池处于放电状态B.该电池可选择含
 的水溶液作离子导体
的水溶液作离子导体C.充电时,a极连接外接电源的正极
D.充电时,b极电板反应为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品。
(1)写出氯碱工业中电解饱和食盐水的离子方程式____ 。
(2)①室温下,0.1mol·L-1NaClO溶液的pH____ 0.1mol·L-1Na2SO3溶液的pH。(填“大于”、“小于”或“等于”)。已知:H2SO3的Ka1=1.54×10-2,Ka2=1.02×10-7;HClO的Ka=2.95×10-8
②设计实验证明NaHSO3溶液中HSO 的电离程度大于水解程度
的电离程度大于水解程度____ 。
(3)氯气含量检测仪中,原电池工作原理示意图如图所示。则Cl2在Pt电极放电的电极反应式为____ 。

(4)工业上用NaClO3氧化酸性FeCl2废液,通过控制条件,使Fe3+水解产物聚合,形成可溶的多聚体,最终析出红棕色胶状沉淀Fe2O3•nH2O。其中水解形成羟桥配离子的离子方程式为:2Fe3++10H2O [Fe(H2O)4(OH)2Fe(H2O)4]4++2H+△H>0。
[Fe(H2O)4(OH)2Fe(H2O)4]4++2H+△H>0。
欲使上述水解平衡正向移动,可采用的方法有____ (填字母)。
(1)写出氯碱工业中电解饱和食盐水的离子方程式
(2)①室温下,0.1mol·L-1NaClO溶液的pH
②设计实验证明NaHSO3溶液中HSO
 的电离程度大于水解程度
的电离程度大于水解程度(3)氯气含量检测仪中,原电池工作原理示意图如图所示。则Cl2在Pt电极放电的电极反应式为

(4)工业上用NaClO3氧化酸性FeCl2废液,通过控制条件,使Fe3+水解产物聚合,形成可溶的多聚体,最终析出红棕色胶状沉淀Fe2O3•nH2O。其中水解形成羟桥配离子的离子方程式为:2Fe3++10H2O
 [Fe(H2O)4(OH)2Fe(H2O)4]4++2H+△H>0。
[Fe(H2O)4(OH)2Fe(H2O)4]4++2H+△H>0。欲使上述水解平衡正向移动,可采用的方法有
| A.加水稀释 | B.加热 | C.加入盐酸 | D.加入NaHCO3 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为_________ (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的pH _________ (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度_________ (填“增大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为_________ ,平衡常数表达式为 _________ ;若有1mol硝酸铵完全分解,转移的电子数为_________ mol。
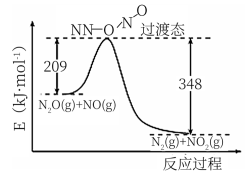
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2, 其△H=_________ kJ·mol-1。
(1)氨的水溶液显弱碱性,其原因为
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2, 其△H=

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】CO2是一种重要的化工原料,依据题给信息,回答下列问题:
Ⅰ.碳酸钠可利用CO2采用氨碱法生产
(1)碳酸钠可作为碱使用的原因是_____________ (用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ΔH1=−127.4 kJ/mol
②NaOH(s)+CO2(g)=NaHCO3(s) ΔH2=−131.5kJ/mol
反应2NaHCO3(s)=Na2CO3(s)+ H2O(g) +CO2(g)的ΔH=___________ kJ/mol。
Ⅱ.在体积为2 L的密闭容器中,充入1mol/LCO2和1mol/L H2,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应为____________ 反应(选填吸热、放热)。
(2)能判断该反应是否达到化学平衡状态的依据是_______________ 。
a.容器中压强不变 b.混合气体中 c(CO)不变
c. υ正(H2)=υ逆(H2O) d. c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____________ ℃。
(4)某温度下经2min反应达到平衡后c(CO)=0.8mol/L,此温度下的平衡常数为________ 。
Ⅰ.碳酸钠可利用CO2采用氨碱法生产
(1)碳酸钠可作为碱使用的原因是
(2)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ΔH1=−127.4 kJ/mol
②NaOH(s)+CO2(g)=NaHCO3(s) ΔH2=−131.5kJ/mol
反应2NaHCO3(s)=Na2CO3(s)+ H2O(g) +CO2(g)的ΔH=
Ⅱ.在体积为2 L的密闭容器中,充入1mol/LCO2和1mol/L H2,进行如下化学反应:
CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:| t℃ | 700 | 800 | 830 | 1000 | 1200 | |||
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为
(2)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中 c(CO)不变
c. υ正(H2)=υ逆(H2O) d. c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
(4)某温度下经2min反应达到平衡后c(CO)=0.8mol/L,此温度下的平衡常数为
您最近一年使用:0次



