废催化剂(含 、
、 、
、 等成分)提取钛、钒工艺流程如下图所示。
等成分)提取钛、钒工艺流程如下图所示。
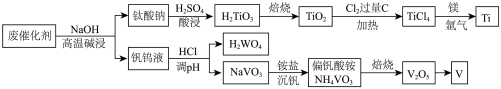
已知:①钛酸钠 难溶于水;
难溶于水;
②溶液的酸性较强时, 价钒主要以
价钒主要以 的形式存在;
的形式存在;
回答下列问题:
(1)Ti的价电子排布式_______ 。
(2)上述流程中,发生的氧化还原反应有_______ 个。
(3)“高温碱浸”中生成钛酸钠的离子方程式是_______ 。
(4)下列金属冶炼方法与上述流程中加入 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。
(5)“沉钒”过程中,一般要加入过量 ,其原因是
,其原因是_______ 。
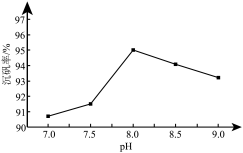
(6)沉钒过程中,沉钒率随溶液pH的变化如图所示。沉钒率随溶液pH的增加先升高后降低的原因可能是_______ 。
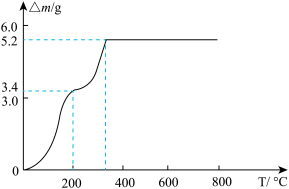
(7)取 固体加热时,固体减少的质量
固体加热时,固体减少的质量 随温度的变化曲线如图所示。加热到200℃时,产生气体的分子式为
随温度的变化曲线如图所示。加热到200℃时,产生气体的分子式为_______ 。
 、
、 、
、 等成分)提取钛、钒工艺流程如下图所示。
等成分)提取钛、钒工艺流程如下图所示。
已知:①钛酸钠
 难溶于水;
难溶于水;②溶液的酸性较强时,
 价钒主要以
价钒主要以 的形式存在;
的形式存在;回答下列问题:
(1)Ti的价电子排布式
(2)上述流程中,发生的氧化还原反应有
(3)“高温碱浸”中生成钛酸钠的离子方程式是
(4)下列金属冶炼方法与上述流程中加入
 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。| A.高炉炼铁 | B.电解熔融氧化铝制铝 | C.铝热反应制钒 | D.氧化汞分解制汞 |
 ,其原因是
,其原因是(6)沉钒过程中,沉钒率随溶液pH的变化如图所示。沉钒率随溶液pH的增加先升高后降低的原因可能是

(7)取
 固体加热时,固体减少的质量
固体加热时,固体减少的质量 随温度的变化曲线如图所示。加热到200℃时,产生气体的分子式为
随温度的变化曲线如图所示。加热到200℃时,产生气体的分子式为
更新时间:2023-10-08 21:42:04
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】次氯酸及其盐溶液有杀菌、消毒、漂白的作用。在此次抗击新冠疫情中发挥了巨大作用。某学习小组根据需要欲制备浓度不小于0.8mol·L-1的次氯酸溶液。
(查阅资料)
资料1:常温常压下,Cl2O是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水,且会与水反应生成次氯酸。
资料2:Cl2O的沸点为3.8℃,42℃以上会分解生成Cl2和O2;Cl2的沸点为-34.6℃
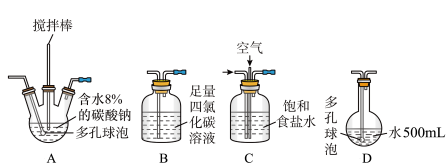
该小组用Cl2与潮湿的碳酸钠制取Cl2O,并进一步制取次氯酸,装置如下。
回答下列问题:
(1)装置连接顺序为Cl2→___ 。(用字母表示)
(2)装置A中反应的化学方程式是___ 。
(3)装置B的作用___ ,整个实验加快反应速率所采用的方法有___ 。
(4)装置D中反应的化学方程式是___ 。
(5)如果要收集Cl2O,则可以在B装置后连接E装置进行收集,这样做的依据是什么___ ,逸出气体的主要成分是___ 。
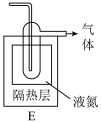
(6)此方法相对于用氯气直接溶于水制备次氯酸溶液的优点是___ (答出一条即可)。
(7)测定反应完成后A中物质的质量分数:取mg样品加适量蒸馏水使之溶解,加入几滴酚酞,用0.1molL-1的盐酸标准溶液滴定至溶液由红色变为无色,消耗盐酸V1mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸V2mL。
①则由上述实验可测定反应完成后A中物质的质量分数为___ (说明具体物质并用含m、V1和V2的代数式表示)。
②若用甲基橙作指示剂滴定结束时,滴定管尖嘴有气泡,对测定结果的影响是___ 。
(查阅资料)
资料1:常温常压下,Cl2O是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水,且会与水反应生成次氯酸。
资料2:Cl2O的沸点为3.8℃,42℃以上会分解生成Cl2和O2;Cl2的沸点为-34.6℃
该小组用Cl2与潮湿的碳酸钠制取Cl2O,并进一步制取次氯酸,装置如下。

回答下列问题:
(1)装置连接顺序为Cl2→
(2)装置A中反应的化学方程式是
(3)装置B的作用
(4)装置D中反应的化学方程式是
(5)如果要收集Cl2O,则可以在B装置后连接E装置进行收集,这样做的依据是什么

(6)此方法相对于用氯气直接溶于水制备次氯酸溶液的优点是
(7)测定反应完成后A中物质的质量分数:取mg样品加适量蒸馏水使之溶解,加入几滴酚酞,用0.1molL-1的盐酸标准溶液滴定至溶液由红色变为无色,消耗盐酸V1mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸V2mL。
①则由上述实验可测定反应完成后A中物质的质量分数为
②若用甲基橙作指示剂滴定结束时,滴定管尖嘴有气泡,对测定结果的影响是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)新型陶瓷Si3N4的熔点高、硬度大、化学性质稳定。工业上可以采用化学气相沉积法,在H2的保护下,使SiCl4与N2反应生成Si3N4沉积在石墨表面,写出该反应的化学方程式:_______ 。
(2)一种工业用硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420 ℃,高温下氧气及水蒸气能明显腐蚀氮化硅。一种合成氮化硅的主要工艺流程如下:
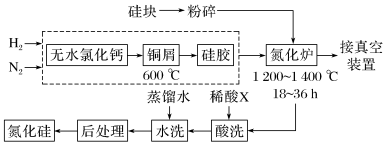
①净化N2和H2时,铜屑的作用是__________ ,硅胶的作用是____________ 。
②在氮化炉中发生反应3SiO2(s)+2N2(g)=Si3N4(s)+3O2(g) ΔH=-727.5 kJ·mol-1,开始时,严格控制氮气的流速以控制温度的原因是_____ ;体系中要通入适量的氢气是为了_____ 。
③X可能是__________ (填“盐酸”“硝酸”“硫酸”或“氢氟酸”)。
(3)工业上可以通过如图所示的流程制取纯硅:
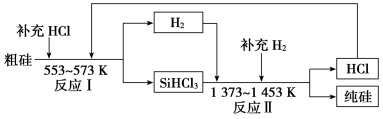
①整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应,写出该反应的化学方程式:_____ 。
②假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应Ⅰ中HCl的利用率为90%,反应Ⅱ中H2的利用率为93.75%。则在第二轮次的生产中,补充投入HCl和H2的物质的量之比是______ 。
(1)新型陶瓷Si3N4的熔点高、硬度大、化学性质稳定。工业上可以采用化学气相沉积法,在H2的保护下,使SiCl4与N2反应生成Si3N4沉积在石墨表面,写出该反应的化学方程式:
(2)一种工业用硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420 ℃,高温下氧气及水蒸气能明显腐蚀氮化硅。一种合成氮化硅的主要工艺流程如下:

①净化N2和H2时,铜屑的作用是
②在氮化炉中发生反应3SiO2(s)+2N2(g)=Si3N4(s)+3O2(g) ΔH=-727.5 kJ·mol-1,开始时,严格控制氮气的流速以控制温度的原因是
③X可能是
(3)工业上可以通过如图所示的流程制取纯硅:

①整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应,写出该反应的化学方程式:
②假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应Ⅰ中HCl的利用率为90%,反应Ⅱ中H2的利用率为93.75%。则在第二轮次的生产中,补充投入HCl和H2的物质的量之比是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】NaClO2是一种重要的杀菌消毒剂,其一种生产工艺如图:
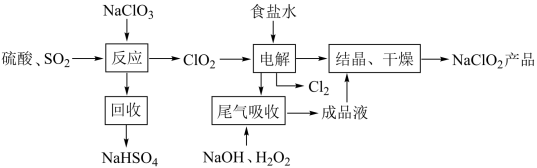
(1)NaClO2中Cl的化合价为_____________ 。
(2)写出“反应”步骤中生成ClO2的化学方程式______________ 。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去杂质SO 和Ca2+,需要加入适当过量的除杂试剂,添加顺序为为
和Ca2+,需要加入适当过量的除杂试剂,添加顺序为为_________ 、_________ 、___________ (填化学式)。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:NaOH+H2O2+ClO2-NaClO2+O2+H2O
①配平化学方程式,并用单线桥表示电子转移方向和数目__________ 。
②此吸收反应中,氧化产物是_______ ,氧化剂与还原剂的物质的量之比为_______ 。
③比较氧化性:ClO2___________ O2(填“>”、“<”或“=”)。
④若270gClO2与过量的NaOH、H2O2完全反应,计算生成的NaClO2的物质的量为_________ mol。

(1)NaClO2中Cl的化合价为
(2)写出“反应”步骤中生成ClO2的化学方程式
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去杂质SO
 和Ca2+,需要加入适当过量的除杂试剂,添加顺序为为
和Ca2+,需要加入适当过量的除杂试剂,添加顺序为为(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:NaOH+H2O2+ClO2-NaClO2+O2+H2O
①配平化学方程式,并用单线桥表示电子转移方向和数目
②此吸收反应中,氧化产物是
③比较氧化性:ClO2
④若270gClO2与过量的NaOH、H2O2完全反应,计算生成的NaClO2的物质的量为
您最近一年使用:0次
【推荐1】氢气是一种新型的绿色能源,又是一种重要的化工原料。以生物材质(以C计)与水蒸气反应制取H2是一种低耗能,高效率的制H2方法。该方法由气化炉制造H2和燃烧炉再生CaO两步构成。气化炉中涉及的反应有:
Ⅰ.C(s)+H2O(g) CO(g)+H2(g) K1;
CO(g)+H2(g) K1;
Ⅱ.CO(g)+H2O(g) CO2(g)+H2(g) K2;
CO2(g)+H2(g) K2;
Ⅲ.CaO(s)+CO2(g) CaCO3(s) K3;
CaCO3(s) K3;
燃烧炉中涉及的反应为:
Ⅳ.C(s)+O2(g)=CO2;
Ⅴ.CaCO3(s)=CaO(s)+CO2(g)。
(1)氢能被视为最具发展潜力的绿色能源,该工艺制H2总反应可表示为C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g),其反应的平衡常数K=
CaCO3(s)+2H2(g),其反应的平衡常数K=____ (用K1、K2、K3的代数式表示)。
(2)在一容积可变的密闭容器中进行反应Ⅰ,恒温恒压条件下,向其中加入1.0mol炭和1.0mol水蒸气,达到平衡时,容器的体积变为原来的1.25倍,平衡时水蒸气的平衡转化率为_____ ;向该容器中补充amol炭,水蒸气的转化率将_____ (填“增大”、“减小”或“不变”)。
(3)对于反应Ⅲ,若平衡时再充入CO2,使其浓度增大到原来的2倍,则平衡_____ 移动( 填“向右”、“向左”或“不”);当重新平衡后,CO2浓度___ (填“变大”、“变小”或“不变”)。
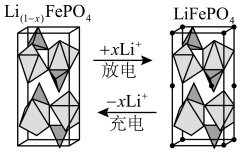
(4)一种新型锂离子二次电池——磷酸铁锂(LiFePO4)电池。作为正极材料的磷酸铁锂在充、放电时的局部放大示意图如图,写出该电池充电时的阳极电极反应式:______ 。
Ⅰ.C(s)+H2O(g)
 CO(g)+H2(g) K1;
CO(g)+H2(g) K1;Ⅱ.CO(g)+H2O(g)
 CO2(g)+H2(g) K2;
CO2(g)+H2(g) K2;Ⅲ.CaO(s)+CO2(g)
 CaCO3(s) K3;
CaCO3(s) K3;燃烧炉中涉及的反应为:
Ⅳ.C(s)+O2(g)=CO2;
Ⅴ.CaCO3(s)=CaO(s)+CO2(g)。
(1)氢能被视为最具发展潜力的绿色能源,该工艺制H2总反应可表示为C(s)+2H2O(g)+CaO(s)
 CaCO3(s)+2H2(g),其反应的平衡常数K=
CaCO3(s)+2H2(g),其反应的平衡常数K=(2)在一容积可变的密闭容器中进行反应Ⅰ,恒温恒压条件下,向其中加入1.0mol炭和1.0mol水蒸气,达到平衡时,容器的体积变为原来的1.25倍,平衡时水蒸气的平衡转化率为
(3)对于反应Ⅲ,若平衡时再充入CO2,使其浓度增大到原来的2倍,则平衡
(4)一种新型锂离子二次电池——磷酸铁锂(LiFePO4)电池。作为正极材料的磷酸铁锂在充、放电时的局部放大示意图如图,写出该电池充电时的阳极电极反应式:

您最近一年使用:0次
【推荐2】CO2是一种常用的化工原料。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)。
CO(NH2)2(s)+H2O(g)。
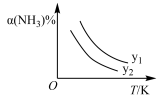
(1)在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率变化情况如图所示。该反应的ΔH_____ 0(填“>”、“<”或“=”,下同),若y表示压强,则y1_______ y2 , 若y表示反应开始时的水碳比[n(NH3)/n(CO2)],则y1_______ y2。
(2)t℃时,若向容积为2L的密闭容器中加入3molNH3和1molCO2,达到平衡时,容器内压强为开始时的0.75倍。若保持条件不变,再向该容器中加入0.5molCO2和1molH2O,NH3的转化率将__________ (填“增大”、“减小”或“不变”)。
Ⅱ.CO2与H2反应可用于生产甲醇。
(3)已知氢气与甲醇的燃烧热分别为-285.8 kJ·mol-1、-726.5kJ·mol-1,则CO2与H2反应产生液态甲醇与液态水的热化学方程式为________________ 。
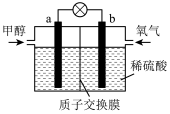
(4)下图是某甲醇燃料电池工作的示意图。质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol·L-1 H2SO4溶液。电极a上发生的电极反应式为________________________ ,当电池中有1mol e-发生转移时左右两侧溶液的质量之差为______ g (假设反应物耗尽,忽略气体的溶解)。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g)。
CO(NH2)2(s)+H2O(g)。 (1)在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率变化情况如图所示。该反应的ΔH

(2)t℃时,若向容积为2L的密闭容器中加入3molNH3和1molCO2,达到平衡时,容器内压强为开始时的0.75倍。若保持条件不变,再向该容器中加入0.5molCO2和1molH2O,NH3的转化率将
Ⅱ.CO2与H2反应可用于生产甲醇。
(3)已知氢气与甲醇的燃烧热分别为-285.8 kJ·mol-1、-726.5kJ·mol-1,则CO2与H2反应产生液态甲醇与液态水的热化学方程式为
(4)下图是某甲醇燃料电池工作的示意图。质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol·L-1 H2SO4溶液。电极a上发生的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】利用合成气(主要成分为CO、CO2、 H2) 一定条件下合成甲醇(CH3OH),发生的主要反应如下:
Ⅰ. CO(g) + 2H2(g)=CH3OH(g) △H。
Ⅱ. CO(g) + H2O(g)=CO2(g) +H2(g) ∆H2=-41.2 kJ/mol
回答下列问题:
(1)已知反应①中的相关化学键键能数据如下:
写出由二氧化碳、氢气制备甲醇的热化学方程式_______ 反应I在_______ (填“高温”、“低温”或“任意温度”)条件下自发进行。
(2)在T℃时,向5L恒容密闭容器中加入0.6 mol CO和0.45 molH2,发生反应Ⅰ。CO和CH3OH的浓度在不同时刻的变化状况如图所示:
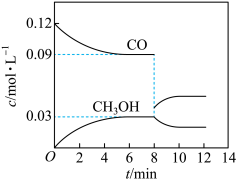
①下列能够说明反应在第6min时达到平衡状态的是______
A.混合气体的平均摩尔质量不再改变
B. CH3OH 的浓度不变
C. v(CO)正 : v(H2)逆= 2:1
D. P(CO):P( H2)= 1:2
第8 min时改变的条件是_______
②在第12 min时升高温度,重新达到平衡时,化学平衡常数将_______ (填 “增大”“不变”或“减小”),理由是_______
(3)某科研小组研究了反应CO(g) + 2H2(g)= CH3OH(g)的动力学,获得其速率方程v=k[c(H2)]1/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:
CO的反应级数m=_______ , 当实验2进行到某时刻,测得c(H3)= 0.010 mol·L-1,则此时的反应速率v_______ mol·L-1·s-1(已知: ≈0.3)。
≈0.3)。
(4)利用CH4重整CO2的催化转化如图所示,CH4与CO2重整反应的方程式为_______ 。有关转化过程,下列说法正确的是_______ (填序号)。
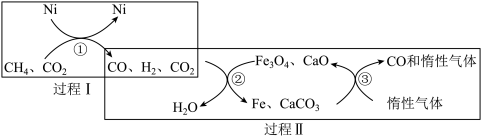
a. 过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d. 转化③中Fe与CaCO3,反应的物质的量之比为4:3
Ⅰ. CO(g) + 2H2(g)=CH3OH(g) △H。
Ⅱ. CO(g) + H2O(g)=CO2(g) +H2(g) ∆H2=-41.2 kJ/mol
回答下列问题:
(1)已知反应①中的相关化学键键能数据如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
(2)在T℃时,向5L恒容密闭容器中加入0.6 mol CO和0.45 molH2,发生反应Ⅰ。CO和CH3OH的浓度在不同时刻的变化状况如图所示:

①下列能够说明反应在第6min时达到平衡状态的是
A.混合气体的平均摩尔质量不再改变
B. CH3OH 的浓度不变
C. v(CO)正 : v(H2)逆= 2:1
D. P(CO):P( H2)= 1:2
第8 min时改变的条件是
②在第12 min时升高温度,重新达到平衡时,化学平衡常数将
(3)某科研小组研究了反应CO(g) + 2H2(g)= CH3OH(g)的动力学,获得其速率方程v=k[c(H2)]1/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:
| 实验序号 | c(H2)/mol/L | c(CO)/mol/L | v/mol/L |
| 1 | 0.100 | 0.100 | 1.2×10-2 |
| 2 | 0.050 | 0.100 | 8.4×10-3 |
| 3 | 0.100 | 0.200 | 2.4×10-2 |
 ≈0.3)。
≈0.3)。(4)利用CH4重整CO2的催化转化如图所示,CH4与CO2重整反应的方程式为

a. 过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d. 转化③中Fe与CaCO3,反应的物质的量之比为4:3
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】化学中的某些元素是与生命活动密不可分的元素,请回答下列问题。
(1)NH4NO3是一种重要的化学肥料,其中N原子的杂化方式是______ 。
(2)维生素C是一种水溶性维生素,水果和蔬菜中含量丰富,该物质结构简式如图所示。以下关于维生素C的说法正确的是______ 。
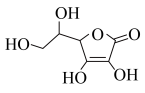
a.分子中既含有极性键又含有非极性键
b.1 mol 分子中含有4 mol π键
c.该物质的熔点可能高于NaCl
d.分子中所含元素电负性由大到小的顺序为O>C>H
(3)维生素C晶体溶于水的过程中要克服的微粒间作用力有______ 。
(4)KSCN溶液可用于Fe3+的检验,原因是铁离子外围有较多能量相近的空轨道,因此能与一些分子或离子形成配合物。Fe3+的价电子排布为______ ,与之形成配合物的分子或离子中的配位原子应具备的结构特征是______ 。
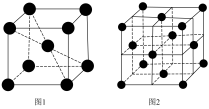
(5)1183K以下纯铁晶体的晶胞如图1所示,1183K以上则转变为图2所示晶胞,则图1和图2中,铁原子的配位数之比为______ 。
(1)NH4NO3是一种重要的化学肥料,其中N原子的杂化方式是
(2)维生素C是一种水溶性维生素,水果和蔬菜中含量丰富,该物质结构简式如图所示。以下关于维生素C的说法正确的是

a.分子中既含有极性键又含有非极性键
b.1 mol 分子中含有4 mol π键
c.该物质的熔点可能高于NaCl
d.分子中所含元素电负性由大到小的顺序为O>C>H
(3)维生素C晶体溶于水的过程中要克服的微粒间作用力有
(4)KSCN溶液可用于Fe3+的检验,原因是铁离子外围有较多能量相近的空轨道,因此能与一些分子或离子形成配合物。Fe3+的价电子排布为
(5)1183K以下纯铁晶体的晶胞如图1所示,1183K以上则转变为图2所示晶胞,则图1和图2中,铁原子的配位数之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硅是地壳中储量仅次于氧的元素,在自然界中主要以SiO2和硅酸盐的形式存在。
(1)基态硅原子的价电子排布式为_______ 。
(2)晶态 SiO2的晶胞如下图所示:
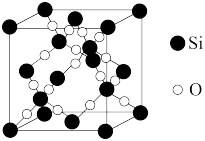
①硅原子的杂化方式为_______ 。
②已知SiO2晶胞的棱长均为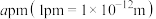 ,阿伏加德罗常数为NA,则SiO2晶体的密度
,阿伏加德罗常数为NA,则SiO2晶体的密度
_______  (列出计算式)。
(列出计算式)。
(3)硅元素最高价氧化物对应的水化物为原硅酸(H4SiO4)。
资料:原硅酸(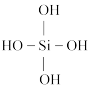 )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
①原硅酸钠(Na4SiO4)溶液吸收空气中的CO2会生成H4SiO4,结合元素周期律解释原因:_______ 。
②从结构的角度解释H4SiO4脱水后溶解度降低的原因:_______ 。
(1)基态硅原子的价电子排布式为
(2)晶态 SiO2的晶胞如下图所示:

①硅原子的杂化方式为
②已知SiO2晶胞的棱长均为
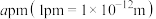 ,阿伏加德罗常数为NA,则SiO2晶体的密度
,阿伏加德罗常数为NA,则SiO2晶体的密度
 (列出计算式)。
(列出计算式)。(3)硅元素最高价氧化物对应的水化物为原硅酸(H4SiO4)。
资料:原硅酸(
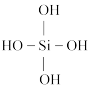 )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。①原硅酸钠(Na4SiO4)溶液吸收空气中的CO2会生成H4SiO4,结合元素周期律解释原因:
②从结构的角度解释H4SiO4脱水后溶解度降低的原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、W、R、Q五种前四周期主族元素,原子序数依次增大。元素Z在地壳中含量最高,W元素的焰色试验呈黄色,R的最外层电子数与其电子总数之比为3:8,X能与W形成离子化合物且W+的半径大于X-的半径,Y的氧化物是形成酸雨的物质之一,Q原子p能级轨道上有三个单电子。
请回答下列问题:
(1)Q元素在周期表中的位置为_______ 。
(2)Y、Z、W、R这四种元素简单离子的离子半径从大到小的顺序是_______ (用离子符号表示)。
(3)M和N均为上述六种元素中的三种组成的化合物,且M和N都为强电解质,M和N溶液反应既有沉淀出现又有气体产生,写出M和N反应的化学方程式:_______ 。
(4)基态Q原子的简化电子排布式为_______ 。单质Q的气态分子构型如图所示,在其中4条棱上各插入1个R原子,形成Q4R4,俗称雄黄,则雄黄可能有_______ 种不同的结构;0.5 mol Q4R4中含有_______ mol Q-R键。
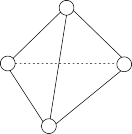
(5)X3QZ3形成的盐可用作长效杀虫剂和除草剂,QZ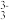 的空间构型为
的空间构型为_______ 。
请回答下列问题:
(1)Q元素在周期表中的位置为
(2)Y、Z、W、R这四种元素简单离子的离子半径从大到小的顺序是
(3)M和N均为上述六种元素中的三种组成的化合物,且M和N都为强电解质,M和N溶液反应既有沉淀出现又有气体产生,写出M和N反应的化学方程式:
(4)基态Q原子的简化电子排布式为

(5)X3QZ3形成的盐可用作长效杀虫剂和除草剂,QZ
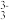 的空间构型为
的空间构型为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
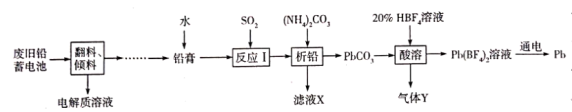
【推荐1】汽车的大量使用给人们的出行带来了便利,但也带来了诸多社会问题,如废旧铅蓄电池的环境污染。通过下列工艺流程对废旧铅蓄电池进行处理,可回收金属铅和粗硫酸。
已知:i.铅膏的成分: 、
、 。
。
ii.常温下,部分铅盐的浓度积: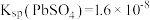 ,
,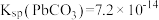 。
。
回答下列有关问题:
(1)“翻料、倾料”操作后所得电解质溶液中的电解质是_______ (填化学式)。
(2)“铅膏”加水的目的是调成悬浊液,作用是_______ 。
(3)反应I的化学方程式是_______ 。
(4)测得“析铅”后的 滤液中,
滤液中,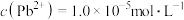 ,对析出的
,对析出的 进行洗涤、干燥,得
进行洗涤、干燥,得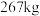 产品,则原铅膏中
产品,则原铅膏中 、
、 的总物质的量为
的总物质的量为_______  ,滤液中
,滤液中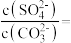
_______ (保留一位小数)。滤液X中主要溶质的用途有_______ (填一种)。
(5)HBF4是一种强酸,则气体Y为_______ (填化学式)。

已知:i.铅膏的成分:
 、
、 。
。ii.常温下,部分铅盐的浓度积:
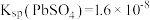 ,
,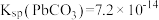 。
。回答下列有关问题:
(1)“翻料、倾料”操作后所得电解质溶液中的电解质是
(2)“铅膏”加水的目的是调成悬浊液,作用是
(3)反应I的化学方程式是
(4)测得“析铅”后的
 滤液中,
滤液中,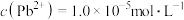 ,对析出的
,对析出的 进行洗涤、干燥,得
进行洗涤、干燥,得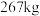 产品,则原铅膏中
产品,则原铅膏中 、
、 的总物质的量为
的总物质的量为 ,滤液中
,滤液中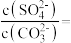
(5)HBF4是一种强酸,则气体Y为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列小题
(1)将相关的含硫物质按一定的规律和方法分为如表所示3组,则第2组中物质X的化学式是_____ 。
(2)利用如图所示的装置探究SO2的性质:
(熔点:SO2为-76.1℃,SO3为16.8℃;沸点:SO2为-10℃,SO3为45℃)
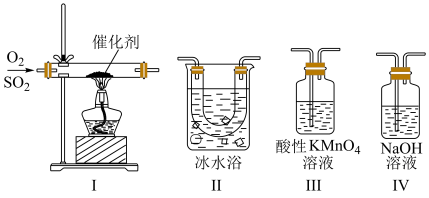
①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是_____ 。
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是_____ 。装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时pH降低,则该反应的离子方程式是_____ 。
(3)硫酸工业生产排放的二氧化硫进入大气,会污染环境,有多种方法可用于SO2的脱除。
①氨法脱硫。该方法是一种高效低耗能的湿法脱硫方式,利用氨水吸收废气中的SO2,并在富氧条件下转化为硫酸铵,该过程中被氧化的元素是_____ ,得到的硫酸铵可用作_____ 。
②用NaClO溶液作为吸收剂,调pH至5.5时吸收SO2,反应离子方程式是_____ 。
③酸性条件下,用MnO2进行脱硫处理的原理如图所示。
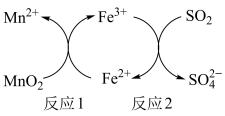
上述过程中可以循环使用的是_____ ,反应1的离子方程式为_____ ,脱硫最终产物的化学式是_____ 。
(1)将相关的含硫物质按一定的规律和方法分为如表所示3组,则第2组中物质X的化学式是
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、X、Na2SO3、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |
(2)利用如图所示的装置探究SO2的性质:
(熔点:SO2为-76.1℃,SO3为16.8℃;沸点:SO2为-10℃,SO3为45℃)

①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是
(3)硫酸工业生产排放的二氧化硫进入大气,会污染环境,有多种方法可用于SO2的脱除。
①氨法脱硫。该方法是一种高效低耗能的湿法脱硫方式,利用氨水吸收废气中的SO2,并在富氧条件下转化为硫酸铵,该过程中被氧化的元素是
②用NaClO溶液作为吸收剂,调pH至5.5时吸收SO2,反应离子方程式是
③酸性条件下,用MnO2进行脱硫处理的原理如图所示。

上述过程中可以循环使用的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
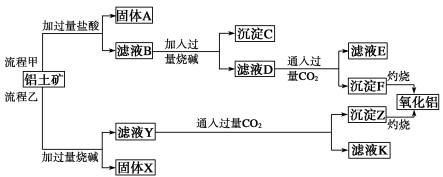
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为_______________________ 。
(2)流程乙加入烧碱后生成AlO2-的离子方程式为____________________ 。
(3)滤液E、K中溶质的主要成分是__________ (填化学式)。
(4)已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱达到沉淀溶解平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=__________ 。

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为
(2)流程乙加入烧碱后生成AlO2-的离子方程式为
(3)滤液E、K中溶质的主要成分是
(4)已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱达到沉淀溶解平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=
您最近一年使用:0次



