下列液体均处于25℃,有关叙述正确的是
| A.某物质的溶液pH<7,则该物质属于酸或强酸弱碱盐 |
| B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
| C.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-) |
| D.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |
2014·福建厦门·一模 查看更多[4]
安徽省宿州市泗县第一中学2023-2024学年高二下学期开学考试化学试题广东省珠海市2020-2021学年高二上学期期末考试化学试题安徽省太和第一中学2019-2020学年高二上学期第一次月考(飞越班)化学试题(已下线)2013-2014福建厦门双十中学高中毕业班测试七化学试卷
更新时间:2016-12-09 06:10:14
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,向20mL0.2mol·L-1二元酸H2A溶液中滴加0.2mol·L-1NaOH溶液,有关微粒物质的量变化如图。下列叙述正确的是( )


| A.当V(NaOH)=20 mL时,溶液的pH大于7 |
| B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大 |
| C.当溶液为中性时,V(NaOH)>20 mL |
D.当V(NaOH)=40mL时,升高温度, 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,下列有关0.1mol·L-1氨水的说法正确的是
| A.溶液的pH>13 |
| B.加水稀释,溶液中c(H+)和c(OH-)都减小 |
| C.该溶液中:c(OH-)=c(NH4+) |
| D.完全中和等物质的量的HCl,消耗的体积与0.1mol•L-1NaOH溶液一样多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列事实不能 用勒夏特列原理解释的是
| A.将AlCl3溶液加热蒸干不能得到AlCl3固体 |
| B.NO2和N2O4的混合气体升温后红棕色加深 |
| C.拦河大坝的钢闸门与外接直流电源的负极相连 |
D.将0.1 mol·L 氨水稀释至0.01 mol·L 氨水稀释至0.01 mol·L ,溶液的pH由11.1降至10.6 ,溶液的pH由11.1降至10.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】温度相同、浓度均为0.2mol/L的①(NH4)2SO4、②NaNO3、③NH4HSO4④NH4NO3 ⑤ NaClO ⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是( )
| A.③①④②⑥⑤ | B.③①④②⑤⑥ |
| C.③②①⑥④⑤ | D.⑤⑥②④①③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
| A.若电工操作中将铝线与铜线直接相连,会导致铜线更快被氧化 |
| B.反应CaC2(s)+N2(g)=CaCN2(s)+C(s)能自发进行,是因为△H<0 |
C.常温下,向0.1mol·L-1氨水中通入少量HCl,溶液中 减小 减小 |
| D.乙酸乙酯的水解反应,加入NaOH溶液会使平衡常数增大,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】Na2CO3溶液(足量)的电解装置图如图所示,下列说法错误的是


A.K闭合后,A电极上发生的电极反应应为4CO +2H2O-4e-=4HCO +2H2O-4e-=4HCO +O2↑ +O2↑ |
| B.a处产生的气体和b处产生的气体的质量比为16∶1 |
C.K未闭合时,左侧电极室溶液中:c(Na+)>c(CO )>c(OH-)>c(HCO )>c(OH-)>c(HCO )>c(H+) )>c(H+) |
| D.当A极室生成1 mol NaHCO3时,B极室NaOH增加1 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,某小组做如下两组实验:
实验Ⅰ:分别往浓度均为 、
、 溶液中通入
溶液中通入 至
至 ;
;
实验Ⅱ:在1.0L、 溶液中加入
溶液中加入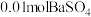 固体,充分反应。
固体,充分反应。
[已知:25℃, 的电离常数
的电离常数 、
、 ;
; 、
、 。混合后溶液体积变化忽略不计]。下列说法
。混合后溶液体积变化忽略不计]。下列说法不正确 的是
实验Ⅰ:分别往浓度均为
 、
、 溶液中通入
溶液中通入 至
至 ;
;实验Ⅱ:在1.0L、
 溶液中加入
溶液中加入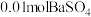 固体,充分反应。
固体,充分反应。[已知:25℃,
 的电离常数
的电离常数 、
、 ;
; 、
、 。混合后溶液体积变化忽略不计]。下列说法
。混合后溶液体积变化忽略不计]。下列说法A. 、 、 溶液中水的电离程度: 溶液中水的电离程度: |
B.实验Ⅰ结束后, 、 、 溶液中均有 溶液中均有 |
C.实验Ⅱ的转化存在平衡常数: |
D.实验Ⅱ中,改用饱和 溶液, 溶液, 的平衡转化率减小 的平衡转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列液体均处于25 ℃,有关叙述正确的是
| A.Na2CO3溶液中,c(OH-)-c(H+)=c(HCO3-) +2c(H2CO3) |
| B.AgCl在同浓度的MgCl2和KCl溶液中的溶解度相同 |
| C.将稀氨水逐滴加入稀硫酸中,当溶液pH =7时,c(SO42-) >c(NH4+) |
| D.Na2S溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,Ksp(MnS)=2.5×10-13,Ksp(FeS)=6.3×10-18。FeS和MnS在水中的沉淀溶解平衡曲线如图所示(X2+表示Fe2+或Mn2+),下列说法错误的是( )
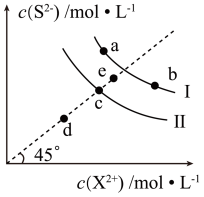

| A.曲线I表示MnS的沉淀溶解平衡曲线 |
| B.升高温度,曲线Ⅱ上的c点可沿虚线平移至d点 |
C.常温下,反应MnS(s)+Fe2+(aq) FeS(s)+Mn2+(aq)的平衡常数K≈4×104 FeS(s)+Mn2+(aq)的平衡常数K≈4×104 |
| D.向b点溶液中加入少量Na2S固体,溶液组成由b点沿工线向a点方向移动 |
您最近一年使用:0次
【推荐3】①已知t℃时AgCl的Ksp=2.0×10-10;②在t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
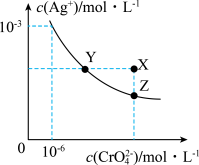

| A.在t℃时,Ag2CrO4的Ksp为1.0×10-12 |
| B.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到Z点 |
C.在t℃时,以0.01mol·L-1AgNO3溶液滴定20.00mL0.01mol·L-1KCl和0.01mol·L-1K2CrO4的混合溶液, 先沉淀 先沉淀 |
D.在t℃时,反应Ag2CrO4(s)+2Cl-(aq) 2AgCl(s)+ 2AgCl(s)+ (aq)的平衡常数K=2.5×107 (aq)的平衡常数K=2.5×107 |
您最近一年使用:0次

 )>2:1
)>2:1

