已知:乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4)。25℃时,草酸的电离平衡常数为K1=5.0×10-2,K2=5.4×10-5;碳酸(H2CO3)的电离平衡常数为K1=4.5×10-7,K2=4.7×10-11。草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。回答下列问题:
(1)写出水溶液中草酸的电离方程式_____________________________________ 。
(2)相同条件下物质的量浓度都为0.1mol/L的Na2C2O4溶液的pH比Na2CO3溶液的pH______________ (填“大”、“小”或“相等”) 。
(3)常温下将0.4mol/L的KOH溶液20mL与0.2mol/L的草酸溶液20mL混合,则混合后溶液中阴离子浓度的大小顺序为_____________________________________ 。
(4)往Na2CO3溶液中加入少量草酸溶液,发生反应的离子方程式为________________ 。
(5)25℃时,向20mL碳酸钙的饱和溶液中逐滴加入c mol/L的草酸钾溶液20mL后,有草酸钙沉淀生成,则c的最小值为__________________________ 。
(1)写出水溶液中草酸的电离方程式
(2)相同条件下物质的量浓度都为0.1mol/L的Na2C2O4溶液的pH比Na2CO3溶液的pH
(3)常温下将0.4mol/L的KOH溶液20mL与0.2mol/L的草酸溶液20mL混合,则混合后溶液中阴离子浓度的大小顺序为
(4)往Na2CO3溶液中加入少量草酸溶液,发生反应的离子方程式为
(5)25℃时,向20mL碳酸钙的饱和溶液中逐滴加入c mol/L的草酸钾溶液20mL后,有草酸钙沉淀生成,则c的最小值为
17-18高二上·河南商丘·期中 查看更多[3]
安徽省当涂一中2017-2018学年高二上学期12月月考化学试题(已下线)黄金30题系列 高二化学(选修4) 大题好拿分【提升版】河南省商丘市第一高级中学2017-2018学年高二上学期期中考试化学试题
更新时间:2017-12-07 17:30:34
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】研究 溶于水后的行为对
溶于水后的行为对 的吸收再利用有重要意义。常温下,水溶液中含碳微粒的pC(
的吸收再利用有重要意义。常温下,水溶液中含碳微粒的pC( ,c表示微粒浓度)随溶液pH的变化如图所示。回答下列问题:
,c表示微粒浓度)随溶液pH的变化如图所示。回答下列问题:
已知:25℃时,HBrO的电离平衡常数
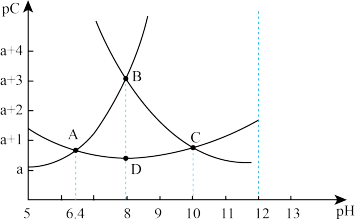
(1)下列说法正确的是_______ (填序号)。
a.A点,溶液中 和
和 浓度相同
浓度相同
b.当 时,
时,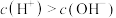
c.A点时水的电离程度小于B点
(2)向B点溶液中逐滴滴加NaOH溶液,溶液状态向_______ (填“A”、“C”或“D”)变化,主要反应的离子方程式是_______ 。
(3) 、HBrO的酸性由强到弱的顺序为
、HBrO的酸性由强到弱的顺序为_______ ,将少量 气体通入NaBrO溶液中发生反应的离子方程式为
气体通入NaBrO溶液中发生反应的离子方程式为_______ ;25℃, NaBrO溶液的
NaBrO溶液的
_______ 。
(4)从盐类水解原理角度设计一个合理且易操作的方案(药品可任取),证明碳酸是弱电解质。_______ 。
 溶于水后的行为对
溶于水后的行为对 的吸收再利用有重要意义。常温下,水溶液中含碳微粒的pC(
的吸收再利用有重要意义。常温下,水溶液中含碳微粒的pC( ,c表示微粒浓度)随溶液pH的变化如图所示。回答下列问题:
,c表示微粒浓度)随溶液pH的变化如图所示。回答下列问题:已知:25℃时,HBrO的电离平衡常数


(1)下列说法正确的是
a.A点,溶液中
 和
和 浓度相同
浓度相同b.当
 时,
时,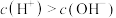
c.A点时水的电离程度小于B点
(2)向B点溶液中逐滴滴加NaOH溶液,溶液状态向
(3)
 、HBrO的酸性由强到弱的顺序为
、HBrO的酸性由强到弱的顺序为 气体通入NaBrO溶液中发生反应的离子方程式为
气体通入NaBrO溶液中发生反应的离子方程式为 NaBrO溶液的
NaBrO溶液的
(4)从盐类水解原理角度设计一个合理且易操作的方案(药品可任取),证明碳酸是弱电解质。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】根据下列物质:① ②
② ③
③ 溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧
溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧ 晶体,回答下列有关问题:
晶体,回答下列有关问题:
(1)以上物质中属于强电解质的是________ (填编号)
(2)常温,测得 中
中 为
为 ,则
,则 在该温度下的电离常数
在该温度下的电离常数 约为
约为___________ (结果保留一位小数)
(3)常温, ,下列有关说法正确的是_________。
,下列有关说法正确的是_________。
(4)室温下,将三支装入含酚酞的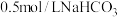 溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入
溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入 晶体,在乙烧杯中加入CaO。写出
晶体,在乙烧杯中加入CaO。写出 溶液中碳元素的守恒关系式:
溶液中碳元素的守恒关系式:___________ ;一段时间后,甲烧杯试管中溶液颜色___________ (填“变深”、“变浅”、“不变”);结合方程式解释乙烧杯中加CaO后其试管内颜色变化的原因:__________ 。
(5)将1g 溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程,
溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程, 始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
 ②
② ③
③ 溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧
溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧ 晶体,回答下列有关问题:
晶体,回答下列有关问题:(1)以上物质中属于强电解质的是
(2)常温,测得
 中
中 为
为 ,则
,则 在该温度下的电离常数
在该温度下的电离常数 约为
约为(3)常温,
 ,下列有关说法正确的是_________。
,下列有关说法正确的是_________。| A.向冰醋酸中加水,溶液的导电能力先增大后减小 |
B.向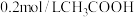 溶液中加水稀释, 溶液中加水稀释, 增大 增大 |
C.等温等浓度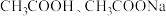 混合溶液中: 混合溶液中: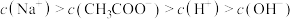 |
D.pH为3的 溶液中,水电离的 溶液中,水电离的 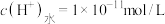 |
(4)室温下,将三支装入含酚酞的
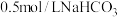 溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入
溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入 晶体,在乙烧杯中加入CaO。写出
晶体,在乙烧杯中加入CaO。写出 溶液中碳元素的守恒关系式:
溶液中碳元素的守恒关系式:(5)将1g
 溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程,
溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程, 始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
始终未完全溶解),观察电导率的变化,重复操作,绘图如下: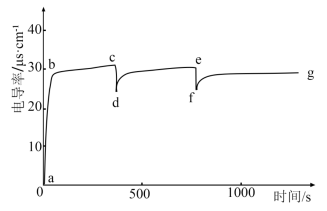
| A.c、e点电导率相等 |
| B.d、f点为饱和溶液 |
C.b→c电导率基本不变的原因是 到溶解平衡 到溶解平衡 |
| D.g点再加10mL蒸馏水可重复c→d、e→f图像 |
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】氟和氟盐是化工原料。由于氟气性质活泼,很晚才制取出来。
(1)不能通过电解纯净的液态HF获得F2,其原因是_________ ;但电解液态KHF2时,两极分别得到F2和H2,写出阳极上HF2—放电产生气体的电极反应式______________ 。
(2)利用化学反应也能制取氟。请配平下列化学方程式:
____ K2MnF6+____ SbF5—____ KSbF6+____ MnF3+____ F2↑;其中还原产物是________ 。
(3)某温度下测得浓度均为0.10mol/L的KF和HF混合液的pH=4,近似计算HF的电离平衡常数Ka(写出计算过程)_________ 。
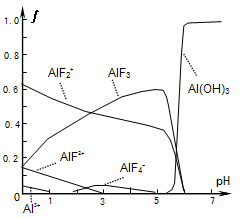
(4)一定浓度的HF和Al2(SO4)3混合液中,铝的各种微粒含量f随PH的分布曲线如图示。用NaOH使混合液的pH从5调整到7,写出有关反应的离子方程式:__________ 。
(1)不能通过电解纯净的液态HF获得F2,其原因是
(2)利用化学反应也能制取氟。请配平下列化学方程式:
(3)某温度下测得浓度均为0.10mol/L的KF和HF混合液的pH=4,近似计算HF的电离平衡常数Ka(写出计算过程)
(4)一定浓度的HF和Al2(SO4)3混合液中,铝的各种微粒含量f随PH的分布曲线如图示。用NaOH使混合液的pH从5调整到7,写出有关反应的离子方程式:

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】柠檬酸是一种重要的工业原料,化学式可表示为 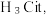 属于三元弱酸。 25℃时,柠檬酸的电离常数分别为:
属于三元弱酸。 25℃时,柠檬酸的电离常数分别为: 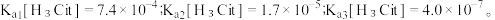
(1)25℃时, 不同pH范围内,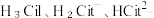 和
和 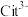 所占的比例 (该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表
所占的比例 (该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表  的曲线是
的曲线是_______ 。
(3)已知25℃时,碳酸的电离常数为: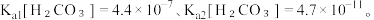 向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式
向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式_______ 。
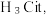 属于三元弱酸。 25℃时,柠檬酸的电离常数分别为:
属于三元弱酸。 25℃时,柠檬酸的电离常数分别为: 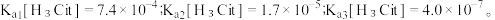
(1)25℃时, 不同pH范围内,
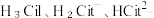 和
和 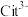 所占的比例 (该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表
所占的比例 (该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表  的曲线是
的曲线是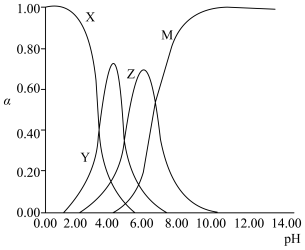
A.Na3Cit溶液中, |
B.Na3Cit溶液中,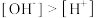 |
C.NaH2Cit溶液中, |
D.Na2HCit溶液中,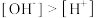 |
(3)已知25℃时,碳酸的电离常数为:
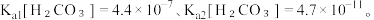 向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式
向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol/L的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,请回答下列问题。
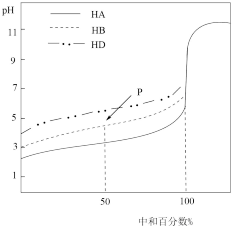
(1)请写出HA溶液与NaOH溶液反应的离子反应方程式____ 。
(2)滴定至P点时,溶液中各微粒(H2O分子除外)的浓度由大到小的关系是____ 。
(3)pH=7时,两溶液中c(B-)____ c(D-)(填“>”“=”或“<”,下同)。
(4)当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)+c(H+)____ c(OH-)。
(5)在常温下,测得NaD溶液的pH=10,则溶液中由水电离出来的c(OH-)____ mol/L。

(1)请写出HA溶液与NaOH溶液反应的离子反应方程式
(2)滴定至P点时,溶液中各微粒(H2O分子除外)的浓度由大到小的关系是
(3)pH=7时,两溶液中c(B-)
(4)当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)+c(H+)
(5)在常温下,测得NaD溶液的pH=10,则溶液中由水电离出来的c(OH-)
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】已知某溶液中只存在OH-、H+、CH3COO-、Na+四种离子,某同学推测其离子浓度大小顺序可能有如下几种关系:
① c(Na+) > c(OH-)>c(CH3COO-)>c(H+)
② c(Na+) >c(OH-)= c(CH3COO-)>c(H+)
③ c(Na+) >c(CH3COO-)> c(OH-)>c(H+)
④ c(Na+) = c(CH3COO-)> c(OH-)=c(H+)
⑤ c(CH3COO-)> c(Na+) >c(H+)>c(OH-)
结合离子关系填写下列空白:
(1)若溶液中只溶解一种溶质,则该溶质是__________ ,离子浓度的大小顺序符合上述序号______ ;若溶液中性,离子浓度的大小顺序符合上述序号________ ;
(2)若溶质为CH3COONa和 CH3COOH,则离子的关系符合上述序号_____________ 。
① c(Na+) > c(OH-)>c(CH3COO-)>c(H+)
② c(Na+) >c(OH-)= c(CH3COO-)>c(H+)
③ c(Na+) >c(CH3COO-)> c(OH-)>c(H+)
④ c(Na+) = c(CH3COO-)> c(OH-)=c(H+)
⑤ c(CH3COO-)> c(Na+) >c(H+)>c(OH-)
结合离子关系填写下列空白:
(1)若溶液中只溶解一种溶质,则该溶质是
(2)若溶质为CH3COONa和 CH3COOH,则离子的关系符合上述序号
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】按要求填写下列相关内容:
(1)实验表明,液氨也能像水那样进行自耦电离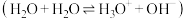 ,碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
,碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
①写出液氨自耦电离的方程式_______ 。
②写出碳酸钠溶于液氨后第一级氨解的离子方程式:_______ 。
(2)室温下 的盐酸和
的盐酸和 的碳酸钠溶液,水电离出的
的碳酸钠溶液,水电离出的 的比值为
的比值为_______ ,将二者等体积混合,溶液显_______ 性。
(3)某温度时, 的
的 溶液的
溶液的 是12,在此温度下,将
是12,在此温度下,将 的盐酸溶液
的盐酸溶液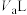 与
与 的
的 溶液
溶液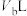 混合,所得混合液为中性,若
混合,所得混合液为中性,若 ,则
,则
_______ 。
(4)若 水解的离子方程式为
水解的离子方程式为 ,室温下该水解反应的平衡常数
,室温下该水解反应的平衡常数
_______ 。(已知室温下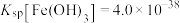 )
)
(5) 在水溶液中的电离如下:
在水溶液中的电离如下: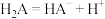 ,
, ,
,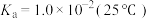
①向 溶液中滴加少量氨水,该反应的离子方程式为
溶液中滴加少量氨水,该反应的离子方程式为_______ 。
②已知 电离平衡常数
电离平衡常数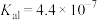 ,
, ,则
,则 和
和 两溶液混合反应的离子方程式为
两溶液混合反应的离子方程式为_______ 。
(1)实验表明,液氨也能像水那样进行自耦电离
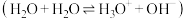 ,碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
,碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。①写出液氨自耦电离的方程式
②写出碳酸钠溶于液氨后第一级氨解的离子方程式:
(2)室温下
 的盐酸和
的盐酸和 的碳酸钠溶液,水电离出的
的碳酸钠溶液,水电离出的 的比值为
的比值为(3)某温度时,
 的
的 溶液的
溶液的 是12,在此温度下,将
是12,在此温度下,将 的盐酸溶液
的盐酸溶液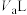 与
与 的
的 溶液
溶液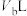 混合,所得混合液为中性,若
混合,所得混合液为中性,若 ,则
,则
(4)若
 水解的离子方程式为
水解的离子方程式为 ,室温下该水解反应的平衡常数
,室温下该水解反应的平衡常数
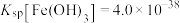 )
)(5)
 在水溶液中的电离如下:
在水溶液中的电离如下: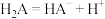 ,
, ,
,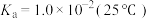
①向
 溶液中滴加少量氨水,该反应的离子方程式为
溶液中滴加少量氨水,该反应的离子方程式为②已知
 电离平衡常数
电离平衡常数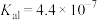 ,
, ,则
,则 和
和 两溶液混合反应的离子方程式为
两溶液混合反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识回答:
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小的顺序为___________ 。
(2)B为0.1 mol·L-1 NaHCO3溶液,请分析NaHCO3溶液显碱性的原因______________ 。
(3)D为含有足量AgCl固体的饱和溶液,氯化银在水中存在沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl-(aq),在25 ℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL 蒸馏水中;②100 mL 0.2 mol·L-1 AgNO3溶液中;③100 mL 0.1 mol·L-1氯化铝溶液中;④100 mL 0.1 mol·L-1盐酸溶液中,充分搅拌后,相同温度下银离子浓度由大到小的顺序是
Ag+(aq)+Cl-(aq),在25 ℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL 蒸馏水中;②100 mL 0.2 mol·L-1 AgNO3溶液中;③100 mL 0.1 mol·L-1氯化铝溶液中;④100 mL 0.1 mol·L-1盐酸溶液中,充分搅拌后,相同温度下银离子浓度由大到小的顺序是________ (填写序号);②中氯离子的浓度为________ mol·L-1。
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小的顺序为
(2)B为0.1 mol·L-1 NaHCO3溶液,请分析NaHCO3溶液显碱性的原因
(3)D为含有足量AgCl固体的饱和溶液,氯化银在水中存在沉淀溶解平衡:AgCl(s)
 Ag+(aq)+Cl-(aq),在25 ℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL 蒸馏水中;②100 mL 0.2 mol·L-1 AgNO3溶液中;③100 mL 0.1 mol·L-1氯化铝溶液中;④100 mL 0.1 mol·L-1盐酸溶液中,充分搅拌后,相同温度下银离子浓度由大到小的顺序是
Ag+(aq)+Cl-(aq),在25 ℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL 蒸馏水中;②100 mL 0.2 mol·L-1 AgNO3溶液中;③100 mL 0.1 mol·L-1氯化铝溶液中;④100 mL 0.1 mol·L-1盐酸溶液中,充分搅拌后,相同温度下银离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】回答下列问题:
(1)将 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是_______ (写化学式)。
(2)已知草酸是二元弱酸,常温下测得0.1mol/L的 的pH为4.8,则此
的pH为4.8,则此 溶液中
溶液中
_______  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
(3)某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。出现上述现象的原因是____________________________ (请用反应的离子方程式表示)。
(4) 、
、 两种温度下
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。

①
______  (填“>”“<”或“=”),
(填“>”“<”或“=”), 温度时
温度时
_______ 。
②根据 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是_______ (填标号)。
A.加入 固体可由a点变为b点
固体可由a点变为b点
B. 温度下,在
温度下,在 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成
C.蒸发溶剂可能由d点变为 曲线上a、b之间(不含a、b)的某一点
曲线上a、b之间(不含a、b)的某一点
D.升温可由b点变为d点
③ 温度时,现有0.2mol的
温度时,现有0.2mol的 沉淀,每次用1L饱和
沉淀,每次用1L饱和 溶液(浓度为1.7mol/L)处理。若使
溶液(浓度为1.7mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理_______ 次。[提示: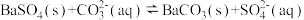 ,
,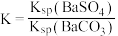 ,
,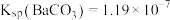 ]
]
(5)已知: (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
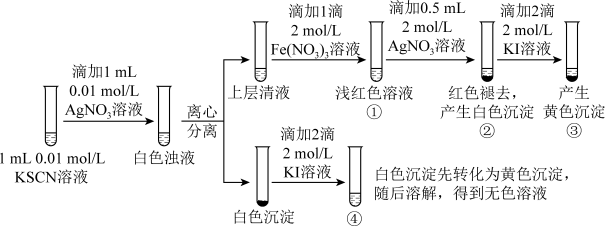
下列说法中不正确的是__________
①中现象能说明 与
与 生成的白色浊液中存在沉淀溶解平衡
生成的白色浊液中存在沉淀溶解平衡
②中现象产生的原因是发生了反应: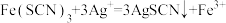
③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小
④中黄色沉淀溶解的原因可能是AgI与KI溶液中的 进一步发生了反应
进一步发生了反应
(1)将
 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是(2)已知草酸是二元弱酸,常温下测得0.1mol/L的
 的pH为4.8,则此
的pH为4.8,则此 溶液中
溶液中
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。(3)某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。出现上述现象的原因是
(4)
 、
、 两种温度下
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
①

 (填“>”“<”或“=”),
(填“>”“<”或“=”), 温度时
温度时
②根据
 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是A.加入
 固体可由a点变为b点
固体可由a点变为b点B.
 温度下,在
温度下,在 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成C.蒸发溶剂可能由d点变为
 曲线上a、b之间(不含a、b)的某一点
曲线上a、b之间(不含a、b)的某一点D.升温可由b点变为d点
③
 温度时,现有0.2mol的
温度时,现有0.2mol的 沉淀,每次用1L饱和
沉淀,每次用1L饱和 溶液(浓度为1.7mol/L)处理。若使
溶液(浓度为1.7mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理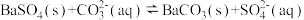 ,
,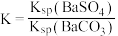 ,
,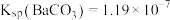 ]
](5)已知:
 (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
下列说法中不正确的是
①中现象能说明
 与
与 生成的白色浊液中存在沉淀溶解平衡
生成的白色浊液中存在沉淀溶解平衡②中现象产生的原因是发生了反应:
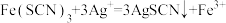
③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小
④中黄色沉淀溶解的原因可能是AgI与KI溶液中的
 进一步发生了反应
进一步发生了反应
您最近一年使用:0次



