根据下列各图曲线表征的信息,得出的结论不正确的是
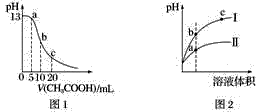


| A.图1表示常温下向体积为10 mL 0.1 mol·L−1NaOH溶液中逐滴加入0.1 mol·L−1CH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH−) |
| B.图2表示用水稀释pH相同的盐酸和醋酸时溶液的pH变化曲线,其中Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a |
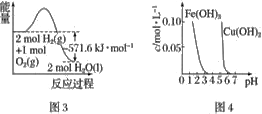
| C.图3表示H2与O2发生反应过程中的能量变化,H2的燃烧热为285.8 kJ·mol−1 |
| D.由图4得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入适量CuO,调节溶液的pH至4左右 |
14-15高三下·甘肃兰州·阶段练习 查看更多[16]
新疆乌苏市第一中学2020-2021学年高二下学期入学检测化学(1-3班)试题甘肃省兰州市第一中学2020-2021学年高二上学期期末考试化学试题【懂做原理题】2020届高三化学选修4二轮专题练——酸碱中和滴定的综合考查【懂做原理题】2020届高三化学选修4二轮专题练——酸碱中和滴定【精编23题】【懂做原理题】2020届高三化学选修4二轮专题练——酸碱溶液中pH值的综合运算【精编23题】吉林省安图县第一中学2019届高三上学期期末考试化学试题【市级联考】山西省吕梁市2019届高三上学期期末考试模拟化学试题【全国百强校】黑龙江省鹤岗市第一中学2019届高三上学期第三次月考化学试题【全国百强校】吉林省实验中学2019届高三上学期第三次月考化学试题辽宁省丹东市2018届高三一模考试理综-化学试题河北省定州中学2018届高三上学期高中毕业班期末考试化学试题黑龙江省牡丹江市第一高级中学2018届高三上学期期末考试化学试题山东省菏泽市第一中学2018届高三12月月考化学试题2016届河北省晋州一中高三上学期期末理综化学试卷2015届四川省南充市高三第三次高考适应性考试理综化学试卷2015届甘肃省兰州市高三下学期诊断考试理综化学试卷
更新时间:2016-12-09 10:55:31
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】在催化剂作用下,CO和H2合成CH3OH的历程如图所示(*表示物种被吸附在催化剂表面)。下列叙述错误的是
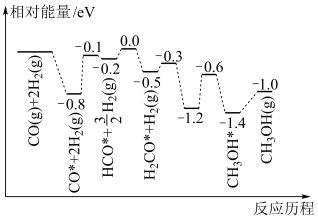

| A.合成甲醇正反应的△H<0 |
B.速控步骤为CO*+2H2(g)=HCO*+ H2(g) H2(g) |
| C.在相同条件下,CH3OH*比CH3OH(g)稳定 |
| D.总反应过程中只断裂σ键和形成σ键 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中●和○代表不同元素的原子。不正确 的是
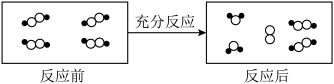
| A.反应物总能量一定低于生成物总能量 | B.一定属于可逆反应 |
| C.一定有非极性共价键断裂 | D.一定属于氧化还原反应 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】以CO和 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为甲醇。
转化为甲醇。
已知:①
 kJ·mol
kJ·mol
②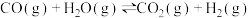
 kJ·mol
kJ·mol
③
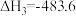 kJ·mol
kJ·mol
下列说法不正确 的是
 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为甲醇。
转化为甲醇。已知:①

 kJ·mol
kJ·mol
②
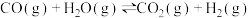
 kJ·mol
kJ·mol
③

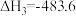 kJ·mol
kJ·mol
下列说法
A.若温度不变,反应①中生成1 mol  时,放出的热量大于90.5 kJ 时,放出的热量大于90.5 kJ |
B. 与 与 合成甲醇的热化学方程式为: 合成甲醇的热化学方程式为:  kJ·mol kJ·mol |
C.通过电解制 和选用高效催化剂,可降低 和选用高效催化剂,可降低 与 与 合成甲醇反应的焓变 合成甲醇反应的焓变 |
D.以 和 和 为原料合成甲醇,同时生成 为原料合成甲醇,同时生成 ,该反应需要吸收能量 ,该反应需要吸收能量 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
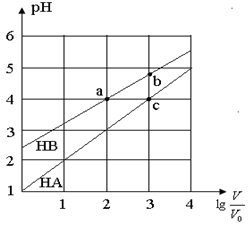
【推荐1】常温下,浓度均为0.10 mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随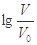 的变化如图所示,下列叙述正确的是
的变化如图所示,下列叙述正确的是
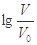 的变化如图所示,下列叙述正确的是
的变化如图所示,下列叙述正确的是
| A.该温度下HB的电离平衡常数a < b |
| B.溶液中水的电离程度:a=c>b |
| C.相同条件下NaA溶液的pH小于NaB溶液的pH |
D.当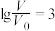 时,若同时微热两种溶液(不考虑HA、HB和H2O的挥发),则 时,若同时微热两种溶液(不考虑HA、HB和H2O的挥发),则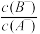 减小 减小 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列图示与对应的叙述相符的是
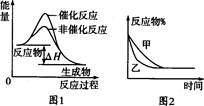
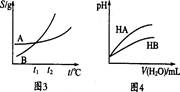


| A.图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
B.图2表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,甲的压强比乙的压强大 3C(g)+D(s)的影响,甲的压强比乙的压强大 |
| C.图3表示A、B两物质的溶解度随温度变化的情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A |
| D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】常温时,l mol·L-1的HClO2和1 mol·L-1的HMnO4两种溶液,起始时的体积均为V0,分别向两溶液中加水稀释至体积为V,所得曲线如图所示。下列说法正确的是
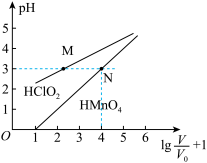

| A.当稀释至pH均为3时,溶液中c(ClO2-)>c(MnO4-) |
B.在0≤pH≤5时,HMnO4溶液满足:pH= |
| C.等pH的HClO2和HMnO4分别与足量Zn反应放出H2的体积HClO2>HMnO4 |
| D.稀释前分别用l mol·L-1的NaOH溶液中和,消耗NaOH溶液的体积:HMnO4>HClO2 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,向10mL0.05mol·L-1的某酸H2B溶液中滴入0.1mol·L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。下列说法不正确 的是
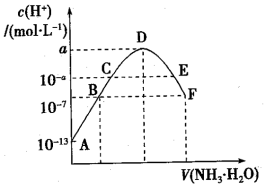

| A.常温下,0.1mol·L-1KHB溶液的pH=1 |
| B.过程中,随着氨水的加入,溶液pH先增后减 |
| C.D、E、F三点中,D点水的电离程度最大 |
D.B点溶液呈酸性,F点溶液c(NH )=2c(B2-) )=2c(B2-) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在某温度时,将nmol/L氨水滴入10mL 盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是
盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是

 盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是
盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是
A.25℃时, 电离常数为 电离常数为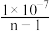 (用n表示) (用n表示) |
B.b点盐酸与氨水恰好完全反应: |
| C.保持温度不变,往0.1mol/L氨水中加水稀释,溶液中各离子浓度均减少 |
| D.a、b、c、d中,c点水的电离程度最大 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温时,用NaOH固体调节0.1mol·L-1的H3AsO4溶液的pH,忽略溶液体积的变化,各含砷微粒的分布分数随pH的变化关系如图所示。下列说法错误的是


A.曲线②④分别代表H2AsO 和AsO 和AsO 的分布分数 的分布分数 |
| B.W、Q、R三点对应溶液中水的电离程度最大的是R点 |
C.R点对应溶液中c(Na+)<c(H2AsO )+5c(AsO )+5c(AsO ) ) |
| D.M点对应溶液的pH=9.22 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】工业上应用两矿法浸出软锰矿(主要成分 )和方铅矿(主要成分PbS、
)和方铅矿(主要成分PbS、 ),制备
),制备 和
和 ,转化流程如下。
,转化流程如下。

已知: 微溶于水,溶液中存在可逆反应:
微溶于水,溶液中存在可逆反应: 。
。
下列说法正确的是
 )和方铅矿(主要成分PbS、
)和方铅矿(主要成分PbS、 ),制备
),制备 和
和 ,转化流程如下。
,转化流程如下。
已知:
 微溶于水,溶液中存在可逆反应:
微溶于水,溶液中存在可逆反应: 。
。下列说法正确的是
| A.Ⅰ中可使用浓盐酸代替稀盐酸和NaCl的混合溶液 |
B.Ⅱ中生成的沉淀Y是 |
| C.Ⅳ中试剂X可能作氧化剂 |
D.Ⅴ中发生反应: |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列解释实验现象的反应方程式正确的是
| A.切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2=Na2O2 |
| B.向AgC1悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2- =Ag2S↓+2Cl- |
| C.Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+CO2=2Na2CO3+O2 |
| D.FeCl2溶液中滴加NaClO溶液生成红褐色沉淀:2Fe2+ + ClO- + 5H2O= 2Fe(OH)3↓+Cl-+ 4H+ |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐3】下列图示与对应的叙述不相符的是


| A.图1表示同温度下,pH=1 的盐酸和醋酸溶液分别加水稀释时pH 的变化曲线,其中曲线Ⅱ为醋酸,且a 点溶液的导电性比b 点强 |
| B.图2 中纯水仅升高温度,不能使a点变到c点 |
| C.图3 表示25 ℃时,用0.100 0 mol・L-1HCl 滴定20 mL 0.100 0 mol・L-1NaOH 溶液,溶液的pH随加入盐酸体积的变化 |
| D.用0.010 0 mol・L-1AgNO3标准溶液滴定浓度均为0.100 0 mol・L-1Cl-、Br-及I-的混合溶液,由图4 曲线,可确定首先沉淀的是I- |
您最近半年使用:0次



