科学处理NOx、SO2等大气污染物,对改善人们的生存环境具有重要的现实意义。
(1)利用甲烷催化还原氮氧化物。已知:
CH4(g) +4NO2(g) =4NO(g)+CO2(g) +2H2O(g);△H=-574kJ•mol-1
CH4(g)+2NO2(g)=N2(g) +CO2(g)+2H2O(g);△H=-867kJ•mol-1
则CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=____________________
(2)利用氧化氮氧化物的流程如下:
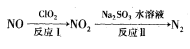
已知反应I的化学方程式为2NO+ClO2+H2O=NO2+HNO3+HCl,若反应I中转移3mol电子,则反应Ⅱ中可生成N2的体积为_____ L(标准状况下)。
(3)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离程度_____ (填“增大”、“减小”或“不变”);请写出Na2SO3溶液中,c(Na+)、c(H2SO3)、c(SO32-)、c(HSO3-)的大小关系:_____ 。
(4)利用Fe2(SO4)3溶液也可处理SO2废气,所得Fe2+溶液有很多重要用途。保存1.8mol•L﹣1的FeSO4溶液时,为防止溶液中Fe2+被氧化,常加入_____ ;为确保溶液中不出现浑浊,应调节溶液的pH不超过_____ 。(常温下,Ksp[Fe(OH) 2]=1.8×10﹣16)
(1)利用甲烷催化还原氮氧化物。已知:
CH4(g) +4NO2(g) =4NO(g)+CO2(g) +2H2O(g);△H=-574kJ•mol-1
CH4(g)+2NO2(g)=N2(g) +CO2(g)+2H2O(g);△H=-867kJ•mol-1
则CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=
(2)利用氧化氮氧化物的流程如下:
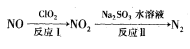
已知反应I的化学方程式为2NO+ClO2+H2O=NO2+HNO3+HCl,若反应I中转移3mol电子,则反应Ⅱ中可生成N2的体积为
(3)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离程度
(4)利用Fe2(SO4)3溶液也可处理SO2废气,所得Fe2+溶液有很多重要用途。保存1.8mol•L﹣1的FeSO4溶液时,为防止溶液中Fe2+被氧化,常加入
更新时间:2018-11-20 15:54:01
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】常见物质之间的转化如下图所示:
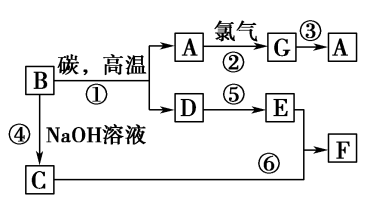
其中B常被用于制造光导纤维,其对应的单质的结构与金刚石的结构是相似的;C、F均含有A物质所含元素;反应中生成的水及次要产物均已略去。
(1)试推测:A________ ,C________ ,F________ 。(写化学式)
(2)试写出反应⑥的离子方程式:_________________________ 。
(3)在反应①中,碳的作用是____________________ ,当生成1 mol A时,转移电子的物质的量为________ 。

其中B常被用于制造光导纤维,其对应的单质的结构与金刚石的结构是相似的;C、F均含有A物质所含元素;反应中生成的水及次要产物均已略去。
(1)试推测:A
(2)试写出反应⑥的离子方程式:
(3)在反应①中,碳的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】高铁酸钠( )是一种新型水处理剂,它能在杀菌消毒的同时生成氢氧化铁胶体而净水。某兴趣小组欲利用废金属屑(主要成分为
)是一种新型水处理剂,它能在杀菌消毒的同时生成氢氧化铁胶体而净水。某兴趣小组欲利用废金属屑(主要成分为 和
和 ,含有少量
,含有少量 )制取高铁酸钠并回收金属Cu,其工艺流程如下:
)制取高铁酸钠并回收金属Cu,其工艺流程如下:
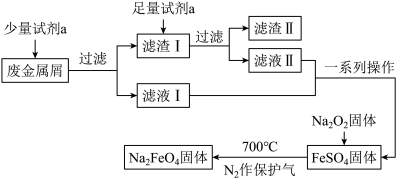
(1)试剂a为_______ (填化学式),滤渣Ⅱ的主要成分为_______ 。
(2)在过滤操作中要使用玻璃棒,其作用是_______ 。
(3)滤液Ⅰ中含有的金属离子是_______ (填离子符号)。检验滤液Ⅰ中是否存在 的实验方法是
的实验方法是_______ 。
(4)加入少量试剂a后发生反应的离子方程式为_______ 。
(5)制备 的反应原理是:
的反应原理是: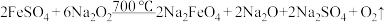 。当反应中转移电子总数约为
。当反应中转移电子总数约为 时,则生成
时,则生成 的物质的量为
的物质的量为_______  。
。
 )是一种新型水处理剂,它能在杀菌消毒的同时生成氢氧化铁胶体而净水。某兴趣小组欲利用废金属屑(主要成分为
)是一种新型水处理剂,它能在杀菌消毒的同时生成氢氧化铁胶体而净水。某兴趣小组欲利用废金属屑(主要成分为 和
和 ,含有少量
,含有少量 )制取高铁酸钠并回收金属Cu,其工艺流程如下:
)制取高铁酸钠并回收金属Cu,其工艺流程如下:
(1)试剂a为
(2)在过滤操作中要使用玻璃棒,其作用是
(3)滤液Ⅰ中含有的金属离子是
 的实验方法是
的实验方法是(4)加入少量试剂a后发生反应的离子方程式为
(5)制备
 的反应原理是:
的反应原理是: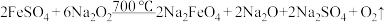 。当反应中转移电子总数约为
。当反应中转移电子总数约为 时,则生成
时,则生成 的物质的量为
的物质的量为 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】化学工业中会产生大量含铬废水,需进行无害化处理检测达标后才能排放。
(1)工业含铬废水中铬常以 形式存在,可按下列流程来除去废水中的铬。
形式存在,可按下列流程来除去废水中的铬。
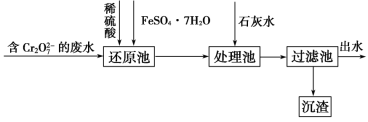
①石灰水处理后生成的沉淀有________ (填化学式)。
②现处理1×102 L含铬元素39 mg·L−1的废水(假设铬元素的存在形式全部为 ),需要绿矾
),需要绿矾________ g。
(2)废水中铬元素总浓度的测定方法如下:向一定量含 和Cr3+的酸性废水样中加入足量(NH4)2S2O8溶液将Cr3+氧化成
和Cr3+的酸性废水样中加入足量(NH4)2S2O8溶液将Cr3+氧化成 ,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,
,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液, 与I−完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系如下:
与I−完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系如下:
Cr3+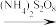

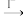 I2
I2

①上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会__________ (填“偏大”“偏小”或“不变”)。
②准确移取含 和Cr3+的酸性废水样100.00 mL,按上述方法测定废水样中铬元素总浓度,消耗0.010 0 mol·L−1 Na2S2O3标准溶液27.00 mL。计算该废水中铬元素总浓度(以mg·L−1表示,写出计算过程)
和Cr3+的酸性废水样100.00 mL,按上述方法测定废水样中铬元素总浓度,消耗0.010 0 mol·L−1 Na2S2O3标准溶液27.00 mL。计算该废水中铬元素总浓度(以mg·L−1表示,写出计算过程)_____________ 。
(1)工业含铬废水中铬常以
 形式存在,可按下列流程来除去废水中的铬。
形式存在,可按下列流程来除去废水中的铬。
①石灰水处理后生成的沉淀有
②现处理1×102 L含铬元素39 mg·L−1的废水(假设铬元素的存在形式全部为
 ),需要绿矾
),需要绿矾(2)废水中铬元素总浓度的测定方法如下:向一定量含
 和Cr3+的酸性废水样中加入足量(NH4)2S2O8溶液将Cr3+氧化成
和Cr3+的酸性废水样中加入足量(NH4)2S2O8溶液将Cr3+氧化成 ,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,
,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液, 与I−完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系如下:
与I−完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系如下:Cr3+
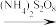

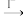 I2
I2

①上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会
②准确移取含
 和Cr3+的酸性废水样100.00 mL,按上述方法测定废水样中铬元素总浓度,消耗0.010 0 mol·L−1 Na2S2O3标准溶液27.00 mL。计算该废水中铬元素总浓度(以mg·L−1表示,写出计算过程)
和Cr3+的酸性废水样100.00 mL,按上述方法测定废水样中铬元素总浓度,消耗0.010 0 mol·L−1 Na2S2O3标准溶液27.00 mL。计算该废水中铬元素总浓度(以mg·L−1表示,写出计算过程)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I、甲醇是重要的化工原料,又可称为燃料.利用合成气(主要成分为 、
、 和
和 )在催化剂的作用下合成甲醇,发生的主反应如下:
)在催化剂的作用下合成甲醇,发生的主反应如下:
①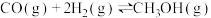

②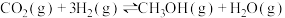
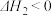
③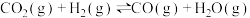
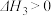
回答下列问题:
(1)反应①的化学平衡常数 的表达式为
的表达式为_______ ;
_______  (填“
(填“ ”、“
”、“ ”)图1中能正确反映反应①平衡常数
”)图1中能正确反映反应①平衡常数 随温度变化关系的曲线为
随温度变化关系的曲线为_______ (填曲线标记字母),其判断理由是_______________________ .
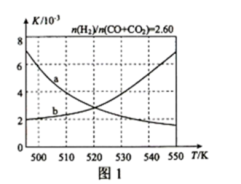
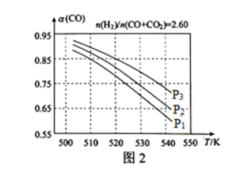
(2)合成气的组成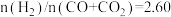 时,体系中的
时,体系中的 平衡转化率(
平衡转化率( )与温度和压强的关系如图2所示.
)与温度和压强的关系如图2所示.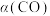 值随温度升高而
值随温度升高而______ (填“增大”或“减小”).图2中的压强由大到小为______ .
II、 是一种廉价的碳资源,其综合利用具有重要意义.反应②在容积为
是一种廉价的碳资源,其综合利用具有重要意义.反应②在容积为 的恒容密闭容器中,充入
的恒容密闭容器中,充入
 和
和
 ,测得反应物
,测得反应物 和
和 的浓度随时间的变化如图所示:
的浓度随时间的变化如图所示:
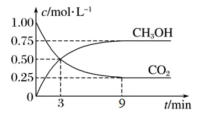
(3)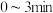 内,
内,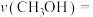
______ (保留两位小数)
(4)平衡时 转化率为
转化率为______
(5)该温度下,反应平衡常数
______ (保留一位小数)。
 、
、 和
和 )在催化剂的作用下合成甲醇,发生的主反应如下:
)在催化剂的作用下合成甲醇,发生的主反应如下:①
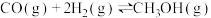

②
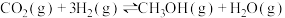
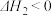
③
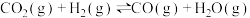
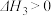
回答下列问题:
(1)反应①的化学平衡常数
 的表达式为
的表达式为
 (填“
(填“ ”、“
”、“ ”)图1中能正确反映反应①平衡常数
”)图1中能正确反映反应①平衡常数 随温度变化关系的曲线为
随温度变化关系的曲线为

(2)合成气的组成
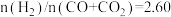 时,体系中的
时,体系中的 平衡转化率(
平衡转化率( )与温度和压强的关系如图2所示.
)与温度和压强的关系如图2所示.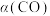 值随温度升高而
值随温度升高而II、
 是一种廉价的碳资源,其综合利用具有重要意义.反应②在容积为
是一种廉价的碳资源,其综合利用具有重要意义.反应②在容积为 的恒容密闭容器中,充入
的恒容密闭容器中,充入
 和
和
 ,测得反应物
,测得反应物 和
和 的浓度随时间的变化如图所示:
的浓度随时间的变化如图所示:
(3)
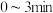 内,
内,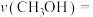
(4)平衡时
 转化率为
转化率为(5)该温度下,反应平衡常数

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】汽车排放的尾气是大气污染气体之一。如何减少污染气体的排放是科学家研究的热门课题。请回答下列问题:
(1)已知:CO的燃烧热为283.0kJ·mol−1,N2(g)+2O2(g) =2NO2(g) ΔH=+64kJ·mol−1,则NO2(g)+2CO(g)= N2(g)+2CO2(g) ΔH=
N2(g)+2CO2(g) ΔH=___ kJ·mol−1,若反应中有14g还原剂发生反应,则转移电子___ mol。
(2)使汽车排放的CO和NO在一定条件下发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6molNO、8molCO充入10L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6molNO、8molCO充入10L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
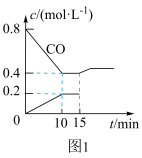
①该反应的化学平衡常数K=___ 。NO的平衡转化率=___ 。
②15min时,若改变反应条件,导致CO浓度发生如图1所示的变化,则改变的条件可能是___ 。
a.缩小容器体积b.增加CO2的量c.体积不变通入少量氩气d.加入催化剂
③当NO与CO的起始浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图2所示,则下列说法正确的是___ 。
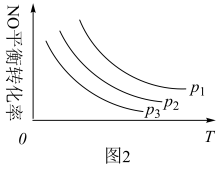
A.该反应ΔH<0 B.p1<p2<p3
C.升高温度正反应速率减小,逆反应速率增大 D.温度不变,增大压强,平衡常数增大
④以下说法中能判断反应2NO(g)+2CO(g) N2(g)+2CO2(g)达到平衡的是
N2(g)+2CO2(g)达到平衡的是___ 。
A.反应物和生成物的物质的量相等 B.单位时间内消耗1molNO同时生成1molCO2
C.混合气体压强不再发生变化 D.NO的浓度不再变化
⑤向反应容器中再分别充入下列气体,能使NO转化率增大的是___ 。
A.O2 B.N2 C.CO D.NO
(1)已知:CO的燃烧热为283.0kJ·mol−1,N2(g)+2O2(g) =2NO2(g) ΔH=+64kJ·mol−1,则NO2(g)+2CO(g)=
 N2(g)+2CO2(g) ΔH=
N2(g)+2CO2(g) ΔH=(2)使汽车排放的CO和NO在一定条件下发生反应:2NO(g)+2CO(g)
 N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6molNO、8molCO充入10L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6molNO、8molCO充入10L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
①该反应的化学平衡常数K=
②15min时,若改变反应条件,导致CO浓度发生如图1所示的变化,则改变的条件可能是
a.缩小容器体积b.增加CO2的量c.体积不变通入少量氩气d.加入催化剂
③当NO与CO的起始浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图2所示,则下列说法正确的是

A.该反应ΔH<0 B.p1<p2<p3
C.升高温度正反应速率减小,逆反应速率增大 D.温度不变,增大压强,平衡常数增大
④以下说法中能判断反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)达到平衡的是
N2(g)+2CO2(g)达到平衡的是A.反应物和生成物的物质的量相等 B.单位时间内消耗1molNO同时生成1molCO2
C.混合气体压强不再发生变化 D.NO的浓度不再变化
⑤向反应容器中再分别充入下列气体,能使NO转化率增大的是
A.O2 B.N2 C.CO D.NO
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)⇌CH3OH(g)△H1
②CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)⇌CO(g)+H2O(g)△H3
回答下列问题:
(1)已知△H1=﹣99kJ·mol﹣1,已知△H2=﹣58kJ·mol﹣1,则△H3=______ kJ·mol﹣1。
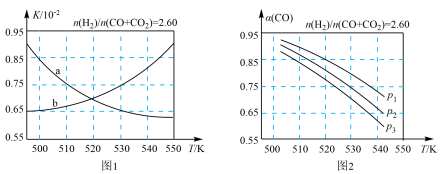
(2)反应①的化学平衡常数K的表达式为______ ;图1中能正确反映平衡常数K随温度变化关系的曲线为________ (填曲线标记字母)。
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(a)与温度和压强的关系如图2所示。a(CO)值随温度升高而________ (填“增大”或“减小”)图2中的压强由大到小为________ 。
①CO(g)+2H2(g)⇌CH3OH(g)△H1
②CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)⇌CO(g)+H2O(g)△H3
回答下列问题:
(1)已知△H1=﹣99kJ·mol﹣1,已知△H2=﹣58kJ·mol﹣1,则△H3=
(2)反应①的化学平衡常数K的表达式为
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(a)与温度和压强的关系如图2所示。a(CO)值随温度升高而

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】完成下列问题
(1)磷是重要的元素,能形成多种含氧酸和含氧酸盐。亚磷酸(H3PO3)的结构如图,亚磷酸可由PCl3水解而成,H3PO3溶液存在电离平衡:H3PO3 H++H2PO
H++H2PO ,H2PO
,H2PO
 H++HPO
H++HPO

回答下列问题:
①Na2HPO3属于___________ (填“正盐”或“酸式盐”)。
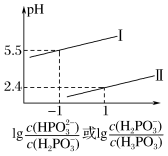
②常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示 的是曲线
的是曲线___________ (填“I”或“Ⅱ”),亚磷酸(H3PO3)的Ka2=___________ 。
(2)25℃时,部分弱碱、弱酸的电离平衡常数如下表:
①向Na2CO3溶液中加入少量的H3PO4溶液反应的离子方程式是___________ 。
②0.1mol/L的NH4NO2溶液中离子浓度大小关系是___________ 。
(3)常温下,将pH=10的Ba(OH)2溶液与pH=5的稀盐酸混合,然后保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为___________ 。(100℃时:Kw=10-12)
(4)已知:Ksp(AgBr)=5.4×10−13,Ksp(AgCl)=1.8×10−10,向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, =
=___________ 。
(5)已知在25℃时,Ksp[Mg(OH)2]=3.2×10−11.25℃时,向0.02 mol∙L−1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的pH最小是___________ (已知lg2=0.3)。
(1)磷是重要的元素,能形成多种含氧酸和含氧酸盐。亚磷酸(H3PO3)的结构如图,亚磷酸可由PCl3水解而成,H3PO3溶液存在电离平衡:H3PO3
 H++H2PO
H++H2PO ,H2PO
,H2PO
 H++HPO
H++HPO

回答下列问题:
①Na2HPO3属于
②常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示
 的是曲线
的是曲线
(2)25℃时,部分弱碱、弱酸的电离平衡常数如下表:
| 弱酸 | NH3·H2O | HNO2 | H2CO3 | H3PO4 |
| 电离平衡常数(25℃) | Kb=1.8×10-5 | Ka=5.0×10-4 | Ka1=4.0×10-7 Ka2=5.0×10-11 | Ka1=8.0×10-3 Ka2=6.0×10-8 Ka3=2.0×10-13 |
②0.1mol/L的NH4NO2溶液中离子浓度大小关系是
(3)常温下,将pH=10的Ba(OH)2溶液与pH=5的稀盐酸混合,然后保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为
(4)已知:Ksp(AgBr)=5.4×10−13,Ksp(AgCl)=1.8×10−10,向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
 =
=(5)已知在25℃时,Ksp[Mg(OH)2]=3.2×10−11.25℃时,向0.02 mol∙L−1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的pH最小是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
真题
解题方法
【推荐2】随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
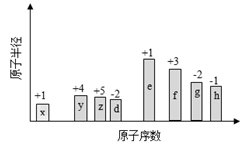
根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________ 。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_______ >__________ ;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______ >__________ 。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________ 。
(4)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:___________________ 。
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
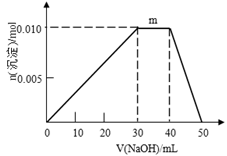
①R离子浓度由大到小的顺序是:__________ 。
②写出m点反应的离子方程式_________________ 。
③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为______ mol。

根据判断出的元素回答问题:
(1)f在元素周期表的位置是
(2)比较d、e常见离子的半径的小(用化学式表示,下同)
(3)任选上述元素组成一种四原子共价化合物,写出其电子式
(4)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:

①R离子浓度由大到小的顺序是:
②写出m点反应的离子方程式
③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)在恒温条件下,1 mol NO2和足量C发生反应:2NO2(g)+2C(s) N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
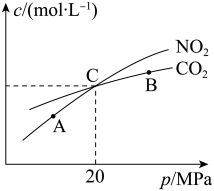
①A B两点的浓度平衡常数关系:Kc(A)___________ Kc(B)(填“<”或“>”或“=”)。
②A B C三点中NO2的转化率最高的是___________ (填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp=___________ (写出计算结果,Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。
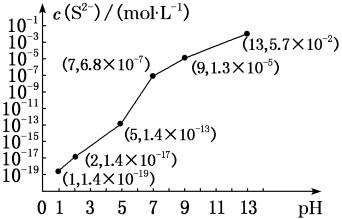
①pH=13时,溶液中的c(H2S)+c(HS-)=___________ mol·L-1;
②某溶液含0.010 mol·L-1Fe2+和0.10 mol·L-1H2S,当溶液pH=___________ 时,Fe2+开始沉淀。【已知:KSP(FeS)=1.4×10-19】
(3)常温下,将pH=a的醋酸溶液与pH=b的NaOH溶液等体积混合后,两者恰好完全反应,则该温度下醋酸的电离平衡常数约为___________ 。
(1)在恒温条件下,1 mol NO2和足量C发生反应:2NO2(g)+2C(s)
 N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
①A B两点的浓度平衡常数关系:Kc(A)
②A B C三点中NO2的转化率最高的是
③计算C点时该反应的压强平衡常数Kp=
(2)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。

①pH=13时,溶液中的c(H2S)+c(HS-)=
②某溶液含0.010 mol·L-1Fe2+和0.10 mol·L-1H2S,当溶液pH=
(3)常温下,将pH=a的醋酸溶液与pH=b的NaOH溶液等体积混合后,两者恰好完全反应,则该温度下醋酸的电离平衡常数约为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】NiC2O4·2H2O主要用于生产镍催化剂,也可用于生产超细氧化镍。从某含镍废渣(主要含Ni、NiO、Fe2O3,还含有少量油脂、Mn2O3等)制备NiC2O4·2H2O的工艺流程如下:
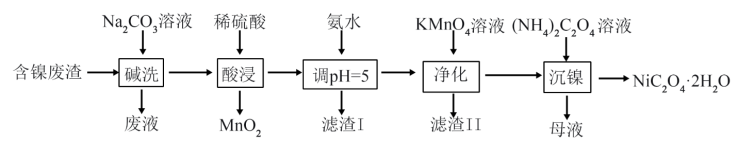
已知:①酸浸后溶液中金属离子有Ni2+、Mn2+、Fe3+;本流程中,Ni2+不被氧化。
②在pH=5时,KMnO4的还原产物为MnO2;
③常温时,Ksp[Fe(OH)3]=1.0×10-39,Ksp[Mn(OH)2]=4.0×10-14,溶液中离子的浓度小于1×10-5认为已除尽;
④Ni2++H2Y2-=[NiY]2-+2H+;紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
回答下列问题:
(1)“碱洗”工序中,加入Na2CO3溶液后应加热煮沸5min,煮沸的目的为_______ 。
(2)“酸浸”工序中Mn2O3发生反应的化学方程式为_______ 。
(3)滤渣I的主要成分为_______ (填化学式),该物质中的金属阳离子在溶液中的残留浓度为_______ mol·L-1。
(4)“净化”工序中加入KMnO4溶液时发生反应的离子方程式为_______ 。
(5)“沉镍”工序中,与选用Na2C2O4溶液相比,选用等浓度的(NH4)2C2O4溶液会大大降低产品中的氢氧化镍杂质含量,原因为_______ 。
(6)测定NiC2O4·2H2O产品中镍元素的含量:取2.500g样品,用硫酸溶解后配成250mL溶液,取25.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.1000mol/L的Na2H2Y溶液进行滴定,达到滴定终点时消耗Na2H2Y溶液的体积12.50mL。达到滴定终点的实验现象为_______ ,NiC2O4·2H2O产品中镍元素的含量为_______ %。

已知:①酸浸后溶液中金属离子有Ni2+、Mn2+、Fe3+;本流程中,Ni2+不被氧化。
②在pH=5时,KMnO4的还原产物为MnO2;
③常温时,Ksp[Fe(OH)3]=1.0×10-39,Ksp[Mn(OH)2]=4.0×10-14,溶液中离子的浓度小于1×10-5认为已除尽;
④Ni2++H2Y2-=[NiY]2-+2H+;紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
回答下列问题:
(1)“碱洗”工序中,加入Na2CO3溶液后应加热煮沸5min,煮沸的目的为
(2)“酸浸”工序中Mn2O3发生反应的化学方程式为
(3)滤渣I的主要成分为
(4)“净化”工序中加入KMnO4溶液时发生反应的离子方程式为
(5)“沉镍”工序中,与选用Na2C2O4溶液相比,选用等浓度的(NH4)2C2O4溶液会大大降低产品中的氢氧化镍杂质含量,原因为
(6)测定NiC2O4·2H2O产品中镍元素的含量:取2.500g样品,用硫酸溶解后配成250mL溶液,取25.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.1000mol/L的Na2H2Y溶液进行滴定,达到滴定终点时消耗Na2H2Y溶液的体积12.50mL。达到滴定终点的实验现象为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是______________ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式______________ 。
(2)“滤液②”中含有的金属离子是______________ 。
(3)“转化”中可替代H2O2的物质是______________ 。若工艺流程改为先“调pH”后“转化”,即
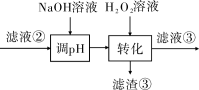
“滤液③”中可能含有的杂质离子为______________ 。
(4)利用上述表格数据,计算Ni(OH)2的Ksp=______________ (列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L−1,则“调pH”应控制的pH范围是______________ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式______________ 。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01 mol·L−1)的pH 沉淀完全时(c=1.0×10−5 mol·L−1)的pH | 7.2 8.7 | 3.7 4.7 | 2.2 3.2 | 7.5 9.0 |
(1)“碱浸”中NaOH的两个作用分别是
(2)“滤液②”中含有的金属离子是
(3)“转化”中可替代H2O2的物质是

“滤液③”中可能含有的杂质离子为
(4)利用上述表格数据,计算Ni(OH)2的Ksp=
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】五氧化二钒主要用作合金添加剂,含钒钢具有强度高,韧性大,耐磨性好等优良特性。工业上常用炼钢残渣(主要含 及少量铁粉、
及少量铁粉、 、
、 、
、 等杂质)为原料制取
等杂质)为原料制取 的一种工艺流程如图所示:
的一种工艺流程如图所示: 难溶于水,
难溶于水, 。
。
回答下列问题:
(1)基态钒原子的价层电子排布式为___________ 。
(2)“焙烧”时通入大量空气的作用是___________ 。
(3)“碱浸”所得滤渣的主要成分是___________ 。
(4)写出“沉硅、铝”反应的离子方程式:___________ 、___________ 。
(5)若滤液中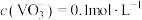 ,为使钒元素沉淀率达到
,为使钒元素沉淀率达到 ,应使“沉钒”后溶液中的
,应使“沉钒”后溶液中的 不低于
不低于___________ 。
(6)“沉钒”析出的 晶体需要洗涤,证明
晶体需要洗涤,证明 已洗涤干净的实验操作及现象为
已洗涤干净的实验操作及现象为___________ 。
(7)在空气中“煅烧”生成的气体可直接排放到空气中,写出反应的化学方程式:___________ 。
 及少量铁粉、
及少量铁粉、 、
、 、
、 等杂质)为原料制取
等杂质)为原料制取 的一种工艺流程如图所示:
的一种工艺流程如图所示: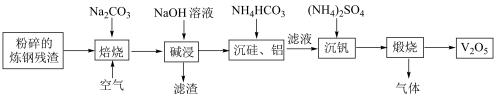
 难溶于水,
难溶于水, 。
。回答下列问题:
(1)基态钒原子的价层电子排布式为
(2)“焙烧”时通入大量空气的作用是
(3)“碱浸”所得滤渣的主要成分是
(4)写出“沉硅、铝”反应的离子方程式:
(5)若滤液中
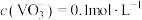 ,为使钒元素沉淀率达到
,为使钒元素沉淀率达到 ,应使“沉钒”后溶液中的
,应使“沉钒”后溶液中的 不低于
不低于(6)“沉钒”析出的
 晶体需要洗涤,证明
晶体需要洗涤,证明 已洗涤干净的实验操作及现象为
已洗涤干净的实验操作及现象为(7)在空气中“煅烧”生成的气体可直接排放到空气中,写出反应的化学方程式:
您最近一年使用:0次



