常温下,某浓度H2A溶液中滴加NaOH溶液,若定义pC=﹣lgC,则测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是( )


| A.曲线II表示pC(HA-)随pH的变化 |
B.常温下,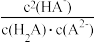 =104.50 =104.50 |
| C.将等浓度等体积的Na2A与H2A溶液混合后,溶液显碱性 |
| D.a、b、c三点对应的溶液,c(HA-)+c(A2-)+c(HA)始终不变 |
19-20高三下·山东青岛·阶段练习 查看更多[3]
山东省青岛市莱西第一中学2020届高三下学期质量检测化学试题浙江省宁波市北仑中学2021-2022学年高二上学期期中考试化学(2-10班)试题(已下线)押广东卷化学第8题 电解质溶液-备战2022年高考化学临考题号押题(广东卷)
更新时间:2020-04-04 15:18:05
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列图示与对应的叙述相符的是
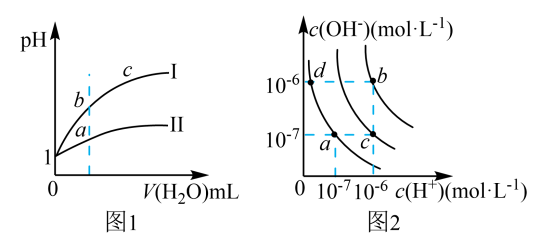

| A.图1表示相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.图1中,中和等体积的两种酸,消耗等浓度的NaOH溶液体积V(Ⅰ)>V(Ⅱ) |
| C.图2中纯水仅升高温度,就可以从a点变到c点 |
| D.图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下列说法不正确的是
| A.常温下,0.1 mol·L-1CH3COONa溶液的pH=8,则该溶液中 c(CH3COOH)=(10-6-10-8)mol·L—1 |
| B.对于相同浓度的弱酸HX和HY(前者的Ka较大)溶液,加水稀释相同倍数时,HY溶液的pH改变值大于HX溶液的pH改变值 |
C.硫酸钡固体在水中存在以下平衡BaSO4(s) Ba2+(aq)+SO42-(aq),当加入饱和碳酸钠溶液时可以生成BaCO3沉淀 Ba2+(aq)+SO42-(aq),当加入饱和碳酸钠溶液时可以生成BaCO3沉淀 |
D.常温下,a mol·L-1的CH3COOH溶液与0.01mol·L-1NaOH溶液等体积混合后溶液呈中性,此温度下醋酸的电离平衡常数Ka=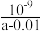 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】 时,将
时,将 气体缓慢通入
气体缓慢通入 的氨水中,溶液的
的氨水中,溶液的 、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [
、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [ ]的关系如下图所示。若忽略溶液体积变化,下列错误的是
]的关系如下图所示。若忽略溶液体积变化,下列错误的是
 时,将
时,将 气体缓慢通入
气体缓慢通入 的氨水中,溶液的
的氨水中,溶液的 、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [
、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [ ]的关系如下图所示。若忽略溶液体积变化,下列错误的是
]的关系如下图所示。若忽略溶液体积变化,下列错误的是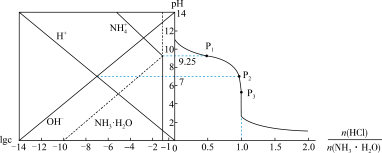
A. 时, 时, 的电离平衡常数为 的电离平衡常数为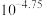 |
B. 时, 时,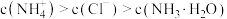 |
C. 所示溶液: 所示溶液: |
D.水的电离程度: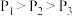 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】室温下,甘氨酸在水溶液中主要以NH -CH2-COO-、NH
-CH2-COO-、NH -CH2-COOH和NH2-CH2-COO-三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是
-CH2-COOH和NH2-CH2-COO-三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是

 -CH2-COO-、NH
-CH2-COO-、NH -CH2-COOH和NH2-CH2-COO-三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是
-CH2-COOH和NH2-CH2-COO-三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是
| A.a点溶液中,水的电离程度大于b点 |
B.c点溶液中,c(NH2-CH2-COO-)>c(NH -CH2-COO-) -CH2-COO-) |
C.NH -CH2-COO-+H2O⇌NH2-CH2-COO-+H3O+的平衡常数为x -CH2-COO-+H2O⇌NH2-CH2-COO-+H3O+的平衡常数为x |
D.a点溶液中,存在关系式:c(NH -CH2-COOH)+c(H+)=c(NH2-CH2-COO-)+c(OH-) -CH2-COOH)+c(H+)=c(NH2-CH2-COO-)+c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】根据下列图示得出的结论正确的是
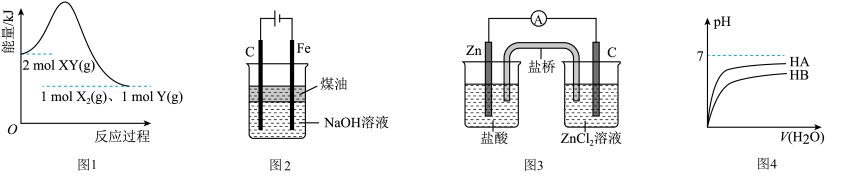

| A.由图1可判断该反应的反应物中化学键的总键能大于生成物中化学键的总键能 |
B.图2装置能制备 并能较长时间观察其颜色 并能较长时间观察其颜色 |
| C.图3装置中电流表指针发生明显偏转 |
D.由图4可证明图示条件下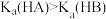 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】25℃时,用NaOH溶液分别滴定HX、CuSO4、FeSO4三种溶液,pM=lgM[M表示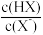 、c(Cu2+)、c(Fe2+)]等]随pH变化关系如图所示,其中③的M代表
、c(Cu2+)、c(Fe2+)]等]随pH变化关系如图所示,其中③的M代表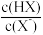 。已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列有关分析正确的是
。已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列有关分析正确的是
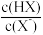 、c(Cu2+)、c(Fe2+)]等]随pH变化关系如图所示,其中③的M代表
、c(Cu2+)、c(Fe2+)]等]随pH变化关系如图所示,其中③的M代表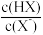 。已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列有关分析正确的是
。已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列有关分析正确的是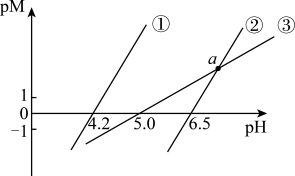
| A.①代表滴定FeSO4溶液的变化关系 |
| B.Ksp[Cu(OH)2]=10-15 |
| C.a点时,③中c(H+)与②中c(M)的关系为:c(H+)=10-5c(M) |
| D.Fe(OH)2、Cu(OH)2固体均易溶解于HX溶液 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】HA是一元弱酸,难溶盐MA的饱和溶液中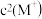 随c(H+)而变化,
随c(H+)而变化, 不发生水解。实验发现,
不发生水解。实验发现, 时
时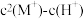 为线性关系,如下图中实线所示。
为线性关系,如下图中实线所示。
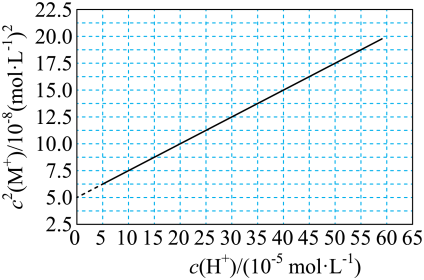
下列叙述错误的是
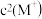 随c(H+)而变化,
随c(H+)而变化, 不发生水解。实验发现,
不发生水解。实验发现, 时
时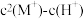 为线性关系,如下图中实线所示。
为线性关系,如下图中实线所示。
下列叙述错误的是
A.溶液 时, 时,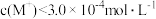 |
B.MA的溶度积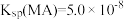 |
C.溶液 时, 时, |
D.HA的电离常数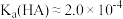 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】含硫各微粒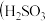 、
、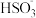 和
和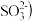 存在于
存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数
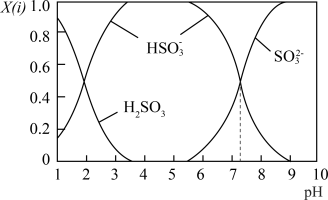
与NaOH溶液反应后的溶液中,它们的物质的量分数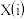 与溶液pH的关系如下图所示.下列说法正确的是
与溶液pH的关系如下图所示.下列说法正确的是
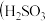 、
、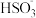 和
和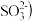 存在于
存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数
与NaOH溶液反应后的溶液中,它们的物质的量分数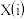 与溶液pH的关系如下图所示.下列说法正确的是
与溶液pH的关系如下图所示.下列说法正确的是 
A. 时,溶液中 时,溶液中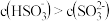 |
B. 时,溶液中 时,溶液中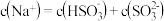 |
C.为获得尽可能纯的 ,可将溶液的pH控制在 ,可将溶液的pH控制在 左右 左右 |
D.由图中数据可估算出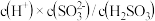 为 为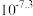 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
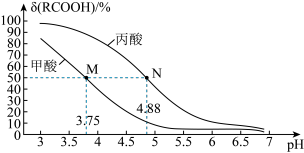
【推荐3】25 ℃时,改变0.1 mol/L弱酸RCOOH溶液的pH,溶液中RCOOH分子的物质的量分数δ(RCOOH)随之改变[已知δ(RCOOH)=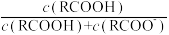 ],甲酸(HCOOH)与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
],甲酸(HCOOH)与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
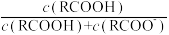 ],甲酸(HCOOH)与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
],甲酸(HCOOH)与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
| A.若弱酸pH增大是通过向弱酸中加入NaOH固体实现的,则图中M、N两点对应溶液中的c(Na+)相等 |
| B.对于甲酸和丙酸,当lg[c(RCOOH)/c(RCOO-)]>0时,溶液都为酸性 |
| C.等浓度的HCOONa和CH3CH2COONa两种溶液中的c(NaOH)相等 |
| D.将0.1 mol/L的HCOOH溶液与0.1 mol/L的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c(HCOO-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下,有体积相同的四种溶液: 的
的 溶液;
溶液; 的硫酸;
的硫酸;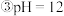 的氨水;
的氨水;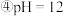 的NaOH溶液.下列说法正确的是
的NaOH溶液.下列说法正确的是
 的
的 溶液;
溶液; 的硫酸;
的硫酸;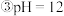 的氨水;
的氨水;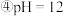 的NaOH溶液.下列说法正确的是
的NaOH溶液.下列说法正确的是
A. 和 和 混合后 混合后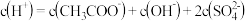 |
B. 和 和 溶液中: 溶液中: |
C. 和 和 混合溶液中: 混合溶液中: |
D.四种溶液各稀释100倍,溶液pH: |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】室温下,向0.1 三元中强酸H3PO4溶液中缓慢加入NaOH固体,忽略温度和溶液体积的变化,溶液中的H3PO4、
三元中强酸H3PO4溶液中缓慢加入NaOH固体,忽略温度和溶液体积的变化,溶液中的H3PO4、 、
、 和
和 的物质的量分数随溶液的pH的变化如图所示[已知
的物质的量分数随溶液的pH的变化如图所示[已知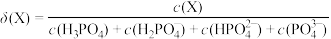 ],下列叙述错误的是
],下列叙述错误的是

 三元中强酸H3PO4溶液中缓慢加入NaOH固体,忽略温度和溶液体积的变化,溶液中的H3PO4、
三元中强酸H3PO4溶液中缓慢加入NaOH固体,忽略温度和溶液体积的变化,溶液中的H3PO4、 、
、 和
和 的物质的量分数随溶液的pH的变化如图所示[已知
的物质的量分数随溶液的pH的变化如图所示[已知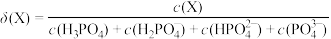 ],下列叙述错误的是
],下列叙述错误的是
A.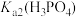 的数量级为 的数量级为 |
B.Q1、Q2和Q3三点溶液中均存在: |
C.Na2HPO4溶液中: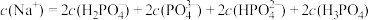 |
D.当pH=13时,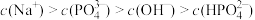 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】已知:pKa=-lgKa,25℃时,H2XO3的pKa1=10-1.85,pKa2=10-7.19,常温下,用0.1mol/LNaOH溶液滴定20mL0.1mol/LH2XO3溶液的滴定曲线如图所示下列说法不正确的是
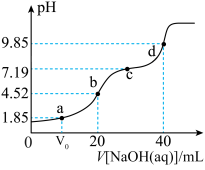

A.a点溶液中:c(H2XO3)=c(HXO ) ) |
B.b点溶液中:c(H2XO3)+c(H+)=c(XO )+c(OH-) )+c(OH-) |
C.c点溶液中:c(Na+)=3c(HXO ) ) |
D.d点溶液中:c(Na+)>c(XO )>c(OH-)>c(HXO )>c(OH-)>c(HXO )>c(H+) )>c(H+) |
您最近一年使用:0次



