名校
1 . 常温下,将pH=5的硫酸溶液稀释到原来的500倍,则稀释后溶液中 与H+的物质的量浓度之比约为
与H+的物质的量浓度之比约为
 与H+的物质的量浓度之比约为
与H+的物质的量浓度之比约为| A.10∶1 | B.1∶10 | C.1∶2 | D.1∶1 |
您最近一年使用:0次
名校
2 . 常温下,在由水电离出的c(H+)=10-13mol/L的溶液中,一定能大量共存的离子组是
A.K+、Na+、 、Cl- 、Cl- | B.K+、Fe3+、Br-、I- |
C.Na+、Cl-、 、 、 | D. 、Al3+、Cl-、 、Al3+、Cl-、 |
您最近一年使用:0次
3 . 下表中物质的分类组合完全正确的是
| 选项 | A | B | C | D |
| 强电解质 | KNO3 | 胆矾 | BaSO4 | HClO4 |
| 弱电解质 | HF | CaCO3 | HClO | NH3 |
| 非电解质 | SO2 | 金属Al | H2O | C2H5OH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . Cl2O又称为次氯酸酐,是强氧化剂,易溶于水且与水反应,受热时容易燃烧、高浓度时容易爆炸。其熔沸点分别为-116℃和3.8℃;Cl2的沸点是-34.6℃。现利用HgO和Cl2以及以下装置制备Cl2O(同时还生成 ):
):

回答下列问题:
(1)用酸性高锰酸钾制备Cl2应采用气体发生装置___________ (填“甲”或“乙”),化学方程式为___________
(2)②、③中盛放的试剂分别是___________ 。
(3)写出HgO和Cl2制备Cl2O的化学方程式:___________ 。
(4)通入干燥空气的目的是___________ 。
(5)实验装置存在一些不足,请指出___________ 。
 ):
):
回答下列问题:
(1)用酸性高锰酸钾制备Cl2应采用气体发生装置
(2)②、③中盛放的试剂分别是
(3)写出HgO和Cl2制备Cl2O的化学方程式:
(4)通入干燥空气的目的是
(5)实验装置存在一些不足,请指出
您最近一年使用:0次
名校
解题方法
5 . 往x g铁铜的混合粉末中加入一定体积某浓度的2.00mol·L-1FeCl3溶液,充分反应后剩余固体的质量与加入FeCl3溶液的体积存在如下关系:
(1)x=___________
(2)混合粉末中Fe和Cu质量之比为_____
(3)加入FeCl3溶液400mL充分反应后的溶液,还能溶解铁粉_____
| 加入FeCl3溶液体积(mL) | 100 | 200 | 300 | 400 |
| 剩余固体质量(g) | 14.8 | 9.20 | 3.20 | 0 |
(2)混合粉末中Fe和Cu质量之比为
(3)加入FeCl3溶液400mL充分反应后的溶液,还能溶解铁粉
您最近一年使用:0次
名校
6 . 平板液晶显示屏生产过程中产生大量的废玻璃粉末,其中含 、
、 、
、 等物质,某实验小组以此粉末为原料回收铈,设计流程如图所示。
等物质,某实验小组以此粉末为原料回收铈,设计流程如图所示。
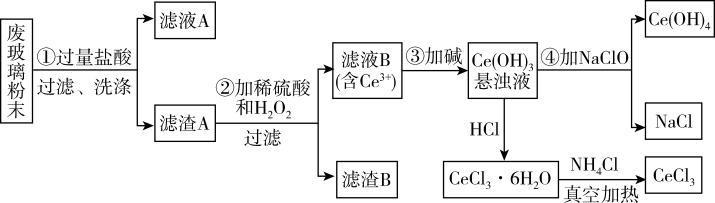
已知: 具有强氧化性,一般不与常见的无机酸反应。
具有强氧化性,一般不与常见的无机酸反应。
(1)检验滤液A中主要存在的金属阳离子方法:___________ 。
(2)步骤②的离子方程式___________ ,为了加快步骤②的反应速率,有人提出在高温下进行,你认为是否恰当并解释理由___________ 。
(3)第④步反应的化学方程式是___________ 。
(4)最后过滤洗涤得到纯净的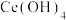 ,请写出洗涤
,请写出洗涤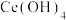 的方法:
的方法:___________ 。
 、
、 、
、 等物质,某实验小组以此粉末为原料回收铈,设计流程如图所示。
等物质,某实验小组以此粉末为原料回收铈,设计流程如图所示。
已知:
 具有强氧化性,一般不与常见的无机酸反应。
具有强氧化性,一般不与常见的无机酸反应。(1)检验滤液A中主要存在的金属阳离子方法:
(2)步骤②的离子方程式
(3)第④步反应的化学方程式是
(4)最后过滤洗涤得到纯净的
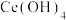 ,请写出洗涤
,请写出洗涤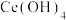 的方法:
的方法:
您最近一年使用:0次
名校
7 . 下表为元素周期表的一部分,请回答下列有关问题
(1)已知元素⑩的一种核素,其中子数为45,用原子符号表示该核素为___________ 。
(2)由元素②和④形成的三核分子的结构式为___________ ,①和②形成的简单氢化物的空间结构是___________ ,元素③所形成的单质的电子式为___________ 。用电子式描述⑨⑦形成的A2B型化合物的形成过程___________ 。
(3)由上述元素构成的淡黄色固体化合物的电子式为___________ ,该化合物所含的化学键类型为___________ (填“离子键”、“极性键”或“非极性键”)。
(4)元素②③⑦⑧的最高价氧化物对应水化物的酸性由强到弱的顺序是___________ ,元素⑨的最高价氧化物对应水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(5)元素的非金属性⑧_____ ⑩(填“>”或“<”);下列事实不能证明上述结论的是_____ 。
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
(6)某同学利用如图装置来验证同主族元素非金属性的变化规律。

①仪器A的名称为___________ ,干燥管D的作用为___________
② 若要证明非金属性Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加入碘化钾和苯的混合溶液,观察到C中溶液出现的现象是___________ ,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,吸收尾气的离子方程式为___________ 。
③若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液出现的现象是___________ ,即可证明。但有的同学认为,应在两装置间添加装有___________ 溶液的洗气瓶才更准确,用这套装置同时可以证明非金属性,Cl>C>Si,需改动的部分是___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)由元素②和④形成的三核分子的结构式为
(3)由上述元素构成的淡黄色固体化合物的电子式为
(4)元素②③⑦⑧的最高价氧化物对应水化物的酸性由强到弱的顺序是
(5)元素的非金属性⑧
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
(6)某同学利用如图装置来验证同主族元素非金属性的变化规律。

①仪器A的名称为
② 若要证明非金属性Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加入碘化钾和苯的混合溶液,观察到C中溶液出现的现象是
③若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液出现的现象是
您最近一年使用:0次
名校
8 . 将金属铁、铜投入FeCl3溶液中充分反应,下列对反应情况设想的评价正确的是
| 选项 | 反应情况设想 | 评价 |
| A | 当铁、铜均不剩余时,溶液中一定有Fe2+、Cu2+,可能有Fe3+ | 正确,Fe3+和铁、铜均可反应,可能会有剩余 |
| B | 当铜剩余,铁不剩余时,溶液中一定只有Fe2+,无Cu2+ | 正确,铜剩余,故无Cu2+ |
| C | 当铁、铜均剩余时,溶液中一定有Fe2+、Cu2+,无Fe3+ | 正确,铁和铜都与Fe3+反应,故无Fe3+ |
| D | 当铁剩余,铜不剩余时,溶液中一定有Fe2+、Cu2+ | 不正确,不可能出现铁剩余而铜不剩余的情况,因为铁的还原性比铜的强,铁先与Fe3+反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 用NA表示阿伏加德罗常数的值,下列叙述中正确的个数是
①2.3g Na与O2完全反应,转移电子个数介于0.1NA和0.2NA之间
②0.1molNaHSO4中含有阳离子数目为0.1NA
③50mL 12mol/L的盐酸与足量MnO2共热,转移电子数为0.3NA
④16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA
⑤30gHCHO和CH3COOH混合物中含C原子数为NA
⑥100g 9%的C6H12O6水溶液中O原子数为0.3NA
⑦0.1molNa2O和Na2O2的混合物中阴离子数目为0.1NA
⑧5.6LCO2与足量Na2O2转移电子数为0.5NA
⑨标准状况下,2.24L SO3含有的质子数为4NA
①2.3g Na与O2完全反应,转移电子个数介于0.1NA和0.2NA之间
②0.1molNaHSO4中含有阳离子数目为0.1NA
③50mL 12mol/L的盐酸与足量MnO2共热,转移电子数为0.3NA
④16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA
⑤30gHCHO和CH3COOH混合物中含C原子数为NA
⑥100g 9%的C6H12O6水溶液中O原子数为0.3NA
⑦0.1molNa2O和Na2O2的混合物中阴离子数目为0.1NA
⑧5.6LCO2与足量Na2O2转移电子数为0.5NA
⑨标准状况下,2.24L SO3含有的质子数为4NA
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
名校
解题方法
10 . 下列方程式书写正确的为
A.向NaClO溶液中通入少量SO2:2ClO-+H2O+SO2=2HClO+SO |
B.稀硫酸与Ba(OH)2溶液反应:H++SO +Ba2++OH-=BaSO4↓+H2O +Ba2++OH-=BaSO4↓+H2O |
| C.向FeBr2溶液中通入等量的氯气:2Fe2++2Br- + 2Cl 2= 2Fe3+ + Br2+ 4Cl- |
D.Ca(OH)2与少量NaHCO3反应的离子方程式为:2HCO +Ca2++2OH-=CaCO3↓+H2O+CO +Ca2++2OH-=CaCO3↓+H2O+CO |
您最近一年使用:0次



