解题方法
1 . 按要求回答下列问题:
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有___________ (填字母,下同),属于酸性氧化物的有___________ 。
②Fe2(SO4)3溶于水的电离方程式为___________ 。
③写出实验室制取Fe(OH)3胶体的离子方程式:___________ 。
④写出H与足量A反应的离子方程式:___________ 。
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:___________ 。

②该反应中的还原剂为___________ (填化学式),被还原的物质与被氧化的物质的物质的量之比为___________ 。
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=___________ 。
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有
②Fe2(SO4)3溶于水的电离方程式为
③写出实验室制取Fe(OH)3胶体的离子方程式:
④写出H与足量A反应的离子方程式:
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:

②该反应中的还原剂为
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为
 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=
您最近一年使用:0次
名校
解题方法
2 . 下列离子反应方程式正确的是
A.氯气通入冷的石灰乳: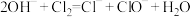 |
B.向NaHCO3溶液中滴入少量澄清石灰水: |
C.向明矾溶液中滴加Ba(OH)2溶液到 恰好完全沉淀时: 恰好完全沉淀时: |
| D.向FeI2溶液中通入少量氯气:Cl2 + 2I- = 2Cl- + I2 |
您最近一年使用:0次
解题方法
3 . 铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)现有铁和铜的混合物,可以通过___________ 把他们分开。
A.盐酸 B.NaOH C.FeCl3
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
请写出FeCl3溶液与铜反应的离子方程式:___________ 。
反应后的废液中含有Fe3+,可以用___________ 检验。
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。___________ ,黄绿色气体C可以把滤液转化成FeCl3腐蚀液,写出反应过程中的离子方程式___________ 。
(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,___________ (补全实验现象),此过程涉及氧化还原反应的化学方程式是___________ 。
(5)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为___________ 。
(1)现有铁和铜的混合物,可以通过
A.盐酸 B.NaOH C.FeCl3
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
请写出FeCl3溶液与铜反应的离子方程式:
反应后的废液中含有Fe3+,可以用
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。

(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(5)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为
您最近一年使用:0次
解题方法
4 . 某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是___________ 。
(2)写出KAl(SO4)2在水中的电离方程式___________ 。
(3)已知H+ +[Al(OH)4]- = Al(OH)3↓+ H2O,根据上述框图反应关系,写出下列B、D、E所含物质的化学式:固体B___________ ;沉淀D___________ ;溶液E是K2SO4和___________ 。
(4)写出①②反应的离子方程式。
①___________ 。
②___________ 。
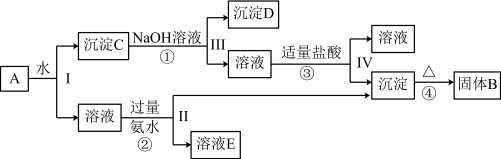
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
(2)写出KAl(SO4)2在水中的电离方程式
(3)已知H+ +[Al(OH)4]- = Al(OH)3↓+ H2O,根据上述框图反应关系,写出下列B、D、E所含物质的化学式:固体B
(4)写出①②反应的离子方程式。
①
②
您最近一年使用:0次
5 . 研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲,黑火药在发生爆炸时,发生如下反应: ,其中作氧化剂的是
,其中作氧化剂的是______ (填化学式,下同),被还原的是______ 。
(2)中国古代著作中有“银针验毒”的记录,其原理为 ,则X的化学式是
,则X的化学式是______ ,其中 在该反应中
在该反应中______ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

①Ⅱ中发生反应的离子方程式为______ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为______ 。
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲,黑火药在发生爆炸时,发生如下反应:
 ,其中作氧化剂的是
,其中作氧化剂的是(2)中国古代著作中有“银针验毒”的记录,其原理为
 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

①Ⅱ中发生反应的离子方程式为
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为
您最近一年使用:0次
6 . 如图为实验室某浓盐酸试剂瓶标签上的部分数据,试根据标签.上的相关数据回答下列问题:.
(1)该浓盐酸中HCl的物质的量浓度为______ mol/L。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.400mol/L的稀盐酸。
①该学生需要量取______ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:______ ;
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:______ 。
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取______ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是______ 。
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:  HCl的质量分数:36.5% |
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的浓度 |
C.溶液中 的数目 的数目 | D.溶液的密度 |
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
名校
解题方法
7 . 铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有Al2O3、Fe2O3、FeO、SiO2等)来制备绿矾(FeSO4•7H2O)和氧化铝,其工艺流程如图:
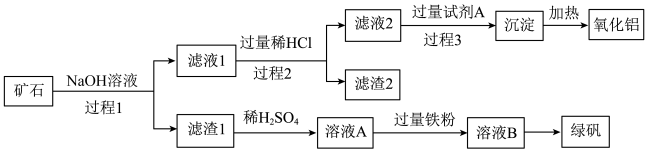
回答下列问题:
(1)滤渣1的成分是_______ ,举例说明滤渣2的用途 _______ 。
(2)用离子方程式表示溶液A加入过量铁粉的目的是_______ 。
(3)写出由滤液1生成滤液2的离子方程式_______ 。
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有_______ 。
(5)过程3需要加入的试剂A是_______ ,写出此过程的离子方程式 _______ 。

回答下列问题:
(1)滤渣1的成分是
(2)用离子方程式表示溶液A加入过量铁粉的目的是
(3)写出由滤液1生成滤液2的离子方程式
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有
(5)过程3需要加入的试剂A是
您最近一年使用:0次
名校
解题方法
8 . “价—类”二维图是研究物质性质的重要工具,如图是硫元素的“价—类”二维图。回答下列问题:_______ 。
(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为_______ 。
(3)溶液e久置于空气中会生成f,该过程溶液的酸性_______ (填“增强”或“减弱”)。
(4)Cl2和c都有漂白作用,先将二者以等物质的量混合后再通入到品红溶液中,品红溶液_______ (填褪色或不褪色),反应的化学方程式为 _______ 。
(5)将c通入到酸性KMnO4溶液中,溶液颜色逐渐变浅,该反应中c表现出_______ (填“还原”或“漂白”)性。
(6)实验室产生c排放到大气中会引起酸雨,应用_______ 溶液吸收,发生的反应方程式为 _______ 。

(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为
(3)溶液e久置于空气中会生成f,该过程溶液的酸性
(4)Cl2和c都有漂白作用,先将二者以等物质的量混合后再通入到品红溶液中,品红溶液
(5)将c通入到酸性KMnO4溶液中,溶液颜色逐渐变浅,该反应中c表现出
(6)实验室产生c排放到大气中会引起酸雨,应用
您最近一年使用:0次
2024-02-22更新
|
227次组卷
|
2卷引用:新疆 乌鲁木齐市第十二中学2023-2024学年高一上学期1月期末化学试题
解题方法
9 .  是一种安全高效灭菌消毒剂,我国从2000年起就逐渐用
是一种安全高效灭菌消毒剂,我国从2000年起就逐渐用 取代
取代 对饮用水进行消毒。下图是某实验室用于制备一定量较纯净的
对饮用水进行消毒。下图是某实验室用于制备一定量较纯净的 的装置(某些夹持装置和垫持用品省略)。已知:
的装置(某些夹持装置和垫持用品省略)。已知:
①实验室可用亚氯酸钠固体 与氯气反应来制备
与氯气反应来制备 ;
;
②通常情况下, 是一种有刺激性气味的黄绿色气体,熔点为
是一种有刺激性气味的黄绿色气体,熔点为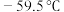 ,沸点为
,沸点为 。常温下
。常温下 水约溶解
水约溶解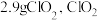 遇热水不稳定。
遇热水不稳定。
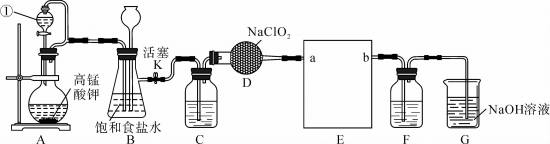
请回答下列问题:
(1)仪器①的名称为___________ 。
(2)检验装置A、B的气密性:___________ ,从长颈漏斗处加水至液面高于锥形瓶中的液面,若一段时间后长颈漏斗内液面不下降,则说明装置气密性良好。
(3)装置B的作用是___________ ,装置C中盛放的试剂是___________ 。
(4)写出装置D中制备 的化学方程式,并用单线桥法标出电子转移的方向和数目
的化学方程式,并用单线桥法标出电子转移的方向和数目_______ 。
(5)装置E采用下图所示装置,其作用是___________ ,正确的连接顺序为a→________ ________ →b。
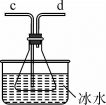
(6)尾气吸收装置中发生反应的离子方程式为___________ 。
 是一种安全高效灭菌消毒剂,我国从2000年起就逐渐用
是一种安全高效灭菌消毒剂,我国从2000年起就逐渐用 取代
取代 对饮用水进行消毒。下图是某实验室用于制备一定量较纯净的
对饮用水进行消毒。下图是某实验室用于制备一定量较纯净的 的装置(某些夹持装置和垫持用品省略)。已知:
的装置(某些夹持装置和垫持用品省略)。已知:①实验室可用亚氯酸钠固体
 与氯气反应来制备
与氯气反应来制备 ;
;②通常情况下,
 是一种有刺激性气味的黄绿色气体,熔点为
是一种有刺激性气味的黄绿色气体,熔点为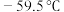 ,沸点为
,沸点为 。常温下
。常温下 水约溶解
水约溶解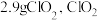 遇热水不稳定。
遇热水不稳定。
请回答下列问题:
(1)仪器①的名称为
(2)检验装置A、B的气密性:
(3)装置B的作用是
(4)写出装置D中制备
 的化学方程式,并用单线桥法标出电子转移的方向和数目
的化学方程式,并用单线桥法标出电子转移的方向和数目(5)装置E采用下图所示装置,其作用是

(6)尾气吸收装置中发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
10 . 某小组为探究 (三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。

(1)在实验进行的过程中,应该持续通入氮气的目的是___________ 。
(2)若实验中观察装置F中澄清石灰水变浑浊,装置E中固体变为红色,则说明 的热分解产物中一定含有
的热分解产物中一定含有___________ 。
(3)该样品完全热分解后,欲检测固体生成物中的组成,某同学待装置冷却后取少量固体加入稀硫酸溶解,再加入 溶液变红,说明
溶液变红,说明___________ 。
(4)已知: 是一种光敏化合物,见光分解。该实验小组在探究
是一种光敏化合物,见光分解。该实验小组在探究 热分解后,用该装置再次探究它光解的产物,现取
热分解后,用该装置再次探究它光解的产物,现取 固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
完成下列小题:
①若反应后 元素的化合价降为
元素的化合价降为 价,K元素的化合价未改变,且两者仍为草酸
价,K元素的化合价未改变,且两者仍为草酸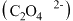 盐,写出三草酸合铁酸钾完全光解的化学方程式
盐,写出三草酸合铁酸钾完全光解的化学方程式___________ 。
②据此计算出该 固体的纯度为
固体的纯度为___________ (保留一位有效数字) 。
③样品完全分解后,实验小组停止通氮气,一段时间后,某同学取少许装置A中的残留物于试管中,加入稀硫酸溶解,滴入1~2滴 溶液,发现溶液变红,这与上述
溶液,发现溶液变红,这与上述 分解产物为
分解产物为 价
价 的结论不符可能的原因是
的结论不符可能的原因是___________ 。
 (三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(1)在实验进行的过程中,应该持续通入氮气的目的是
(2)若实验中观察装置F中澄清石灰水变浑浊,装置E中固体变为红色,则说明
 的热分解产物中一定含有
的热分解产物中一定含有(3)该样品完全热分解后,欲检测固体生成物中的组成,某同学待装置冷却后取少量固体加入稀硫酸溶解,再加入
 溶液变红,说明
溶液变红,说明(4)已知:
 是一种光敏化合物,见光分解。该实验小组在探究
是一种光敏化合物,见光分解。该实验小组在探究 热分解后,用该装置再次探究它光解的产物,现取
热分解后,用该装置再次探究它光解的产物,现取 固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。完成下列小题:
①若反应后
 元素的化合价降为
元素的化合价降为 价,K元素的化合价未改变,且两者仍为草酸
价,K元素的化合价未改变,且两者仍为草酸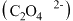 盐,写出三草酸合铁酸钾完全光解的化学方程式
盐,写出三草酸合铁酸钾完全光解的化学方程式②据此计算出该
 固体的纯度为
固体的纯度为③样品完全分解后,实验小组停止通氮气,一段时间后,某同学取少许装置A中的残留物于试管中,加入稀硫酸溶解,滴入1~2滴
 溶液,发现溶液变红,这与上述
溶液,发现溶液变红,这与上述 分解产物为
分解产物为 价
价 的结论不符可能的原因是
的结论不符可能的原因是
您最近一年使用:0次



