名校
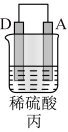
1 . 理论上讲,任何自发的氧化还原反应都可以设计成原电池。某同学利用“Cu+2Ag+=2Ag+Cu2+”反应设计一个化学电池,如图所示,已知该电池在外电路中,电流从a极流向b极。请回答下列问题:___________ 极,写出该电极的反应式___________ 。
(2)c溶液是___________ 。
A.CuSO4溶液 B.AgNO3溶液 C.酒精溶液
(3)若该反应过程中有0.2mol电子发生转移,则生成Ag为___________ 克。
(4)已知12g石墨转变为12g金刚石需吸收能量。常温常压下,石墨与金刚石更稳定的是___________ 。
(5)已知某反应的能量变化图如下图所示,下列化学反应过程中的能量变化能用下图表示的有___________ 。
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.二氧化碳通过炽热的碳
(6)从断键和成键的角度分析2H2(g)+O2(g)=2H2O(g)反应中能量的变化,则生成1molH2O(g)可以放出热量___________ kJ。

(2)c溶液是
A.CuSO4溶液 B.AgNO3溶液 C.酒精溶液
(3)若该反应过程中有0.2mol电子发生转移,则生成Ag为
(4)已知12g石墨转变为12g金刚石需吸收能量。常温常压下,石墨与金刚石更稳定的是
(5)已知某反应的能量变化图如下图所示,下列化学反应过程中的能量变化能用下图表示的有

b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.二氧化碳通过炽热的碳
(6)从断键和成键的角度分析2H2(g)+O2(g)=2H2O(g)反应中能量的变化,则生成1molH2O(g)可以放出热量
| 化学键 | H-H | O=O | H-O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
您最近一年使用:0次
2 . 某化学兴趣小组用下图装置(部分夹持装置已略去)制取氨气并探究其性质。___________ 。(填化学式)
(2)气体通过C、D装置时,试纸颜色发生变化的是___________ (填字母),原因是氨水呈___________ 性。
(3)当E装置中集满 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到E中的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到E中的现象是___________ 。
(4)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。___________ ,证明氨气具有___________ (填“氧化性”或“还原性”)。
(5)NH3易溶于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为___________ mol∙L-1。
(6)已知加热条件下,氨气可以与铝发生置换反应生成AlN;AlN加热时可溶于浓碱溶液并产生氨气,写出浓碱中发生反应的化学方程式:___________ 。

(2)气体通过C、D装置时,试纸颜色发生变化的是
(3)当E装置中集满
 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到E中的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到E中的现象是(4)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

(5)NH3易溶于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为
(6)已知加热条件下,氨气可以与铝发生置换反应生成AlN;AlN加热时可溶于浓碱溶液并产生氨气,写出浓碱中发生反应的化学方程式:
您最近一年使用:0次
名校
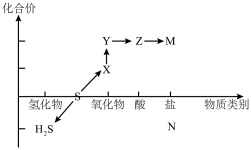
3 . 硫及其化合物的“价-类”二维图体现了化学变化之美。___________ (用化学式表示,下同),从硫元素的化合价角度分析,图中所示物质既有氧化性又有还原性的物质有___________ 。
(2)将X与H2S混合,反应的化学方程式为___________ ,其中氧化产物与还原产物的物质的量之比为___________ 。
(3)Z的稀溶液可与Ba(OH)2溶液发生反应,其离子方程式为___________ ;
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___________;
(5)某小组实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2,有同学认为制得的SO2中可能混有杂质(不考虑水蒸气),其杂质气体的化学式为___________ 。
(2)将X与H2S混合,反应的化学方程式为
(3)Z的稀溶液可与Ba(OH)2溶液发生反应,其离子方程式为
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___________;
| A.Na2S+S | B.Na2SO3+S | C.SO2+Na2SO4 | D.Na2SO3+Na2SO4 |
(5)某小组实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2,有同学认为制得的SO2中可能混有杂质(不考虑水蒸气),其杂质气体的化学式为
您最近一年使用:0次
名校
4 . A、B、C、D四种金属按下表中装置进行实验。根据实验现象,下列判断错误的是
| 装置 |
|
|
|
| 现象 | 电子从A到B | C的质量增加 | A上有气体产生 |
| A.装置甲中溶液中的阴离子移向A极 |
| B.装置乙中正极的电极反应式为Cu2++2e-=Cu |
| C.四种金属活动性由强到弱的顺序是D>A>B>C |
| D.装置丙的溶液中电子从D流向A |
您最近一年使用:0次
名校
5 . 符合某些特征的化学反应理论上都可以设计成原电池。下列化学反应不能设计成原电池的是
| A.2H2+O2=2H2O |
| B.Fe+CuSO4=FeSO4+Cu |
| C.2NaOH+H2SO4=Na2SO4+2H2O |
| D.Pb+PbO2+2H2SO4=2PbSO4+2H2O |
您最近一年使用:0次
名校
解题方法
6 . 喷泉实验装置如图所示,应用下列各组气体及溶液,不能出现喷泉现象的是
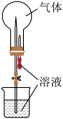
| A.NH3和稀盐酸 |
| B.HCl和氢氧化钠稀溶液 |
| C.CO2和饱和碳酸氢钠溶液 |
| D.SO2和氨水 |
您最近一年使用:0次
名校
7 . 下列环境问题与氮的氧化物排放无关的是
①酸雨②光化学烟雾③臭氧层空洞④白色污染⑤温室效应
①酸雨②光化学烟雾③臭氧层空洞④白色污染⑤温室效应
| A.①② | B.②③④ | C.③④⑤ | D.①③ |
您最近一年使用:0次
名校
解题方法
8 . 氮和硫是化工生产中的重要元素。下列相关物质的性质与用途具有对应关系的是
| A.液氨汽化时吸收大量热,可用作制冷剂 |
| B.碳酸氢铵受热易分解,可用作化学肥料 |
| C.二氧化硫易溶于水,可用作纸浆漂白剂 |
| D.浓硫酸具有吸水性,可用来作氨气的干燥剂 |
您最近一年使用:0次
名校
9 . 下列化学用语不正确的是
A.NH3的球棍模型: |
B.铵根离子的电子式: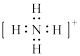 |
C.CO2分子的空间填充模型: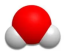 |
| D.N2的结构式:N≡N |
您最近一年使用:0次
名校
解题方法
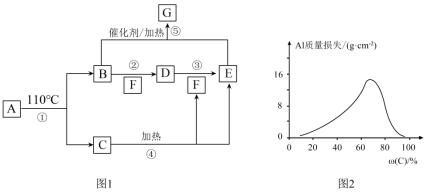
10 . A~G的转化关系如图1所示(部分产物略去),其中E为红棕色气体,G为单质。常温下,将Al片浸在不同质量分数的C溶液中,经过相同时间的腐蚀后,Al片的质量损失情况如图2所示。
(1)写出下列物质的化学式:A___________ 、E___________ 。
(2)反应④、⑤的化学方程式:④___________ 、⑤___________ 。
(3)图2中Al质量损失随C溶液质量分数的变化先增大后减小,减小的原因为___________ 。
(4)足量Al与一定浓度的C反应,得到H溶液和D、E的混合物,这些混合物与1.68LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成C.若向所得H溶液中加入5mol/LNaOH溶液至Al3+恰好完全沉淀,则消耗NaOH溶液的体积是___________ mL。
(1)写出下列物质的化学式:A
(2)反应④、⑤的化学方程式:④
(3)图2中Al质量损失随C溶液质量分数的变化先增大后减小,减小的原因为
(4)足量Al与一定浓度的C反应,得到H溶液和D、E的混合物,这些混合物与1.68LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成C.若向所得H溶液中加入5mol/LNaOH溶液至Al3+恰好完全沉淀,则消耗NaOH溶液的体积是
您最近一年使用:0次