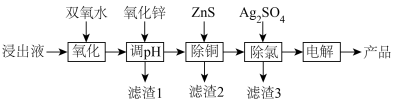
1 . 工业上将一种以ZnSO4为主要成分的浸出液(含有Fe3+、Fe2+、Cu2+、Cl-等杂质)经过一系列处理后,用于制备金属锌,其流程如下:
回答下列问题:
(1)“调pH”时选择氧化锌的目的是_______ ,优点是_______ 。
(2)若“滤渣1”的主要成分是Fe(OH)3,“调pH”的范围应是_______ ,写出相关反应的离子方程式:_______ 。
(3)“除氯”时发生反应: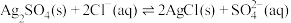 。已知:25℃时,
。已知:25℃时,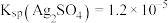 ,
, ,请计算该反应的平衡常数K=
,请计算该反应的平衡常数K=_______ (列出计算式即可)。
(4)“电解”时生成产品的一极是_______ (填“阴极”或“阳极”);缺少“除氯”步骤的影响是_______ 。
| 金属离子 | Fe3+ | Fe2 | Cu2+ | Zn2+ |
| 开始沉淀的pH | 2.3 | 6.8 | 4.7 | 6.2 |
| 完全沉淀的pH | 3.2 | 8.3 | 6.7 | 8.2 |
(1)“调pH”时选择氧化锌的目的是
(2)若“滤渣1”的主要成分是Fe(OH)3,“调pH”的范围应是
(3)“除氯”时发生反应:
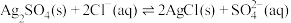 。已知:25℃时,
。已知:25℃时,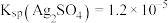 ,
, ,请计算该反应的平衡常数K=
,请计算该反应的平衡常数K=(4)“电解”时生成产品的一极是
您最近一年使用:0次
解题方法
2 . 湿法炼锌净化钴渣中含有 、
、 、
、 和
和 的单质及
的单质及 ,可利用过硫酸钠(
,可利用过硫酸钠( )氧化水解法实现钴的富集,其工艺流程如下:
)氧化水解法实现钴的富集,其工艺流程如下: 见下表:
见下表:
回答下列问题:
(1)“浸渣”的主要成分为_______ 。
(2)根据以上流程判断离子的还原性:
_______ (填“小于”或“大于”) 。
。
(3)利用上述表格数据,计算 的
的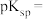
_______ 。如果“滤液I”中 浓度为
浓度为 ,则“除铁”应控制的
,则“除铁”应控制的 范围是
范围是_______ 。( )
)
(4)①已知过硫酸钠中 的化合价为+6,则
的化合价为+6,则 过硫酸钠中含有的过氧键(
过硫酸钠中含有的过氧键( )数目为
)数目为_______ 。(用 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)
②写出“沉钴”时发生反应的离子方程式:_______ 。
(5)上述流程中_______ (填字母)可返回湿法炼锌系统,提高锌的利用率。
A.浸渣 B.滤渣I C.滤液I D.滤渣Ⅱ E.滤液Ⅱ
 、
、 、
、 和
和 的单质及
的单质及 ,可利用过硫酸钠(
,可利用过硫酸钠( )氧化水解法实现钴的富集,其工艺流程如下:
)氧化水解法实现钴的富集,其工艺流程如下: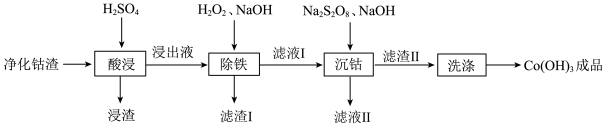
 见下表:
见下表:| 金属离子 |  |  |  |
开始沉淀( )的 )的 | 2.2 | 6.8 | 7.7 |
沉淀完全( )的 )的 | 3.2 | 8.3 | 9.2 |
(1)“浸渣”的主要成分为
(2)根据以上流程判断离子的还原性:

 。
。(3)利用上述表格数据,计算
 的
的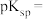
 浓度为
浓度为 ,则“除铁”应控制的
,则“除铁”应控制的 范围是
范围是 )
)(4)①已知过硫酸钠中
 的化合价为+6,则
的化合价为+6,则 过硫酸钠中含有的过氧键(
过硫酸钠中含有的过氧键( )数目为
)数目为 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)②写出“沉钴”时发生反应的离子方程式:
(5)上述流程中
A.浸渣 B.滤渣I C.滤液I D.滤渣Ⅱ E.滤液Ⅱ
您最近一年使用:0次
3 .  的资源化有利于实现“碳中和”,利用
的资源化有利于实现“碳中和”,利用 氧化烷烃可制得烯烃。以
氧化烷烃可制得烯烃。以 和乙苯(
和乙苯(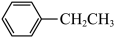 )为原料合成苯乙烯(
)为原料合成苯乙烯(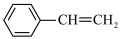 )为例,涉及以下反应:
)为例,涉及以下反应:
I.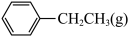

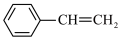 (g)+
(g)+
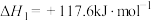
Ⅱ.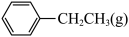
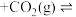
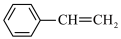 (g)
(g)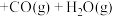
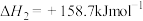
(1)写出
 与
与 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:(2)下列说法正确的是_______。(填字母)
A.当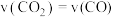 时,反应Ⅱ达到平衡状态 时,反应Ⅱ达到平衡状态 |
| B.升高温度,反应Ⅱ的正、逆反应速率都增大 |
C.增大压强,反应I平衡逆向移动,平衡常数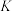 减小 减小 |
| D.反应I加入催化剂,可降低该反应的活化能 |
(3)在刚性容器中,进料浓度比[
 (乙苯):
(乙苯): ]分别等于1∶5、1∶15、1∶50时,乙苯的平衡转化率随反应温度的变化关系如图所示:
]分别等于1∶5、1∶15、1∶50时,乙苯的平衡转化率随反应温度的变化关系如图所示: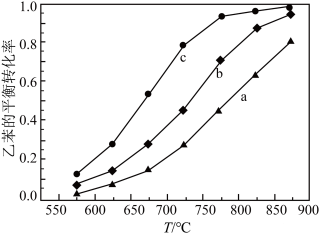
 的进料浓度比[
的进料浓度比[ (乙苯):
(乙苯): ]为
]为(4)某温度下,等物质的量的乙苯和
 在刚性容器内只发生反应Ⅱ,若初始的总压强为
在刚性容器内只发生反应Ⅱ,若初始的总压强为 ,平衡时乙苯的转化率为40%,则平衡时的总压强为
,平衡时乙苯的转化率为40%,则平衡时的总压强为 表示,下同),反应Ⅱ的平衡常数
表示,下同),反应Ⅱ的平衡常数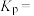
 物质的量分数)
物质的量分数)
您最近一年使用:0次
4 . 利用下列装置进行的实验,不能达到预期目的的是
|
|
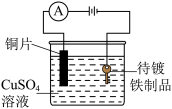
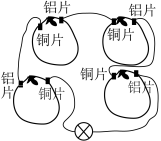
| A.在铁制品上电镀铜 | B.制作水果(柠檬)电池 |
|
|
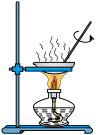
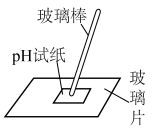
C.将 溶液蒸干制备无水 溶液蒸干制备无水 | D.粗测碳酸钠溶液的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列叙述中,不能用盐类水解原理解释的是
A.常用明矾 作净水剂 作净水剂 |
B.向沸水中滴加饱和 溶液制备 溶液制备 胶体 胶体 |
C.施肥时,草木灰(有效成分 )与铵态氮肥不可混用 )与铵态氮肥不可混用 |
| D.抢救钡离子中毒者时,可用硫酸钠溶液洗胃 |
您最近一年使用:0次
解题方法
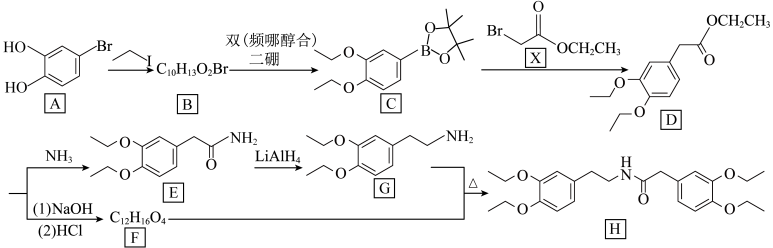
6 . 盐酸屈他维林主要用于治疗胃肠道痉挛,肠易激综合症等。有机化合物H是盐酸屈他维林的合成中间体,其合成路线如图所示。
(1)A的化学名称为___________ 。
(2)B的结构简式为___________ 。
(3)H所含官能团的名称是___________ 。
(4)E→G的反应类型为___________ 。
(5)F+G→H反应的化学方程式为___________ 。
(6)X有多种同分异构体,与X具有相同官能团的同分异构体有___________ 种(不考虑立体异构),核磁共振氢谱显示为3组峰,且峰面积比为3:3:1的同分异构体的结构简式为___________ 。
(1)A的化学名称为
(2)B的结构简式为
(3)H所含官能团的名称是
(4)E→G的反应类型为
(5)F+G→H反应的化学方程式为
(6)X有多种同分异构体,与X具有相同官能团的同分异构体有
您最近一年使用:0次
解题方法
7 . “低碳经济”已成为全世界科学研究的重要课题, 资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
方案一:以 为原料合成乙烯
为原料合成乙烯
(1)以 和
和 催化合成乙烯:
催化合成乙烯: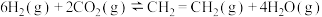
 。
。
在一定压强下,将 和
和 加入1L容积不变的密闭容器中,已知温度对
加入1L容积不变的密闭容器中,已知温度对 的平衡转化率、实际转化率和催化剂催化效率的影响如图所示,结合图像分析该反应实际反应温度定于250℃的原因可能是
的平衡转化率、实际转化率和催化剂催化效率的影响如图所示,结合图像分析该反应实际反应温度定于250℃的原因可能是___________ 。 为原料合成甲醇
为原料合成甲醇
(2)以 合成甲醇涉及的反应如下:
合成甲醇涉及的反应如下:
反应Ⅰ:

反应Ⅱ:
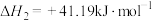
反应Ⅲ:
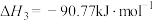

___________  ,反应Ⅲ能自发进行的条件是
,反应Ⅲ能自发进行的条件是___________ (填“高温”或“低温”)。
(3)催化剂活化: (无活性)
(无活性)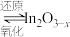 (有活性),
(有活性), 与
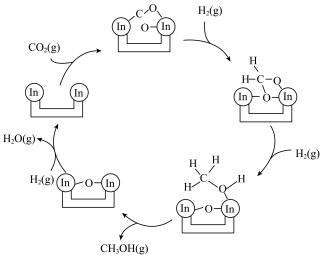
与 在活化后的催化剂表面发生反应Ⅰ,其反应历程如图,同时伴随反应Ⅱ:
在活化后的催化剂表面发生反应Ⅰ,其反应历程如图,同时伴随反应Ⅱ: 。
。 选择性
选择性 。
。
①对于以上 制甲醇的过程,以下描述正确的是
制甲醇的过程,以下描述正确的是___________ (填序号)。
A.反应中经历了 、
、 键的形成和断裂
键的形成和断裂
B.加压可以提高 的平衡转化率
的平衡转化率
C.升高温度可以提高甲醇在平衡时的选择性
② 与
与 混合气体以不同的流速通过反应器,气体流速与
混合气体以不同的流速通过反应器,气体流速与 转化率、
转化率、 选择性的关系如图3,流速加快可减少产物中
选择性的关系如图3,流速加快可减少产物中 的积累,减少反应
的积累,减少反应___________ (用化学方程式表示)的发生,从而减少催化剂的失活,提高甲醇选择性。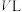 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 发生上述(2)中的反应Ⅰ、Ⅱ、Ⅲ,达到平衡时,容器中
发生上述(2)中的反应Ⅰ、Ⅱ、Ⅲ,达到平衡时,容器中 为
为 ,
, 为
为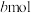 ,此时
,此时 的浓度为
的浓度为___________  ,反应Ⅱ的平衡常数为
,反应Ⅱ的平衡常数为___________ 。(用含 、
、 、
、 的代数式表示)
的代数式表示)
 资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
资源化利用是解决资源和能源短缺、减少碳排放的一种途径。方案一:以
 为原料合成乙烯
为原料合成乙烯(1)以
 和
和 催化合成乙烯:
催化合成乙烯: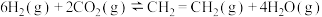
 。
。在一定压强下,将
 和
和 加入1L容积不变的密闭容器中,已知温度对
加入1L容积不变的密闭容器中,已知温度对 的平衡转化率、实际转化率和催化剂催化效率的影响如图所示,结合图像分析该反应实际反应温度定于250℃的原因可能是
的平衡转化率、实际转化率和催化剂催化效率的影响如图所示,结合图像分析该反应实际反应温度定于250℃的原因可能是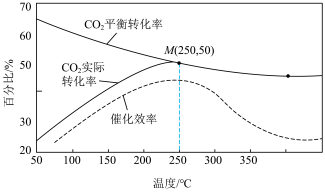
 为原料合成甲醇
为原料合成甲醇(2)以
 合成甲醇涉及的反应如下:
合成甲醇涉及的反应如下:反应Ⅰ:


反应Ⅱ:

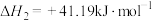
反应Ⅲ:

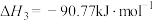

 ,反应Ⅲ能自发进行的条件是
,反应Ⅲ能自发进行的条件是(3)催化剂活化:
 (无活性)
(无活性)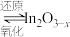 (有活性),
(有活性), 与
与 在活化后的催化剂表面发生反应Ⅰ,其反应历程如图,同时伴随反应Ⅱ:
在活化后的催化剂表面发生反应Ⅰ,其反应历程如图,同时伴随反应Ⅱ: 。
。
 选择性
选择性 。
。①对于以上
 制甲醇的过程,以下描述正确的是
制甲醇的过程,以下描述正确的是A.反应中经历了
 、
、 键的形成和断裂
键的形成和断裂B.加压可以提高
 的平衡转化率
的平衡转化率C.升高温度可以提高甲醇在平衡时的选择性
②
 与
与 混合气体以不同的流速通过反应器,气体流速与
混合气体以不同的流速通过反应器,气体流速与 转化率、
转化率、 选择性的关系如图3,流速加快可减少产物中
选择性的关系如图3,流速加快可减少产物中 的积累,减少反应
的积累,减少反应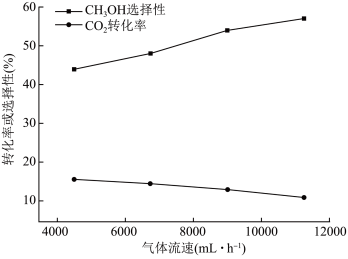
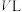 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 发生上述(2)中的反应Ⅰ、Ⅱ、Ⅲ,达到平衡时,容器中
发生上述(2)中的反应Ⅰ、Ⅱ、Ⅲ,达到平衡时,容器中 为
为 ,
, 为
为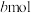 ,此时
,此时 的浓度为
的浓度为 ,反应Ⅱ的平衡常数为
,反应Ⅱ的平衡常数为 、
、 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
8 . “鱼浮灵”是一种常用的化学增氧剂,其主要成分是过碳酸钠( ),也被称作“固体双氧水”,具有
),也被称作“固体双氧水”,具有 和
和 的双重性质,50℃开始分解,溶解度随温度的升高而增大,在乙醇中溶解度较低。
的双重性质,50℃开始分解,溶解度随温度的升高而增大,在乙醇中溶解度较低。
Ⅰ.过碳酸钠的合成
某学习小组用 与稳定剂的混合溶液和
与稳定剂的混合溶液和 化合制备过碳酸钠。称取
化合制备过碳酸钠。称取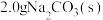 配制成饱和溶液后加入三颈烧瓶中,加入稳定剂,搅拌使其溶解。接着加入11mL乙醇搅匀,再加入
配制成饱和溶液后加入三颈烧瓶中,加入稳定剂,搅拌使其溶解。接着加入11mL乙醇搅匀,再加入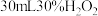 溶液搅匀。然后将盛有反应混合物的三颈烧瓶置于冰水浴中,搅拌反应30min,装置如图所示。
溶液搅匀。然后将盛有反应混合物的三颈烧瓶置于冰水浴中,搅拌反应30min,装置如图所示。___________ 。反应过程中冰水浴的目的是___________ 。
(2)写出生成过碳酸钠的化学方程式:___________ 。
(3)反应生成物用减压过滤装置抽滤,其优点是___________ 。
(4)为了获得更纯的过碳酸钠固体,最后进行静置、过滤、洗涤、低温烘干,洗涤应选用的试剂是___________ 。
A.热水 B.碳酸钠溶液 C.乙醇
Ⅱ.过碳酸钠含量的测定
取0.14g过碳酸钠样品和少量二氧化锰倒入气囊Q(Q为弹性良好的气球,气囊内外气压差可忽略,导管内气体体积可忽略不计)中进行测定,装置如下。
(6)若无其他杂质,同温同压下量筒Ⅰ与量筒Ⅱ所测气体的体积比理论值为___________ 。若测得量筒Ⅱ中气体的体积为11.2mL(已折算成标准状况),则样品中过碳酸钠的含量为___________ %(保留两位有效数字)。
 ),也被称作“固体双氧水”,具有
),也被称作“固体双氧水”,具有 和
和 的双重性质,50℃开始分解,溶解度随温度的升高而增大,在乙醇中溶解度较低。
的双重性质,50℃开始分解,溶解度随温度的升高而增大,在乙醇中溶解度较低。Ⅰ.过碳酸钠的合成
某学习小组用
 与稳定剂的混合溶液和
与稳定剂的混合溶液和 化合制备过碳酸钠。称取
化合制备过碳酸钠。称取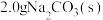 配制成饱和溶液后加入三颈烧瓶中,加入稳定剂,搅拌使其溶解。接着加入11mL乙醇搅匀,再加入
配制成饱和溶液后加入三颈烧瓶中,加入稳定剂,搅拌使其溶解。接着加入11mL乙醇搅匀,再加入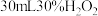 溶液搅匀。然后将盛有反应混合物的三颈烧瓶置于冰水浴中,搅拌反应30min,装置如图所示。
溶液搅匀。然后将盛有反应混合物的三颈烧瓶置于冰水浴中,搅拌反应30min,装置如图所示。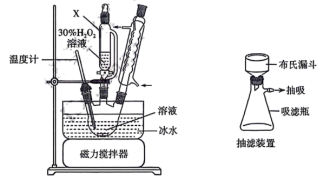
(2)写出生成过碳酸钠的化学方程式:
(3)反应生成物用减压过滤装置抽滤,其优点是
(4)为了获得更纯的过碳酸钠固体,最后进行静置、过滤、洗涤、低温烘干,洗涤应选用的试剂是
A.热水 B.碳酸钠溶液 C.乙醇
Ⅱ.过碳酸钠含量的测定
取0.14g过碳酸钠样品和少量二氧化锰倒入气囊Q(Q为弹性良好的气球,气囊内外气压差可忽略,导管内气体体积可忽略不计)中进行测定,装置如下。
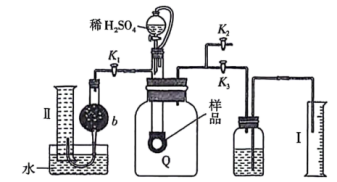
A.气囊Q中产生的气体主要成分为 、 、 |
B.测定气体总体积必须关闭 、 、 ,打开 ,打开 |
| C.量筒Ⅰ用于测二氧化碳的量,干燥管b中装入碱石灰,量筒Ⅱ用于测氧气的量 |
D.读完气体总体积后,关闭 ,缓缓打开 ,缓缓打开 、 、 ,可观察到气囊Q慢慢缩小 ,可观察到气囊Q慢慢缩小 |
您最近一年使用:0次
9 . 某冶炼厂电解精炼铜产生的阳极泥经分铜、分金后得到的分银渣中仍含有Pb、Sn、Bi、Sb和极少量的Au、Ag等多种富有经济价值的稀贵金属元素。选择“ 、
、 熔融盐法”对分银渣加以利用,回收Sn、Pb元素的部分工艺流程如下:
熔融盐法”对分银渣加以利用,回收Sn、Pb元素的部分工艺流程如下: 、
、 。
。
回答下列问题:
(1)将分银渣“球磨”的目的是___________ 。
(2)滤渣①中所含金属元素主要有___________ 。
(3)写出Sn在“熔炼”时反应的化学方程式:___________ 。
(4)向“含铅溶液”加入 可生成PbS,写出该反应的离子方程式:
可生成PbS,写出该反应的离子方程式:___________ ,经处理得到可以循环利用的物质是___________ (填化学式)。
(5)选取“球磨”后的分银渣,在熔炼温度700℃进行试验,熔炼时间对金属回收率的影响如图所示,“熔炼”选择的合适时间是___________ 。 )具有介电性质,晶体属于钙钛矿结构的立方晶系,锡酸钙贮锂材料有着高能量密度、无污染、资源丰富及价格便宜等优点,是极具发展潜力的一种负极材料。
)具有介电性质,晶体属于钙钛矿结构的立方晶系,锡酸钙贮锂材料有着高能量密度、无污染、资源丰富及价格便宜等优点,是极具发展潜力的一种负极材料。 中金属离子与氧离子间的作用力为
中金属离子与氧离子间的作用力为___________ ,该晶体中每个氧离子周围与它最近且距离相等的氧离子有___________ 个。若晶胞参数为 ,则晶体密度为
,则晶体密度为___________  (设
(设 表示阿伏加德罗常数的值,列出计算式即可)。
表示阿伏加德罗常数的值,列出计算式即可)。
 、
、 熔融盐法”对分银渣加以利用,回收Sn、Pb元素的部分工艺流程如下:
熔融盐法”对分银渣加以利用,回收Sn、Pb元素的部分工艺流程如下: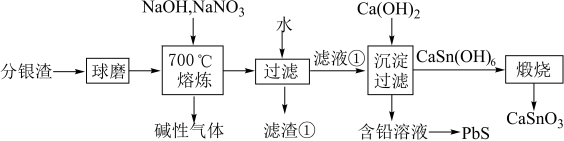
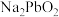 、
、 。
。回答下列问题:
(1)将分银渣“球磨”的目的是
(2)滤渣①中所含金属元素主要有
(3)写出Sn在“熔炼”时反应的化学方程式:
(4)向“含铅溶液”加入
 可生成PbS,写出该反应的离子方程式:
可生成PbS,写出该反应的离子方程式:(5)选取“球磨”后的分银渣,在熔炼温度700℃进行试验,熔炼时间对金属回收率的影响如图所示,“熔炼”选择的合适时间是

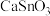 )具有介电性质,晶体属于钙钛矿结构的立方晶系,锡酸钙贮锂材料有着高能量密度、无污染、资源丰富及价格便宜等优点,是极具发展潜力的一种负极材料。
)具有介电性质,晶体属于钙钛矿结构的立方晶系,锡酸钙贮锂材料有着高能量密度、无污染、资源丰富及价格便宜等优点,是极具发展潜力的一种负极材料。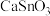 中金属离子与氧离子间的作用力为
中金属离子与氧离子间的作用力为 ,则晶体密度为
,则晶体密度为 (设
(设 表示阿伏加德罗常数的值,列出计算式即可)。
表示阿伏加德罗常数的值,列出计算式即可)。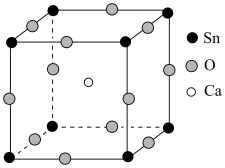
您最近一年使用:0次
10 . 甲醇( )是一种重要的有机化工原料,可用于制取甲醚(
)是一种重要的有机化工原料,可用于制取甲醚( )。在3个容积均为1L的恒容密闭容器中发生反应:
)。在3个容积均为1L的恒容密闭容器中发生反应: 。下列说法正确的是
。下列说法正确的是
 )是一种重要的有机化工原料,可用于制取甲醚(
)是一种重要的有机化工原料,可用于制取甲醚( )。在3个容积均为1L的恒容密闭容器中发生反应:
)。在3个容积均为1L的恒容密闭容器中发生反应: 。下列说法正确的是
。下列说法正确的是| 容器编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
 |  |  | ||
| Ⅰ | 387 | 0.2 | 0.08 | 0.08 |
| Ⅱ | 387 | 0.4 | ||
| Ⅲ | 207 | 0.2 | 0.09 | 0.09 |
A.该反应的 |
B.达到平衡时,容器Ⅰ中的 体积分数比容器Ⅱ中的小 体积分数比容器Ⅱ中的小 |
C.若容器Ⅲ中反应达到平衡所需时间为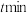 ,则用甲醇浓度变化表示 ,则用甲醇浓度变化表示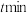 内的平均反应速率 内的平均反应速率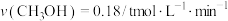 |
D.若在387℃,某时刻混合物的浓度分别为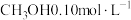 、 、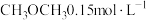 和 和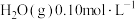 ,则该反应逆向进行 ,则该反应逆向进行 |
您最近一年使用:0次