名校
解题方法
1 . 某高分子化合物M常用于制作眼镜镜片,可由N和P两种物质合成,M、N、P的结构如图所示,下列说法正确的是
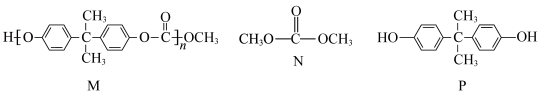
| A.N与P合成M的反应为加聚反应 | B.M的链节中在同一平面的碳原子最多有14个 |
| C.P在空气中很稳定,可以保存在广口瓶中 | D.常温下,M、N、P均易溶于水 |
您最近一年使用:0次
7日内更新
|
347次组卷
|
4卷引用:2024届山西省晋中市和诚高中高三下学期理综冲刺卷(二)-高中化学
名校
2 . 已知 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法错误 的是
 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法| A.甲组同学用到500mL容量瓶、玻璃棒、烧杯、胶头滴管等玻璃仪器 |
B.乙组实验中 将 将 氧化为 氧化为 |
C.丙组实验发生反应的离子方程式: |
D.丁组实验说明还原性: |
您最近一年使用:0次
7日内更新
|
245次组卷
|
5卷引用:2024届山西省晋中市和诚高中高三下学期理综冲刺卷(二)-高中化学
2024届山西省晋中市和诚高中高三下学期理综冲刺卷(二)-高中化学河北省2024届高三下学期普通高中学业水平选择性考试化学冲刺卷(二)河南省许昌高级中学2023-2024学年高三下学期5月月考化学试题2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
解题方法
3 . 下列有关物质结构与性质的说法正确的是
A. 和 和 中C、O、N杂化方式均相同 中C、O、N杂化方式均相同 |
| B.含有手性碳原子的分子叫做手性分子 |
| C.NaClO和NaCl均为离子化合物,他们所含的化学键类型相同 |
D. 的空间结构为V形 的空间结构为V形 |
您最近一年使用:0次
解题方法
4 . 2023年9月23日晚,第19届亚运会在杭州开幕。下列有关说法错误的是
| A.火炬“薪火”使用的铝合金熔点比纯铝低 |
| B.“亚运莲花尊”的青瓷是以黏土为主要原料,经高温烧结而成 |
| C.会馆使用的防滑剂主要成分石墨烯与乙烯互为同系物 |
| D.主火炬塔的燃料首次使用废碳再生的绿色甲醇,有利于实现碳中和 |
您最近一年使用:0次
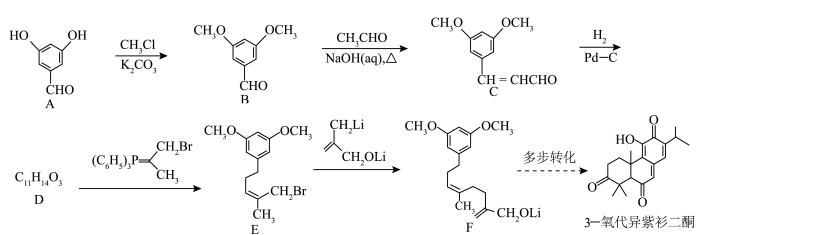
5 . 3-氧代异紫杉二酮是从台湾杉中提取的具有抗癌活性的天然产物。最近科学家完成了该物质的全合成,其关键中间体(F)的合成路线如下:
(1)A的化学名称为_______ (用系统命名法命名), 的反应中
的反应中 的作用为
的作用为_______ 。
(2)C→D反应的化学方程式为_______ 。
(3)E的分子式为_______ 。
(4)3-氧代异紫杉二酮中所含官能团的名称为羰基、_______ 。
(5)化合物R是B的同分异构体,满足以下条件的R有_______ 种(不考虑立体异构);
①含有苯环且苯环上有两个取代基
②能与银氨溶液发生银镜反应,并且能发生水解反应
③能与金属钠反应放出氢气
其中一种分子的核磁共振氢谱有6组峰,峰面积之比为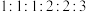 ,且遇
,且遇 溶液显紫色,该分子的结构简式为
溶液显紫色,该分子的结构简式为_______ (任写一种)。
已知:
(1)A的化学名称为
 的反应中
的反应中 的作用为
的作用为(2)C→D反应的化学方程式为
(3)E的分子式为
(4)3-氧代异紫杉二酮中所含官能团的名称为羰基、
(5)化合物R是B的同分异构体,满足以下条件的R有
①含有苯环且苯环上有两个取代基
②能与银氨溶液发生银镜反应,并且能发生水解反应
③能与金属钠反应放出氢气
其中一种分子的核磁共振氢谱有6组峰,峰面积之比为
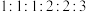 ,且遇
,且遇 溶液显紫色,该分子的结构简式为
溶液显紫色,该分子的结构简式为
您最近一年使用:0次
6 . 常温下,用KOH溶液分别滴定 、
、 溶液、
溶液、 溶液,
溶液, [
[ 表示负对数,
表示负对数, 表示
表示 、
、 、
、 ]随pH变化的关系图,已知
]随pH变化的关系图,已知 ,下列说法正确的是
,下列说法正确的是
 、
、 溶液、
溶液、 溶液,
溶液, [
[ 表示负对数,
表示负对数, 表示
表示 、
、 、
、 ]随pH变化的关系图,已知
]随pH变化的关系图,已知 ,下列说法正确的是
,下列说法正确的是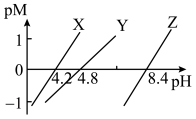
A. 的电离平衡常数 的电离平衡常数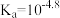 |
B.直线X代表滴定 溶液的变化关系 溶液的变化关系 |
C.将物质的量均为0.1mol的 、 、 溶于 溶于 水中快速搅拌均匀,该分散系中 水中快速搅拌均匀,该分散系中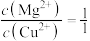 |
D. 易溶于 易溶于 |
您最近一年使用:0次
解题方法
7 . 下列符号表征和说法正确的是
A. 电离: 电离: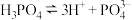 | B. 位于元素周期表s区 位于元素周期表s区 |
C. 空间结构:三角锥形 空间结构:三角锥形 | D. 电子式: 电子式: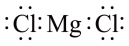 |
您最近一年使用:0次
8 . 水煤气变换反应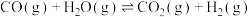
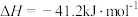 可用于制氢,该反应可分两步完成:
可用于制氢,该反应可分两步完成:
①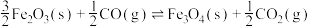
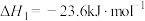
②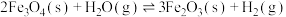
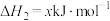
请回答下列问题:
(1)x=___________ 。
(2)下列有利于提高H2的平衡产率的措施是___________(填字母)。
(3)总反应的催化剂是___________ (填化学式),测定其属于晶体的方法是___________ ,在其活性温度范围内,反应历程包含吸附(快速的过程)、反应及脱附等过程。随着温度升高,该反应的反应速率先增大后减小,其速率减小的原因与___________ 因素有关(填一条)。
(4)保持压强为1.7MPa,按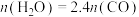 进行投料,曲线a、b分别表示不同条件下反应达到平衡,相应物质的分压[如
进行投料,曲线a、b分别表示不同条件下反应达到平衡,相应物质的分压[如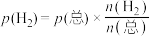 ]如图所示。
]如图所示。___________ ,平衡常数
___________ 。
②根据图中信息,曲线a中H2的产率比曲线b低的主要原因可能是___________ (用化学方程式表示,不考虑 )。
)。
(5)整个反应过程都是“气-固”反应,有利于气固接触的措施是___________ (填一条)。
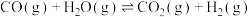
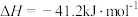 可用于制氢,该反应可分两步完成:
可用于制氢,该反应可分两步完成:①
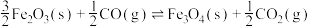
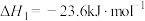
②
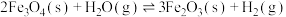
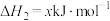
请回答下列问题:
(1)x=
(2)下列有利于提高H2的平衡产率的措施是___________(填字母)。
| A.升高温度 | B.保持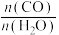 一定,增大体系总压 一定,增大体系总压 |
| C.向体系中投入一定量的纳米CaO | D.增大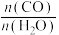 |
(3)总反应的催化剂是
(4)保持压强为1.7MPa,按
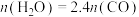 进行投料,曲线a、b分别表示不同条件下反应达到平衡,相应物质的分压[如
进行投料,曲线a、b分别表示不同条件下反应达到平衡,相应物质的分压[如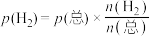 ]如图所示。
]如图所示。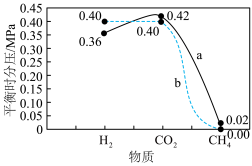

②根据图中信息,曲线a中H2的产率比曲线b低的主要原因可能是
 )。
)。(5)整个反应过程都是“气-固”反应,有利于气固接触的措施是
您最近一年使用:0次
解题方法
9 . 近年来,随着新能源汽车行业高速发展,市场对磷酸铁锂( )的需求量也随之增加。以硫铁矿(主要成分是
)的需求量也随之增加。以硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 为原料制备)
为原料制备) 的流程如图所示:
的流程如图所示:
请回答下列问题:
(1)写出磷酸铁锂中相应价态基态铁离子的电子排布式:___________ 。
(2)“焙烧”生成 的化学方程式为
的化学方程式为___________ 。
(3)“还原”选用足量FeS的优点是___________ ;“除铝”时,溶液的pH应控制的范围是___________ 。
(4)“氧化”加入 的目的除了可以增强H2O2的氧化性外,还可以
的目的除了可以增强H2O2的氧化性外,还可以___________ 。
(5)“沉铁”后的滤液中阴离子除了 外,还检验出
外,还检验出 和
和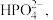 写出“沉铁”反应的离子方程式:
写出“沉铁”反应的离子方程式:___________ 。
(6)“高温煅烧”条件下,由 制备
制备 ,理论上
,理论上 和
和 的投料比为
的投料比为
___________ 。
(7) 的晶胞结构如图a所示,Li⁺分别处于顶点、部分的棱心和面心。电池充电时
的晶胞结构如图a所示,Li⁺分别处于顶点、部分的棱心和面心。电池充电时 脱出部分Li⁺形成
脱出部分Li⁺形成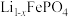 ,结构如图b所示,则
,结构如图b所示,则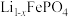 中
中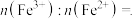
___________ (填最简整数比)。
 )的需求量也随之增加。以硫铁矿(主要成分是
)的需求量也随之增加。以硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 为原料制备)
为原料制备) 的流程如图所示:
的流程如图所示:
| 金属氢氧化物 |  |  |  |
| 开始沉淀的pH | 2.3 | 6.8 | 3.5 |
| 完全沉淀的pH | 3.2 | 8.3 | 4.6 |
(1)写出磷酸铁锂中相应价态基态铁离子的电子排布式:
(2)“焙烧”生成
 的化学方程式为
的化学方程式为(3)“还原”选用足量FeS的优点是
(4)“氧化”加入
 的目的除了可以增强H2O2的氧化性外,还可以
的目的除了可以增强H2O2的氧化性外,还可以(5)“沉铁”后的滤液中阴离子除了
 外,还检验出
外,还检验出 和
和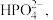 写出“沉铁”反应的离子方程式:
写出“沉铁”反应的离子方程式:(6)“高温煅烧”条件下,由
 制备
制备 ,理论上
,理论上 和
和 的投料比为
的投料比为
(7)
 的晶胞结构如图a所示,Li⁺分别处于顶点、部分的棱心和面心。电池充电时
的晶胞结构如图a所示,Li⁺分别处于顶点、部分的棱心和面心。电池充电时 脱出部分Li⁺形成
脱出部分Li⁺形成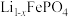 ,结构如图b所示,则
,结构如图b所示,则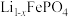 中
中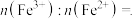

您最近一年使用:0次
解题方法
10 .  还原
还原 是实现“双碳”经济的有效途径之一。在密闭容器中(
是实现“双碳”经济的有效途径之一。在密闭容器中( 和
和 按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现
按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现 的高效转化。
的高效转化。
 还原
还原 是实现“双碳”经济的有效途径之一。在密闭容器中(
是实现“双碳”经济的有效途径之一。在密闭容器中( 和
和 按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现
按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现 的高效转化。
的高效转化。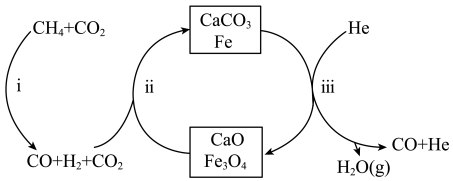
A.该反应的催化剂为 和 和 |
| B.过程iii在恒压条件下通入He,有利于增加CO的产量 |
| C.过程i、ii、iii均涉及置换反应 |
D.每生成4mol的CO,转移的电子数约为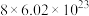 |
您最近一年使用:0次



