名校
解题方法
1 . 丙烯是一种重要的化工原料,但丙烯的产量仅通过石油的催化裂解反应无法满足工业生产需求。工业上以WO3/SiO2为催化剂,利用丁烯和乙烯的催化歧化反应制丙烯: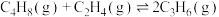
 。请回答下列问题:
。请回答下列问题:
(1)相关物质的燃烧热数据如下表所示:
催化歧化反应的
___________  ;
;
(2)利用丁烯和乙烯的催化歧化反应制备丙烯时,仅 发生如下反应:
反应ⅰ: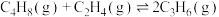
反应ⅱ:
一定条件下,经相同反应时间,丙烯的产率、丁烯的转化率随温度变化的关系如图所示:___________ ,500~550℃丙烯产率下降的原因为___________ 。
②某温度下,保持体系总压强为1.0 MPa,按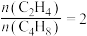 投料,达平衡状态时,C4H8、C2H4的转化率分别为96%、32%,则平衡时
投料,达平衡状态时,C4H8、C2H4的转化率分别为96%、32%,则平衡时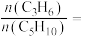
___________ ;反应ⅰ的压强平衡常数
___________ (保留三位有效数字)。
(3)反应ⅱ中,WO3/SiO2催化机理如图,关于该过程中的说法错误的是___________(填字母)。
(4)为了增强WO3/SiO2催化剂的活性和吸附能力,其他条件一定时,可向WO3/SiO2催化剂中添加催化剂助剂。下图为不同催化剂助剂的加入对丁烯的转化率、丙烯的选择性(产率 转化率
转化率 选择性)的影响,选择
选择性)的影响,选择___________ 作催化剂助剂为优选方案(填化学式)。
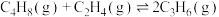
 。请回答下列问题:
。请回答下列问题:(1)相关物质的燃烧热数据如下表所示:
| 物质 |  |  | 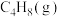 |
燃烧热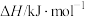 | -1411 | -2049 | -2539 |

 ;
;(2)利用丁烯和乙烯的催化歧化反应制备丙烯时,
反应ⅰ:
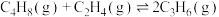
反应ⅱ:

一定条件下,经相同反应时间,丙烯的产率、丁烯的转化率随温度变化的关系如图所示:

②某温度下,保持体系总压强为1.0 MPa,按
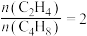 投料,达平衡状态时,C4H8、C2H4的转化率分别为96%、32%,则平衡时
投料,达平衡状态时,C4H8、C2H4的转化率分别为96%、32%,则平衡时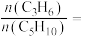

(3)反应ⅱ中,WO3/SiO2催化机理如图,关于该过程中的说法错误的是___________(填字母)。
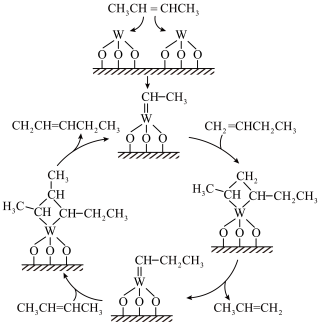
| A.有加成反应发生 | B.能将2-丁烯转化为1-丁烯 |
| C.W元素的成键数目一直未发生变化 | D.存在碳碳单键的断裂和形成 |
 转化率
转化率 选择性)的影响,选择
选择性)的影响,选择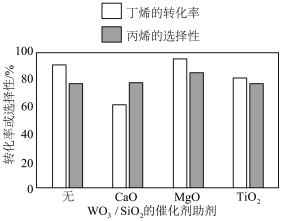
您最近半年使用:0次
今日更新
|
632次组卷
|
4卷引用:东北三省2024届高三下学期三校二模联考化学试题
名校
解题方法
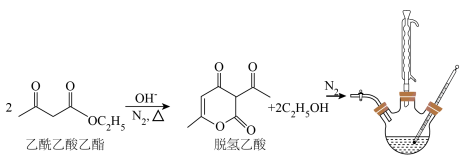
2 . 脱氢乙酸是一种重要的有机合成中间体和低毒高效食品防腐剂,实验室以乙酰乙酸乙酯为原料,在OH-的催化作用下制备脱氢乙酸的反应原理和实验装置如图(夹持和加热装置已省略):
Ⅰ.脱氢乙酸的合成
①在N2氛围中,向三颈烧瓶中加入100 mL乙酰乙酸乙酯和0.05 g催化剂,磁力搅拌加热10 min后再升高至某温度,回流一段时间。
②反应结束后,将其改为蒸馏装置,控制温度为80℃左右蒸出乙醇,在三颈烧瓶中得到脱氢乙酸粗产品。
Ⅱ.脱氢乙酸的分离与提纯
将盛有脱氢乙酸粗产品的三颈烧瓶改为下图中的装置B,进行水蒸气蒸馏(夹持和加热装置已省略),蒸出乙酰乙酸乙酯和脱氢乙酸,过滤装置C中的混合物,得白色晶体,再用乙醇洗涤该晶体,干燥后得固体产品56.0 g。
(1)步骤Ⅰ中通入N2的目的是___________ 。
(2)步骤Ⅰ中②过程中不需要用到的仪器为___________ (填字母)。___________ ℃、___________ h、___________ 作催化剂。与其他催化剂相比,所选催化剂使脱氢乙酸产率最高的原因可能为___________ 。___________ ,漏斗的作用为___________ 。
(5)脱氢乙酸的产率约为___________(填字母)。
| 名称 | 相对分子质量 | 性状 | 密度/ | 熔点/℃ | 沸点/℃ | 物理性质 |
| 乙酰乙酸乙酯 | 130 | 无色透明液体 | 1.03 | -39 | 180.8 | 微溶于水,易溶于乙醇等有机溶剂 |
| 脱氢乙酸 | 168 | 白色晶体 | — | 109~111 | 269.9 | 微溶于乙醇和冷水,具有较强的还原性 |
| 乙醇 | 46 | 无色透明液体 | 0.79 | -114.1 | 78.3 | 与水任意比例互溶,易溶于有机溶剂 |
①在N2氛围中,向三颈烧瓶中加入100 mL乙酰乙酸乙酯和0.05 g催化剂,磁力搅拌加热10 min后再升高至某温度,回流一段时间。
②反应结束后,将其改为蒸馏装置,控制温度为80℃左右蒸出乙醇,在三颈烧瓶中得到脱氢乙酸粗产品。
Ⅱ.脱氢乙酸的分离与提纯
将盛有脱氢乙酸粗产品的三颈烧瓶改为下图中的装置B,进行水蒸气蒸馏(夹持和加热装置已省略),蒸出乙酰乙酸乙酯和脱氢乙酸,过滤装置C中的混合物,得白色晶体,再用乙醇洗涤该晶体,干燥后得固体产品56.0 g。
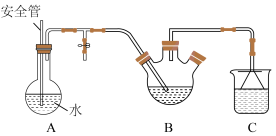
(1)步骤Ⅰ中通入N2的目的是
(2)步骤Ⅰ中②过程中不需要用到的仪器为


(5)脱氢乙酸的产率约为___________(填字母)。
| A.54% | B.64% | C.74% | D.84% |
您最近半年使用:0次
昨日更新
|
432次组卷
|
3卷引用:东北三省2024届高三下学期三校二模联考化学试题
名校
3 . 回答下列问题
(1)Si原子结构示意图为___________ ,在硅酸盐中, 四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,Si与O的原子数之比为
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,Si与O的原子数之比为___________ 。___________ ,写出检验过程中生成配位数为6的配合物的离子方程式 ___________ 。
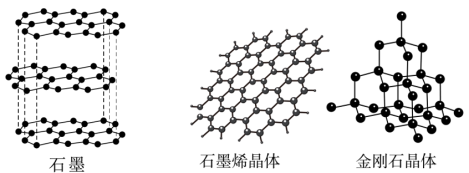
(3)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示,石墨烯是从石墨材料中剥离出来的,下列说法正确的是___________ 。
B.石墨中的碳原子采取sp2杂化,金刚石晶体中,C原子采取 杂化
杂化
C.石墨属于混合型晶体,层与层之间存在分子间作用力
D.在金刚石晶体中,C原子所连接的最小环为六元环,每个C原子连接12个六元环,六元环中最多有4个C原子在同一平面
E.石墨烯中平均每个六元碳环含有3个碳原子
(4)经X射线衍射测定发现,晶体钴的晶胞和堆积方式剖面图如下图所示,则该晶胞中含钴原子个数为___________ 个,若该堆积方式下钴原子的半径为r,则该晶体的空间利用率为___________ (用含π的代数式表示。空间利用率=原子总体积与晶胞体积之比)。
(1)Si原子结构示意图为
 四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,Si与O的原子数之比为
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,Si与O的原子数之比为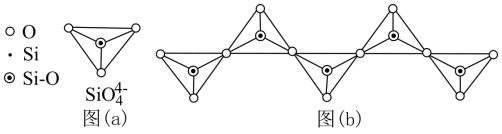
(3)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示,石墨烯是从石墨材料中剥离出来的,下列说法正确的是
B.石墨中的碳原子采取sp2杂化,金刚石晶体中,C原子采取
 杂化
杂化C.石墨属于混合型晶体,层与层之间存在分子间作用力
D.在金刚石晶体中,C原子所连接的最小环为六元环,每个C原子连接12个六元环,六元环中最多有4个C原子在同一平面
E.石墨烯中平均每个六元碳环含有3个碳原子
(4)经X射线衍射测定发现,晶体钴的晶胞和堆积方式剖面图如下图所示,则该晶胞中含钴原子个数为


您最近半年使用:0次
2024·黑龙江·模拟预测
4 . 下列有关物质的结构与性质说法正确的是
| A.第二、三周期B、Al的第一电离能高于相邻元素,N、P的第一电离能低于相邻元素 |
| B.键能:F-F大于Cl-Cl |
| C.O3是极性分子,它在水中溶解度高于在四氯化碳的溶解度 |
| D.甲醇分子间的氢键键能大于水分子间的氢键键能 |
您最近半年使用:0次
5 . 在工业流程题中常使用 作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对
作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对 与Mn+的反应情况进行了以下探究:
与Mn+的反应情况进行了以下探究:
已知:①Ca2++2 =CaCO3↓+CO2↑+H2O K1=5×104
=CaCO3↓+CO2↑+H2O K1=5×104
②Ca2++2 =Ca(OH)2↓+2CO2↑ K2=1×10-10
=Ca(OH)2↓+2CO2↑ K2=1×10-10
③Cu2++2 =CuCO3↓+CO2↑+H2O K3=8×106
=CuCO3↓+CO2↑+H2O K3=8×106
④Cu2++2 =Cu(OH)2↓+2CO2↑ K4=3×104
=Cu(OH)2↓+2CO2↑ K4=3×104
下列关于该探究实验的叙述正确的是
 作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对
作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对 与Mn+的反应情况进行了以下探究:
与Mn+的反应情况进行了以下探究:| 操作 | 现象 | |
| 1 | 0.5mol·L-1CaCl2溶液与NaHCO3溶液混合 | 产生气泡,生成白色沉淀 |
| 2 | 0.5mol·L-1CuCl2溶液与NaHCO3溶液混合 | 产生气泡,生成蓝色沉淀 |
| 3 | 0.5mol·L-1FeCl3溶液与NaHCO3溶液混合 | 产生大量气泡,生成红褐色沉淀 |
| 4 | 取2中的蓝色沉淀加热并将氧化产物依次通过无水CuSO4和澄清石灰水 | 无水CuSO4变蓝,澄清石灰水变浑浊 |
 =CaCO3↓+CO2↑+H2O K1=5×104
=CaCO3↓+CO2↑+H2O K1=5×104②Ca2++2
 =Ca(OH)2↓+2CO2↑ K2=1×10-10
=Ca(OH)2↓+2CO2↑ K2=1×10-10③Cu2++2
 =CuCO3↓+CO2↑+H2O K3=8×106
=CuCO3↓+CO2↑+H2O K3=8×106④Cu2++2
 =Cu(OH)2↓+2CO2↑ K4=3×104
=Cu(OH)2↓+2CO2↑ K4=3×104下列关于该探究实验的叙述正确的是
| A.实验1生成的沉淀为Ca(OH)2 |
| B.实验2生成的沉淀为Cu(OH)2 |
C. 与M2+反应生成MCO3沉淀的离子方程式为M2++ 与M2+反应生成MCO3沉淀的离子方程式为M2++ =MCO3↓+H+ =MCO3↓+H+ |
D.实验3发生反应的离子方程式为Fe3++3 =Fe(OH)3↓+3CO2↑ =Fe(OH)3↓+3CO2↑ |
您最近半年使用:0次
2024·黑龙江·模拟预测
解题方法
6 . 中华文化源远流长,化学与文化传承密不可分。下列叙述错误的是
| A.江西博物馆中“《论语》竹简”中竹简的主要成分是纤维素 |
| B.安徽古代科学家方以智在其《物理小识》“有硇水者,剪银块投之,则旋而为水”,其中的“硇水”指醋酸 |
| C.甘肃出土的春秋早期秦国的铜柄铁剑中,铁元素有化合态和游离态两种存在形式 |
| D.广西壮锦的主要原料是蚕丝等,蚕丝属于有机高分子化合物 |
您最近半年使用:0次
2024·湖南常德·一模
名校
解题方法
7 . 我国是世界上最大的糠醛生产国和出口国,糠酸是一种重要的医药中间体和化工中间体,工业上以 为催化剂,催化氧化糠醛制备糠酸,其反应原理如下:
为催化剂,催化氧化糠醛制备糠酸,其反应原理如下:
②碱性条件下,糠醛分子间易发生自聚反应而生成高聚物。
回答下列问题:
(1)实验室利用图1所示装置完成步骤I,该步骤采用的加热方式为___________ 。三颈烧瓶中发生的反应的化学方程式为___________ 。 、
、 下端的活塞,并使滴加速度相同,以便反应物滴加到三颈烧瓶内能与氧化铜瞬时混合。该操作的优点为
下端的活塞,并使滴加速度相同,以便反应物滴加到三颈烧瓶内能与氧化铜瞬时混合。该操作的优点为___________ 。
(3)步骤III中,悬浊液经“过滤、洗涤、干燥”得到糠酸粗品。进一步提纯糠酸的实验操作方法是___________ 。
(4)糠酸纯度的测定:取1.120g提纯后的糠酸样品,配成100mL溶液,准确量取25.00mL于锥形瓶中,加入几滴酚酞溶液,用
 标准溶液滴定,平行滴定三次,平均消耗
标准溶液滴定,平行滴定三次,平均消耗 标准溶液24.80mL。
标准溶液24.80mL。
①量取糠酸溶液的仪器是___________ (填仪器名称)。
②糠酸的纯度为___________ 。
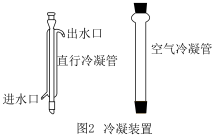
(5)为了提高糠酸的纯度,需提纯糠醛。实验室常用蒸馏方法得到较纯糠醛。因蒸气温度高于140℃,实验时选用图2中空气冷凝管而不是直形冷凝管的原因是___________ 。
 为催化剂,催化氧化糠醛制备糠酸,其反应原理如下:
为催化剂,催化氧化糠醛制备糠酸,其反应原理如下: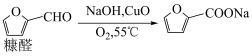
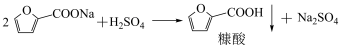
其反应的步骤为:
| 熔点 | 沸点 | 溶解性 | 相对分子质量 | |
| 糠醛 | -36.5℃ | 161℃ | 常温下与水部分互溶 | 96 |
| 糠酸 | 133℃ | 230℃ | 微溶于冷水、易溶于热水 | 112 |
回答下列问题:
(1)实验室利用图1所示装置完成步骤I,该步骤采用的加热方式为

 、
、 下端的活塞,并使滴加速度相同,以便反应物滴加到三颈烧瓶内能与氧化铜瞬时混合。该操作的优点为
下端的活塞,并使滴加速度相同,以便反应物滴加到三颈烧瓶内能与氧化铜瞬时混合。该操作的优点为(3)步骤III中,悬浊液经“过滤、洗涤、干燥”得到糠酸粗品。进一步提纯糠酸的实验操作方法是
(4)糠酸纯度的测定:取1.120g提纯后的糠酸样品,配成100mL溶液,准确量取25.00mL于锥形瓶中,加入几滴酚酞溶液,用

 标准溶液滴定,平行滴定三次,平均消耗
标准溶液滴定,平行滴定三次,平均消耗 标准溶液24.80mL。
标准溶液24.80mL。①量取糠酸溶液的仪器是
②糠酸的纯度为
(5)为了提高糠酸的纯度,需提纯糠醛。实验室常用蒸馏方法得到较纯糠醛。因蒸气温度高于140℃,实验时选用图2中空气冷凝管而不是直形冷凝管的原因是
您最近半年使用:0次
7日内更新
|
499次组卷
|
4卷引用:化学(新七省高考“15+4”)-2024年高考押题预测卷
(已下线)化学(新七省高考“15+4”)-2024年高考押题预测卷湖南省常德市2024届高三下学期模拟考试化学试卷 (已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届宁夏回族自治区银川一中高三下学期第二次模拟考试理科综合试卷-高中化学
2024·河北石家庄·二模
解题方法
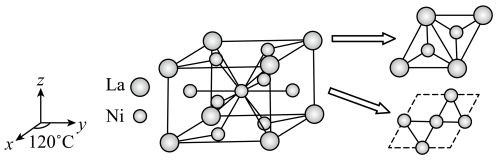
8 . 镧镍合金是一种储氢材料,其晶胞可认为由两种结构不同的层交替堆积而成,如下图所示,该合金的密度为p g·cm-3.已知该合金的晶胞中最多可容纳9个氢原子。下列叙述错误的是
| A.基态Ni原子的价电子排布式为3d84s2 |
| B.该合金的化学式为LaNi5 |
C.设La的原子坐标为(0,0,0),则晶胞底面上Ni的原子坐标为系( , ,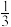 ,0)或( ,0)或( , , ,0) ,0) |
D.假定吸氢后体积不变,则合金中氢的最大密度为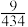 ρg·cm-3 ρg·cm-3 |
您最近半年使用:0次
2024·河南·二模
9 . Oppenauer氧化反应,是以酮类为氧化剂,以异丙基氧化铝[ ]为催化剂,将醇类氧化为醛或酮,比如:
]为催化剂,将醇类氧化为醛或酮,比如:
 ]为催化剂,将醇类氧化为醛或酮,比如:
]为催化剂,将醇类氧化为醛或酮,比如: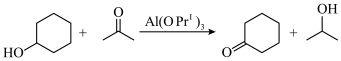

| A.反应过程中铝元素的化合价发生了变化 | B.反应①中,有异丙醇生成 |
| C.Oppenauer氧化反应的过程中没有还原反应发生 | D.反应②只涉及到了C-O、C-H和O-H的变化 |
您最近半年使用:0次
名校
解题方法
10 . KMnO4是重要氧化剂,广泛用于化工、防腐以及制药等领域。以软锰矿(主要成分为MnO2)为原料,经中间产物K2MnO4制备KMnO4的流程如图。下列说法错误的是
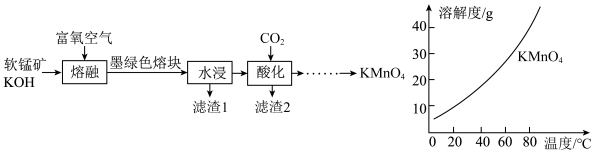
A.“熔融”过程中,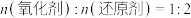 |
| B.滤渣2经处理后可循环回“熔融”过程以提高锰元素的利用率 |
| C.用盐酸替代CO2能加快“酸化”时的速率 |
| D.得到KMnO4晶体的操作为蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥 |
您最近半年使用:0次
7日内更新
|
392次组卷
|
4卷引用:东北三省2024届高三下学期三校二模联考化学试题
东北三省2024届高三下学期三校二模联考化学试题黑龙江省哈尔滨市三校联考2024届高三二模化学试题(已下线)化学(新七省高考“15+4”)-2024年高考押题预测卷东北三省2024届高三下学期三校二模联考化学试题



