名校
1 . 利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;②沉淀I中只含有两种沉淀;③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)浸出过程中Co2O3发生反应的离子反应方程式为_________________ 。
(2)NaClO3在浸出液中发生的离子反应方程式为______________ 。
(3)加入Na2CO3调PH至5.2,目的是________ ;萃取剂层含锰元素,则沉淀II的主要成分为_____ 。
(4)操作I包括:将水层加入浓盐酸调整PH为2-3,______ 、_____ 、过滤、洗涤、减压烘干等过程。
(5)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是_____ (回答一条原因即可)。

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;②沉淀I中只含有两种沉淀;③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中Co2O3发生反应的离子反应方程式为
(2)NaClO3在浸出液中发生的离子反应方程式为
(3)加入Na2CO3调PH至5.2,目的是
(4)操作I包括:将水层加入浓盐酸调整PH为2-3,
(5)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是
您最近一年使用:0次
2019-10-10更新
|
428次组卷
|
5卷引用:黑龙江省大兴安岭漠河县第一中学2020届高三上学期月考化学试题
11-12高三上·辽宁大连·期中
2 . 下列实验过程能引起结果偏高的是 ( )
①配制100gl0%CuSO4溶液,称取l0g硫酸铜晶体溶于90g水中
②测定硫酸铜晶体中结晶水的百分含量时,所用的晶体已经受潮
③配制一定物质的量浓度的硫酸溶液时,定容时俯视容量瓶的刻度线
④质量分数为10%和90%的两种硫酸等质量混合配制50%的硫酸溶液
①配制100gl0%CuSO4溶液,称取l0g硫酸铜晶体溶于90g水中
②测定硫酸铜晶体中结晶水的百分含量时,所用的晶体已经受潮
③配制一定物质的量浓度的硫酸溶液时,定容时俯视容量瓶的刻度线
④质量分数为10%和90%的两种硫酸等质量混合配制50%的硫酸溶液
| A.①④ | B.②④ | C.②③ | D.②③④ |
您最近一年使用:0次
2016-12-09更新
|
96次组卷
|
5卷引用:黑龙江省大兴安岭漠河县第一中学2019-2020学年高一上学期11月月考化学试题
黑龙江省大兴安岭漠河县第一中学2019-2020学年高一上学期11月月考化学试题(已下线)2012届辽宁省大连二十四中高三上学期期中考试化学试卷(已下线)2012届辽宁省本溪一中、庄河高中高三上学期期末联考卷三化学试卷(已下线)2012届辽宁省大连24中上学期高三年级期中考试化学试卷 2014-2015学年湖北省枣阳一中高二下学期第三次月检测化学试卷
3 . 氰基丙烯酸酯在碱性条件下能快速聚合为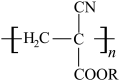 ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
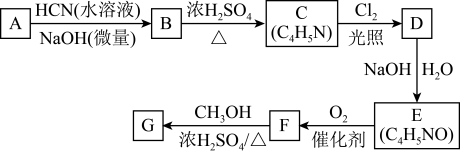
已知:①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A的化学名称为_______ 。
(2)B的结构简式为____ ,其核磁共振氢谱显示为_____ 组峰,峰面积比为_______ 。
(3)由C生成D的反应类型为_______ 。
(4)由D生成E的化学方程式为_______ 。
(5)G中的官能团有_______ 、 _______ 、_______ 。(填官能团名称)
 ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
已知:①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②

回答下列问题:
(1)A的化学名称为
(2)B的结构简式为
(3)由C生成D的反应类型为
(4)由D生成E的化学方程式为
(5)G中的官能团有
您最近一年使用:0次
名校
解题方法
4 . 亚氯酸钠( )在溶液中会生成
)在溶液中会生成 、
、 、
、 、
、 等,其中
等,其中 和
和 都具有漂白作用。已知
都具有漂白作用。已知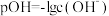 ,经测定
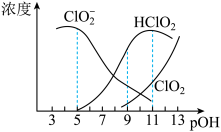
,经测定 时各组分含量随
时各组分含量随 变化情况如图所示(
变化情况如图所示( 没有画出),此温度下,下列分析正确的是
没有画出),此温度下,下列分析正确的是
 )在溶液中会生成
)在溶液中会生成 、
、 、
、 、
、 等,其中
等,其中 和
和 都具有漂白作用。已知
都具有漂白作用。已知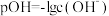 ,经测定
,经测定 时各组分含量随
时各组分含量随 变化情况如图所示(
变化情况如图所示( 没有画出),此温度下,下列分析正确的是
没有画出),此温度下,下列分析正确的是
A. 的电离平衡常数的数值 的电离平衡常数的数值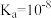 |
B.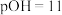 时, 时, 部分转化成 部分转化成 和 和 离子的方程式为 离子的方程式为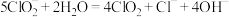 |
C. 时,溶液中含氯微粒的浓度大小为 时,溶液中含氯微粒的浓度大小为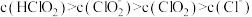 |
D.同浓度的 溶液和 溶液和 溶液等体积混合,则混合溶液中有 溶液等体积混合,则混合溶液中有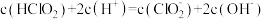 |
您最近一年使用:0次
2011·浙江嘉兴·一模
名校
5 . 若以w1和w2分别表示浓度为c1mol/L和c2mol/L的氨水的质量分数,且知2c1=c2,则下列推断正确的是
| A.2 w1= w2 | B.2 w2= w1 | C.w2>2 w1 | D.w1< w2<2 w1 |
您最近一年使用:0次
2021-12-01更新
|
163次组卷
|
40卷引用:黑龙江省大兴安岭漠河县第一中学2019-2020学年高一上学期第一次阶段考试化学试题
黑龙江省大兴安岭漠河县第一中学2019-2020学年高一上学期第一次阶段考试化学试题(已下线)2012届浙江省海盐元济高级中学高三上学期摸底考试化学试卷(已下线)2012届山东省莱州一中高三第一次质量检测化学试卷(已下线)2012届甘肃省天水一中高三上学期第一阶段考试化学试卷(已下线)2012届河北省唐山一中高三上学期期中考试化学试卷(已下线)上海市崇明中学2012届高三上学期期中考试化学试卷(已下线)2011-2012学年湖北省襄阳市四校高一上学期期中考试化学试卷(已下线)2011-2012学年广东省深圳高级中高一上学期期末考试化学试卷(已下线)2013届湖南省浏阳一中高考复习阶段测试化学试卷(已下线)2012-2013学年黑龙江大庆铁人中学高一上学期期中考试化学试卷(已下线)2015届湖南省益阳市箴言中学高三上学期第二次模拟考试化学试卷(已下线)2014-2015学年云南省玉溪市一中高一上学期期中化学试卷2015届江西省吉安市白鹭洲中学高三上学期期中化学试卷2016届甘肃省兰州第一中学高三9月月考化学试卷2016届河北省衡水市冀州中学高三上一轮复习检测一化学试卷2017届河北省望都中学高三8月月考化学试卷2017届甘肃省兰州一中高三上学期9月月考化学试卷2017届河北省定兴第三中学高三上学期第一次月考化学试卷河北省石家庄市第一中学2016-2017学年高二下学期期中考试化学试题河北省武邑中学2018届高三上学期第一次月考化学试题辽宁省葫芦岛市第一中学2017-2018学年高一上学期第一次月考化学试题辽宁省葫芦岛市第一高级中学2017-2018学年高一上学期第一次月考化学试题安徽省太和县第一中学2018-2019学年高一(超越班、飞越班)上学期第一次月考学情调研化学试题【全国百强校】江西省新余市第四中学2018-2019学年高一上学期10月月考化学试题【全国百强校】安徽省师范大学附属中学2018-2019学年高一上学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2020届高三9月月考化学试题湖南岳阳七中2020届高三9月化学考试题安徽省安庆市桐城中学2019-2020学年高一上学期第一次月考化学试题河南省辉县市第一高级中学2019-2020学年高一10月月考化学试题吉林省白城市第一中学2019-2020学年高一上学期期中考试化学试题云南省金平县第一中学2019-2020学年高一上学期期末考试化学试题安徽省亳州市涡阳县育萃中学2019-2020学年高一上学期第二次月考化学试题吉林省辽源市第五中学校2019-2020学年高一上学期第一次月考化学试题(已下线)【浙江新东方】双师(27)黑龙江省哈尔滨市第三中学2020-2021学年高一上学期期末考试化学试卷江西省景德镇市第一中学2021-2022学年高一上学期期中17班化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高一上学期期末考试化学试题安徽省宿城第一中学2022-2023学年高一上学期阶段检测化学试题江西省宜春市宜丰中学2023-2024学年高三下学期3月月考化学试题(已下线)第02讲 物质的量浓度(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
6 . 设阿伏加德罗常数的值为NA,下列说法正确的是
A.1mol NH 中含电子数目为11NA 中含电子数目为11NA |
| B.22.4LHCl含原子数目为NA |
| C.100g 质量分数为98% 的H2SO4溶液中含有氧原子的数目为4NA |
| D.标准状况下,2.7g Al与足量盐酸充分反应,生成H2的体积为3.36L |
您最近一年使用:0次
9-10高二下·江苏淮安·期末
名校
7 . 在一密闭容器中,反应aX(g) bY(g)达平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,Y的浓度是原来的60%,则
bY(g)达平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,Y的浓度是原来的60%,则
 bY(g)达平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,Y的浓度是原来的60%,则
bY(g)达平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,Y的浓度是原来的60%,则| A.平衡向正反应方向移动了 | B.物质X的转化率减小了 |
| C.物质Y的质量分数降低了 | D.a>b |
您最近一年使用:0次
2021-05-25更新
|
353次组卷
|
76卷引用:黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期第一次月考化学试题
黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期第一次月考化学试题(已下线)2010年江苏省淮安市淮阴区高二第二学期期末化学试卷(已下线)2010年青海省青海师大附中高二上学期期中考试化学试卷(已下线)2010—2011学年内蒙古赤峰二中高一下学期期末考试化学试卷(已下线)2011-2012年河北省南宫中学高二上学期9月份月考化学(理)试卷(已下线)2011-2012年广东省汕头市金山中学高二上学期期中考试化学试卷(理科)(已下线)2011-2012学年贵州省湄潭中学高二上学期期末考试化学试卷(已下线)2011-2012学年福建省龙岩一中上学期高二期末考试化学试卷(已下线)2011-2012学年山西省康杰中学高二下学期期中考试化学试卷(已下线)2012-2013学年江苏泰州二中高二上学期期中考试化学(选修)试卷(已下线)2013届辽宁省实验中学分校高三12月月考化学试卷(已下线)2012-2013学年陕西省长安一中高二下学期期中考试化学试卷(已下线)2013-2014学年河北省遵化市高二上学期期中质量检测化学试卷(已下线)2013-2014江西省鹰潭市下学期期末质量检测高一化学试卷(已下线)2014届江西省九江一中上学期期中考试高二化学试卷2014-2015河南省濮阳市一中高二上学期第三次质量检测化学试卷2014-2015河南省濮阳市一中高二上学期第三次月考化学试卷2014-2015江西省德镇市高二上学期期末化学试卷2015-2016学年河北大名县第一中学高二上学期第一次月考试化学试卷2015-2016学年重庆市杨家坪中学高二上学期第一次月考化学试卷2016届浙江省建人高复学校高三上学期第三次月考化学试卷2015-2016学年浙江省桐乡市高级中学高二上期中(普通班)化学试卷2015-2016学年吉林省松原市油田高中高一下期中化学试卷2015-2016学年辽宁省实验中学分校高一下学期6月月考化学试卷2017届山东省滕州市第二中学高三上学期10月月考化学试卷2016-2017学年河北省卓越联盟高二上第一次月考化学试卷2016-2017学年甘肃省民乐一中高二上10月月考化学试卷2016-2017学年黑龙江哈尔滨六中高二上期末化学卷2016-2017学年湖南省长沙市第一中学高二上学期期末考试化学试卷安徽省蚌埠市第二中学2017-2018学年高二8月月考化学试题2018版化学(苏教版)高考总复习专题七增分补课7--化学平衡分析中的虚拟过程--化学反应的方向和限度新疆呼图壁县第一中学2017-2018学年高二上学期期中考试化学试题新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题贵州省铜仁伟才学校2017-2018学年高二上学期期中考试化学(理)试题(已下线)2018年9月19日 《每日一题》人教选修4-平衡转化率的判断新疆维吾尔自治区昌吉市第四中学2018-2019学年第一学期高二第一次月考化学试题四川省成都市实验中学2018-2019学年高二上学期期中模拟考试化学试题【校级联考】江西省南昌市八一中学、洪都中学七校2018-2019学年高二上学期期中考试化学试题【全国百强校】湖南省衡阳市第一中学2018-2019学年高二上学期期中考试化学试题新疆自治区昌吉市第九中学2018-2019学年高二上学期第二次月考化学试题山东省微山县第二中学2018-2019学年高二上学期第三学段教学质量监测化学试题河北省承德第一中学2019-2020学年高二上学期开学考试化学试题河北省大名县第一中学2019-2020学年高二9月月考化学试题河北省邯郸大名一中2019-2020学年高二上学期第一次月考化学试题浙江省台州市五校2020届高三10月联考化学试题山东省日照市第一中学2019-2020学年高二10月月考化学试题天津市静海区大邱庄中学等四校2019-2020学年高二10联考化学试题安徽省蚌埠铁路中学2019-2020学年高二上学期期中考试化学试题黑龙江省海林市朝鲜族中学2019-2020学年高二上学期期中考试化学试题安徽省滁州市六校2019-2020学年高二12月联考化学试题宁夏贺兰县景博中学2019-2020学年高二上学期第一次月考化学试题河南省三门峡市第一高级中学2020-2021学年高二上学期9月月考化学试题宁夏银川市第二中学2020-2021学年高二上学期月考(一)化学试题山西省朔州市怀仁县怀仁一中云东校区2020-2021学年高二上学期第二次月考化学试题安徽省马鞍山市含山县含山中学2020-2021学年高二上学期第一次月考化学试题河北省张家口市宣化区宣化第一中学2020-2021学年高二上学期10月月考化学试题辽宁省锦州市义县高级中学2020-2021学年高二10月月考化学试题四川省广安市武胜烈面中学校2020-2021学年高二上学期10月月考化学试题湖北省汉川市第二中学2020-2021学年高二上学期期中考试化学试题海南省海口市灵山中学2019—2020学年高二上学期期中测试化学试题内蒙古通辽市科左后旗甘旗卡第二高级中学2020-2021学年高二下学期开学考试化学试题宁夏大学附属中学2020-2021学年高二下学期第一次月考化学试题陕西省西安市高新一中2020-2021学年高一下学期5月月考化学试题(已下线)作业06 化学反应的调控-2021年高二化学暑假作业(人教版2019)重庆市第七中学校2021-2022学年高二上学期第一次月考化学试题海南省东方市琼西中学2021-2022学年高二上学期第一次月考化学试题陕西省渭南市咸林中学2021-2022学年高二上学期第三阶段检测化学试题(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)内蒙古包头市第四中学2020-2021学年高二上学期第一次月考化学试题重庆市石柱中学校2021-2022学年高二上学期第一次月考化学试题山东省枣庄滕州市第一中学2022-2023学年高二上学期10月月考化学试题苏教2020版选择性必修1专题2第三单元 化学平衡的移动课后习题辽宁省大连庄河市高级中学2022-2023学年高二上学期12月月考化学(B卷)试题宁夏中卫市中宁县2022-2023学年高二上学期质量测查(期末)化学试题2.3.1浓度 压强变化对化学平衡的影响 课中重庆市璧山来凤中学2023-2024学年高二上学期9月月考化学试题
8 . (1)3.6克H2O的物质的量是_________ ,含有____________ 个H2O。
(2)物质的量浓度为18.4 mol·L-1,密度为1.84 g·mL-1的硫酸的质量分数为____ ,配制1000 mL浓度为1.84 mol·L-1 的硫酸,需要物质的量浓度为18.4 mol·L-1的硫酸______ L。
(3)将190 g MgCl2溶于水配制成1 L溶液。溶液中MgCl2的物质的量浓度为________ 。从中取出50 mL溶液,含有Cl-的物质的量为________ 。
(2)物质的量浓度为18.4 mol·L-1,密度为1.84 g·mL-1的硫酸的质量分数为
(3)将190 g MgCl2溶于水配制成1 L溶液。溶液中MgCl2的物质的量浓度为
您最近一年使用:0次
2013·上海奉贤·二模
9 . 只给出下列甲中和乙中对应的量,可以组成一个物质的量的公式的是 ( )
| ① | ② | ③ | ④ | ⑤ | |
| 甲 | 物质微粒数 | 标准状况气体摩尔体积 | 固体体积 | 非标况物质质量 | 溶液质量分数 |
| 乙 | 阿伏加 德罗常数 | 标准状况气体体积 | 固体密度 | 物质的摩尔质量 | 溶液体积 |
| A.①② | B.①②③ | C.①②④ | D.①②⑤ |
您最近一年使用:0次
解题方法
10 . T ℃时一个恒容的密闭容器中发生可逆反应:mA(g)+nB(g) pC(g)+qD(g)。当m、n、p、q为任意正整数时,不能判断反应达到平衡状态的是
pC(g)+qD(g)。当m、n、p、q为任意正整数时,不能判断反应达到平衡状态的是
 pC(g)+qD(g)。当m、n、p、q为任意正整数时,不能判断反应达到平衡状态的是
pC(g)+qD(g)。当m、n、p、q为任意正整数时,不能判断反应达到平衡状态的是| A.v正(A)=v逆(A) |
| B.各组分的浓度不再改变 |
| C.各组分的质量分数不再改变 |
| D.反应速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q |
您最近一年使用:0次
2020-01-18更新
|
136次组卷
|
2卷引用:黑龙江省大兴安岭漠河县第一中学2018-2019学年高二上学期新高考教学质量检测化学试题



