名校
1 . 硼、氮、铁、钴、镍等元素可形成结构、性质各异的物质,在生产、科研中发挥着重要用途。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
(2)硼酸( )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在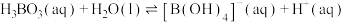 的平衡,回答下列问题。
的平衡,回答下列问题。__________ 。
②下列关于硼酸的说法正确的是__________ (填序号)。
a. 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
c.硼酸分子的稳定性与氢键有关 d.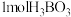 晶体中有
晶体中有 氢键
氢键
(3)叠氮化合物在化工上有重要应用, 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式__________ (写出一种即可),其立体构型为__________ 。
(4) 的结构如图所示,
的结构如图所示, 中
中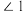 、
、 、
、 由大到小的顺序是
由大到小的顺序是____________________ 。 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于__________ 位置。
①从该晶胞中能分割出来的结构图有_______ (填标号)。 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有__________ 个,该距离为__________ pm(仅列式不计算)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
A.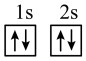 | B. |
C.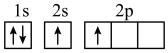 | D.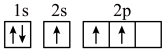 |
(2)硼酸(
 )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在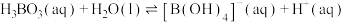 的平衡,回答下列问题。
的平衡,回答下列问题。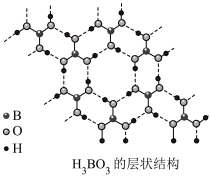
②下列关于硼酸的说法正确的是
a.
 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制c.硼酸分子的稳定性与氢键有关 d.
 晶体中有
晶体中有 氢键
氢键(3)叠氮化合物在化工上有重要应用,
 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式(4)
 的结构如图所示,
的结构如图所示, 中
中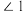 、
、 、
、 由大到小的顺序是
由大到小的顺序是
 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于
①从该晶胞中能分割出来的结构图有
a.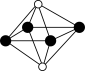 b.
b.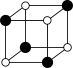 c.
c.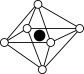 d.
d. e.
e.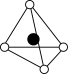
 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
您最近一年使用:0次
名校
2 . A、B、M是生活中最常见的前四周期金属元素,A元素的单质既可与强酸反应也可与强碱反应,B位于周期表的第八纵行,其+3价离子比+2价离子在水溶液中稳定,M原子的价电子排布为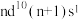 。回答下列问题:
。回答下列问题:
(1) 的价电子排布式为
的价电子排布式为___________ 。
(2) 为黄色粘稠状液体,60℃在空气中可自燃,其结构和部分键长如图所示。
为黄色粘稠状液体,60℃在空气中可自燃,其结构和部分键长如图所示。 更接近于
更接近于___________ (填晶体类型)。下列说法错误的是___________ (填标号)。 中B的化合价为0
中B的化合价为0
B.配体与B原子所形成的配位键的键能相同
C.B在周期表中位于VIII族,属于d区元素
D.制备 应在隔绝空气的条件下进行
应在隔绝空气的条件下进行
(3) 中存在的
中存在的 键有
键有___________ mol。 具有对称的空间结构,其中2个
具有对称的空间结构,其中2个 分别被
分别被 取代能得到两种不同结构的
取代能得到两种不同结构的 ,则
,则 中由4个
中由4个 围成的图形是
围成的图形是___________ 。
(4)金属A与M可形成多种组成不同的合金,其中一种合金的晶胞如图甲所示(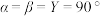 ),图乙为晶胞在z轴方向的投影。
),图乙为晶胞在z轴方向的投影。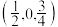 ,则b点原子的分数坐标为
,则b点原子的分数坐标为___________ 。
②该晶体的密度为___________  (用含NA的计算式回答)。
(用含NA的计算式回答)。
(5) 能与
能与 、
、 形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为
形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为___________ 。
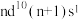 。回答下列问题:
。回答下列问题:(1)
 的价电子排布式为
的价电子排布式为(2)
 为黄色粘稠状液体,60℃在空气中可自燃,其结构和部分键长如图所示。
为黄色粘稠状液体,60℃在空气中可自燃,其结构和部分键长如图所示。 更接近于
更接近于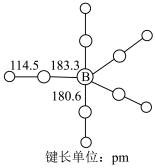
 中B的化合价为0
中B的化合价为0B.配体与B原子所形成的配位键的键能相同
C.B在周期表中位于VIII族,属于d区元素
D.制备
 应在隔绝空气的条件下进行
应在隔绝空气的条件下进行(3)
 中存在的
中存在的 键有
键有 具有对称的空间结构,其中2个
具有对称的空间结构,其中2个 分别被
分别被 取代能得到两种不同结构的
取代能得到两种不同结构的 ,则
,则 中由4个
中由4个 围成的图形是
围成的图形是(4)金属A与M可形成多种组成不同的合金,其中一种合金的晶胞如图甲所示(
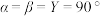 ),图乙为晶胞在z轴方向的投影。
),图乙为晶胞在z轴方向的投影。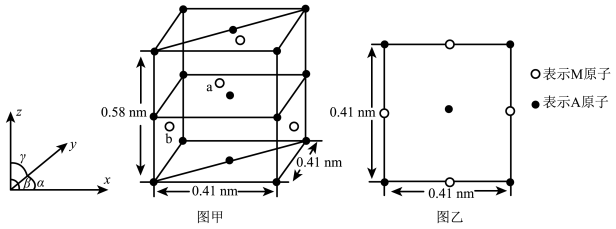
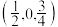 ,则b点原子的分数坐标为
,则b点原子的分数坐标为②该晶体的密度为
 (用含NA的计算式回答)。
(用含NA的计算式回答)。(5)
 能与
能与 、
、 形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为
形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为
您最近一年使用:0次
名校
解题方法
3 . 在稀土开采技术方面,我国遥遥领先。我国科学家最早研究的是稀土——钴化合物的结构。请回答下列问题:
(1)基态钴原子的核外未成对电子数为_______ 。
(2)一种钴的配合物乙二胺四乙酸合钴的结构如图所示,碳原子的杂化类型有_______ 。_______ (填“极性”或“非极性”)分子,其VSEPR模型为_______ 。
(4)橙红色晶体羰基钴的熔点为52℃,分子式为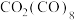 ,是一种重要的无机金属配合物,可溶于多数有机溶剂。配体CO中与Co形成配位键的原子是C而非O,原因是
,是一种重要的无机金属配合物,可溶于多数有机溶剂。配体CO中与Co形成配位键的原子是C而非O,原因是_______ 。
(1)基态钴原子的核外未成对电子数为
(2)一种钴的配合物乙二胺四乙酸合钴的结构如图所示,碳原子的杂化类型有

(4)橙红色晶体羰基钴的熔点为52℃,分子式为
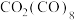 ,是一种重要的无机金属配合物,可溶于多数有机溶剂。配体CO中与Co形成配位键的原子是C而非O,原因是
,是一种重要的无机金属配合物,可溶于多数有机溶剂。配体CO中与Co形成配位键的原子是C而非O,原因是
您最近一年使用:0次
名校
解题方法
4 . 下表为周期表的一部分,其中的编号代表对应的元素,请用元素符号回答下列问题_______ 。(填元素符号)
(2)③、④与⑤三种元素的第一电离能由小到大的顺序_______ (填元素符号)。
(3)对于元素⑨与⑩,不能说明⑨的金属性比⑩强的是_______。
(4)元素⑧与⑩形成的化合物的电子式为_______ 。
(5)元素④与①形成的最简单化合物X具有极易溶于水的性质,其原因为_______ 。
(6)元素⑫与CO可形成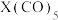 型化合物,该化合物常温下呈液态,熔点为
型化合物,该化合物常温下呈液态,熔点为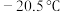 ,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于_______ 晶体(填晶体类型)1mol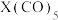 中含有σ键数目为
中含有σ键数目为_______ 。
(7)⑦的最高价氧化物的水化物与⑨的最高价氧化物的水化物反应的离子方程式为_______ 。
(8)⑦单质为面心立方晶体,晶胞中⑦原子的配位数为_______ 。
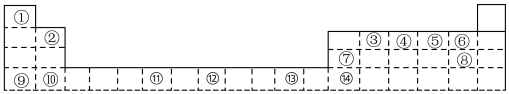
(2)③、④与⑤三种元素的第一电离能由小到大的顺序
(3)对于元素⑨与⑩,不能说明⑨的金属性比⑩强的是_______。
A.⑨与 反应比⑩与 反应比⑩与 反应剧烈; 反应剧烈; |
| B.⑨单质的熔、沸点比⑩的低; |
| C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强; |
| D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少。 |
(4)元素⑧与⑩形成的化合物的电子式为
(5)元素④与①形成的最简单化合物X具有极易溶于水的性质,其原因为
(6)元素⑫与CO可形成
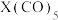 型化合物,该化合物常温下呈液态,熔点为
型化合物,该化合物常温下呈液态,熔点为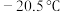 ,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于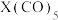 中含有σ键数目为
中含有σ键数目为(7)⑦的最高价氧化物的水化物与⑨的最高价氧化物的水化物反应的离子方程式为
(8)⑦单质为面心立方晶体,晶胞中⑦原子的配位数为
您最近一年使用:0次
名校
5 . 下表是元素周期表的一部分,其中所列数字分别代表某一元素
(1)表中属于d区的元素是___________ (填编号)。
(2)⑤⑥⑦三种元素中电负性最大的是___________ (填写元素符号),在第二周期中第一电离能介于②和③之间的元素有___________ 种。
(3)元素⑨在周期表中的位置___________ 。
(4)元素⑧和⑦能形成一种常见的干燥剂,它的电子式为___________ 。
(5)⑥和⑦相比较,非金属性较弱的是___________ (填元素符号),可以验证你的结论的是下列中的___________ (填编号)。
A.气态氢化物的稳定性 B.两元素的电负性 C.含氧酸的酸性 D.最高化合价
(6)①与③的元素形成的10电子中性分子X的空间构型为___________ ,它极易溶于水中,请简要说明该物质易溶于水的原因___________ 。

(1)表中属于d区的元素是
(2)⑤⑥⑦三种元素中电负性最大的是
(3)元素⑨在周期表中的位置
(4)元素⑧和⑦能形成一种常见的干燥剂,它的电子式为
(5)⑥和⑦相比较,非金属性较弱的是
A.气态氢化物的稳定性 B.两元素的电负性 C.含氧酸的酸性 D.最高化合价
(6)①与③的元素形成的10电子中性分子X的空间构型为
您最近一年使用:0次
名校
6 . 下列说法不正确的是
| A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶规律解释 |
B.乳酸分子(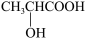 )中含有一个手性碳原子 )中含有一个手性碳原子 |
| C.亚硝酰氟(NOF)的空间构型为V形 |
D.键角大小: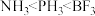 |
您最近一年使用:0次
名校
7 . 某原子的结构示意图为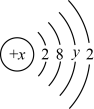 ,则x、y及该原子3p能级上的电子数不可能分别为
,则x、y及该原子3p能级上的电子数不可能分别为
| A.20、8、6 | B.24、12、6 | C.26、14、6 | D.30、18、6 |
您最近一年使用:0次
名校
解题方法
8 . 设 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是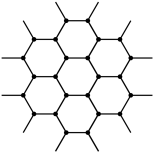
A.HCl分子中的共价键是s-p 键 键 |
B. 键可以绕键轴旋转,π键一定不能绕键轴旋转 键可以绕键轴旋转,π键一定不能绕键轴旋转 |
C. , , 、 、 中σ键都是C—H键 中σ键都是C—H键 |
D.如图表示石墨的层状结构,24g石墨中含有 个六元环 个六元环 |
您最近一年使用:0次
名校
9 . 某种废弃电子元器件的主要成分为 、
、 ,还含有少量的
,还含有少量的 、
、 等,实验室中以其为原料提取金属
等,实验室中以其为原料提取金属 和胆矾的工艺流程如图。
和胆矾的工艺流程如图。 如表。
如表。
回答下列问题:
(1)基态 、
、 原子核外未成对电子数之比为
原子核外未成对电子数之比为_______ 。
(2) 为两性氧化物,
为两性氧化物, 在“碱浸”时发生反应的离子方程式为
在“碱浸”时发生反应的离子方程式为_______ 。
(3)滤渣2的主要成分为_______ , 中心原子的杂化方式是
中心原子的杂化方式是_______ 。
(4)“氧化”时 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(5)加试剂X调 可得
可得 沉淀和滤液2,则所加试剂X为
沉淀和滤液2,则所加试剂X为_______ ,所调 的范围为
的范围为_______ 。
(6)请你以 、铁粉和稀硫酸为原料,设计一个简单的实验方案制备绿矾:
、铁粉和稀硫酸为原料,设计一个简单的实验方案制备绿矾:_______ 。
可以不写满也可以自己划线继续补充:
①_______,
②_______,
③_______,
④_______,
⑤_______。
 、
、 ,还含有少量的
,还含有少量的 、
、 等,实验室中以其为原料提取金属
等,实验室中以其为原料提取金属 和胆矾的工艺流程如图。
和胆矾的工艺流程如图。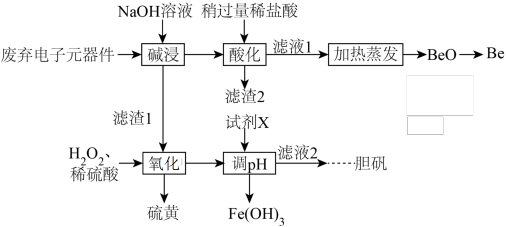
 如表。
如表。| 金属阳离子 |  |  |  |
开始沉淀的 | 2.2 | 5.8 | 4.2 |
沉淀完全的 | 3.2 | 8.8 | 7.7 |
(1)基态
 、
、 原子核外未成对电子数之比为
原子核外未成对电子数之比为(2)
 为两性氧化物,
为两性氧化物, 在“碱浸”时发生反应的离子方程式为
在“碱浸”时发生反应的离子方程式为(3)滤渣2的主要成分为
 中心原子的杂化方式是
中心原子的杂化方式是(4)“氧化”时
 发生反应的离子方程式为
发生反应的离子方程式为(5)加试剂X调
 可得
可得 沉淀和滤液2,则所加试剂X为
沉淀和滤液2,则所加试剂X为 的范围为
的范围为(6)请你以
 、铁粉和稀硫酸为原料,设计一个简单的实验方案制备绿矾:
、铁粉和稀硫酸为原料,设计一个简单的实验方案制备绿矾:可以不写满也可以自己划线继续补充:
①_______,
②_______,
③_______,
④_______,
⑤_______。
您最近一年使用:0次
名校
10 . 下列化学用语或示意图正确的是
A. 的结构式: 的结构式: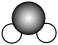 | B. 的VSEPR模型: 的VSEPR模型: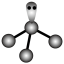 |
C. 的名称:1,4-戊二烯 的名称:1,4-戊二烯 | D.羟基的电子式: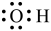 |
您最近一年使用:0次



