1 . 用如图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0.7克镁带(已打磨光亮),按如图连接好装置,从A中加入20.0ml0.5mol/LH2SO4。记录注射器活塞的位置和相应的时间。记录数据如表:
(1)仪器A的名称是____ ,其使用前必须进行的操作是____ 。
(2)0-t时间段与t-2t时间段,化学反应速率最快的是____ 时间段,原因是____ 。
(3)用上述装置探究Fe3+、Cu2+对双氧水分解速率的影响,所用试剂:5%H2O2、0.1mol/LFeC13、0.2mol/LCuCl2。完成表格的实验设计:
表中需要添加的物质是_____ mLFeCl3溶液。
(4)查阅资料,FeCl3溶液和CuCl2溶液都能对H2O2分解起催化作用,起作用的微粒分别是Fe3+和Cu2+,且Fe3+比Cu2+催化效果更好。设计实验证实这种说法的正确性。
试管乙中滴加的试剂_____ ,进行丙试管实验的目的_____ 。
| 时间/s | t | 2t | …… |  | |
| 活塞的位置/mL | 17.3 | 25.6 | 36.6 | …… |
(2)0-t时间段与t-2t时间段,化学反应速率最快的是
(3)用上述装置探究Fe3+、Cu2+对双氧水分解速率的影响,所用试剂:5%H2O2、0.1mol/LFeC13、0.2mol/LCuCl2。完成表格的实验设计:
| 实验序号 | 双氧水体积/mL | 蒸馏水体积/mL | 添加的物质 |
| I | 10 | 0 | _____mLFeCl3 |
| 2 | 10 | 2 | 2mLCuCl2 |
(4)查阅资料,FeCl3溶液和CuCl2溶液都能对H2O2分解起催化作用,起作用的微粒分别是Fe3+和Cu2+,且Fe3+比Cu2+催化效果更好。设计实验证实这种说法的正确性。
| 试管 | 甲 | 乙 | 丙 |
| 盛装试剂 | 10mL5%H2O2 | 10mL5%H2O2 | 10mL5%H2O2 |
| 滴加试剂 | 5滴0.lmol/LFeC13溶液 | 5滴_____溶液 | 5滴0.3mol/LNaCl溶液 |
| 产生气泡情况 | 较快产生细小气泡 | 缓慢产生细小气泡 | 无气泡产生 |
您最近一年使用:0次
名校
2 . 2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效灭活新冠病毒,为阻断疫情做出了巨大贡献。二氧化氯(ClO2)就是其中一种高效消毒灭菌剂。氯酸钠还原法是目前使用较为广泛的ClO2制备方法,其中一种是用NaClO3与CH3OH在催化剂、60℃时,发生反应得到ClO2,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
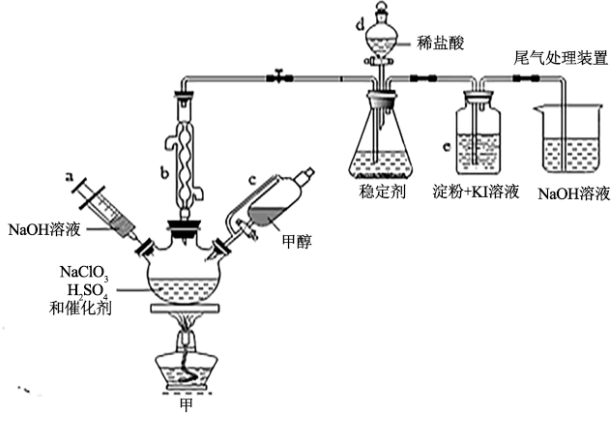
已知:①ClO2的浓度较大时易分解爆炸,一般用CO2或空气稀释到10%以下,实验室也常用稳定剂吸收ClO2,生成NaClO2,使用时加酸只释放出ClO2一种气体;
②ClO2与KI反应的离子方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O
③有关物质沸点如下表;
请回答:
(1)仪器b的名称是___________ ,在装置中的作用是___________ ;比较仪器c和d,实验中c的优点是___________ 。
(2)根据反应条件判断制备装置甲中需改进的一项措施是___________ 。
(3)反应中甲醇被氧化为甲酸,写出制备ClO2的化学方程式:___________ 。该制备法可选用不同的还原性物质作为还原剂例如草酸(草酸的氧化产物为CO2),相比甲醇法,草酸法的优点是___________ 。
(4)下列有关说法正确的是___________ 。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的ClO2
B.装置e主要用于检验是否有Cl2生成
C.在ClO2释放实验中,发生的离子反应方程式是:4H++5 =Cl-+4ClO2↑+2H2O
=Cl-+4ClO2↑+2H2O
D.ClO2和Cl2都为强氧化剂,在相同条件下,等物质的量时,Cl2的氧化能力是ClO2的2.5倍
(5)采用以下方法可以测定所制备的ClO2的量:
Ⅰ.将足量KI用100mL水溶解后加入到锥形瓶,再加3mL稀 ;
;
Ⅱ.将生成的ClO2气体通过导管在锥形瓶中被吸收
Ⅲ.滴加几滴淀粉溶液,用cmol/L的 标准溶液滴定(
标准溶液滴定( ),共用去
),共用去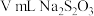 溶液:
溶液:
①达到滴定终点的现象是___________ 。
②实验测得所通入的ClO2的质量为___________ 。

已知:①ClO2的浓度较大时易分解爆炸,一般用CO2或空气稀释到10%以下,实验室也常用稳定剂吸收ClO2,生成NaClO2,使用时加酸只释放出ClO2一种气体;
②ClO2与KI反应的离子方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O
③有关物质沸点如下表;
| 物质 | CH3OH | HCOOH | ClO2 |
| 沸点 | 64.7℃ | 100.8℃ | 11℃ |
(1)仪器b的名称是
(2)根据反应条件判断制备装置甲中需改进的一项措施是
(3)反应中甲醇被氧化为甲酸,写出制备ClO2的化学方程式:
(4)下列有关说法正确的是
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的ClO2
B.装置e主要用于检验是否有Cl2生成
C.在ClO2释放实验中,发生的离子反应方程式是:4H++5
 =Cl-+4ClO2↑+2H2O
=Cl-+4ClO2↑+2H2OD.ClO2和Cl2都为强氧化剂,在相同条件下,等物质的量时,Cl2的氧化能力是ClO2的2.5倍
(5)采用以下方法可以测定所制备的ClO2的量:
Ⅰ.将足量KI用100mL水溶解后加入到锥形瓶,再加3mL稀
 ;
;Ⅱ.将生成的ClO2气体通过导管在锥形瓶中被吸收
Ⅲ.滴加几滴淀粉溶液,用cmol/L的
 标准溶液滴定(
标准溶液滴定( ),共用去
),共用去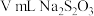 溶液:
溶液:①达到滴定终点的现象是
②实验测得所通入的ClO2的质量为
您最近一年使用:0次
2021-05-23更新
|
612次组卷
|
2卷引用:西藏自治区昌都市第一高级中学2021届高三第一次仿真考试理科综合化学试题
名校
解题方法
3 . 下列实验操作和现象所得结论正确的是( )
选项 | 实验操作 | 现象 | 结 论 |
A | 向某无色溶液中滴加稀盐酸 | 溶液变浑浊 | 原溶液中一定存在Ag+ |
B | 向某无色溶液中滴加稀NaOH溶液 | 未观察到明显现象 | 原溶液中一定不存在NH4+ |
C | 向酸性KMnO4溶液中通入SO2 | 溶液紫红色褪去 | SO2具有还原性 |
D | 向某溶液中通入Cl2,再滴入KSCN溶液 | 溶液变红 | 原溶液中一定含有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-05-12更新
|
504次组卷
|
5卷引用:西藏昌都市第一高级中学2021届高三上学期期末考试理综化学试题
解题方法
4 . 钴具有广泛用途,其正三价化合物具有强氧化性。利用低硫钴矿(含Ca、Fe、Al、Mn、Mg、Co等元素的硫化物及SiO2)可以制取多种化工试剂,采用以下工艺流程可利用低硫钴矿制备CoCO3。
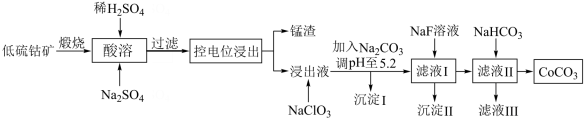
已知下列信息:
①常温下,Ksp(CaF2)=4.9×10-10,Ksp(MgF2)=6.4×10-12;
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)进行“酸溶”时,能提高“酸溶”速率的方法有___________ (任写1种)。
(2)酸溶时Co2O3被还原为Co2+,同时还有___________ 离子被还原。写出Co2O3转化为Co2+反应的离子方程式___________ 。
(3)加入NaClO的作用是___________ 。
(4)加入Na2CO3调pH至5.2,目的是___________ 。沉淀的I主要成分为___________
(5)为了将Mg2+、Ca2+除去[c(Mg2+)、c(Ca2+)≤1×10-5mol/L],加入NaF使“滤液I”中c(F-)最小为___________ mol/L。
(6)“沉钴”步骤的离子方程式是___________ 。

已知下列信息:
①常温下,Ksp(CaF2)=4.9×10-10,Ksp(MgF2)=6.4×10-12;
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 1.9 | 7.0 | 7.6 | 3.0 | 8.1 |
| 完全沉淀 | 3.2 | 9.0 | 9.2 | 4.7 | 10.1 |
(1)进行“酸溶”时,能提高“酸溶”速率的方法有
(2)酸溶时Co2O3被还原为Co2+,同时还有
(3)加入NaClO的作用是
(4)加入Na2CO3调pH至5.2,目的是
(5)为了将Mg2+、Ca2+除去[c(Mg2+)、c(Ca2+)≤1×10-5mol/L],加入NaF使“滤液I”中c(F-)最小为
(6)“沉钴”步骤的离子方程式是
您最近一年使用:0次
5 . 如图是五种短周期元素的原子序数与其在氢化物中化合价的关系图,则下列说法不正确的是
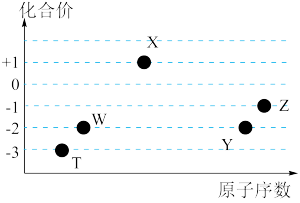

| A.X的氢化物具有很强的还原性 |
| B.YW2、ZW2、X2W2都能使品红溶液褪色,且褪色原理相同 |
| C.Y、Z元素的最高价氧化物对应的水化物都呈酸性,而且酸性:HZO4 > H2YO4 |
| D.元素W、T的氢化物的沸点比同主族中相邻的氢化物高,是因为这两种氢化物分子间存在氢键 |
您最近一年使用:0次
2020-02-06更新
|
177次组卷
|
2卷引用:西藏自治区昌都市第一高级中学2020届高三下学期第二次模拟考试理综化学试题
解题方法
6 . 化学与生产、生活和社会发展密切相关,下列叙述正确的是
| A.“蜡炬成灰泪始干”中的“蜡”为高级脂肪酸酯,属于天然高分子化合物 |
| B.“九秋风露越窑开,夺得千峰翠色来”描写的是越窑青瓷,青瓷的显色成分为氧化铁 |
| C.现代科技已经能够拍到氢键的“照片”,从而可直观地证实乙醇分子间存在氢键 |
| D.二氧化氯泡腾片和酒精均可杀灭新型冠状病毒,二者消毒时均表现为强氧化性 |
您最近一年使用:0次
名校
解题方法
7 . 废水废气对自然环境有严重的破坏作用,大气和水污染治理刻不容缓。
(1)某化工厂产生的废水中含有Fe2+、Mn2+等金属离子,可用过硫酸铵[(NH4)2S2O8]氧化除去。
①过硫酸铵与Mn2+反应生成MnO2的离子方程式为_____ 。
②温度与Fe2+、Mn2+氧化程度之间的关系如图所示:

实验过程中应将温度控制在_____ 。Fe2+与Mn2+被氧化后形成胶体絮状粒子,常加入活性炭处理,加入活性炭的目的为_____ 。
③H2O2也有较强氧化性,在实际生产中不用H2O2氧化Mn2+的原因是_____ 。
(2)利用某分子筛作催化剂,NH3可脱除废气中NO、NO2,其反应机理如图所示。A包含物质的化学式为N2和_____ 。

(3)工业上废气中SO2可用Na2CO3溶液吸收,反应过程中溶液组成变化如图所示。
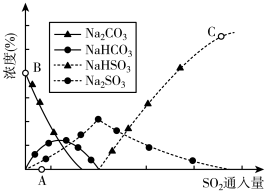
①吸收初期(图中A点以前)反应的化学方程式为_____ 。
②C点高于B点的原因是_______
(1)某化工厂产生的废水中含有Fe2+、Mn2+等金属离子,可用过硫酸铵[(NH4)2S2O8]氧化除去。
①过硫酸铵与Mn2+反应生成MnO2的离子方程式为
②温度与Fe2+、Mn2+氧化程度之间的关系如图所示:

实验过程中应将温度控制在
③H2O2也有较强氧化性,在实际生产中不用H2O2氧化Mn2+的原因是
(2)利用某分子筛作催化剂,NH3可脱除废气中NO、NO2,其反应机理如图所示。A包含物质的化学式为N2和

(3)工业上废气中SO2可用Na2CO3溶液吸收,反应过程中溶液组成变化如图所示。

①吸收初期(图中A点以前)反应的化学方程式为
②C点高于B点的原因是
您最近一年使用:0次
2018-02-07更新
|
410次组卷
|
6卷引用:西藏自治区昌都第四高级中学2019届高三下学期4月月考理科综合化学试题
西藏自治区昌都第四高级中学2019届高三下学期4月月考理科综合化学试题江苏省苏北四市2018届高三一模化学江苏省淮安市等四市2018届高三上学期第一次模拟 化学(已下线)【优等生百日捷进提升系列】专题02 氧化还原反应原理综合应用江苏省南通市海安高级中学2020届高三9月月考化学试题江苏省扬州中学2021届高三上学期12月月考化学试题
8 . 硫化氢大量存在于天然气及液化石油气中,近年来发现 可用于制取氢气、合成硫醇等。回答下列问题:
可用于制取氢气、合成硫醇等。回答下列问题:
(1)D.Berk等学者设计的用FeS催化分解 包括下列反应:
包括下列反应:
Ⅰ.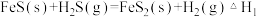
Ⅱ.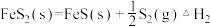
Ⅲ.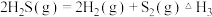
①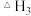 =
=____________ (用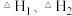 表示)。
表示)。
②已知单质硫气态时以 形式存在(结构为S=S)。键能E(H-S)=339
形式存在(结构为S=S)。键能E(H-S)=339 、E(H-H)=436
、E(H-H)=436 、E(S=S)=225
、E(S=S)=225 ,则
,则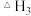 =
=____________  。
。
③ 是离子化合物,Fe显+2价,
是离子化合物,Fe显+2价, 的电子式为
的电子式为______________ 。
(2)银器长期露置在含 的空气中表面会生成
的空气中表面会生成 而变黑,该反应的氧化剂为
而变黑,该反应的氧化剂为________ ;将表面变黑的银器放在盛有食盐水的铝制容器中煮沸,表面重新变为光亮,正极发生的电极反应为________ 。
(3)实验室用粗锌制取氢气时常含有少量的 ,可用酸性
,可用酸性 溶液(
溶液( 被还原为
被还原为 )将
)将 氧化为S而除去,该反应的离子方程式为
氧化为S而除去,该反应的离子方程式为_______ 。
(4) 与
与 合成硫醇
合成硫醇 的反应
的反应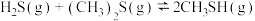 在不同温度及不同物质的量之比时
在不同温度及不同物质的量之比时 的平衡转化率如图所示:
的平衡转化率如图所示:

①该反应的
______ 0(填“>”或“<");
_________  (填“>”或“<”)。
(填“>”或“<”)。
②在2L密闭容器中充入0.2mol 和0.1mol
和0.1mol ,在A点达到平衡时,A点对应温度下反应的平衡常数为K=
,在A点达到平衡时,A点对应温度下反应的平衡常数为K=_________ 。
③为提高 的平衡转化率,除改变温度及投料比(m)外,还可采取的措施是
的平衡转化率,除改变温度及投料比(m)外,还可采取的措施是_____
 可用于制取氢气、合成硫醇等。回答下列问题:
可用于制取氢气、合成硫醇等。回答下列问题:(1)D.Berk等学者设计的用FeS催化分解
 包括下列反应:
包括下列反应:Ⅰ.
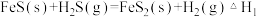
Ⅱ.
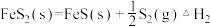
Ⅲ.
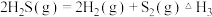
①
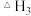 =
=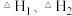 表示)。
表示)。②已知单质硫气态时以
 形式存在(结构为S=S)。键能E(H-S)=339
形式存在(结构为S=S)。键能E(H-S)=339 、E(H-H)=436
、E(H-H)=436 、E(S=S)=225
、E(S=S)=225 ,则
,则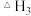 =
= 。
。③
 是离子化合物,Fe显+2价,
是离子化合物,Fe显+2价, 的电子式为
的电子式为(2)银器长期露置在含
 的空气中表面会生成
的空气中表面会生成 而变黑,该反应的氧化剂为
而变黑,该反应的氧化剂为(3)实验室用粗锌制取氢气时常含有少量的
 ,可用酸性
,可用酸性 溶液(
溶液( 被还原为
被还原为 )将
)将 氧化为S而除去,该反应的离子方程式为
氧化为S而除去,该反应的离子方程式为(4)
 与
与 合成硫醇
合成硫醇 的反应
的反应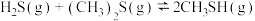 在不同温度及不同物质的量之比时
在不同温度及不同物质的量之比时 的平衡转化率如图所示:
的平衡转化率如图所示:
①该反应的


 (填“>”或“<”)。
(填“>”或“<”)。②在2L密闭容器中充入0.2mol
 和0.1mol
和0.1mol ,在A点达到平衡时,A点对应温度下反应的平衡常数为K=
,在A点达到平衡时,A点对应温度下反应的平衡常数为K=③为提高
 的平衡转化率,除改变温度及投料比(m)外,还可采取的措施是
的平衡转化率,除改变温度及投料比(m)外,还可采取的措施是
您最近一年使用:0次
2020-04-13更新
|
90次组卷
|
2卷引用:西藏昌都市第一高级中学2021届高三上学期期末考试理综化学试题
解题方法
9 . 亚硝酸钠广泛用于媒染剂、漂白剂等。某兴趣小组用下列装置制取较纯净的NaNO2。
甲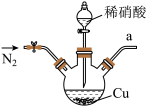 乙
乙 丙
丙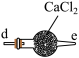 丁
丁
反应原理为:2NO+Na2O2=2NaNO2。已知:NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。下列分析错误的是
甲
 乙
乙 丙
丙 丁
丁
反应原理为:2NO+Na2O2=2NaNO2。已知:NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。下列分析错误的是
| A.甲中滴入稀硝酸前需通入N2 |
| B.仪器的连接顺序为a-f-g-d-e-b |
| C.丙中CaCl2用于干燥NO |
| D.乙中吸收尾气时发生的离子反应为3MnO4-+5NO+4H+=3Mn2++5NO3-+2H2O |
您最近一年使用:0次
2020-04-10更新
|
595次组卷
|
6卷引用:西藏自治区昌都市第一高级中学2020届高三下学期第二次模拟考试理综化学试题
西藏自治区昌都市第一高级中学2020届高三下学期第二次模拟考试理综化学试题四川省成都市2020届高中毕业班第二次诊断性检测理综化学试题湖南省邵阳市重点学校2020届高三综合模拟考试理综化学试题(已下线)第二单元 化学物质的变化测试题-2021年高考化学一轮复习名师精讲练(已下线)第26讲 化学实验基本操作及实验安全-2021年高考化学一轮复习名师精讲练福建省龙岩市第一中学锦山学校2021-2022学年高三上学期第三次月考化学试题



