1 . 下列实验目的对应的方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2~3mL蒸馏水 | 若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2 |
| B | Fe2+是否具有还原性 | 向2mL1.0mol·L−1FeSO4溶液中滴加几滴0.5mol·L−1酸性KMnO4溶液 | 若溶液不变紫红色,则Fe2+具有还原性;若溶液变紫红色,则Fe2+不具有还原性 |
| C | 比较Cl2、Br2、I2的氧化性 | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色,证明氧化性:Cl2>Br2>I2 |
| D | 比较H2CO3与CH3COOH的酸性 | 用pH计测定pH:①NaHCO3溶液②CH3COONa溶液 | pH①>②,证明H2CO3酸性弱于CH3COOH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 大苏打( )易溶于水,难溶于乙醇,在中性和碱性环境中稳定,在酸性环境中易变质。某实验小组用下列装置制备
)易溶于水,难溶于乙醇,在中性和碱性环境中稳定,在酸性环境中易变质。某实验小组用下列装置制备 并探究其性质。
并探究其性质。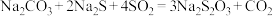 ;
;
② 中S元素的化合价为-2、+6。
中S元素的化合价为-2、+6。
回答下列问题:
(1)给装置A加热应选择_______ (填“水浴”或“酒精灯”)加热。
(2)为了保证 的产量,实验中通入的
的产量,实验中通入的 不能过量,需控制装置A中
不能过量,需控制装置A中 的生成速率,采取的措施是
的生成速率,采取的措施是_______ 。
(3)配制 和
和 混合溶液时,先将
混合溶液时,先将 固体溶于水配成溶液,再将
固体溶于水配成溶液,再将 固体溶于
固体溶于 溶液中,其目的是
溶液中,其目的是_______ 。
(4) 性质的探究。
性质的探究。
①称取一定量的样品,溶解,配成 溶液。
溶液。
②取4mL溶液,向其中加入1mL饱和氯水( ),溶液立即出现浑浊,经检验浑浊物为S。
),溶液立即出现浑浊,经检验浑浊物为S。
假设1:氧化剂氧化: 、HClO等含氯的氧化性微粒氧化了硫元素。
、HClO等含氯的氧化性微粒氧化了硫元素。
假设2:_______(不考虑空气中氧气氧化)。
设计实验方案:
①假设2是_______ 。
②第Ⅱ组实验中胶头滴管加入的试剂是_______ ,发生反应的离子方程式为_______ 。
③依据现象,产生S的主要原因可能是_______ 。
 )易溶于水,难溶于乙醇,在中性和碱性环境中稳定,在酸性环境中易变质。某实验小组用下列装置制备
)易溶于水,难溶于乙醇,在中性和碱性环境中稳定,在酸性环境中易变质。某实验小组用下列装置制备 并探究其性质。
并探究其性质。
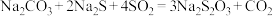 ;
;②
 中S元素的化合价为-2、+6。
中S元素的化合价为-2、+6。回答下列问题:
(1)给装置A加热应选择
(2)为了保证
 的产量,实验中通入的
的产量,实验中通入的 不能过量,需控制装置A中
不能过量,需控制装置A中 的生成速率,采取的措施是
的生成速率,采取的措施是(3)配制
 和
和 混合溶液时,先将
混合溶液时,先将 固体溶于水配成溶液,再将
固体溶于水配成溶液,再将 固体溶于
固体溶于 溶液中,其目的是
溶液中,其目的是(4)
 性质的探究。
性质的探究。①称取一定量的样品,溶解,配成
 溶液。
溶液。②取4mL溶液,向其中加入1mL饱和氯水(
 ),溶液立即出现浑浊,经检验浑浊物为S。
),溶液立即出现浑浊,经检验浑浊物为S。
假设1:氧化剂氧化:
 、HClO等含氯的氧化性微粒氧化了硫元素。
、HClO等含氯的氧化性微粒氧化了硫元素。假设2:_______(不考虑空气中氧气氧化)。
设计实验方案:
| 实验组别 | 胶头滴管滴加试剂 | 现象 |
| 第I组 | 1mL饱和氯水 | 立即出现浑浊 |
| 第Ⅱ组 | _______ | 一段时间后出现浑浊,但浑浊度比第I组小,且有少量气泡生成 |
②第Ⅱ组实验中胶头滴管加入的试剂是
③依据现象,产生S的主要原因可能是
您最近一年使用:0次
名校
3 . 工业废水中常含有一定量的 ,易被人体吸收积累而导致病变。处理工业含铬废水的方法通常是将
,易被人体吸收积累而导致病变。处理工业含铬废水的方法通常是将 转化为
转化为 。可以利用工业废气中的
。可以利用工业废气中的 处理酸性含铬废水,发生的反应为
处理酸性含铬废水,发生的反应为 (已知:
(已知: 具有强氧化性),下列说法正确的是
具有强氧化性),下列说法正确的是
 ,易被人体吸收积累而导致病变。处理工业含铬废水的方法通常是将
,易被人体吸收积累而导致病变。处理工业含铬废水的方法通常是将 转化为
转化为 。可以利用工业废气中的
。可以利用工业废气中的 处理酸性含铬废水,发生的反应为
处理酸性含铬废水,发生的反应为 (已知:
(已知: 具有强氧化性),下列说法正确的是
具有强氧化性),下列说法正确的是| A.加入过量的氢硫酸,有利于反应正向进行 |
B.含铬的酸性废水中存在的反应有 |
| C.加入过量的氢氧化钠溶液,有利于反应正向进行 |
| D.加入足量的水,则正、逆反应速率均增大 |
您最近一年使用:0次
2023-11-12更新
|
323次组卷
|
6卷引用:选择题11-14
名校
4 . Ⅰ.目前合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用氧化气化法提纯,其反应式为:
___C+ K2Cr2O7+___H2SO4===___CO2↑+___Cr2(SO4)3+___K2SO4+___H2O
(1)配平上述化学反应方程式(请将配平的计量数依次填入上式)_____________ 。
(2)该反应的氧化剂是______________ ,氧化产物的电子式为__________________ 。
(3)H2SO4在上述反应中表现出来的性质是________ (填选项编号)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生0.2 mol CO2 ,则转移电子的物质的量是_________ mol。
Ⅱ.三氟化氮(NF3)是一种无色无味的气体,可由氟与氨在一定条件下反应制得。
(1)写出该反应化学方程式并标明电子转移的方向和数目____________________________ 。
(2)27.0 mL NF3和水充分反应,生成 18.0 mL NO(同温、同压下),写出反应的化学方程式:______________________________________________________________________ 。
(3)NF3是一种无色无味的气体,但一旦NF3在空气中泄漏,还是易于发现的。该气体泄漏时的现象是_________________________________________________________________ 。
___C+ K2Cr2O7+___H2SO4===___CO2↑+___Cr2(SO4)3+___K2SO4+___H2O
(1)配平上述化学反应方程式(请将配平的计量数依次填入上式)
(2)该反应的氧化剂是
(3)H2SO4在上述反应中表现出来的性质是
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生0.2 mol CO2 ,则转移电子的物质的量是
Ⅱ.三氟化氮(NF3)是一种无色无味的气体,可由氟与氨在一定条件下反应制得。
(1)写出该反应化学方程式并标明电子转移的方向和数目
(2)27.0 mL NF3和水充分反应,生成 18.0 mL NO(同温、同压下),写出反应的化学方程式:
(3)NF3是一种无色无味的气体,但一旦NF3在空气中泄漏,还是易于发现的。该气体泄漏时的现象是
您最近一年使用:0次
名校
解题方法
5 . 铁及其化合物的制备与性质探究。
Ⅰ.乳酸亚铁[CH3CH(OH)COO]2Fe是一种常见的补血剂,可由FeCO3与乳酸反应制得,实验室经常采用如图装置制备FeCO3(夹持装置略)。
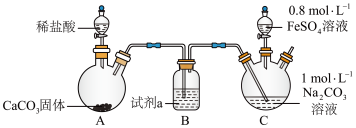
具体实验流程如下:装置C中,先通入CO2至pH约为7,滴加一定量FeSO4,将所得白色沉淀过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a为___________ 。
(2)写出C中pH约为7后,滴入FeSO4溶液制备FeCO3反应的离子方程式:___________ 。
(3)某实验小组依据酸性高锰酸钾标准液与亚铁离子的反应,来测定乳酸亚铁的质量分数,经过反复多次测定乳酸亚铁的质量分数总是大于100%,其原因是___________ 。
Ⅱ.无水FeCl3是一种常见的化工原料,实验室可采用下列装置制备。
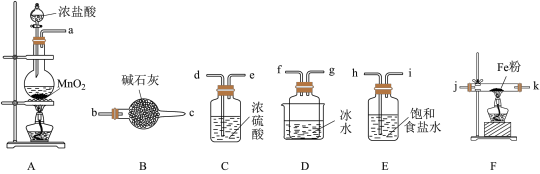
已知:①FeCl3极易水解;②FeCl3在300℃以上升华。
(4)装置的连接顺序为a→h,i→___________ →j,k→f,g→___________ (按气流方向,用小写字母表示)。
(5)某兴趣小组在FeCl3溶液中通入SO2,观察到的主要现象为随着SO2的通入,溶液迅速由黄色变为红棕色,静置一小时后溶液变为浅绿色。通过查阅资料得知,溶液中主要有两种变化,反应1:Fe2+与SO2会生成一种络合物[Fe(SO2)6]3+(红棕色);反应2:Fe3+与SO2发生氧化还原反应。
①写出第二种情况下反应的离子方程式:___________ 。
②这两种反应平衡常数的大小关系为K1___________ K2(填“<”“>”或“=”)。
Ⅰ.乳酸亚铁[CH3CH(OH)COO]2Fe是一种常见的补血剂,可由FeCO3与乳酸反应制得,实验室经常采用如图装置制备FeCO3(夹持装置略)。

具体实验流程如下:装置C中,先通入CO2至pH约为7,滴加一定量FeSO4,将所得白色沉淀过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a为
(2)写出C中pH约为7后,滴入FeSO4溶液制备FeCO3反应的离子方程式:
(3)某实验小组依据酸性高锰酸钾标准液与亚铁离子的反应,来测定乳酸亚铁的质量分数,经过反复多次测定乳酸亚铁的质量分数总是大于100%,其原因是
Ⅱ.无水FeCl3是一种常见的化工原料,实验室可采用下列装置制备。

已知:①FeCl3极易水解;②FeCl3在300℃以上升华。
(4)装置的连接顺序为a→h,i→
(5)某兴趣小组在FeCl3溶液中通入SO2,观察到的主要现象为随着SO2的通入,溶液迅速由黄色变为红棕色,静置一小时后溶液变为浅绿色。通过查阅资料得知,溶液中主要有两种变化,反应1:Fe2+与SO2会生成一种络合物[Fe(SO2)6]3+(红棕色);反应2:Fe3+与SO2发生氧化还原反应。
①写出第二种情况下反应的离子方程式:
②这两种反应平衡常数的大小关系为K1
您最近一年使用:0次
名校
解题方法
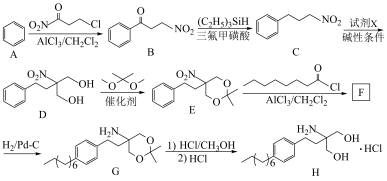
6 . 盐酸芬戈莫德(H)是一种治疗多发性硬化症的新型免疫抑制剂,以下是其中一种合成路线(部分反应条件已简化)。
(1)化合物A中碳的2p轨道形成_______ 中心______ 电子的大π键。
(2)由B生成C的反应类型为________ 。
(3)试剂X的化学名称为_________ 。
(4)由D生成E的反应目的是________ 。
(5)写出由E生成F的化学反应方程式________ 。
(6)在C的同分异构体中,同时满足下列条件的可能结构共有____ 种(不含立体异构)
a)含有苯环和硝基;
b)核磁共振氢谱显示有四组峰,峰面积之比为6:2:2:1。
上述同分异构体中,硝基和苯环直接相连的结构简式为_____ 。
(7)参照上述反应路线,以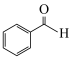 和
和 为原料,设计合成
为原料,设计合成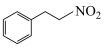 的路线
的路线_________ (无机试剂任选)。
已知:i)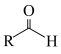 +R′CH2NO2
+R′CH2NO2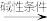
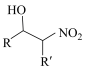
ii) 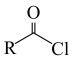 +R′OH
+R′OH
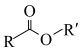
(1)化合物A中碳的2p轨道形成
(2)由B生成C的反应类型为
(3)试剂X的化学名称为
(4)由D生成E的反应目的是
(5)写出由E生成F的化学反应方程式
(6)在C的同分异构体中,同时满足下列条件的可能结构共有
a)含有苯环和硝基;
b)核磁共振氢谱显示有四组峰,峰面积之比为6:2:2:1。
上述同分异构体中,硝基和苯环直接相连的结构简式为
(7)参照上述反应路线,以
 和
和 为原料,设计合成
为原料,设计合成 的路线
的路线
您最近一年使用:0次
2024-01-23更新
|
857次组卷
|
5卷引用:2024年1月“九省联考”江西卷真题完全解读与考后提升
(已下线)2024年1月“九省联考”江西卷真题完全解读与考后提升(已下线)T18-有机综合题2024年1月江西普通高等学校招生考试适应性测试化学试题四川省遂宁市射洪市四川省射洪中学校2023-2024学年高三下学期开学理综试题-高中化学(已下线)专题11 有机推断综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
解题方法
7 . 乙酸乙酯在工业上有非常重要的作用。采用乙醇氧化脱氢法制备乙酸乙酯的反应原理及步骤如下:
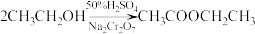
I.将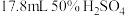 溶液加入至
溶液加入至 的三颈烧瓶中,冰盐浴条件下,加入
的三颈烧瓶中,冰盐浴条件下,加入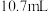 乙醇。
乙醇。
Ⅱ. 将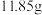
 溶于
溶于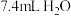 中,搅拌下逐滴加入三颈烧瓶中,反应温度控制在
中,搅拌下逐滴加入三颈烧瓶中,反应温度控制在 。
。
当混合物的粘度变大时,将温度升高到 ,继续反应。
,继续反应。
Ⅲ.将反应得到的绿色乳浊液用等量水稀释,分液,收集上层清液,纯化,干燥。
Ⅳ.分馏,收集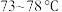 馏分。
馏分。
回到下列问题:
(1)步骤I中,使用冰盐浴(−25~−10℃)的原因是_______(填标号)。
(2)步骤Ⅱ中,升温到 的目的是
的目的是_______ 。
(3)步骤Ⅲ中,上层清液中含有的主要杂质为_______ 、________ 。
(4)步骤Ⅲ中,纯化操作步骤为:先用________ 、再用水洗涤。
(5)分馏装置如下图所示,玻璃仪器X的名称为_______ ;指出装置(不含夹持、加热等装置)中错误之处_______ 。______ 。
(7)为实现含铬废液的再生利用,可在含 酸性废液中加入
酸性废液中加入 ,写出该反应的离子方程式
,写出该反应的离子方程式______ 。
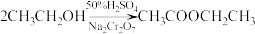
I.将
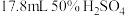 溶液加入至
溶液加入至 的三颈烧瓶中,冰盐浴条件下,加入
的三颈烧瓶中,冰盐浴条件下,加入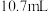 乙醇。
乙醇。Ⅱ. 将
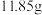
 溶于
溶于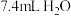 中,搅拌下逐滴加入三颈烧瓶中,反应温度控制在
中,搅拌下逐滴加入三颈烧瓶中,反应温度控制在 。
。当混合物的粘度变大时,将温度升高到
 ,继续反应。
,继续反应。Ⅲ.将反应得到的绿色乳浊液用等量水稀释,分液,收集上层清液,纯化,干燥。
Ⅳ.分馏,收集
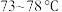 馏分。
馏分。回到下列问题:
(1)步骤I中,使用冰盐浴(−25~−10℃)的原因是_______(填标号)。
| A.增强乙醇还原性 | B.有利于降温 | C.减少乙醇挥发 | D.减少硫酸挥发 |
(2)步骤Ⅱ中,升温到
 的目的是
的目的是(3)步骤Ⅲ中,上层清液中含有的主要杂质为
(4)步骤Ⅲ中,纯化操作步骤为:先用
(5)分馏装置如下图所示,玻璃仪器X的名称为

(7)为实现含铬废液的再生利用,可在含
 酸性废液中加入
酸性废液中加入 ,写出该反应的离子方程式
,写出该反应的离子方程式
您最近一年使用:0次
8 . 下列实验操作能达到相应实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 除去 溶液中混有的 溶液中混有的 | 加入过量Cu粉,充分反应后,过滤 |
| B | 除去 固体中的 固体中的 | 用酒精灯充分加热 |
| C | 证明淀粉发生水解反应生成还原性糖 | 将淀粉和稀硫酸混合后加热,冷却后加入新制 浊液 浊液 |
| D | 证明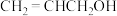 中含有碳碳双键 中含有碳碳双键 | 向酸性 溶液中加入 溶液中加入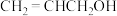 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
12-13高三上·辽宁朝阳·阶段练习
名校
解题方法
9 . 下列有关物质的性质与应用不相对应的是
| A.SO2具有氧化性,可用于漂白纸浆 |
| B.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
| C.明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
您最近一年使用:0次
解题方法
10 . 以下探究目的对应的实验方案最合适的是
| 实验方案 | 探究目的 | |
| A | 向 溶液中加入金属 溶液中加入金属 | 比较 和 和 的还原能力 的还原能力 |
| B | 分别向稀硝酸和稀醋酸中加入铜粉 | 比较稀硝酸和稀醋酸的酸性强弱 |
| C | 将浓硫酸滴入乙醇中,加热至 ,生成的气体通入酸性重铬酸钾溶液 ,生成的气体通入酸性重铬酸钾溶液 | 验证乙烯具有还原性 |
| D | 向 溶液中同时通入 溶液中同时通入 和 和 | 比较 和 和 的氧化能力 的氧化能力 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-23更新
|
1001次组卷
|
5卷引用:2024年1月“九省联考”江西卷真题完全解读与考后提升
(已下线)2024年1月“九省联考”江西卷真题完全解读与考后提升(已下线)选择题1-52024年1月江西普通高等学校招生考试适应性测试化学试题(已下线)热点08 表格型实验方案的设计与评价2024届陕西省咸阳市乾县第一中学高三下学期第一次模拟考试理综试题-高中化学



