名校
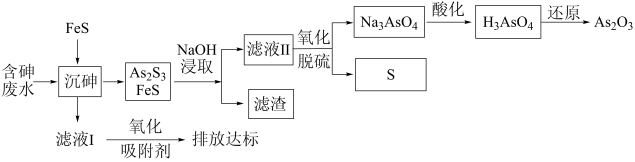
1 . 一种从含砷废水[砷主要以亚砷酸(H3AsO3)形式存在]中回收砷的工艺流程如图:
已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq) 2AsS
2AsS (aq)
(aq)
III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是

已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq)
 2AsS
2AsS (aq)
(aq)III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是
| A.As2S3中砷元素的化合价为+3价 |
| B.“沉砷”过程中FeS可以用过量的Na2S代替 |
C.用氧气进行“氧化脱硫”涉及离子方程式AsS +2O2=AsO +2O2=AsO +3S↓ +3S↓ |
| D.能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸 |
您最近一年使用:0次
2022-04-27更新
|
250次组卷
|
3卷引用:选择题11-15
解题方法
2 . 根据下列实验操作和现象,所得结论或推论正确的是
| 选项 | 操作 | 现象 | 结论或推论 |
| A | 用铂丝蘸取溶液 X进行焰色反应实验 | 火焰呈黄色 | 溶液 X 一定是钠盐溶液 |
| B | 向某无色溶液中滴加少量稀盐酸 | 无明显现象 | 该溶液和盐酸不反应 |
| C | 燃烧匙加热至红热后放入绿豆粒大小的钠,迅速伸入集满 CO2 的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2 具有氧化性 |
| D | 分别向含 Mn2+的草酸溶液X 和不含 Mn2+的草酸溶液Y 中滴加酸性高锰酸钾溶液 | 高锰酸钾溶液在X 溶液中褪色较快 | Mn2+也能还原高锰酸钾 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 化学与人们的生活、生产密切相关。下列有关叙述正确的是
| A.“沙里淘金”、“丹炉炼丹”过程均涉及物理变化和化学变化 |
| B.中国天眼FAST用到的碳化硅是一种新型无机非金属材料 |
| C.漂白粉、酒精、双氧水杀菌消毒均利用其氧化性 |
D.光伏发电的核心材料是 ,光导纤维的成分是单质Si ,光导纤维的成分是单质Si |
您最近一年使用:0次
4 . 铁和钛是重要的金属材料。 合金是优良的储氢合金。一种利用钛铁矿(主要成分为
合金是优良的储氢合金。一种利用钛铁矿(主要成分为 ,另含
,另含 和
和 等杂质)制备钛和绿矾的工艺流程如下。下列说法错误的是
等杂质)制备钛和绿矾的工艺流程如下。下列说法错误的是

 合金是优良的储氢合金。一种利用钛铁矿(主要成分为
合金是优良的储氢合金。一种利用钛铁矿(主要成分为 ,另含
,另含 和
和 等杂质)制备钛和绿矾的工艺流程如下。下列说法错误的是
等杂质)制备钛和绿矾的工艺流程如下。下列说法错误的是
| A.“浸出”过程中Ti元素的化合价没有发生改变 |
B.氧化性: |
C.若制得 金属钛,则步骤Ⅲ中转移电子的物质的量至少为 金属钛,则步骤Ⅲ中转移电子的物质的量至少为 |
D. 被还原为Ti的过程也可以用Na代替Mg 被还原为Ti的过程也可以用Na代替Mg |
您最近一年使用:0次
2023-10-28更新
|
190次组卷
|
3卷引用:选择题11-15
5 . 利用闪锌矿{主要成分为ZnS,还有Fe、Co、In(铟)、F、Cl等元素}生产Zn的一种工艺流程如图所示。下列说法中正确的是
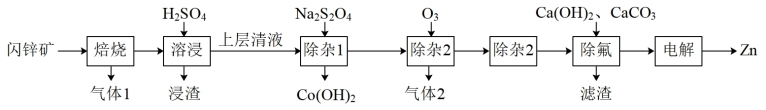
已知:焙烧时,Fe、Co均转化为+3价的氧化物; 易成胶状。
易成胶状。

已知:焙烧时,Fe、Co均转化为+3价的氧化物;
 易成胶状。
易成胶状。A. 在“除杂1”中作氧化剂 在“除杂1”中作氧化剂 |
B.“气体2”中含有有色气体,由此说明氧化性: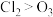 |
C.“除氟”时,适量的 可以防止形成氟化钙胶体,提高氟的沉降率 可以防止形成氟化钙胶体,提高氟的沉降率 |
D.“溶浸”时,易形成难溶的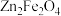 和 和 ,其中Fe元素的化合价为+6价 ,其中Fe元素的化合价为+6价 |
您最近一年使用:0次
6 . 根据下列实验操作和现象所得出的结论或推论正确的是
| 实验操作和现象 | 实验结论或推论 | |
| A | 向FeCl3溶液中加入Cu片,振荡,溶液颜色变化 | Cu与FeCl3发生了置换反应 |
| B | 向Ba(NO3)2溶液中通入SO2气体,产生白色沉淀 | SO2具有还原性 |
| C | 用pH试纸测得NaA、NaB溶液的pH分别为9和8 | 酸性:HB>HA |
| D | 用AgNO3标准溶液滴定待测液中Cl-,以K2CrO4为指示剂 | Ksp(Ag2CrO4)>Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 对乙酰氨基酚是一种常用的解热镇痛药,2023年1月国家药监局批准对乙酰氨基酚为新冠病毒的对症治疗药物之一。某学习小组在实验室制备对乙酰氨基酚,制备原理如下:

相关信息列表如下:

装置示意图如图所示,实验步骤为:
①在圆底烧瓶中加入21.8g对氨基苯酚、稍过量的醋酸酐,边搅拌边加热,至固体全部溶解。加热至80℃,保持30分钟。
②冷却至室温,析出大量晶体,减压过滤,洗涤,得到对乙酰氨基酚粗品24.0g。
③粗品置于锥形瓶中,加水,加热溶解,再加活性炭,煮沸5分钟后趁热过滤。
④滤液冷却结晶、过滤、洗涤、干燥得纯度较高的对乙酰氨基酚产品16.0g。
回答下列问题:
(1)仪器A中应加入_______ (填“水”或“油”)作为热传导介质。
(2)仪器B的作用是_______ 。
(3)步骤②洗涤滤渣时最合适的洗涤试剂是_______ (填序号)。
a.热水 b.冷水 c.热乙醇 d.冷乙醇
(4)步骤③加入活性炭是为了除去粗品中的_______ 。步骤③趁热过滤时,先在收集滤液的装置中加入少量的NaHSO3固体。NaHSO3的作用是_______ 。
(5)为检验步骤④产品中的对乙酰氨基酚,某同学设计了如下方案:用FeCl3溶液滴加到产品溶液中,发生显色反应,说明产品中有对乙酰氨基酚。该方案是否可行_______ ?简述判断理由:_______ 。
(6)本实验的产率合理的范围是_______ (填序号)。
a.产率>79.4% b.53.0%≤产率<79.4% c.产率<53.0%

相关信息列表如下:
| 物质 | 摩尔质量(g/mol) | 性状 | 溶解性 | 性质 |
| 对氨基苯酚 | 109 | 白色晶体 | 微溶于冷水,可溶于热水和乙醇 | 易被氧化成有色物质 |
| 对乙酰氨基酚 | 151 | 白色晶体 | 微溶于冷水,易溶于热水和乙醇 | 易被氧化 |
| 醋酸酐 | —— | 无色液体 | 易挥发,缓慢溶于水变成乙酸 | |

装置示意图如图所示,实验步骤为:
①在圆底烧瓶中加入21.8g对氨基苯酚、稍过量的醋酸酐,边搅拌边加热,至固体全部溶解。加热至80℃,保持30分钟。
②冷却至室温,析出大量晶体,减压过滤,洗涤,得到对乙酰氨基酚粗品24.0g。
③粗品置于锥形瓶中,加水,加热溶解,再加活性炭,煮沸5分钟后趁热过滤。
④滤液冷却结晶、过滤、洗涤、干燥得纯度较高的对乙酰氨基酚产品16.0g。
回答下列问题:
(1)仪器A中应加入
(2)仪器B的作用是
(3)步骤②洗涤滤渣时最合适的洗涤试剂是
a.热水 b.冷水 c.热乙醇 d.冷乙醇
(4)步骤③加入活性炭是为了除去粗品中的
(5)为检验步骤④产品中的对乙酰氨基酚,某同学设计了如下方案:用FeCl3溶液滴加到产品溶液中,发生显色反应,说明产品中有对乙酰氨基酚。该方案是否可行
(6)本实验的产率合理的范围是
a.产率>79.4% b.53.0%≤产率<79.4% c.产率<53.0%
您最近一年使用:0次
8 . 化合物F是一种重要的药物中间体,其人工合成路线如下:___________ 。
(2)C→D过程中经历C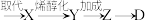 。
。
①Z结构简式为___________ 。
②Z→D的反应类型为___________ 。
(3)G的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___________ 。
①能与FeCl3发生显色反应;
②在酸性条件下能发生水解,所得产物中均含有三种不同化学环境的氢原子。
(4)设计以 、
、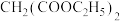 为原料制备
为原料制备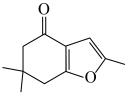 的合成路线(无机试剂任用,合成路线流程图示例见本题题干)
的合成路线(无机试剂任用,合成路线流程图示例见本题题干)_______ 。

已知:① (R1、R2为烃基或者氢原子)。
(R1、R2为烃基或者氢原子)。
②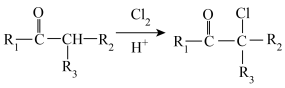 (R1、R2、R3为烃基或者氢原子)。
(R1、R2、R3为烃基或者氢原子)。
(2)C→D过程中经历C
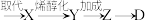 。
。①Z结构简式为
②Z→D的反应类型为
(3)G的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:
①能与FeCl3发生显色反应;
②在酸性条件下能发生水解,所得产物中均含有三种不同化学环境的氢原子。
(4)设计以
 、
、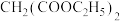 为原料制备
为原料制备 的合成路线(无机试剂任用,合成路线流程图示例见本题题干)
的合成路线(无机试剂任用,合成路线流程图示例见本题题干)
您最近一年使用:0次
解题方法
9 . 我国科学家设计如图装置实现了分步电解制氢、制氧,下列说法正确的是
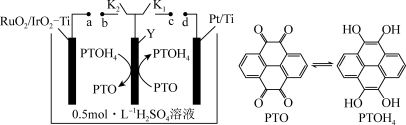

| A.c接电源正极,b接电源负极 |
| B.闭合K2,Y极发生氧化反应,H+向Y电极移动 |
| C.闭合K1,Y极电极反应式为PTO+4e-+4H+=PTOH4 |
| D.该电池实现了PTO、PTOH4的循环利用,且硫酸的浓度保持不变 |
您最近一年使用:0次



