名校
1 . 低品质能源利用是指对热值较低、含杂物较高等特点的一类能源的利用。如图所示装置,可同时利用低温废热和含铜废液,并达到对含铜废液富集和产生电能的目的。起始时电极均为泡沫铜且质量相等,含铜废液的浓度为0.1 ,以2.5
,以2.5
 溶液作为电解质溶液,向M极区液体中加入2
溶液作为电解质溶液,向M极区液体中加入2 氨水开始反应。下列说法正确的是
氨水开始反应。下列说法正确的是
 ,以2.5
,以2.5
 溶液作为电解质溶液,向M极区液体中加入2
溶液作为电解质溶液,向M极区液体中加入2 氨水开始反应。下列说法正确的是
氨水开始反应。下列说法正确的是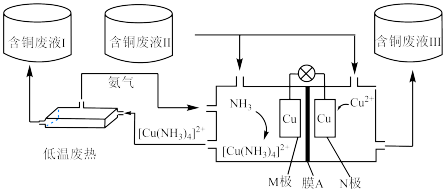
| A.向M极区液体中加入氨水可使M极电势高于N极电势 |
B.含铜废液Ⅰ、Ⅲ中的 均高于含铜废液Ⅱ中的 均高于含铜废液Ⅱ中的 |
| C.电子由M极经导线移向N极 |
| D.电极质量差为6.4g时,电路中通过0.2mol电子 |
您最近一年使用:0次
2024-06-09更新
|
299次组卷
|
5卷引用:2024届广东省湛江市第二十一中学高三模拟预测化学试题
名校
2 . 部分含硫物质的类别与相应化合价的关系如图所示。下列说法不正确的是
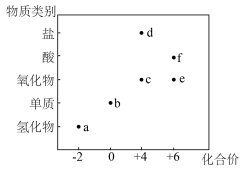
A.气体a可用 溶液吸收 溶液吸收 | B.b难溶于水,微溶于 ,易溶于酒精 ,易溶于酒精 |
| C.c可由d与较浓的f溶液反应制备 | D.标准状况下,1mol a、1mol c的体积均约为22.4L |
您最近一年使用:0次
2024-06-09更新
|
362次组卷
|
3卷引用:2024届广东省湛江市第二十一中学高三模拟预测化学试题
名校
解题方法
3 . 化学用语是学习化学的重要工具。下列化学用语表述不正确的是
A.用原子轨道描述氢原子形成氢分子的过程: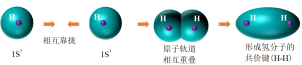 |
B. 的电子式为: 的电子式为: |
C.基态溴原子电子占据最高能级的电子云轮廓图: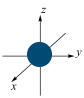 |
D. 的VSEPR模型: 的VSEPR模型: |
您最近一年使用:0次
2024-05-12更新
|
138次组卷
|
3卷引用:2024届广东省湛江市第二十一中学高三模拟预测化学试题
4 . 某立方卤化物可用于制作光电材料,其晶胞结构如图所示。该晶胞在体对角线方向的投影为

A. | B. | C. | D.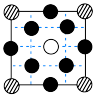 |
您最近一年使用:0次
2024-05-12更新
|
358次组卷
|
2卷引用:广东省湛江市2024届高三下学期第二次模拟测试化学试题
解题方法
5 . 宏观辨识与微观探析是高中化学核心素养的重要组成部分。下列解释相应实验现象的离子方程式错误的是
A.往AgCl沉淀中加入KI溶液,沉淀由白色变为黄色: |
B.向 溶液中滴入过量 溶液中滴入过量 溶液: 溶液: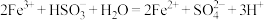 |
C.南方水果运往北方时,用浸泡了酸性高锰酸钾溶液的硅藻土除去乙烯,防止水果腐烂: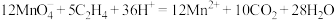 |
D.苯甲醛与新制的 共热: 共热: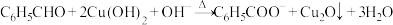 |
您最近一年使用:0次
2024-05-12更新
|
555次组卷
|
2卷引用:广东省湛江市2024届高三下学期第二次模拟测试化学试题
名校
6 . 有机物G是合成中草药活性成分Psoralidin的中间体,其合成路线如下:
(1)化合物A的名称为______ ;C中官能团的名称为______ 。
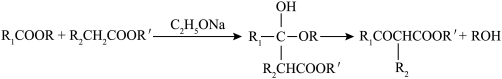
(2)结合已有知识,写出E→F的方程式:______ ;该反应类型为______ 。
(3)下列关于反应F→G的说法中,正确的有______
(4)化合物E的芳香族同分异构体中,同时满足如下条件的有______ 种,
a)只含一种官能团且能与碳酸钠反应生成 ;
;
b)核磁共振氢谱确定分子中有9个化学环境相同的氢原子。
其中核磁共振氢谱有4组峰的结构简式为______ 。(写出一种即可)
(5)对甲氧基苯甲酸(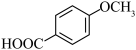 )可用作防腐剂或制备香料,结合上述信息,写出以苯酚为主要原料制备
)可用作防腐剂或制备香料,结合上述信息,写出以苯酚为主要原料制备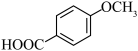 的合成路线
的合成路线____ 。

(1)化合物A的名称为
(2)结合已有知识,写出E→F的方程式:
(3)下列关于反应F→G的说法中,正确的有______
| A.反应过程中有极性键、非极性键的断裂和形成 |
| B.化合物F存在顺反异构体 |
| C.该反应有乙醇生成 |
| D.化合物G中碳原子的杂化方式有两种 |
(4)化合物E的芳香族同分异构体中,同时满足如下条件的有
a)只含一种官能团且能与碳酸钠反应生成
 ;
;b)核磁共振氢谱确定分子中有9个化学环境相同的氢原子。
其中核磁共振氢谱有4组峰的结构简式为
(5)对甲氧基苯甲酸(
 )可用作防腐剂或制备香料,结合上述信息,写出以苯酚为主要原料制备
)可用作防腐剂或制备香料,结合上述信息,写出以苯酚为主要原料制备 的合成路线
的合成路线
您最近一年使用:0次
2024-04-28更新
|
718次组卷
|
2卷引用:2024届广东省湛江市第二十一中学高三模拟预测化学试题
名校
7 . 2024年春节,汕头文化旅游不断“出圈”,下列有关材料属于有机合成纤维的是
|
|
A东海岸风筝尼龙线 | B潮阳英歌舞木棍 |
|
|
C汕头烟花表演邮轮金属外壳 | D无人机表演碳纤维机翼 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-28更新
|
425次组卷
|
2卷引用:2024届广东省湛江市第二十一中学高三模拟预测化学试题
8 . Fe(OH)2具有较强的还原性,新制的白色Fe(OH)2会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色Fe(OH)2,某实验小组做了如下探究实验。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、___________ 、___________ 。
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是___________ 。
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:___________ 。___________ (用离子方程式表示)。
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:___________ 。
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
①由以上实验可得到的规律是___________ 。
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为___________ (填“1.0”“1.5”或“2.0”)mol/L。
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为___________ (任写一条)。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:

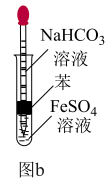
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
c(NaHCO3)/(mol/L) c(FeSO4)/(mol/L) | 1.0 | 1.5 | 2.0 | |
| 1.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 3.5 min | 9 min | 24 min | |
| 1.5 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 13 min | 15 min | 22 min | |
| 2.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率加快 | 常温下无现象,加热后产生白色沉淀 |
| 稳定时间 | 3 min | 8 min | 30 min | |
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为
您最近一年使用:0次
2024-04-16更新
|
335次组卷
|
2卷引用:广东省湛江市2024届高三下学期第二次模拟测试化学试题
9 . 下列有关物质结构与性质的表述结构正确的是
A.N-H键的极性大于C-H键的极性, 分子的极性小于 分子的极性小于 |
B. 易溶于 易溶于 ,可从 ,可从 和 和 都是非极性分子的角度解释 都是非极性分子的角度解释 |
C. 中的氢键数量比 中的氢键数量比 少,可推断 少,可推断 的稳定性比 的稳定性比 差 差 |
| D.超分子是两种或两种以上的分子(包括离子)通过化学键形成的分子聚集体 |
您最近一年使用:0次
解题方法
10 . 化学渗透在社会生活的各个方面。下列叙述错误的是
| A.“九章三号”光量子计算原型机所用芯片的主要成分Si能溶于NaOH溶液 |
| B.用于制作飞机轴承的氮化硅陶瓷材料具有耐高温、耐磨蚀等优良性能 |
| C.宇航员餐食中的油脂属于天然高分子化合物 |
| D.稀土永磁材料是电子技术通信中的重要材料,稀土元素均为金属元素 |
您最近一年使用:0次







