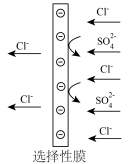
1 . 环氧乙烷( )可用于生产乙二醇。电化学合成环氧乙烷(
)可用于生产乙二醇。电化学合成环氧乙烷( )的装置如图所示:
)的装置如图所示:

已知:
A. 电极接电源负极 电极接电源负极 |
B.制备 环氧乙烷, 环氧乙烷, 电极区产生 电极区产生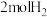 |
C. 电极区的反应方程式为: 电极区的反应方程式为: |
| D.电解完成后,将阳极区和阴极区溶液混合才可得到环氧乙烷 |
您最近一年使用:0次
2024-05-23更新
|
567次组卷
|
2卷引用:广东省惠州市2024届高三一模化学试题
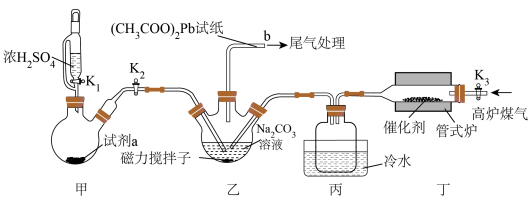
2 . 高炉煤气(主要成分为CO、N2、H2、H2S和少量COS)是炼铁过程中所得到的一种副产品,直接排放会污染空气。某化学兴趣小组利用高炉煤气和SO2制备Na2S2O3·5H2O,装置如图所示。回答下列问题: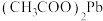 试纸可鉴别
试纸可鉴别 ,方程式为:
,方程式为: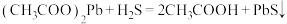 (黑色)
(黑色)
Ⅰ.Na2S2O3的制备
步骤一:关闭K1、K2,打开K3,通入高炉煤气。
发生的反应有:丁中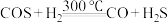 ;乙中
;乙中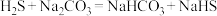 。
。
(1)当润湿的(CH3COO)2Pb试纸_____ (填现象),关闭K3,停止通入高炉煤气。
(2)导管b接盛有醋酸亚铜氨溶液的洗气瓶。醋酸亚铜氨溶液的洗气瓶用于吸收CO气体,方程式为: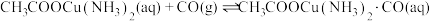
 。
。
①过量H2S会导致吸收CO的能力下降的原因是_____ 。
②将吸收液通过_____ (任写一种)的方法实现吸收液的再生,同时释放CO,达到资源再利用。
步骤二:打开K1、K2,通入SO2气体。
(3)试剂a为_____ (填化学式)。
(4)装置乙中生成Na2S2O3的化学方程式为_____ 。
(5)导管b接盛有_____ (填化学式)溶液的洗气瓶用于尾气处理。
Ⅱ.Na2S2O3·5H2O纯度的测定
(6)测定某样品中Na2S2O3·5H2O的含量的实验步骤如下(杂质不参加反应):
i.取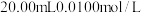 的
的 溶液,用硫酸酸化后,加入过量
溶液,用硫酸酸化后,加入过量 溶液,发生反应:
溶液,发生反应:
ii.称取 样品,配制成
样品,配制成 溶液,取该溶液滴定步骤i所得溶液(淀粉作指示剂)至终点。三次平行实验,平均消耗
溶液,取该溶液滴定步骤i所得溶液(淀粉作指示剂)至终点。三次平行实验,平均消耗 样品溶液。发生的反应为:
样品溶液。发生的反应为:
①判断步骤ii的滴定终点方法为_____ 。
②样品中Na2S2O3·5H2O的质量分数为_____ 。
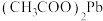 试纸可鉴别
试纸可鉴别 ,方程式为:
,方程式为: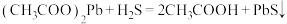 (黑色)
(黑色)Ⅰ.Na2S2O3的制备
步骤一:关闭K1、K2,打开K3,通入高炉煤气。
发生的反应有:丁中
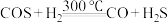 ;乙中
;乙中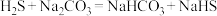 。
。(1)当润湿的(CH3COO)2Pb试纸
(2)导管b接盛有醋酸亚铜氨溶液的洗气瓶。醋酸亚铜氨溶液的洗气瓶用于吸收CO气体,方程式为:
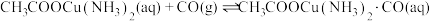
 。
。①过量H2S会导致吸收CO的能力下降的原因是
②将吸收液通过
步骤二:打开K1、K2,通入SO2气体。
(3)试剂a为
(4)装置乙中生成Na2S2O3的化学方程式为
(5)导管b接盛有
Ⅱ.Na2S2O3·5H2O纯度的测定
(6)测定某样品中Na2S2O3·5H2O的含量的实验步骤如下(杂质不参加反应):
i.取
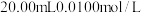 的
的 溶液,用硫酸酸化后,加入过量
溶液,用硫酸酸化后,加入过量 溶液,发生反应:
溶液,发生反应:
ii.称取
 样品,配制成
样品,配制成 溶液,取该溶液滴定步骤i所得溶液(淀粉作指示剂)至终点。三次平行实验,平均消耗
溶液,取该溶液滴定步骤i所得溶液(淀粉作指示剂)至终点。三次平行实验,平均消耗 样品溶液。发生的反应为:
样品溶液。发生的反应为:
①判断步骤ii的滴定终点方法为
②样品中Na2S2O3·5H2O的质量分数为
您最近一年使用:0次
3 . 实验探究是化学学习的方法之一、下列实验设计、现象和实验结论均正确的是
| 选项 | 实验设计 | 现象 | 实验结论 |
| A | 向鸡蛋清溶液中滴入几滴硫酸铜溶液 | 产生白色沉淀,加水后沉淀不溶解 | 蛋白质发生了变性 |
| B | 室温下用pH计测定同浓度的NaClO溶液和CH3COONa溶液的pH | NaClO溶液的pH较大 | 酸性: HClO>CH3COOH |
| C | 向溶液中先滴加新制氯水,再加KSCN溶液 | 溶液变红 | 该溶液一定含有Fe2+ |
| D | 取少量 | 紫红色褪去 | 该有机物中含有醛基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . CO与H2S反应可以制得COS,其化学方程式为 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是
 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是A.2.8g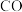 中含有的中子数为1.4NA 中含有的中子数为1.4NA |
B.pH=3的H2S溶液中 的数目为0.001NA 的数目为0.001NA |
C.0.1molCOS中 键数目为0.4NA 键数目为0.4NA |
| D.生成2.24LH2(标准状况),转移电子数目为0.4NA |
您最近一年使用:0次
解题方法
5 . 氯碱厂制备的原盐中含有的杂质主要为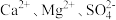 及大分子有机物和难溶性泥沙等物质。为供给电解槽以合格的盐水,可采用以下工艺流程精制盐水。
及大分子有机物和难溶性泥沙等物质。为供给电解槽以合格的盐水,可采用以下工艺流程精制盐水。 的电离常数
的电离常数
(1)溶浸工序中,以下除杂试剂:①过量的 ②过量的
②过量的 ③过量的
③过量的 ,正确的加入顺序为
,正确的加入顺序为_____ 。
A.②①③ B.③①② C.①③②
(2)在脱氯工序中加入 除去游离的氯的离子方程式为
除去游离的氯的离子方程式为_____ 。
(3)用 溶液吸收一定量
溶液吸收一定量 气体形成
气体形成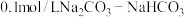 缓冲溶液,
缓冲溶液, 时,溶液中
时,溶液中
_____ 。
(4)利用膜的选择性,可除去脱氯过程中引入的 ,通过“错流”方式截留下
,通过“错流”方式截留下 ,使
,使 以渗透液的形式输送到后续工序。不同膜对介质的截留率,相关离子系数如下表:
以渗透液的形式输送到后续工序。不同膜对介质的截留率,相关离子系数如下表:
最好的选择是_____ 膜,该膜脱硫率高的原因是_____ 。
(5)一种镧镍储氢合金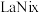 晶体的结构单元如图所示,“电解2”产生的
晶体的结构单元如图所示,“电解2”产生的 与其结合后形成
与其结合后形成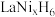 (
( 进入合金后解离成氢原子并填充在晶胞空隙中,晶胞体积不变)。
进入合金后解离成氢原子并填充在晶胞空隙中,晶胞体积不变)。 中,
中,
_____ , 的配位数为
的配位数为_____ 。
② 该合金可以储存
该合金可以储存_____ 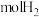 。
。
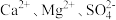 及大分子有机物和难溶性泥沙等物质。为供给电解槽以合格的盐水,可采用以下工艺流程精制盐水。
及大分子有机物和难溶性泥沙等物质。为供给电解槽以合格的盐水,可采用以下工艺流程精制盐水。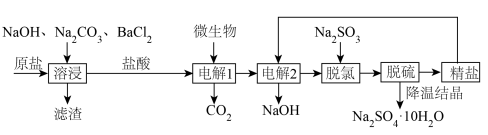
 的电离常数
的电离常数
(1)溶浸工序中,以下除杂试剂:①过量的
 ②过量的
②过量的 ③过量的
③过量的 ,正确的加入顺序为
,正确的加入顺序为A.②①③ B.③①② C.①③②
(2)在脱氯工序中加入
 除去游离的氯的离子方程式为
除去游离的氯的离子方程式为(3)用
 溶液吸收一定量
溶液吸收一定量 气体形成
气体形成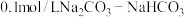 缓冲溶液,
缓冲溶液, 时,溶液中
时,溶液中
(4)利用膜的选择性,可除去脱氯过程中引入的
 ,通过“错流”方式截留下
,通过“错流”方式截留下 ,使
,使 以渗透液的形式输送到后续工序。不同膜对介质的截留率,相关离子系数如下表:
以渗透液的形式输送到后续工序。不同膜对介质的截留率,相关离子系数如下表:| 截留率 物质 | 反渗透膜(%) | 纳滤膜(%) | 超滤膜(%) |
|
 | 99 | 15.6 | 0 | |
 | 99 | 99 | 0 | |
| 系数 离子 | 水合离子半径 | 扩散系数/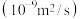 | ||
 | 0.397 | 1.065 | ||
 | 0.332 | 2.032 | ||
(5)一种镧镍储氢合金
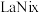 晶体的结构单元如图所示,“电解2”产生的
晶体的结构单元如图所示,“电解2”产生的 与其结合后形成
与其结合后形成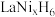 (
( 进入合金后解离成氢原子并填充在晶胞空隙中,晶胞体积不变)。
进入合金后解离成氢原子并填充在晶胞空隙中,晶胞体积不变)。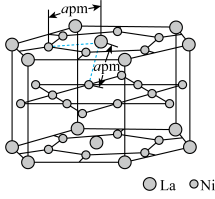
 中,
中,
 的配位数为
的配位数为②
 该合金可以储存
该合金可以储存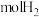 。
。
您最近一年使用:0次
6 . 对氮氧化物 的资源化利用,运用多种方式促进氮的循环转化,具有重要的研究意义。
的资源化利用,运用多种方式促进氮的循环转化,具有重要的研究意义。
(1)已知a:

b:C的燃烧热为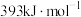 ;
;
c:
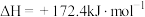
①请写出 与
与 反应生成两种无污染性气体的热化学方程式:
反应生成两种无污染性气体的热化学方程式:_____ 。
②将等物质的量的 与
与 混合气体分别通入体积均为
混合气体分别通入体积均为 的恒温密闭容器Ⅰ和绝热密闭容器Ⅱ中,反应一段时间后两容器内达到平衡状态,下列说法正确的是
的恒温密闭容器Ⅰ和绝热密闭容器Ⅱ中,反应一段时间后两容器内达到平衡状态,下列说法正确的是_____ 。
A.两容器内混合气体密度相等
B. 转化率
转化率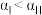
C.反应平衡常数
(2)可利用钴氨配合物吸收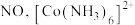 对
对 的配合能力很强,而
的配合能力很强,而 对
对 的配合能力极低。
的配合能力极低。 溶液脱除
溶液脱除 的效率如图1所示,有氧环境下,发生总反应:
的效率如图1所示,有氧环境下,发生总反应: ,在
,在 的有氧环境下,往
的有氧环境下,往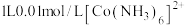 溶液中持续通入试样气体
溶液中持续通入试样气体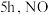 脱除率为60%(假设溶液体积不发生改变),结合图1信息,计算此时钴氨溶液中
脱除率为60%(假设溶液体积不发生改变),结合图1信息,计算此时钴氨溶液中 有效含钴率为
有效含钴率为_____ 。
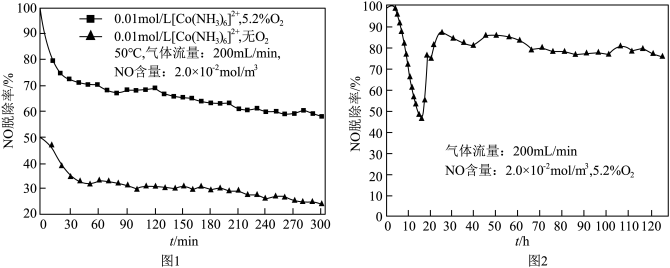
(有效含钴率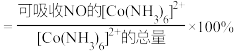 )
) 后,其吸收
后,其吸收 的能力变化如图2所示,前
的能力变化如图2所示,前 内钴氨溶液吸收
内钴氨溶液吸收 的能力不断下降的原因是
的能力不断下降的原因是_____ 。
(3)催化电解 吸收液可将
吸收液可将 还原为
还原为 ,其催化机理如图3所示,在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率
,其催化机理如图3所示,在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率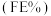 随电解电压的变化如图4所示。已知
随电解电压的变化如图4所示。已知 表示电解生还原产物X所转移电子的物质的量,F表示法拉第常数;
表示电解生还原产物X所转移电子的物质的量,F表示法拉第常数; 表示电解过程中通过的总电量。
表示电解过程中通过的总电量。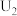 时,催化电解
时,催化电解 生成
生成 的电极反应式为
的电极反应式为_____ 。
②当电解电压为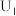 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为_____ 。
 的资源化利用,运用多种方式促进氮的循环转化,具有重要的研究意义。
的资源化利用,运用多种方式促进氮的循环转化,具有重要的研究意义。(1)已知a:


b:C的燃烧热为
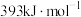 ;
;c:

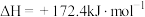
①请写出
 与
与 反应生成两种无污染性气体的热化学方程式:
反应生成两种无污染性气体的热化学方程式:②将等物质的量的
 与
与 混合气体分别通入体积均为
混合气体分别通入体积均为 的恒温密闭容器Ⅰ和绝热密闭容器Ⅱ中,反应一段时间后两容器内达到平衡状态,下列说法正确的是
的恒温密闭容器Ⅰ和绝热密闭容器Ⅱ中,反应一段时间后两容器内达到平衡状态,下列说法正确的是A.两容器内混合气体密度相等
B.
 转化率
转化率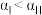
C.反应平衡常数

(2)可利用钴氨配合物吸收
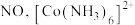 对
对 的配合能力很强,而
的配合能力很强,而 对
对 的配合能力极低。
的配合能力极低。①已知 的结构如图所示
的结构如图所示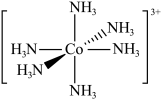 ,
, 中含有
中含有 键的数目是
键的数目是
 溶液脱除
溶液脱除 的效率如图1所示,有氧环境下,发生总反应:
的效率如图1所示,有氧环境下,发生总反应: ,在
,在 的有氧环境下,往
的有氧环境下,往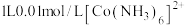 溶液中持续通入试样气体
溶液中持续通入试样气体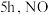 脱除率为60%(假设溶液体积不发生改变),结合图1信息,计算此时钴氨溶液中
脱除率为60%(假设溶液体积不发生改变),结合图1信息,计算此时钴氨溶液中 有效含钴率为
有效含钴率为(有效含钴率
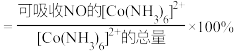 )
)
 后,其吸收
后,其吸收 的能力变化如图2所示,前
的能力变化如图2所示,前 内钴氨溶液吸收
内钴氨溶液吸收 的能力不断下降的原因是
的能力不断下降的原因是(3)催化电解
 吸收液可将
吸收液可将 还原为
还原为 ,其催化机理如图3所示,在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率
,其催化机理如图3所示,在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率 随电解电压的变化如图4所示。已知
随电解电压的变化如图4所示。已知 表示电解生还原产物X所转移电子的物质的量,F表示法拉第常数;
表示电解生还原产物X所转移电子的物质的量,F表示法拉第常数; 表示电解过程中通过的总电量。
表示电解过程中通过的总电量。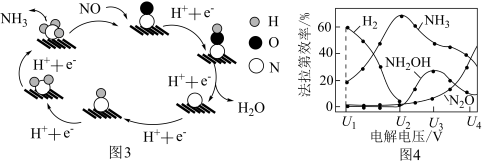
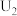 时,催化电解
时,催化电解 生成
生成 的电极反应式为
的电极反应式为②当电解电压为
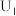 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
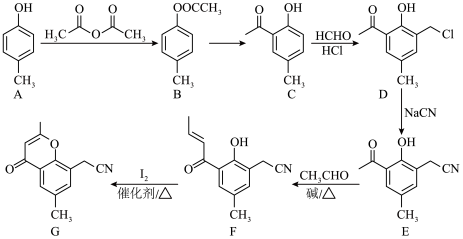
7 . 化合物G是合成具有抗菌、消炎作用的黄酮醋酸类药物的中间体,其合成路线如下:
(1)A的名称是_____ ,B中含有的官能团名称是:_____ 。
(2)满足下列条件的C的同分异构体有_____ 种。
a.苯环上有两个取代基 b.能发生银镜反应 c.能发生水解反应
(3)C生成D的化学方程式为_____ 。
(4)下列关于 的说法不正确的是_____。
的说法不正确的是_____。
(5)化合物G的一种同分异构体结构简式为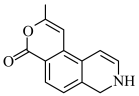 ,分析预测其可能的具有的化学性质,完成下表。
,分析预测其可能的具有的化学性质,完成下表。
(6)参照以上合成路线及条件,以苯、 和
和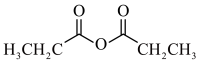 为原料制备
为原料制备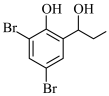 。
。
基于你设计的路线,回答下列问题。
①第一步反应产物的核磁共振氢谱峰面积之比为_____ 。
②最后一步为取代反应,对应的化学方程式为_____ 。
(1)A的名称是
(2)满足下列条件的C的同分异构体有
a.苯环上有两个取代基 b.能发生银镜反应 c.能发生水解反应
(3)C生成D的化学方程式为
(4)下列关于
 的说法不正确的是_____。
的说法不正确的是_____。A.可通过红外光谱检测出有机物E中含有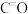 键和 键和 键 键 |
| B.有机物F中所有碳原子一定共平面 |
C.该反应过程有 键的断裂和 键的断裂和 键的形成 键的形成 |
| D.有机物E中碳原子的杂化方式有2种 |
(5)化合物G的一种同分异构体结构简式为
 ,分析预测其可能的具有的化学性质,完成下表。
,分析预测其可能的具有的化学性质,完成下表。| 所用试剂 | 反应生成的新结构 | 反应类型 |
 的 的 溶液 溶液 | ① | 加成反应 |
 溶液 溶液 | ② | ③ |
(6)参照以上合成路线及条件,以苯、
 和
和 为原料制备
为原料制备 。
。基于你设计的路线,回答下列问题。
①第一步反应产物的核磁共振氢谱峰面积之比为
②最后一步为取代反应,对应的化学方程式为
您最近一年使用:0次
8 . 中华民族文明源远流长,下列文物的主要成分属于无机非金属材料的是
|
|
| A.九霄环佩木古琴 | B.银鎏金累丝烧蓝山水纹扇 |
|
|
| C.曾侯乙编钟 | D.青玉交龙钮玉玺 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),该电池可将可乐 中的葡萄糖转化成葡萄糖内酯,下列说法正确的是
中的葡萄糖转化成葡萄糖内酯,下列说法正确的是
 中的葡萄糖转化成葡萄糖内酯,下列说法正确的是
中的葡萄糖转化成葡萄糖内酯,下列说法正确的是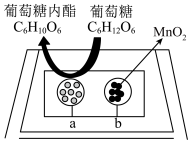
| A.葡萄糖发生还原反应 |
| B.MnO2在正极失电子 |
| C.H+由a极移向b极 |
| D.当电路中转移0.1NA个电子时,生成0.1mol葡萄糖内酯 |
您最近一年使用:0次
解题方法
10 . 25℃条件下研究溶液的酸碱性对反应X(aq)→2Y(aq)的影响,各物质浓度c随反应时间t的变化曲线如图,下列说法正确的是
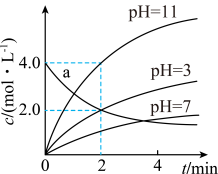
A. 时,反应不能发生 时,反应不能发生 |
| B.H+与OH-相比,H+使反应活化能更低 |
C.a曲线表示 时X的浓度随t的变化 时X的浓度随t的变化 |
D.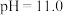 时, 时, 内, 内, |
您最近一年使用:0次

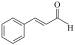 于试管中,滴加酸性KMnO4溶液
于试管中,滴加酸性KMnO4溶液