1 . 某校化学学习小组探究 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题:
(1)写出实验中制备 的化学方程式
的化学方程式________ 。
(2)配制100mL
 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和________ 。
【实验探究】
向3mL
 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
猜想1: 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;
猜想2: 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。
(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,________ ,证明猜想1不成立。
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。
已知:常温下,溶液中 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。________ (填写微粒符号),依据的实验证据是________ 。
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度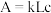 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验结果讨论:若 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若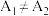 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。
(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如: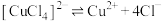 。
。
丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为: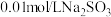 溶液,
溶液,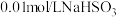 溶液,
溶液, 固体,
固体,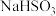 固体
固体
 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题: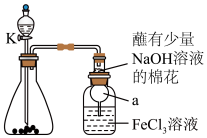
(1)写出实验中制备
 的化学方程式
的化学方程式(2)配制100mL

 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和【实验探究】
向3mL

 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:猜想1:
 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;猜想2:
 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是
 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。组别 | 溶液1(1mL) | 溶液2(2mL) | 现象 |
a |
|
| 溶液1和溶液2混合后,组别a、b、c所得溶液红棕色依次加深。 |
b |  的饱和溶液,用 的饱和溶液,用 固体调节. 固体调节. | ||
c |  的饱和溶液,用 的饱和溶液,用 固体调节 固体调节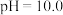 |
 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。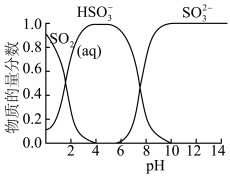
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度
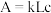 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验序号 | 操作 | 吸光度 |
1 | 把1mL 0.1mol/L 溶液与2mL 溶液与2mL 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 |
|
2 |
|
 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若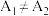 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如:
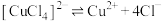 。
。丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为:
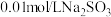 溶液,
溶液,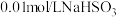 溶液,
溶液, 固体,
固体,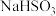 固体
固体实验序号 | 操作 | 吸光度 | 结论 |
3 | 向3mL 0.1mol/L 溶液中通入 溶液中通入 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 |
| |
4 |
  (填“大于”、“小于”或“等于”) (填“大于”、“小于”或“等于”) | 平衡向 |
您最近一年使用:0次
名校
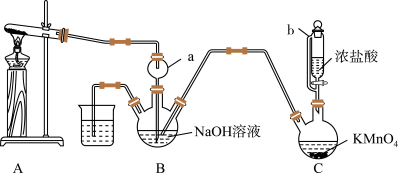
2 . 肼(N2H4)可作火箭发射的燃料。某实验兴趣小组利用氨气与次氯酸钠反应制备N2H4,并探究N2H4的性质,其制备装置如图所示。
(1)N2H4的电子式是_________________________________ 。
(2)仪器b的名称为_________________________ ,仪器a的作用是_________________________________ 。
(3)装置 中发生反应的化学方程式为
中发生反应的化学方程式为_________________________________ 。
(4)采用上述装置制备N2H4时产率较低,可能的原因是_________________________________ 。
(5)写出装置 中生成N2H4的化学方程式
中生成N2H4的化学方程式_________________________________ 。
(6)探究N2H4的性质。将制得的N2H4分离提纯后,进行如下实验。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
(7)肼是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg肼可除去水中溶解的O2的质量为_________________ kg。
(1)N2H4的电子式是
(2)仪器b的名称为
(3)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为(4)采用上述装置制备N2H4时产率较低,可能的原因是
(5)写出装置
 中生成N2H4的化学方程式
中生成N2H4的化学方程式(6)探究N2H4的性质。将制得的N2H4分离提纯后,进行如下实验。
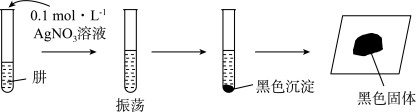
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
操作 | 现象 | 结论 |
 取少量黑色固体于试管中,加入足量 取少量黑色固体于试管中,加入足量 | 黑色固体部分溶解 | 黑色固体中有Ag2O |
 取少量黑色固体于试管中,加入足量稀硝酸,振荡 取少量黑色固体于试管中,加入足量稀硝酸,振荡 | 黑色固体是Ag和Ag2O,则肼具有的性质是碱性和 |
(7)肼是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg肼可除去水中溶解的O2的质量为
您最近一年使用:0次
2024-04-20更新
|
524次组卷
|
2卷引用:广东省韶关市2023-2024学年高三上学期第一次综合检测化学试题
3 . “回望飞天路,逐梦新征程”。下列说法正确的是
| A.月球中的3He与地球上的3H互为同位素 |
| B.“太空快递小哥”天舟六号壳体材料主要为铝合金,其强度大于纯铝 |
C.“问天”实验舱使用砷化镓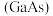 太阳能电池,其中 太阳能电池,其中 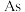 位于周期表的d区 位于周期表的d区 |
| D.长征七号遥七运载火箭采用液氧、煤油等燃料作为推进剂,液氧和煤油均属于混合物 |
您最近一年使用:0次
2024-04-16更新
|
540次组卷
|
3卷引用:广东省韶关市2023-2024学年高三上学期第一次综合检测化学试题
解题方法
4 . H2O2俗称双氧水,是常用的绿色氧化剂,在生产和生活中发挥重要的作用。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:________ 。
②图示历程包含________ 个基元反应,写出决速步骤的化学方程式________________ 。
③C60间的作用力是________ 。
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)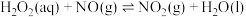
(ii)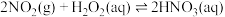
(iii)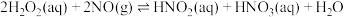
(iv)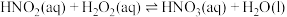
①上述反应体系在一定条件下建立平衡后,下列说法正确的有________ (填序号)。
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
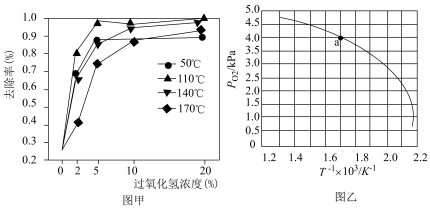
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为________ 。
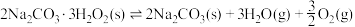 平衡时
平衡时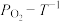 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=________ kPa,平衡常数Kp=________ 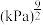 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而________ (填“增大”、“减少”或“不变”)。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:
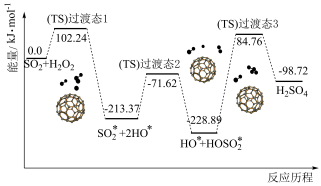
②图示历程包含
③C60间的作用力是
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)
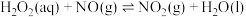
(ii)
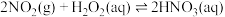
(iii)
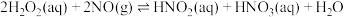
(iv)
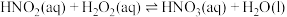
①上述反应体系在一定条件下建立平衡后,下列说法正确的有
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为
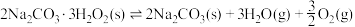 平衡时
平衡时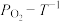 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=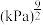 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而
您最近一年使用:0次
2024-04-07更新
|
641次组卷
|
2卷引用:广东省韶关市2024届高三下学期综合测试(二)化学试题
5 . 韶博文物展现了韶州地区的整体社会生活风貌。下列文物主要材料不属于硅酸盐的是
|
|
|
|
| A.明编织纹铜盖豆 | B.东晋陶谷仓 | C.东晋青黄釉瓷钵 | D.清款粉彩龙凤纹赏瓶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 百年变局,科技创新是“关键变量”。下列说法不正确的是
| A.手机芯片的主要成分硅属于共价晶体 |
| B.C919大飞机的燃料煤油属于混合物 |
| C.新能源汽车的锂电池充电时将化学能转化为电能 |
| D.奋斗者号潜水器使用钛合金外壳利用了合金的高强度特点 |
您最近一年使用:0次
7 . 化学无处不在,下列有关说法正确的是
| A.淀粉、纤维素、油脂均属于天然高分子 |
| B.炒菜后铁锅不及时清理容易生锈,因为潮湿环境中铁锅发生析氢腐蚀 |
| C.打开汽水瓶盖有大量气泡冒出,可用勒夏特列原理解释 |
| D.向鸡蛋清溶液中加入食盐浓溶液有白色沉淀析出,因为食盐能使蛋白质变性 |
您最近一年使用:0次
解题方法
8 . 负载金属催化剂对有效提高产率、发展绿色化学技术和有机合成新方法意义重大。其参与合成化合物Ⅸ的路线如下:
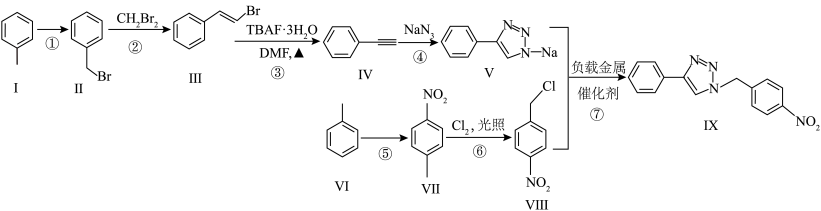
(1)化合物Ⅰ的分子式为________ ,化合物Ⅲ中碳原子的杂化轨道类型为________ 。
(2)化合物Ⅱ发生水解反应生成有机产物的官能团名称为________ ,根据生成新的有机产物的结构特征,分析预测其可能的化学性质,完成下表。
(3)下列关于反应⑦正确的有________(填序号)。
(4)在Ⅷ的芳香同分异构体中,其中含 和
和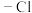 结构的有
结构的有________ 种(不考虑立体异构),核磁共振氢谱图上有四组峰且峰面积之比为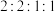 的结构简式为
的结构简式为________ (写一种)。
(5)设计以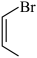 和
和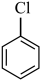 为原料合成
为原料合成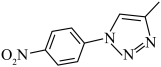 。基于你设计的合成路线,回答下列问题:
。基于你设计的合成路线,回答下列问题:
(a)最后一步反应中,有机反应物为________ (写结构简式)。
(b)相关步骤涉及到卤代烃制炔烃的反应,其反应类型为________ 。
(c)从氯苯出发,第一步反应的化学方程式为________ (注明反应条件)。

(1)化合物Ⅰ的分子式为
(2)化合物Ⅱ发生水解反应生成有机产物的官能团名称为
序号 | 反应试剂与条件 | 反应形成的新结构 | 反应类型 |
a | 加成反应 | ||
b | 氧化反应(生成有机产物) |
(3)下列关于反应⑦正确的有________(填序号)。
| A.该反应为原子利用率100%的反应 |
| B.反应过程中,有σ键、π键的断裂和形成 |
| C.反应物Ⅷ的质谱图中最大质荷比为171.5 |
| D.生成物Ⅸ属于极性分子,且无手性 |
(4)在Ⅷ的芳香同分异构体中,其中含
 和
和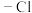 结构的有
结构的有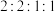 的结构简式为
的结构简式为(5)设计以
 和
和 为原料合成
为原料合成 。基于你设计的合成路线,回答下列问题:
。基于你设计的合成路线,回答下列问题:(a)最后一步反应中,有机反应物为
(b)相关步骤涉及到卤代烃制炔烃的反应,其反应类型为
(c)从氯苯出发,第一步反应的化学方程式为
您最近一年使用:0次
9 . 劳动创造美好生活。下列生活、生产活动中,没有运用相应化学原理的是
选项 | 生活、生产活动 | 化学原理 |
A | 施肥时草木灰和铵态氮肥不能混合使用 |  溶液与铵盐发生双水解 溶液与铵盐发生双水解 |
B | 葡萄糖与银氨溶液制银镜 | 葡萄糖具有还原性 |
C | 液氨常用作制冷剂 | 液氨汽化时吸收大量的热 |
D | 漂白粉漂白有色物质放置一段时间后效果更好 |  酸性强于 酸性强于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 某同学在培养皿上做如下实验(如图所示),a、b、c、d是浸有相关溶液的滤纸。向 晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
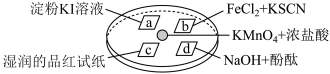
下列对实验现象的“解释或结论”描述,不正确的是
 晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
下列对实验现象的“解释或结论”描述,不正确的是
选项 | 实验现象 | 解释或结论 |
A | a处试纸变蓝 | 还原性: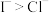 |
B | b处试纸变红 |  |
C | c处试纸褪色 |  与 与 反应生成了具有漂白性的物质 反应生成了具有漂白性的物质 |
D | d处红色褪去 |  和 和 反应使溶液呈中性 反应使溶液呈中性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 溶液
溶液







