名校
1 . 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。
(1)制备N2H4
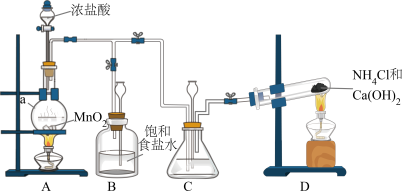
制备N2H4的离子方程式为___________ 。
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
(2)滴定到达终点的现象是___________ 。
(3)实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合肼的质量分数为___________ 。
Ⅲ.探究肼的性质。
(4)写出肼的电子式___________ ,肼为___________ 分子。(填“极性”或“非极性”)。
(5)预设肼可能具有___________ (a.氧化性 b.还原性 c.酸性 d.碱性)。
将制得的肼分离提纯后,进行如图实验探究。
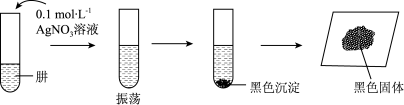
【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
(6)请完成表中的空白部分:①___________ ;②___________ 。
(7)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:___________ 。
(1)制备N2H4

制备N2H4的离子方程式为
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
(2)滴定到达终点的现象是
(3)实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合肼的质量分数为
Ⅲ.探究肼的性质。
(4)写出肼的电子式
(5)预设肼可能具有
将制得的肼分离提纯后,进行如图实验探究。

【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
| 操作 | 现象 | 实验结论 |
| i.取少量黑色固体于试管中,加入适量①___________ | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ii.取少量黑色固体于试管中加入足量稀硝酸,振荡 | ②___________ | 黑色固体是Ag和Ag2O |
(7)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:
您最近一年使用:0次
2 . 亚硝酸钠 主要用于医药、食品保鲜、染料等行业。某小组拟利用氮氧化物(可用
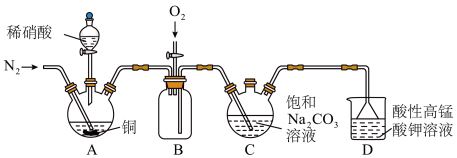
主要用于医药、食品保鲜、染料等行业。某小组拟利用氮氧化物(可用 表示)制备亚硝酸钠,实验装置如图。
表示)制备亚硝酸钠,实验装置如图。
已知: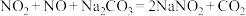 ,
,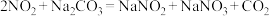
 溶液和饱和
溶液和饱和 液在加热条件下反应可制得
液在加热条件下反应可制得 ,该反应的化学方程式为
,该反应的化学方程式为_________________ ;实验时装置B中应间断性通入适量的 ,其目的是
,其目的是_________________ 。
(2)装置C中盛装饱和 溶液的仪器的名称是
溶液的仪器的名称是_________________ ; 不能单独被纯碱溶液吸收,为了使
不能单独被纯碱溶液吸收,为了使 全被纯碱溶液吸收且产品纯度最高,
全被纯碱溶液吸收且产品纯度最高,
_________________ 。
(3)装置D的作用是_________________ ,采用“倒置漏斗”措施的目的是_________________
(4)设计实验探究 的性质。制备
的性质。制备 实验完毕后,从装置C中分离出
实验完毕后,从装置C中分离出 固体粗产品(不含
固体粗产品(不含 杂质),取少量
杂质),取少量粗产品 配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如下表。
上述实验_________ (填标号)的结论不严谨;你判断的依据是:_____________________________________________ 。
 主要用于医药、食品保鲜、染料等行业。某小组拟利用氮氧化物(可用
主要用于医药、食品保鲜、染料等行业。某小组拟利用氮氧化物(可用 表示)制备亚硝酸钠,实验装置如图。
表示)制备亚硝酸钠,实验装置如图。已知:
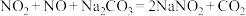 ,
,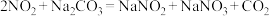
 溶液和饱和
溶液和饱和 液在加热条件下反应可制得
液在加热条件下反应可制得 ,该反应的化学方程式为
,该反应的化学方程式为 ,其目的是
,其目的是(2)装置C中盛装饱和
 溶液的仪器的名称是
溶液的仪器的名称是 不能单独被纯碱溶液吸收,为了使
不能单独被纯碱溶液吸收,为了使 全被纯碱溶液吸收且产品纯度最高,
全被纯碱溶液吸收且产品纯度最高,
(3)装置D的作用是
(4)设计实验探究
 的性质。制备
的性质。制备 实验完毕后,从装置C中分离出
实验完毕后,从装置C中分离出 固体粗产品(不含
固体粗产品(不含 杂质),取少量
杂质),取少量| 实验 | 实验操作及现象 | 结论 |
| 甲 | 滴入无色酚酞溶液中,无色酚酞溶液变红 |  是弱酸 是弱酸 |
| 乙 | 滴入少量酸性 淀粉溶液中,振荡,酸性 淀粉溶液中,振荡,酸性 淀粉溶液变蓝 淀粉溶液变蓝 | 酸性条件下, 具有氧化性 具有氧化性 |
| 丙 | 滴入少量酸性 溶液中,振荡,酸性 溶液中,振荡,酸性 溶液褪色 溶液褪色 | 酸性条件下, 有还原性 有还原性 |
您最近一年使用:0次
名校
3 . 某小组设计实验探究 的漂白原理,装置如图所示。
的漂白原理,装置如图所示。
下列叙述正确的是
 的漂白原理,装置如图所示。
的漂白原理,装置如图所示。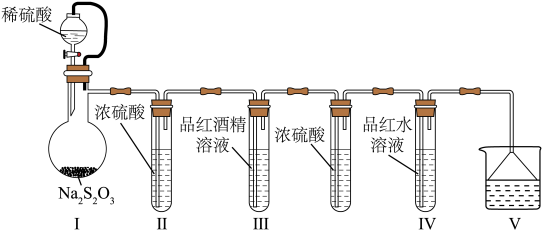
下列叙述正确的是
A.Ⅰ中 表现还原性, 表现还原性, 表现氧化性 表现氧化性 |
| B.撤去Ⅱ装置也能得出正确的实验结论 |
C.比较Ⅲ、Ⅳ中现象可知,在水存在下 表现漂白性 表现漂白性 |
D.若V中装酸性 溶液,可能观察到溶液褪色 溶液,可能观察到溶液褪色 |
您最近一年使用:0次
名校
解题方法
4 . 亚硝酸钠 主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物(可用
主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物(可用 表示)制备亚硝酸钠,简易流程如图。
表示)制备亚硝酸钠,简易流程如图。

已知: ,
,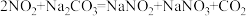
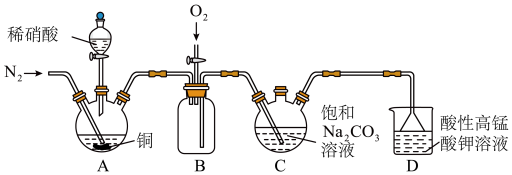
回答下列问题:
(1)利用饱和 溶液和饱和
溶液和饱和 溶液在加热条件下反应可制得
溶液在加热条件下反应可制得 ,该反应的化学方程式为
,该反应的化学方程式为_______ ;实验时装置B中应间断性通入适量的 ,其目的是
,其目的是_______ 。
(2)装置C中盛装饱和 溶液的仪器的名称是
溶液的仪器的名称是_______ ;NO不能单独被纯碱溶液吸收,为了使 完全被纯碱溶液吸收且产品纯度最高,
完全被纯碱溶液吸收且产品纯度最高,
_______ 。
(3)装置D的作用是_______ ,采用“倒置漏斗”措施的目的是_______ 。
(4)设计实验探究 的性质。实验完毕后,从装置C中分离出
的性质。实验完毕后,从装置C中分离出 固体粗产品(不含
固体粗产品(不含 杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
上述实验_______ (填标号)的结论不可靠,理由是_______ 。经实验测得实验丙反应后的溶液中氮元素仅以 的形式存在,酸性
的形式存在,酸性 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为_______ 。
 主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物(可用
主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物(可用 表示)制备亚硝酸钠,简易流程如图。
表示)制备亚硝酸钠,简易流程如图。
已知:
 ,
,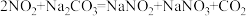

回答下列问题:
(1)利用饱和
 溶液和饱和
溶液和饱和 溶液在加热条件下反应可制得
溶液在加热条件下反应可制得 ,该反应的化学方程式为
,该反应的化学方程式为 ,其目的是
,其目的是(2)装置C中盛装饱和
 溶液的仪器的名称是
溶液的仪器的名称是 完全被纯碱溶液吸收且产品纯度最高,
完全被纯碱溶液吸收且产品纯度最高,
(3)装置D的作用是
(4)设计实验探究
 的性质。实验完毕后,从装置C中分离出
的性质。实验完毕后,从装置C中分离出 固体粗产品(不含
固体粗产品(不含 杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。| 实验 | 实验操作及现象 | 结论 |
| 甲 | 滴入无色酚酞溶液中,无色酚酞溶液变红 |  是弱酸 是弱酸 |
| 乙 | 滴入少量酸性KI-淀粉溶液中,振荡,酸性KI-淀粉溶液变蓝 | 酸性条件下, 具有氧化性 具有氧化性 |
| 丙 | 滴入少量酸性 溶液中,振荡,酸性 溶液中,振荡,酸性 溶液褪色 溶液褪色 | 酸性条件下, 具有还原性 具有还原性 |
 的形式存在,酸性
的形式存在,酸性 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 物质的性质决定用途,下列前后对应关系正确的是
A. 溶液显酸性,可除燃气中的 溶液显酸性,可除燃气中的 |
B. 溶液显碱性,可除废水中的 溶液显碱性,可除废水中的 |
| C.活性炭具有还原性,可吸附自来水中的悬浮物 |
D. 具有氧化性,可用于水的高效消毒杀菌 具有氧化性,可用于水的高效消毒杀菌 |
您最近一年使用:0次
6 . 下列说法中正确的是( )
①钠在空气中燃烧生成淡黄色的Na2O2 ②常温下铝制容器可储运浓硫酸或浓硝酸
③盐酸既有氧化性又有还原性 ④ Fe(OH)3、FeCl2、H2SiO3都不能直接用化合反应制备
⑤ SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
①钠在空气中燃烧生成淡黄色的Na2O2 ②常温下铝制容器可储运浓硫酸或浓硝酸
③盐酸既有氧化性又有还原性 ④ Fe(OH)3、FeCl2、H2SiO3都不能直接用化合反应制备
⑤ SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
| A.②③ | B.①②③ | C.①②③④ | D.①②③⑤ |
您最近一年使用:0次
2016-06-27更新
|
286次组卷
|
7卷引用:2016届海南省海口中学高三全真模拟二化学试卷
2016届海南省海口中学高三全真模拟二化学试卷(已下线)2011-2012学年河南省信阳高中高一下学期期中考试化学试卷(已下线)2015届甘肃省高台县第一中学高三9月月考化学试卷2016届内蒙古赤峰市宁城县高三上学期第一次统考化学试卷2016-2017学年贵州省贵阳六中高二上入学考试化学试卷2017届内蒙古临河区巴彦淖尔一中高三上9月月考化学卷河南省南阳市第一中学2018届高三第四次考试化学试题
名校
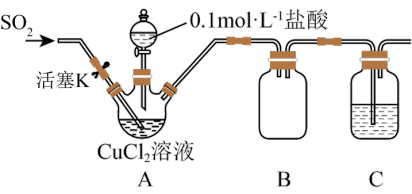
7 . 氯化亚铜(CuCl)是一种重要的化工原料,化学小组用如图装置(部分夹持装置略去)制备CuCl。
②在酸性条件下,某些中间价态的离子能发生自身氧化还原反应。
实验步骤:
I.打开分液漏斗活塞,向三颈瓶中加盐酸调pH至2~3,打开活塞K,通入SO2,溶液中产生白色沉淀,待反应完全后,再通一段时间气体。
Ⅱ.将反应混合液过滤、洗涤、干燥得CuCl粗产品,纯化后得CuCl产品。
回答下列问题:
(1)装置B的作用是_______ ,置C中的试剂为_______ 。
(2)步骤I中通入SO2发生反应的离子方程式是_______ 。
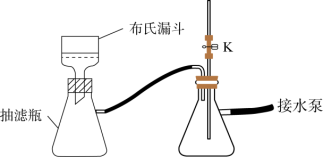
(3)步骤Ⅱ中采用抽滤法过滤的主要目的是:_____ ;抽滤采用下图装置。滤完毕需进行下列操作,从实验安全角度考虑,你认为最合理的第一步操作为_______ (填标号)。
(4)某小组同学发现,将分液漏斗中的0.1 mol·L-1盐酸换为6 mol·L-1盐酸,通入SO2,最终未得到白色沉淀。对此现象有如下猜想:
猜想一:Cl-浓度过大,与CuCl发生反应查阅资料知: CuCl+Cl- CuCl
CuCl ,据此设计实验:将上述未得到沉淀的溶液
,据此设计实验:将上述未得到沉淀的溶液__________ (填操作),若观察到有白色沉淀析出,证明猜想一正确。
猜想二:________ 。设计验证猜想二是否成立的实验方案:________ 。
②在酸性条件下,某些中间价态的离子能发生自身氧化还原反应。
实验步骤:
I.打开分液漏斗活塞,向三颈瓶中加盐酸调pH至2~3,打开活塞K,通入SO2,溶液中产生白色沉淀,待反应完全后,再通一段时间气体。
Ⅱ.将反应混合液过滤、洗涤、干燥得CuCl粗产品,纯化后得CuCl产品。
回答下列问题:
(1)装置B的作用是
(2)步骤I中通入SO2发生反应的离子方程式是
(3)步骤Ⅱ中采用抽滤法过滤的主要目的是:
(4)某小组同学发现,将分液漏斗中的0.1 mol·L-1盐酸换为6 mol·L-1盐酸,通入SO2,最终未得到白色沉淀。对此现象有如下猜想:
猜想一:Cl-浓度过大,与CuCl发生反应查阅资料知: CuCl+Cl-
 CuCl
CuCl ,据此设计实验:将上述未得到沉淀的溶液
,据此设计实验:将上述未得到沉淀的溶液猜想二:
您最近一年使用:0次
8 . 下列陈述Ⅰ和陈述Ⅱ均正确且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A |  能用作膨松剂 能用作膨松剂 |  溶液显碱性 溶液显碱性 |
| B | FeS去除工业废水中的 、 、 | 金属硫化物具有还原性 |
| C | 浓氨水可检验氯气管道是否泄漏 |  被氧化为 被氧化为 |
| D | 氢氟酸不能保存在玻璃瓶中 |  可与HF反应 可与HF反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 部分含N的纯净物的“价-类”二维图如图所示。下列叙述正确的是
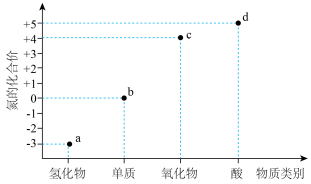
| A.a只有还原性,没有氧化性 | B.一定条件下,a和c反应可生成b |
| C.a的催化氧化可直接生成c | D.c和水反应生成b和d |
您最近一年使用:0次
10 . 物质的性质决定用途。下列物质的性质和用途不匹配的是
| 选项 | 性质 | 用途 |
| A | 氮气的化学性质稳定 | 常作粮食的保护气 |
| B |  具有漂白性 具有漂白性 | 常作红葡萄酒的保鲜剂 |
| C | 活性炭具有强还原性 | 常作冰箱和汽车的除味剂 |
| D |  具有强氧化性 具有强氧化性 | 常作饮用水的消毒剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-16更新
|
218次组卷
|
2卷引用:海南省2023-2024学年高三上学期高考全真模拟卷(四)化学试题



