解题方法
1 . 高铁酸钾(K2FeO4)是一种强氧化剂和环境友好型水处理剂,易分解,遇水和酸易变质。某学习小组在实验室对高铁酸钾的制备和一些性质进行探究。回答下列问题:
(1)高铁酸钾的制备,装置如图1所示。
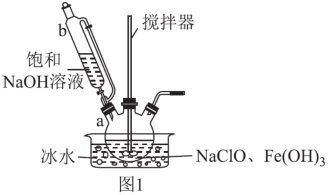
步骤一:将b中饱和NaOH溶液全部逐滴滴入a中,充分反应;
步骤二:由b向a中反应后液体中加入饱和KOH溶液;
步骤三:将a中所得浊液移出,分离提纯。
①仪器b的名称是_______ ,其侧管的作用为_______ 。
②a中制备Na2FeO4反应的离子方程式为_______ 。
③K2FeO4悬浊液经过滤、洗涤,可得粗产品。粗产品中的可溶性杂质可通过_______ 方法进一步提纯。
(2)K2FeO4遇水转化为Fe(OH)3,则其能用于净水的原理为:_______ 。
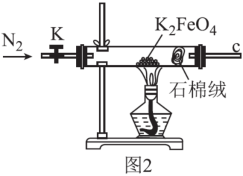
(3)用图2所示装置探究K2FeO4受热分解的产物。设计实验方案证明完全分解后的固体产物中不含Fe(II):取完全分解后的少量固体,溶于稀硫酸,_______ 。
(4)实验室可用间接碘量法测定含少量KCl杂质的K2FeO4样品的纯度:称取0.9000gK2FeO4样品溶于碱性KI溶液中,调节pH使混合液充分反应。用1.000mol·L-1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液15.00mL。请计算K2FeO4样品的纯度:_______ 。
已知: +4I-+8H+=Fe2++2I2+4H2O;I2+2
+4I-+8H+=Fe2++2I2+4H2O;I2+2 =
= +2I-。
+2I-。
(1)高铁酸钾的制备,装置如图1所示。

步骤一:将b中饱和NaOH溶液全部逐滴滴入a中,充分反应;
步骤二:由b向a中反应后液体中加入饱和KOH溶液;
步骤三:将a中所得浊液移出,分离提纯。
①仪器b的名称是
②a中制备Na2FeO4反应的离子方程式为
③K2FeO4悬浊液经过滤、洗涤,可得粗产品。粗产品中的可溶性杂质可通过
(2)K2FeO4遇水转化为Fe(OH)3,则其能用于净水的原理为:
(3)用图2所示装置探究K2FeO4受热分解的产物。设计实验方案证明完全分解后的固体产物中不含Fe(II):取完全分解后的少量固体,溶于稀硫酸,

(4)实验室可用间接碘量法测定含少量KCl杂质的K2FeO4样品的纯度:称取0.9000gK2FeO4样品溶于碱性KI溶液中,调节pH使混合液充分反应。用1.000mol·L-1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液15.00mL。请计算K2FeO4样品的纯度:
已知:
 +4I-+8H+=Fe2++2I2+4H2O;I2+2
+4I-+8H+=Fe2++2I2+4H2O;I2+2 =
= +2I-。
+2I-。
您最近一年使用:0次
2 . 由下列操作与现象推出的相应结论正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 光束通过蛋白质溶液 | 产生光亮通路 | 蛋白质溶液属于胶体 |
| B | 将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已变质 |
| C | 向某溶液中加入盐酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中不一定含有SO42﹣ |
| D | 测定0.1mol•L﹣1和0.01mol•L﹣1的醋酸溶液导电性 | 前者导电性更强 | 浓度越大,醋酸电离程度越大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-09-06更新
|
287次组卷
|
3卷引用:海南省海口市2020届高三6月等级模拟试卷化学试题
名校
解题方法
3 . K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图,请回答下列问题:
I.某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
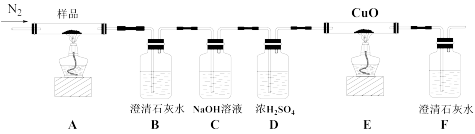
(1)通入氮气的目的是_____ 。
(2)实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有____ 和_____ 。
(3)为防止倒吸,停止实验时应进行的操作是____ 。
(4)样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:_ 。
II.测定三草酸合铁酸钾中铁的含量。
(5)称量mg样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol∙L−1KMnO4,溶液滴定至终点。在滴定管中装入KMnO4溶液(装液)的前一步,应进行的操作为____ 。滴定终点的现象是___ 。
(6)向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol∙L−1KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。该晶体中铁的质量分数的表达式为___ 。若在滴定终点读取滴定管刻度时,俯视KMnO4溶液液面,则测定结果____ (填“偏高”或“偏低”)。
(7)过滤、洗涤实验操作过程需要的玻璃仪器有____ 。
I.某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

(1)通入氮气的目的是
(2)实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
(3)为防止倒吸,停止实验时应进行的操作是
(4)样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:
II.测定三草酸合铁酸钾中铁的含量。
(5)称量mg样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol∙L−1KMnO4,溶液滴定至终点。在滴定管中装入KMnO4溶液(装液)的前一步,应进行的操作为
(6)向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol∙L−1KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。该晶体中铁的质量分数的表达式为
(7)过滤、洗涤实验操作过程需要的玻璃仪器有
您最近一年使用:0次
2021-09-07更新
|
261次组卷
|
2卷引用:2021年海南高考化学试题变式题11-19
解题方法
4 . 黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含SiO2),为了测定该黄铜矿的纯度,甲同学设计了如下图实验:

现称取研细的黄铜矿样品1.84g,在空气存在下进行煅烧,生成Cu、Fe3O 4和SO2气体,实验后取d中溶液的1/10 置于锥形瓶中,用0.05mol/L 标准碘溶液进行滴定,消耗标准溶液 20mL。
请回答下列问题:
(1)将样品研细后再反应,其目的是________________________ 。
(2)装置a和c的作用分别是_______ 和________ (填标号,可以多选)。
a.除去SO2气体 b.除去空气中的水蒸气 c.有利于气体混合
d.有利于观察空气流速 e.除去反应后多余的氧气
(3)滴定达终点时的现象是________________________ 。
(4)上述反应结束后,仍需通一段时间的空气,其目的是_____________________ 。
(5)通过计算可知,该黄铜矿的纯度为________________________ 。
乙同学在甲同学实验的基础上,设计了两种与甲不同的吸收方法,并对吸收产物进行有关处理,同样也测出了黄铜矿的纯度。
(6)方法一:用如下图装置替代上述实验装置 d,同样可以达到实验目的是______ (填序号)。

(7)方法二:将原装置 d 中的试液改为Ba(OH)2,但测得的黄铜矿纯度却产生了+1%的误差,假设实验操作均正确,可能的原因主要有________________________ 。

现称取研细的黄铜矿样品1.84g,在空气存在下进行煅烧,生成Cu、Fe3O 4和SO2气体,实验后取d中溶液的1/10 置于锥形瓶中,用0.05mol/L 标准碘溶液进行滴定,消耗标准溶液 20mL。
请回答下列问题:
(1)将样品研细后再反应,其目的是
(2)装置a和c的作用分别是
a.除去SO2气体 b.除去空气中的水蒸气 c.有利于气体混合
d.有利于观察空气流速 e.除去反应后多余的氧气
(3)滴定达终点时的现象是
(4)上述反应结束后,仍需通一段时间的空气,其目的是
(5)通过计算可知,该黄铜矿的纯度为
乙同学在甲同学实验的基础上,设计了两种与甲不同的吸收方法,并对吸收产物进行有关处理,同样也测出了黄铜矿的纯度。
(6)方法一:用如下图装置替代上述实验装置 d,同样可以达到实验目的是

(7)方法二:将原装置 d 中的试液改为Ba(OH)2,但测得的黄铜矿纯度却产生了+1%的误差,假设实验操作均正确,可能的原因主要有
您最近一年使用:0次
2016-12-09更新
|
251次组卷
|
3卷引用:2016届海南省农垦中学高三考前押题理综化学试卷



