1 . 下列实验操作、现象和所得结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A | 在灼热木炭中加入浓硫酸,将生成的气体依次通过品红溶液、饱和NaHCO3溶液、澄清石灰水 | 品红溶液褪色,澄清石灰水变浑浊 | 浓硫酸和木炭反应产生SO2和CO2气体 |
| B | 惰性电极电解CuCl2溶液,并用湿润的淀粉KI试纸检验阳极产生的气体 | 试纸先变蓝后褪色 | 阳极有氯气产生且氯气具有漂白性 |
| C | 取少量Na2SO3样品溶于蒸馏水,滴加足量稀盐酸,再加入足量BaCl2溶液 | 有白色沉淀生成 | 样品已经变质 |
| D | 用pH试纸测定浓度均为0.1mol·L-1的CH3COONa溶液和NaClO溶液的pH比较溶液pH大小 | 最终CH3COONa溶液对应的pH试纸蓝色较浅 | 酸性:CH3COOH>HClO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列实验方案、现象和结论均正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 取两份新制氯水,分别滴加AgNO3溶液和淀粉KI溶液 | 前者有白色沉淀,后者溶液变蓝 | 氯气与水反应存在限度 |
| B | 向稀硫酸中加入铜粉,再加入少量KNO3固体 | 开始无明显现象,加入KNO3后,溶液变蓝 | KNO3起催化作用 |
| C | 取少量Na2SO3样品溶于蒸馏水,滴加足量稀盐酸,再加入足量BaCl2溶液 | 有白色沉淀生成 | 样品已经变质 |
| D | 向浓度均为0.1mol·L-1的NaCl和Na2CO3溶液中分别滴加酚酞 | 前者不变色,后者变红 | 非金属性:C<Cl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-16更新
|
104次组卷
|
2卷引用:重庆市康德2024年普通高中学业水平选择性考试高三下学期高考模拟调研卷(三)化学试题
名校
解题方法
3 . 下列实验方案设计、现象与结论均正确的是
选项 | 目的 | 方案设计 | 现象与结论 |
A | 比较B元素和C元素的非金属性强弱 | 向 硼酸溶液中加入 硼酸溶液中加入 碳酸氢钠溶液 碳酸氢钠溶液 | 若无明显变化,说明非金属性: |
B | 检验 固体是否变质 固体是否变质 | 取少量固体溶于水,滴加少量 ,再滴入KSCN溶液,振荡,观察溶液颜色变化 ,再滴入KSCN溶液,振荡,观察溶液颜色变化 | 若溶液变红,说明样品已变质 |
C | 证明蔗糖是否水解 | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 悬浊液 悬浊液 | 若无砖红色沉淀,说明蔗糖未发生水解 |
D | 探究不同价态硫元素之间的转化 | 向 和 和 混合溶液中,加入大量浓硫酸 混合溶液中,加入大量浓硫酸 | 若溶液中出现淡黄色沉淀,则说明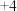 价和 价和 价硫可归中 价硫可归中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018·江西南昌·模拟预测
名校
4 . 下列说法正确的是( )
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B.SO3与Ba(NO3)2溶液可得到BaSO4,SO2与Ba(NO3)2溶液可得到BaSO3 |
| C.将Fe(NO3)3样品溶于稀硫酸后,滴加KSCN溶液,变红,不能说明样品变质 |
| D.室温下,SiO2(s)+3C(s) ═ SiC(s)+2CO(g)不能自发进行,则该反应的ΔH<0 |
您最近一年使用:0次
名校
解题方法
5 . 下列有关实验、现象、及结论等叙述正确的有
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向某溶液加入稀硫酸,有淡黄色沉淀和刺激性气味的气体,该溶液中一定含有S2O32-
④向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
⑤向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑥取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向某溶液加入稀硫酸,有淡黄色沉淀和刺激性气味的气体,该溶液中一定含有S2O32-
④向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
⑤向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑥取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
| A.1条 | B.2条 | C.3条 | D.4条 |
您最近一年使用:0次
2019-12-10更新
|
996次组卷
|
3卷引用:2024届重庆市乌江新高考协作体高三下学期模拟预测化学试题
名校
6 . 三水合硝酸铜[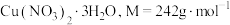 ]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
Ⅰ.三水合硝酸铜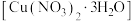 的制备。
的制备。
实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙醇洗涤后得到三水合硝酸铜晶体。
(1)制备硝酸铜时发生反应的离子方程式为___________ 。
(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的最佳试剂为___________ (填化学式)。
Ⅱ. 溶液的配制。
溶液的配制。
(3)实验室里需要450mL0.1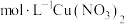 溶液。用三水合硝酸铜
溶液。用三水合硝酸铜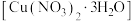 配制该溶液时,下列仪器不需要的是
配制该溶液时,下列仪器不需要的是___________ (填仪器名称)。___________ g。
Ⅲ.测定产品中 的含量
的含量
(5)准备称量ag产品,溶于水后加入过量KI溶液(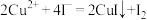 ):充分反应后,以淀粉溶液为指示剂,用c
):充分反应后,以淀粉溶液为指示剂,用c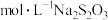 标准溶液滴定(
标准溶液滴定(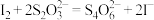 ),达到滴定终点时消耗标准液的体积为VmL。
),达到滴定终点时消耗标准液的体积为VmL。
①达到滴定终点的现象为___________ 。
②产品中 的质量分数为
的质量分数为___________ (用含a、c、V的代数式表示)。
③若所用KI溶液中部分KI被空气氧化,会导致所测结果___________ (填“偏高”“偏低”或“无影响”)。
Ⅳ.三水合硝酸铜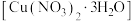 热分解实验。
热分解实验。
(6)将24.2g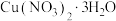 样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示,则升温至
样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示,则升温至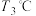 时生成的固体产物为
时生成的固体产物为___________ (填化学式)。
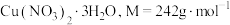 ]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:Ⅰ.三水合硝酸铜
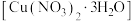 的制备。
的制备。实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙醇洗涤后得到三水合硝酸铜晶体。
(1)制备硝酸铜时发生反应的离子方程式为
(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的最佳试剂为
Ⅱ.
 溶液的配制。
溶液的配制。(3)实验室里需要450mL0.1
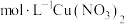 溶液。用三水合硝酸铜
溶液。用三水合硝酸铜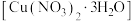 配制该溶液时,下列仪器不需要的是
配制该溶液时,下列仪器不需要的是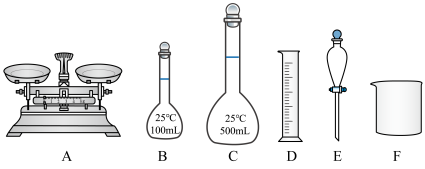
Ⅲ.测定产品中
 的含量
的含量(5)准备称量ag产品,溶于水后加入过量KI溶液(
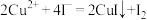 ):充分反应后,以淀粉溶液为指示剂,用c
):充分反应后,以淀粉溶液为指示剂,用c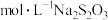 标准溶液滴定(
标准溶液滴定(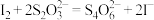 ),达到滴定终点时消耗标准液的体积为VmL。
),达到滴定终点时消耗标准液的体积为VmL。①达到滴定终点的现象为
②产品中
 的质量分数为
的质量分数为③若所用KI溶液中部分KI被空气氧化,会导致所测结果
Ⅳ.三水合硝酸铜
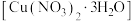 热分解实验。
热分解实验。(6)将24.2g
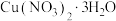 样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示,则升温至
样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示,则升温至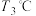 时生成的固体产物为
时生成的固体产物为
您最近一年使用:0次
名校
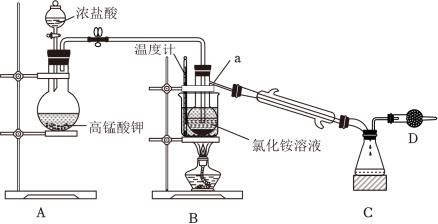
7 . NCl3是一种黄色油状液体,熔点﹣40℃,沸点71℃,常温下密度为1.65g•mL﹣1.95℃以上爆炸,弱酸性环境稳定,中性水中易发生水解。常用于面粉的漂白和杀菌。实验室可用Cl2和NH4Cl 溶液在常温下反应制取,所用装置如图:
(1)仪器a的名称为___________ ;实验室利用装置A还可以制备下列哪些物质 ___________ (填字母)。
a.乙炔 b.硝基苯 c.溴苯 d.乙酸乙酯
(2)打开活塞K1,将浓盐酸滴入圆底烧瓶中,仪器a中制备NCl3的化学反应方程式为___________ ,待反应至仪器a中有大量油状液体生成,关闭活塞K1。将产物分离并用无水MgSO4干燥后,利用B、C装置将NCl3提纯,提纯过程中水浴温度应控制在 ___________ 。
(3)将提纯后的NCl3滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是___________ (使用化学用语结合文字解释)。
(4)液氯储罐中常混有NCl3.为测定氯气中的NCl3含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为:NCl3+4HCl=NH4Cl+3Cl2),产生的气体通过饱和食盐水后再用足量NaOH溶液吸收,测得吸收后NaOH溶液增重35.125g。经测定NCl3吸收管内 质量为0.180g。该样品中NCl3的质量分数为
质量为0.180g。该样品中NCl3的质量分数为 ___________ %(保留三位有效数字);若产生的气体未通过饱和食盐水,则测定结果 ___________ (填“偏高”、“偏低”或“无影响”)。
(1)仪器a的名称为
a.乙炔 b.硝基苯 c.溴苯 d.乙酸乙酯
(2)打开活塞K1,将浓盐酸滴入圆底烧瓶中,仪器a中制备NCl3的化学反应方程式为
(3)将提纯后的NCl3滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是
(4)液氯储罐中常混有NCl3.为测定氯气中的NCl3含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为:NCl3+4HCl=NH4Cl+3Cl2),产生的气体通过饱和食盐水后再用足量NaOH溶液吸收,测得吸收后NaOH溶液增重35.125g。经测定NCl3吸收管内
 质量为0.180g。该样品中NCl3的质量分数为
质量为0.180g。该样品中NCl3的质量分数为
您最近一年使用:0次
名校
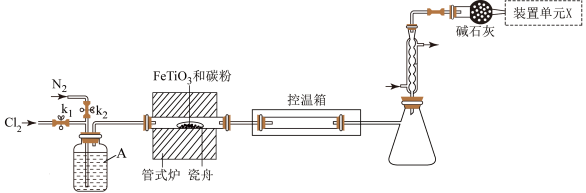
8 . 钛在医疗领域、航空航天材料方面的使用非常广泛。某小组利用如图所示装置在实验室制备并收集 ,并用
,并用 制备纳米
制备纳米 (夹持装置略去)。
(夹持装置略去)。
【实验一】制备无水
已知:① 高温时能与
高温时能与 反应,遇水极易水解;
反应,遇水极易水解;
②瓷舟中物质反应后除生成 、
、 外,还生成一种有毒氧化物气体和少量副产物
外,还生成一种有毒氧化物气体和少量副产物 ;
;
③相关物质的部分物理性质如表:
(1)洗气瓶A中的试剂为________ 。
(2)管式炉加热至900℃,瓷舟中主要发生的化学反应方程式为________ 。
(3)实验过程中需要先后通入 两次,第二次通入
两次,第二次通入 作用是
作用是________ 。装置单元X的作用为________ 。
(4)为除去产物中的 ,控温箱的温度应控制的范围是
,控温箱的温度应控制的范围是________ 。欲分离锥形瓶中的液态混合物,所采用的操作名称是________ 。
【实验二】用 制备纳米
制备纳米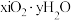
(5)可由 直接水解产生
直接水解产生 ,再经焙烧得
,再经焙烧得 。请写出
。请写出 直接水解产生
直接水解产生 的化学方程式:
的化学方程式:________ 。
(6)实验室可用电位滴定法测定纳米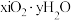 组成,方法如下:
组成,方法如下:
步骤I:取样品纳米 6.94g用稀硫酸充分溶解得到
6.94g用稀硫酸充分溶解得到 ,再用足量单质Al将
,再用足量单质Al将 还原为
还原为 ,过滤并洗涤,将所得滤液和洗涤液合并注入500mL容量瓶,定容得到待测液。
,过滤并洗涤,将所得滤液和洗涤液合并注入500mL容量瓶,定容得到待测液。
步骤Ⅱ:取待测液50.00mL于烧杯中,用 标准溶液滴定,将
标准溶液滴定,将 氧化为
氧化为 时,溶液中
时,溶液中 浓度不断变化,指示电极的电位发生相应变化,根据测量工作电池电动势的变化就可确定滴定终点。
浓度不断变化,指示电极的电位发生相应变化,根据测量工作电池电动势的变化就可确定滴定终点。
用 的
的 标准溶液滴定时,三次滴定消耗标准溶液的平均值为40.00mL。通过计算,该样品的组成为
标准溶液滴定时,三次滴定消耗标准溶液的平均值为40.00mL。通过计算,该样品的组成为________ 。
 ,并用
,并用 制备纳米
制备纳米 (夹持装置略去)。
(夹持装置略去)。
【实验一】制备无水

已知:①
 高温时能与
高温时能与 反应,遇水极易水解;
反应,遇水极易水解;②瓷舟中物质反应后除生成
 、
、 外,还生成一种有毒氧化物气体和少量副产物
外,还生成一种有毒氧化物气体和少量副产物 ;
;③相关物质的部分物理性质如表:
熔点/℃ | 沸点/℃ | 水溶性 | |
| -23.2 | 136.4 | 极易水解生成白色沉淀,能溶于 |
| 306 | 315 | 易水解生成红褐色沉淀 |
| -23 | 76.8 | 难溶于水 |
(2)管式炉加热至900℃,瓷舟中主要发生的化学反应方程式为
(3)实验过程中需要先后通入
 两次,第二次通入
两次,第二次通入 作用是
作用是(4)为除去产物中的
 ,控温箱的温度应控制的范围是
,控温箱的温度应控制的范围是【实验二】用
 制备纳米
制备纳米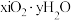
(5)可由
 直接水解产生
直接水解产生 ,再经焙烧得
,再经焙烧得 。请写出
。请写出 直接水解产生
直接水解产生 的化学方程式:
的化学方程式:(6)实验室可用电位滴定法测定纳米
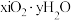 组成,方法如下:
组成,方法如下:步骤I:取样品纳米
 6.94g用稀硫酸充分溶解得到
6.94g用稀硫酸充分溶解得到 ,再用足量单质Al将
,再用足量单质Al将 还原为
还原为 ,过滤并洗涤,将所得滤液和洗涤液合并注入500mL容量瓶,定容得到待测液。
,过滤并洗涤,将所得滤液和洗涤液合并注入500mL容量瓶,定容得到待测液。步骤Ⅱ:取待测液50.00mL于烧杯中,用
 标准溶液滴定,将
标准溶液滴定,将 氧化为
氧化为 时,溶液中
时,溶液中 浓度不断变化,指示电极的电位发生相应变化,根据测量工作电池电动势的变化就可确定滴定终点。
浓度不断变化,指示电极的电位发生相应变化,根据测量工作电池电动势的变化就可确定滴定终点。用
 的
的 标准溶液滴定时,三次滴定消耗标准溶液的平均值为40.00mL。通过计算,该样品的组成为
标准溶液滴定时,三次滴定消耗标准溶液的平均值为40.00mL。通过计算,该样品的组成为
您最近一年使用:0次
2023-05-29更新
|
487次组卷
|
3卷引用:重庆市第八中学校2023届高三下学期全真模拟考试(二模)化学试题
9 . 镍及其化合物在工业上有广泛的应用。工业上用镍矿渣(主要含 、NiS,还含FeO、
、NiS,还含FeO、 、MgO、CaO和
、MgO、CaO和 )制备
)制备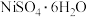 的过程如图所示(已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表)。
的过程如图所示(已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表)。

(1) 的价电子排布式为
的价电子排布式为_______ ;电离一个电子需要吸收的能量
_______________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(2)“酸溶”过程中,NiS发生反应的离子方程式为_________________________ ;如何判断 已足量:
已足量:______________________ (写出具体操作过程)。
(3)滤渣1的成分有_______________ 。
(4)滤渣3的成分为 和
和 。若滤液1中
。若滤液1中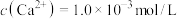 ,当滤液2中
,当滤液2中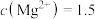
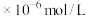 时,除钙率为
时,除钙率为_______________ (忽略沉淀前后溶液体积变化)。(已知: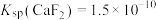 、
、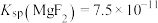 )
)
(5)“滤液2”加入碳酸钠溶液后所得沉淀可表示为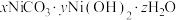 。进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO),则该样品的化学式为
。进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO),则该样品的化学式为_________________ 。

(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。由 溶液获得稳定的
溶液获得稳定的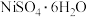 晶体的操作M依次是蒸发浓缩、
晶体的操作M依次是蒸发浓缩、_______________ 、过滤、洗涤、干燥。
 、NiS,还含FeO、
、NiS,还含FeO、 、MgO、CaO和
、MgO、CaO和 )制备
)制备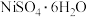 的过程如图所示(已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表)。
的过程如图所示(已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表)。
金属离子 |
|
|
|
|
开始沉淀时的pH | 6.8 | 2.2 | 7.5 | 9.4 |
沉淀完全时的pH | 9.2 | 3.2 | 9.0 | 12.4 |
 的价电子排布式为
的价电子排布式为
 (填“大于”或“小于”)。
(填“大于”或“小于”)。(2)“酸溶”过程中,NiS发生反应的离子方程式为
 已足量:
已足量:(3)滤渣1的成分有
(4)滤渣3的成分为
 和
和 。若滤液1中
。若滤液1中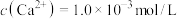 ,当滤液2中
,当滤液2中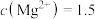
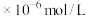 时,除钙率为
时,除钙率为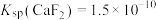 、
、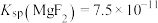 )
)(5)“滤液2”加入碳酸钠溶液后所得沉淀可表示为
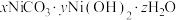 。进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO),则该样品的化学式为
。进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO),则该样品的化学式为
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。由
 溶液获得稳定的
溶液获得稳定的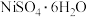 晶体的操作M依次是蒸发浓缩、
晶体的操作M依次是蒸发浓缩、温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 280℃ |
晶体形态 |
|
| 多种结晶水合物 |
|
您最近一年使用:0次
名校
解题方法
10 . 甲醛与新制氢氧化铜反应的产物随反应条件改变而有所不同。实验室对该反应在一定条件下所得产物成分进行探究,具体过程如下。
取一定量的 溶液、
溶液、 溶液和甲醛于锥形瓬中,控制温度为40~50℃回流
溶液和甲醛于锥形瓬中,控制温度为40~50℃回流 ,收集到大量气体
,收集到大量气体 ,并有红色沉淀生成。
,并有红色沉淀生成。
(1)①“控制温度为40~50℃”的常用加热方法是___________ 。
②气体 能燃烧且完全燃烧产物不会使澄清石床水变浑浊,说明该气体是
能燃烧且完全燃烧产物不会使澄清石床水变浑浊,说明该气体是___________ 。
(2)在探究甲醛的氧化产物时,发现未生成 。为了进一步确定甲醛是否被氧化为
。为了进一步确定甲醛是否被氧化为 ,进行如图实验(夹持装置和加热装置已省略,甲酸与浓硫酸反应能生成
,进行如图实验(夹持装置和加热装置已省略,甲酸与浓硫酸反应能生成 ,而
,而 可将银氨溶液还原成银单质)。
可将银氨溶液还原成银单质)。
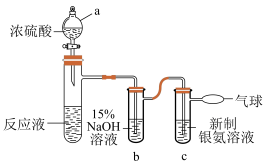
①仪器a的名称是___________ 。
②b中, 溶液的作用是
溶液的作用是___________ 。
③c中,银氨溶液中出现黑色沉淀,则氧化剂与还原剂的物质的量之比为___________ 。
(3)已知: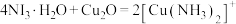 (无色)
(无色) ,
, 遇空气容易被氧化成
遇空气容易被氧化成 (蓝色);验证红色沉淀中含
(蓝色);验证红色沉淀中含 ,进行如下实验步骤和现象记录:取样品,
,进行如下实验步骤和现象记录:取样品,___________ ,说明红色固体中含 。
。
(4)若最终测得红色沉淀为 和少量的
和少量的 ,且
,且 的物质的量和气体X的相等,则该条件下甲醛与新制氢氧化铜、氢氧化钠溶液反应生成
的物质的量和气体X的相等,则该条件下甲醛与新制氢氧化铜、氢氧化钠溶液反应生成 和气体X的化学方程式
和气体X的化学方程式___________ 。
取一定量的
 溶液、
溶液、 溶液和甲醛于锥形瓬中,控制温度为40~50℃回流
溶液和甲醛于锥形瓬中,控制温度为40~50℃回流 ,收集到大量气体
,收集到大量气体 ,并有红色沉淀生成。
,并有红色沉淀生成。(1)①“控制温度为40~50℃”的常用加热方法是
②气体
 能燃烧且完全燃烧产物不会使澄清石床水变浑浊,说明该气体是
能燃烧且完全燃烧产物不会使澄清石床水变浑浊,说明该气体是(2)在探究甲醛的氧化产物时,发现未生成
 。为了进一步确定甲醛是否被氧化为
。为了进一步确定甲醛是否被氧化为 ,进行如图实验(夹持装置和加热装置已省略,甲酸与浓硫酸反应能生成
,进行如图实验(夹持装置和加热装置已省略,甲酸与浓硫酸反应能生成 ,而
,而 可将银氨溶液还原成银单质)。
可将银氨溶液还原成银单质)。
①仪器a的名称是
②b中,
 溶液的作用是
溶液的作用是③c中,银氨溶液中出现黑色沉淀,则氧化剂与还原剂的物质的量之比为
(3)已知:
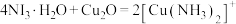 (无色)
(无色) ,
, 遇空气容易被氧化成
遇空气容易被氧化成 (蓝色);验证红色沉淀中含
(蓝色);验证红色沉淀中含 ,进行如下实验步骤和现象记录:取样品,
,进行如下实验步骤和现象记录:取样品, 。
。(4)若最终测得红色沉淀为
 和少量的
和少量的 ,且
,且 的物质的量和气体X的相等,则该条件下甲醛与新制氢氧化铜、氢氧化钠溶液反应生成
的物质的量和气体X的相等,则该条件下甲醛与新制氢氧化铜、氢氧化钠溶液反应生成 和气体X的化学方程式
和气体X的化学方程式
您最近一年使用:0次






