名校
1 . 碳酸亚铁( )是制备“速力菲”(主要成分:琥珀酸亚铁,一种常见的补铁药物)的重要物质。某学习小组同学设计实验制备
)是制备“速力菲”(主要成分:琥珀酸亚铁,一种常见的补铁药物)的重要物质。某学习小组同学设计实验制备 ,并探究
,并探究 的还原性。回答下列问题:Ⅰ.碳酸亚铁的制备。实验装置(夹持仪器已省略)如图所示。
的还原性。回答下列问题:Ⅰ.碳酸亚铁的制备。实验装置(夹持仪器已省略)如图所示。
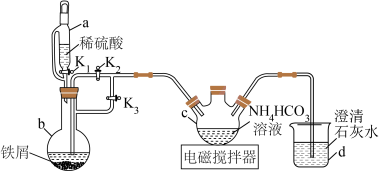
(1)仪器 的名称为
的名称为______ 。
(2)实验开始时,先打开______ (填“ 、
、 或
或 ”,下同)、关闭
”,下同)、关闭______ ;一段时间后,______ , 中反应获得
中反应获得 。
。
(3)已知 中澄清石灰水变浑浊,写出
中澄清石灰水变浑浊,写出 中反应的离子方程式:
中反应的离子方程式:______ 。
(4)反应结束后,将 中的混合液过滤,洗涤。简述证明
中的混合液过滤,洗涤。简述证明 已洗涤干净的操作:
已洗涤干净的操作:____________ 。
Ⅱ.定性定量探究碳酸亚铁有还原性
【查阅资料】氧化亚铁是一种黑色粉末,不稳定,在空气中加热,迅速被氧化成四氧化三铁。
(5)定性探究碳酸亚铁和氧气反应的固体成分:
【提出设想】
假设1固体成分是氧化铁;
假设2固体成分是四氧化三铁;
假设3______ 。
【实验验证】所用装置如下图所示,装药品,打开止水夹 ,通入
,通入 ,加热玻璃管。澄清石灰水不产生沉淀时,停止加热,继续通入
,加热玻璃管。澄清石灰水不产生沉淀时,停止加热,继续通入 至玻璃管冷却。
至玻璃管冷却。
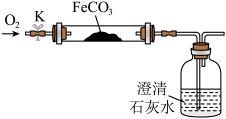
取少量玻璃管里固体于试管中,滴加稀硫酸,微热,固体完全溶解。将溶液分成甲、乙两份,进行后续实验。
【实验评价】上述实验(填“ⅰ”或“ⅱ”)不能确定固体成分。
【实验结论】由上述实验结果分析可知,碳酸亚铁在氧气中高温灼烧得到的产物是______ ,证明 具有还原性。
具有还原性。
(6)定量探究:取______ g纯净固体碳酸亚铁,在空气中高温灼烧至恒重,称得固体质量净减少7.2g,通过计算确定固体成分是 。
。
 )是制备“速力菲”(主要成分:琥珀酸亚铁,一种常见的补铁药物)的重要物质。某学习小组同学设计实验制备
)是制备“速力菲”(主要成分:琥珀酸亚铁,一种常见的补铁药物)的重要物质。某学习小组同学设计实验制备 ,并探究
,并探究 的还原性。回答下列问题:Ⅰ.碳酸亚铁的制备。实验装置(夹持仪器已省略)如图所示。
的还原性。回答下列问题:Ⅰ.碳酸亚铁的制备。实验装置(夹持仪器已省略)如图所示。
(1)仪器
 的名称为
的名称为(2)实验开始时,先打开
 、
、 或
或 ”,下同)、关闭
”,下同)、关闭 中反应获得
中反应获得 。
。(3)已知
 中澄清石灰水变浑浊,写出
中澄清石灰水变浑浊,写出 中反应的离子方程式:
中反应的离子方程式:(4)反应结束后,将
 中的混合液过滤,洗涤。简述证明
中的混合液过滤,洗涤。简述证明 已洗涤干净的操作:
已洗涤干净的操作:Ⅱ.定性定量探究碳酸亚铁有还原性
【查阅资料】氧化亚铁是一种黑色粉末,不稳定,在空气中加热,迅速被氧化成四氧化三铁。
(5)定性探究碳酸亚铁和氧气反应的固体成分:
【提出设想】
假设1固体成分是氧化铁;
假设2固体成分是四氧化三铁;
假设3
【实验验证】所用装置如下图所示,装药品,打开止水夹
 ,通入
,通入 ,加热玻璃管。澄清石灰水不产生沉淀时,停止加热,继续通入
,加热玻璃管。澄清石灰水不产生沉淀时,停止加热,继续通入 至玻璃管冷却。
至玻璃管冷却。
取少量玻璃管里固体于试管中,滴加稀硫酸,微热,固体完全溶解。将溶液分成甲、乙两份,进行后续实验。
实验编号 | 实验步骤 | 实验现象 |
ⅰ | 滴加 | 溶液变红色 |
ⅱ | 向乙溶液中滴加酸性高锰酸钾溶液 | 溶液不褪色 |
【实验结论】由上述实验结果分析可知,碳酸亚铁在氧气中高温灼烧得到的产物是
 具有还原性。
具有还原性。(6)定量探究:取
 。
。
您最近一年使用:0次
2 . Ⅰ.(1) P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是______
a.NH3 b.HI c.SO2 d.CO2
(2)工业生产甲醇的常用方法是:CO(g)+2H2(g) CH3OH(g) △H1 = —90.8kJ/mol。
CH3OH(g) △H1 = —90.8kJ/mol。
已知:2H2(g)+O2(g)=2H2O(l) △H2 = -571.6kJ/mol;
2CO(g)+O2(g)=2CO2(g) △H3= -566.0kJ/mol
计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) △H4 =___________ 。
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4 + 3Zn ="=" Fe2O3 +ZnO +2K2ZnO2
该电池正极发生的反应的电极反应式为____________________________ 。
II.用如图所示装置进行实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
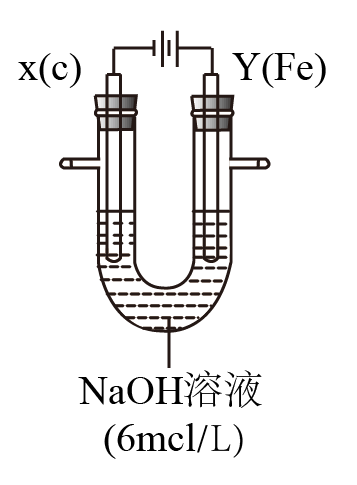
(4)电解过程中,X极区溶液的pH____________ (填“增大” 、“减小”或“不变”)。
(5)电解过程中,Y极发生的电极反应为Fe - 6e- + 8OH-=FeO42- + 4H2O和___________________ 。
(6)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少___________ g。
a.NH3 b.HI c.SO2 d.CO2
(2)工业生产甲醇的常用方法是:CO(g)+2H2(g)
 CH3OH(g) △H1 = —90.8kJ/mol。
CH3OH(g) △H1 = —90.8kJ/mol。已知:2H2(g)+O2(g)=2H2O(l) △H2 = -571.6kJ/mol;
2CO(g)+O2(g)=2CO2(g) △H3= -566.0kJ/mol
计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) △H4 =
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4 + 3Zn ="=" Fe2O3 +ZnO +2K2ZnO2
该电池正极发生的反应的电极反应式为
II.用如图所示装置进行实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。

(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为Fe - 6e- + 8OH-=FeO42- + 4H2O和
(6)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
您最近一年使用:0次
2016-12-09更新
|
122次组卷
|
3卷引用:2016届甘肃省嘉峪关一中高三上第三次模拟考试化学试卷
名校
解题方法
3 . 下图装置可用于收集气体并验证其某些化学性质,下列相关的选项正确的是
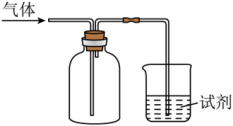
| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A | NH3 | 酚酞溶液 | 溶液变红色 | 氨气显碱性 |
| B | SO2 | 酸性KMnO4溶液 | 溶液褪色 | SO2具有漂白性 |
| C | HCl | 硅酸钠溶液 | 生成白色沉淀 | Cl的非金属性比Si强 |
| D | Cl2 | KI-淀粉溶液 | 溶液变蓝 | Cl2具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-16更新
|
541次组卷
|
5卷引用:2024届甘肃省兰州市高三下学期诊断考试化学试卷
4 . 高铁酸钠(Na2FeO4)是一种绿色净水剂。
①实验室制备原理是 ;
;
②在酸性介质中高铁酸钠不稳定,发生反应: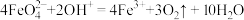 ,在碱性介质中能稳定存在;
,在碱性介质中能稳定存在;
③已知氧化剂的电势是衡量其氧化性强度的主要参数,电势越高,对应条件下氧化剂的氧化性越强,酸性条件下,电势:FeO >Cl2。
>Cl2。
下列叙述错误的是
①实验室制备原理是
 ;
;②在酸性介质中高铁酸钠不稳定,发生反应:
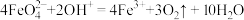 ,在碱性介质中能稳定存在;
,在碱性介质中能稳定存在;③已知氧化剂的电势是衡量其氧化性强度的主要参数,电势越高,对应条件下氧化剂的氧化性越强,酸性条件下,电势:FeO
 >Cl2。
>Cl2。下列叙述错误的是
| A.配制Na2FeO4溶液时添加少量NaOH溶液 |
| B.由反应①知,氧化性:NaClO>Na2FeO4 |
| C.由反应②知,产生11.2LO2时转移2mol电子 |
| D.向Na2FeO4溶液中滴加浓盐酸产生的气体不只一种 |
您最近一年使用:0次
名校
5 . 储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应式为:3C+2K2Cr2O7 +8H2SO4===3CO2↑+2K2SO4
+2Cr2(SO4)3 +8H2O。
(1)请用双线桥法标出电子转移方向和数目________________________________ 。
(2)上述反应中氧化剂是______ (填化学式),被氧化的元素是________ (填元素符号)。
(3)H2SO4 在上述反应中表现出来的性质是____________ (填序号)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为_________ L。
+2Cr2(SO4)3 +8H2O。
(1)请用双线桥法标出电子转移方向和数目
(2)上述反应中氧化剂是
(3)H2SO4 在上述反应中表现出来的性质是
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为
您最近一年使用:0次
2018-09-29更新
|
1013次组卷
|
4卷引用:【全国百强校】甘肃省静宁县第一中学2019届高三上学期第一次模拟考试化学试题
6 . 我国科学家用粗氢氧化高钴 制备硫酸钴晶体(
制备硫酸钴晶体(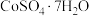 ),其工艺流程如下:
),其工艺流程如下:

已知:ⅰ.还原浸出液中的阳离子有: 、
、 、
、 和
和 等
等
ⅱ.部分物质的溶度积常数(25℃)
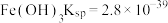
ⅲ.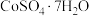 溶解度随温度升高而明显增大
溶解度随温度升高而明显增大
(1)Co元素位于元素周期表的_______ 区,基态Co原子的核外电子排布式为_______ 。
(2)浸出 时,理论上还原性离子和氧化性离子物质的量比为
时,理论上还原性离子和氧化性离子物质的量比为_______ 。
(3)写出“氧化沉铁”的离子方程式_______ ,25℃时,浊液中铁离子浓度为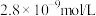 ,此时溶液
,此时溶液
_______ 。
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因_______ 。
(5)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氯化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为: 。
。
已知:铁氰化钾标准液浓度为 ,Co(Ⅱ)标准液质量浓度为
,Co(Ⅱ)标准液质量浓度为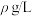 。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗
。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗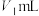 铁氰化钾标准液、
铁氰化钾标准液、 Co(Ⅱ)标准液。
Co(Ⅱ)标准液。
计算样品中钴含量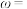
_______ (以钴的质量分数 计)。
计)。
(6)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,该物质的化学式为_______ 。已知:晶体密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞六棱柱底面边长为
,晶胞六棱柱底面边长为 ,则该晶胞的高
,则该晶胞的高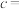
_______  (列出计算式)。
(列出计算式)。

 制备硫酸钴晶体(
制备硫酸钴晶体(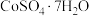 ),其工艺流程如下:
),其工艺流程如下:
已知:ⅰ.还原浸出液中的阳离子有:
 、
、 、
、 和
和 等
等ⅱ.部分物质的溶度积常数(25℃)

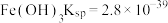
ⅲ.
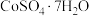 溶解度随温度升高而明显增大
溶解度随温度升高而明显增大(1)Co元素位于元素周期表的
(2)浸出
 时,理论上还原性离子和氧化性离子物质的量比为
时,理论上还原性离子和氧化性离子物质的量比为(3)写出“氧化沉铁”的离子方程式
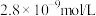 ,此时溶液
,此时溶液
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因
(5)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氯化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为:
 。
。已知:铁氰化钾标准液浓度为
 ,Co(Ⅱ)标准液质量浓度为
,Co(Ⅱ)标准液质量浓度为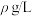 。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗
。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗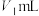 铁氰化钾标准液、
铁氰化钾标准液、 Co(Ⅱ)标准液。
Co(Ⅱ)标准液。计算样品中钴含量
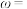
 计)。
计)。(6)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,该物质的化学式为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞六棱柱底面边长为
,晶胞六棱柱底面边长为 ,则该晶胞的高
,则该晶胞的高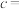
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
名校
解题方法
7 . 亚硝酸钠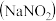 是一种工业盐,外观与食盐相似。下面是某学习小组设计的
是一种工业盐,外观与食盐相似。下面是某学习小组设计的 制取实验和纯度检验实验。该小组收集了相关资料:
制取实验和纯度检验实验。该小组收集了相关资料:
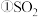 和
和 溶液反应生成
溶液反应生成 和
和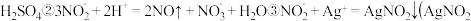 为淡黄色接近白色固体,在水中形成沉淀
为淡黄色接近白色固体,在水中形成沉淀
Ⅰ 亚硝酸钠的制取实验
亚硝酸钠的制取实验

 仪器a的名称为
仪器a的名称为___________ ,A装置中发生的化学反应方程式为________________ 。
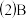 装置中多孔球泡的作用
装置中多孔球泡的作用_________________________ 。
 若装置B中逸出的NO与
若装置B中逸出的NO与 气体物质的量之比为
气体物质的量之比为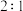 ,则装置B中发生反应的化学方程式为
,则装置B中发生反应的化学方程式为_______ 。
 实验过程中需控制C装置中溶液
实验过程中需控制C装置中溶液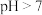 ,否则C中生成的
,否则C中生成的 的产量会下降,理由是
的产量会下降,理由是_______________ 。
 请根据题干所给信息设计实验证明C装置中有
请根据题干所给信息设计实验证明C装置中有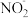 产生:
产生:__________ 。  限选用的试剂: 稀硝酸、硝酸银溶液、NaOH溶液
限选用的试剂: 稀硝酸、硝酸银溶液、NaOH溶液
Ⅱ 亚硝酸钠的纯度检验
亚硝酸钠的纯度检验
已知: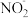

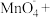
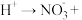

 反应结束后C中溶液通过结晶获得
反应结束后C中溶液通过结晶获得 粗产品mg,溶解后稀释至250mL,分别取
粗产品mg,溶解后稀释至250mL,分别取  用
用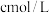 的酸性
的酸性 溶液平行滴定三次,平均每次消耗酸性
溶液平行滴定三次,平均每次消耗酸性 溶液的体积为VmL。则粗产品中
溶液的体积为VmL。则粗产品中 的质量分数为
的质量分数为_______  用含c、V、m的式子表示
用含c、V、m的式子表示 。
。
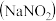 是一种工业盐,外观与食盐相似。下面是某学习小组设计的
是一种工业盐,外观与食盐相似。下面是某学习小组设计的 制取实验和纯度检验实验。该小组收集了相关资料:
制取实验和纯度检验实验。该小组收集了相关资料: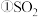 和
和 溶液反应生成
溶液反应生成 和
和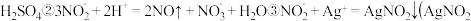 为淡黄色接近白色固体,在水中形成沉淀
为淡黄色接近白色固体,在水中形成沉淀
Ⅰ
 亚硝酸钠的制取实验
亚硝酸钠的制取实验
 仪器a的名称为
仪器a的名称为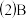 装置中多孔球泡的作用
装置中多孔球泡的作用 若装置B中逸出的NO与
若装置B中逸出的NO与 气体物质的量之比为
气体物质的量之比为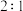 ,则装置B中发生反应的化学方程式为
,则装置B中发生反应的化学方程式为 实验过程中需控制C装置中溶液
实验过程中需控制C装置中溶液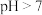 ,否则C中生成的
,否则C中生成的 的产量会下降,理由是
的产量会下降,理由是 请根据题干所给信息设计实验证明C装置中有
请根据题干所给信息设计实验证明C装置中有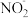 产生:
产生: 限选用的试剂: 稀硝酸、硝酸银溶液、NaOH溶液
限选用的试剂: 稀硝酸、硝酸银溶液、NaOH溶液
Ⅱ
 亚硝酸钠的纯度检验
亚硝酸钠的纯度检验已知:
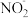

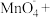
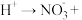

 反应结束后C中溶液通过结晶获得
反应结束后C中溶液通过结晶获得 粗产品mg,溶解后稀释至250mL,分别取
粗产品mg,溶解后稀释至250mL,分别取  用
用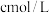 的酸性
的酸性 溶液平行滴定三次,平均每次消耗酸性
溶液平行滴定三次,平均每次消耗酸性 溶液的体积为VmL。则粗产品中
溶液的体积为VmL。则粗产品中 的质量分数为
的质量分数为 用含c、V、m的式子表示
用含c、V、m的式子表示 。
。
您最近一年使用:0次
2019-12-26更新
|
254次组卷
|
5卷引用:【全国百强校】甘肃省天水市第一中学2019届高三下学期第三次模拟考试理科综合化学试题
名校
解题方法
8 . 下列根据实验操作和现象能得出结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向含有 的 的 溶液中通气体 溶液中通气体 | 产生白色沉淀 |  一定体现氧化性 一定体现氧化性 |
| B | 向 溶液中加入足量氯水再加 溶液中加入足量氯水再加 萃取 萃取 |  层呈橙红色 层呈橙红色 |  的还原性强于 的还原性强于 |
| C | 向等浓度的 与 与 混合溶液中滴加少量 混合溶液中滴加少量 溶液 溶液 | 先生成黄色沉淀 | 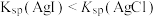 |
| D |  缓慢通入滴有酚酞的 缓慢通入滴有酚酞的 溶液中 溶液中 | 溶液红色褪去 |  具有漂白性 具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-08更新
|
370次组卷
|
3卷引用:甘肃省2024届高三上学期新高考备考模拟考试化学试题
名校
解题方法
9 . 利用熔融碱焙烧工艺可从铝热法生产金属铬所得铬渣(Al、Al2O3、 Cr2O3等)中浸出铬和铝,实现铬和铝的再生利用。其工作流程如下:
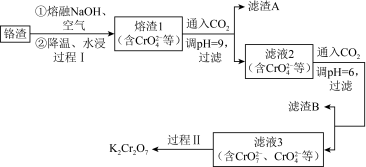
(1)铝热法冶炼金属铬,是利用了金属铝的_______ (填“氧化性”或“还原性”)。
(2)溶液1中的阴离子有 、
、_______ 。
(3)过程I,在Cr2O3参与的反应中,若生成0.4 mol ,消耗氧化剂的物质的量是
,消耗氧化剂的物质的量是_______ 。
(4)通入CO2调节溶液pH实现物质的分离。
①滤渣A煅烧得到Al2O3,再用电解法冶炼Al。冶炼Al的化学方程式是_______ 。
②滤渣B受热分解所得物质可以循环利用,B是_______ 。
③已知:2 +2H+
+2H+
 +H2O K=4.0×1014,滤液3中
+H2O K=4.0×1014,滤液3中 的浓度是0.04 mol/L,则
的浓度是0.04 mol/L,则 的浓度是
的浓度是_______ mol/L。
(5)过程II的目的是得到K2Cr2O7粗品,粗品再重结晶可制得纯净的K2Cr2O7,不同温度下化合物的溶解度(g/100gH2O)
结合表中数据分析,过程II得到K2Cr2O7粗品的操作是:_______ ,过滤得到K2Cr2O7粗品。

(1)铝热法冶炼金属铬,是利用了金属铝的
(2)溶液1中的阴离子有
 、
、(3)过程I,在Cr2O3参与的反应中,若生成0.4 mol
 ,消耗氧化剂的物质的量是
,消耗氧化剂的物质的量是(4)通入CO2调节溶液pH实现物质的分离。
①滤渣A煅烧得到Al2O3,再用电解法冶炼Al。冶炼Al的化学方程式是
②滤渣B受热分解所得物质可以循环利用,B是
③已知:2
 +2H+
+2H+
 +H2O K=4.0×1014,滤液3中
+H2O K=4.0×1014,滤液3中 的浓度是0.04 mol/L,则
的浓度是0.04 mol/L,则 的浓度是
的浓度是(5)过程II的目的是得到K2Cr2O7粗品,粗品再重结晶可制得纯净的K2Cr2O7,不同温度下化合物的溶解度(g/100gH2O)
| 化合物名称 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 |
| K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 |
| K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 |
| Na2Cr2O7 | 163 | 183 | 215 | 269 | 376 |
您最近一年使用:0次
2022-05-25更新
|
133次组卷
|
5卷引用:甘肃省天水市第一中学2018届高三第二次模拟考试理综化学试题
名校
解题方法
10 . 某化学兴趣小组设计如图实验装置(夹持装置已省略),探究 、
、 和
和 的氧化性强弱。
的氧化性强弱。
(1)玻璃管a的作用是__________ 。
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞 ,关闭活塞
,关闭活塞 ,通入
,通入 。
。
①装置A中制备 的离子方程式为
的离子方程式为__________ 。
②证明 的氧化性大于
的氧化性大于 的现象是
的现象是__________ 。
③装置C的作用是__________ ,装置D中所盛试剂为__________ (填化学式)溶液。
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞 ,打开
,打开 ,通入
,通入 气体,验证
气体,验证 的氧化性比
的氧化性比 强。
强。
① 发生反应的化学方程式为
发生反应的化学方程式为__________ 。
②实验完成后,打开弹簧夹,持续通入 的目的是
的目的是__________ 。
(4)淀粉 溶液中
溶液中 的测定:取10.00mL淀粉
的测定:取10.00mL淀粉 溶液,加入足量的硫酸酸化的
溶液,加入足量的硫酸酸化的 溶液,然后加入少量的
溶液,然后加入少量的 粉末除去
粉末除去 ,然后用
,然后用 的
的 标准溶液滴定,达到滴定终点时三次测量平均消耗
标准溶液滴定,达到滴定终点时三次测量平均消耗 标准溶液的体积为25.00mL(
标准溶液的体积为25.00mL(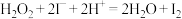 ,
, )。
)。
①滴定终点现象是__________ 。
②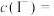
__________  。
。
 、
、 和
和 的氧化性强弱。
的氧化性强弱。
(1)玻璃管a的作用是
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞
 ,关闭活塞
,关闭活塞 ,通入
,通入 。
。①装置A中制备
 的离子方程式为
的离子方程式为②证明
 的氧化性大于
的氧化性大于 的现象是
的现象是③装置C的作用是
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞
 ,打开
,打开 ,通入
,通入 气体,验证
气体,验证 的氧化性比
的氧化性比 强。
强。①
 发生反应的化学方程式为
发生反应的化学方程式为②实验完成后,打开弹簧夹,持续通入
 的目的是
的目的是(4)淀粉
 溶液中
溶液中 的测定:取10.00mL淀粉
的测定:取10.00mL淀粉 溶液,加入足量的硫酸酸化的
溶液,加入足量的硫酸酸化的 溶液,然后加入少量的
溶液,然后加入少量的 粉末除去
粉末除去 ,然后用
,然后用 的
的 标准溶液滴定,达到滴定终点时三次测量平均消耗
标准溶液滴定,达到滴定终点时三次测量平均消耗 标准溶液的体积为25.00mL(
标准溶液的体积为25.00mL(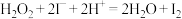 ,
, )。
)。①滴定终点现象是
②
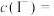
 。
。
您最近一年使用:0次
2024-04-10更新
|
199次组卷
|
3卷引用:甘肃省2024届高三普通高中三模化学试卷

 溶液
溶液

