解题方法
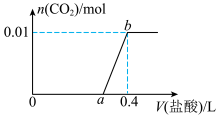
1 . 向NaOH和Na2CO3混合溶液中滴加0.1 mol·L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示回答下列问题_______ 。_______
(2)ab段发生的化学反应方程式为_______ 。
(3)a的值是_______ 、NaOH的物质的量为_______ 、NaOH和Na2CO3的物质的量浓度之比为_______ 。
(2)ab段发生的化学反应方程式为
(3)a的值是
您最近一年使用:0次
解题方法
2 . 现有下列10种物质:①Fe(OH)3胶体②铜③干冰④3%硫酸溶液 ⑤硫酸⑥盐酸⑦烧碱 ⑧纯碱⑨水 ⑩乙醇,用序号填空:
属于混合物的是_______ ;属于氧化物的是_______ ;属于酸的是_______ ;属于碱的是_______ ;属于盐的是_______ ;属于有机物的是_______ ;可以导电的有_______ 。
属于混合物的是
您最近一年使用:0次
3 . 工业废水中含有重铬酸根离子( )有毒,必须处理达标后才能排放。工业上常用绿矾(Feso4·7H2O)处理,反应离子方程式如下:
)有毒,必须处理达标后才能排放。工业上常用绿矾(Feso4·7H2O)处理,反应离子方程式如下: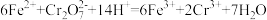 。回答下列问题:
。回答下列问题:
(1)重铬酸根离子( )中铬元素的化合价为
)中铬元素的化合价为_______ 、在该反应中体现_______ (填氧化性或还原性),绿矾在该反应中体现_______ (填氧化性或还原性),该反应中氧化剂和还原剂的原子个数之比为_______ 。
(2)尝试分别用单箭头法、双箭头法表示其电子转移的方向
①_______ (单箭头)
②_______ (双箭头)
(3)能不能将绿矾换为其他物质_______ ?若能则将其与重铬酸根离子反应方程式书写出来:_______ 。
 )有毒,必须处理达标后才能排放。工业上常用绿矾(Feso4·7H2O)处理,反应离子方程式如下:
)有毒,必须处理达标后才能排放。工业上常用绿矾(Feso4·7H2O)处理,反应离子方程式如下: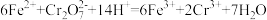 。回答下列问题:
。回答下列问题:(1)重铬酸根离子(
 )中铬元素的化合价为
)中铬元素的化合价为(2)尝试分别用单箭头法、双箭头法表示其电子转移的方向
①
②
(3)能不能将绿矾换为其他物质
您最近一年使用:0次
解题方法
4 . 某白色粉末中可能含有Ba(OH)2、KNO3、Na2CO3、CaCl2,现进行如下实验;
I.取少量粉末加入水中溶解、振荡,有白色沉淀生产;
II.向I悬浊液加入盐酸溶液,白色沉淀消失并伴有气泡产生;
III.取少量II溶液滴加硫酸,产生白色沉淀。
根据上诉实验及现象,判断:
(1)原白色粉末中一定含有的物质是_______ 。
(2)可能含有的物质是_______ 。
(3)写出相关离子方程式_______ 。
I.取少量粉末加入水中溶解、振荡,有白色沉淀生产;
II.向I悬浊液加入盐酸溶液,白色沉淀消失并伴有气泡产生;
III.取少量II溶液滴加硫酸,产生白色沉淀。
根据上诉实验及现象,判断:
(1)原白色粉末中一定含有的物质是
(2)可能含有的物质是
(3)写出相关离子方程式
您最近一年使用:0次
解题方法
5 . 用离子方程式表达下列应用或现象
(1)水垢的主要成分是碳酸钙和氢氧化镁,实验室中可以用盐酸将其除去(任写一个即可)_______ 。
(2)向澄清石灰水中通过量二氧化碳气体_______ 。
(3)小苏打治疗胃酸过多_______ 。
(4)向KHSO4溶液中加入铁粉_______ 。
(5)将等体积等物质的量浓度的硫酸和氢氧化钡混合_______ 。
(1)水垢的主要成分是碳酸钙和氢氧化镁,实验室中可以用盐酸将其除去(任写一个即可)
(2)向澄清石灰水中通过量二氧化碳气体
(3)小苏打治疗胃酸过多
(4)向KHSO4溶液中加入铁粉
(5)将等体积等物质的量浓度的硫酸和氢氧化钡混合
您最近一年使用:0次
6 . 完成下列填空
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较时间保持稳定的放电电压。
高铁电池的总反应为: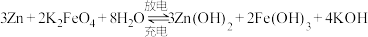
请回答下列问题:
①高铁电池放电时,负极发生___________ (填“氧化”或“还原”)反应,则正极电极反应式为___________ 。
②放电时,___________ (填“正极”或“负极”)附近溶液的碱性减弱。
(2)某种燃料电池的工作原理如图所示,a、b均为惰性电极。
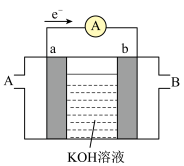
①使用时,空气从___________ 口通入(填“A”或“B”);
②假设使用的“燃料”是甲烷,a极的电极反应式为___________
③假设使用的“燃料”是水煤气(成分为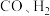 ),如用这种电池在待镀金属表面镀银,待镀金属的质量增加
),如用这种电池在待镀金属表面镀银,待镀金属的质量增加 ,则至少消耗标准状况下水煤气的体积为
,则至少消耗标准状况下水煤气的体积为___________ L。
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较时间保持稳定的放电电压。
高铁电池的总反应为:
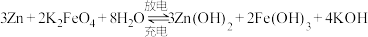
请回答下列问题:
①高铁电池放电时,负极发生
②放电时,
(2)某种燃料电池的工作原理如图所示,a、b均为惰性电极。

①使用时,空气从
②假设使用的“燃料”是甲烷,a极的电极反应式为
③假设使用的“燃料”是水煤气(成分为
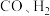 ),如用这种电池在待镀金属表面镀银,待镀金属的质量增加
),如用这种电池在待镀金属表面镀银,待镀金属的质量增加 ,则至少消耗标准状况下水煤气的体积为
,则至少消耗标准状况下水煤气的体积为
您最近一年使用:0次
名校
7 . 回答下列问题
(1)甲醇是一种可再生能源,由 制备甲醇可能涉及的反应如下:
制备甲醇可能涉及的反应如下:
反应Ⅰ: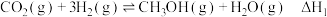
反应Ⅱ: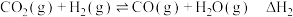
反应Ⅲ: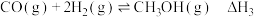
反应Ⅰ、Ⅱ、Ⅲ平衡常数分别为 ,则
,则
___________ (用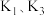 表示)。
表示)。
(2)某探究小组用 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为
浓度为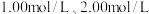 ,大理石有细颗粒和粗颗粒两种规格,实验温度为
,大理石有细颗粒和粗颗粒两种规格,实验温度为 、
、 ,每次实验
,每次实验 的用量为
的用量为 ,大理石用量为
,大理石用量为 。
。
请完成实验设计表,其中a为___________ ,e为___________ 。
(3)①氯气是制备系列含氯化合物的主要原料,可采用如图A所示的装置来制取氯气。装置中的离子膜只允许___________ (填“ ”或“
”或“ ”)通过,氯气的逸出口是
”)通过,氯气的逸出口是___________ (填标号“ ”或“b”)。
”或“b”)。

② 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为___________ 。

(1)甲醇是一种可再生能源,由
 制备甲醇可能涉及的反应如下:
制备甲醇可能涉及的反应如下:反应Ⅰ:
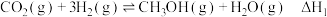
反应Ⅱ:
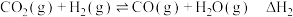
反应Ⅲ:
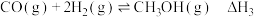
反应Ⅰ、Ⅱ、Ⅲ平衡常数分别为
 ,则
,则
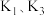 表示)。
表示)。(2)某探究小组用
 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为
浓度为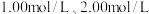 ,大理石有细颗粒和粗颗粒两种规格,实验温度为
,大理石有细颗粒和粗颗粒两种规格,实验温度为 、
、 ,每次实验
,每次实验 的用量为
的用量为 ,大理石用量为
,大理石用量为 。
。| 实验编号 | 温度( ) ) | 大理石规格 |  (浓度) (浓度)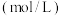 | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响; (Ⅱ)实验①和③探究温度对反应速率的影响; (Ⅲ)实验①和④探究e___________对反应速率的影响 |
| ② | 25 | 粗颗粒 | a___________ | |
| ③ | b___________ | 粗颗粒 | 2.00 | |
| ④ | c___________ | 细颗粒 | d___________ |
(3)①氯气是制备系列含氯化合物的主要原料,可采用如图A所示的装置来制取氯气。装置中的离子膜只允许
 ”或“
”或“ ”)通过,氯气的逸出口是
”)通过,氯气的逸出口是 ”或“b”)。
”或“b”)。
②
 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为
您最近一年使用:0次
名校
8 . 将气体 置于固定容积为2L的密闭容器中,发生如下反应:
置于固定容积为2L的密闭容器中,发生如下反应: ,反应进行到10s末,达到平衡,测得
,反应进行到10s末,达到平衡,测得 的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为
的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为 。
。
(1)用 表示
表示 内反应的平均反应速率为
内反应的平均反应速率为___________ 。
(2)反应前B的物质的量浓度是___________ 。
(3)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①增大压强___________ ;
②降低温度___________ 。
(4)下列叙述能说明该反应已达到化学平衡状态的是___________ (填标号)。
A.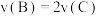
B. 的体积分数不再变化
的体积分数不再变化
C.容器内气体密度不再发生变化
D.容器内压强不再发生变化
E.相同时间内生成 的B的同时生成
的B的同时生成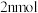 的D
的D
(5)向平衡后的容器中继续充入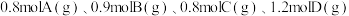 ,此时,v(正)
,此时,v(正)___________ v(逆)。(填“>”、“=”或“<”)
 置于固定容积为2L的密闭容器中,发生如下反应:
置于固定容积为2L的密闭容器中,发生如下反应: ,反应进行到10s末,达到平衡,测得
,反应进行到10s末,达到平衡,测得 的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为
的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为 。
。(1)用
 表示
表示 内反应的平均反应速率为
内反应的平均反应速率为(2)反应前B的物质的量浓度是
(3)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①增大压强
②降低温度
(4)下列叙述能说明该反应已达到化学平衡状态的是
A.
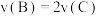
B.
 的体积分数不再变化
的体积分数不再变化C.容器内气体密度不再发生变化
D.容器内压强不再发生变化
E.相同时间内生成
 的B的同时生成
的B的同时生成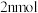 的D
的D(5)向平衡后的容器中继续充入
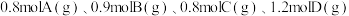 ,此时,v(正)
,此时,v(正)
您最近一年使用:0次
名校
解题方法
9 . 研究发现,在 低压合成甲醇的反应(
低压合成甲醇的反应(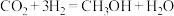 )中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。根据要求回答下列问题:
)中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。根据要求回答下列问题:
(1)在 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为___________ 。
(2)液态水中,三种作用力① 键、②范德华力、③氢键从强到弱的顺序为
键、②范德华力、③氢键从强到弱的顺序为___________ (用标号进行排序)。
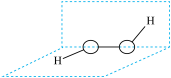
(3) 是一种无色液体,其结构如图所示。根据“相似相溶”原理,
是一种无色液体,其结构如图所示。根据“相似相溶”原理, 在水中的溶解度
在水中的溶解度___________ (填“大于”“小于”或“等于”)其在 中的溶解度。
中的溶解度。
 低压合成甲醇的反应(
低压合成甲醇的反应(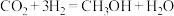 )中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。根据要求回答下列问题:
)中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。根据要求回答下列问题:(1)在
 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为(2)液态水中,三种作用力①
 键、②范德华力、③氢键从强到弱的顺序为
键、②范德华力、③氢键从强到弱的顺序为(3)
 是一种无色液体,其结构如图所示。根据“相似相溶”原理,
是一种无色液体,其结构如图所示。根据“相似相溶”原理, 在水中的溶解度
在水中的溶解度 中的溶解度。
中的溶解度。
您最近一年使用:0次
10 . 回答下列小题
(1)第四周期的元素的基态原子的电子排布中4s轨道只有1个电子的元素有_______ (填元素名称)。
(2)写出Cr3+的价层电子排布式_______ 。
(3)Fe3+的化学性质比Fe2+稳定,其原因是_______ 。
(4)三价铬离子能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中提供电子对形成配位键的原子是_______ ,中心离子的配位数为_______ 。
(1)第四周期的元素的基态原子的电子排布中4s轨道只有1个电子的元素有
(2)写出Cr3+的价层电子排布式
(3)Fe3+的化学性质比Fe2+稳定,其原因是
(4)三价铬离子能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中提供电子对形成配位键的原子是
您最近一年使用:0次



