解题方法
1 . 回答下列问题:
(1)工业上用H2和Cl2反应制HCl,各键能数据为:H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是_______ ;
(2)已知25℃、101kPa时:①2SO2(g)+O2(g)⇌2SO3(g) ΔH1=-197kJ·mol-1
②H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式为_______ ;
(3)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(中的ΔH表示生成1mol产物的数据)。
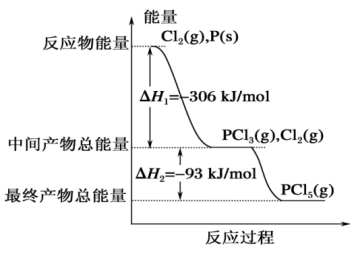
根据上图回答问题:PCl5(g)=PCl3(g)+Cl2(g) ΔH2=_______ ;
(1)工业上用H2和Cl2反应制HCl,各键能数据为:H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是
(2)已知25℃、101kPa时:①2SO2(g)+O2(g)⇌2SO3(g) ΔH1=-197kJ·mol-1
②H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式为
(3)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(中的ΔH表示生成1mol产物的数据)。

根据上图回答问题:PCl5(g)=PCl3(g)+Cl2(g) ΔH2=
您最近一年使用:0次
2 . 已知有机化合物X中各元素的质量分数分别为C:60%、H:13.3%、O:26.7%。
请填空:
(1)有机物X的实验式为____________ ,若0.1mol X在足量氧气中充分燃烧需消耗氧气10.08L(标准状况),则X的分子式为___________________________ ;
(2)实验表明:X能与金属钠反应产生H2,X分子的核磁共振氢谱中有4个吸收峰,且面积之比为3∶2∶2∶1,则X分子中含有的官能团的名称为__________________________ ,X的结构简式为_______________________________ ;
(3)X有两种同分异构体Y和Z,其中Y能与金属钠反应产生H2,而Z不能,则Y、Z的结构简式分别为_____________________ 、_______________________________ 。
请填空:
(1)有机物X的实验式为
(2)实验表明:X能与金属钠反应产生H2,X分子的核磁共振氢谱中有4个吸收峰,且面积之比为3∶2∶2∶1,则X分子中含有的官能团的名称为
(3)X有两种同分异构体Y和Z,其中Y能与金属钠反应产生H2,而Z不能,则Y、Z的结构简式分别为
您最近一年使用:0次
解题方法
3 . (1)3.01×1023个OH-的物质的量为_____ mol,含有电子的物质的量为_____ mol,这些OH-所含的电子数和_____ gNa+含有的电子数相同。
(2)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为_____________ ,R的相对原子质量为__________ ,含R的质量为3.2g的Na2R,其物质的量为__________
(2)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为
您最近一年使用:0次
2016高二·全国·课时练习
4 . 为了提高煤的利用率,人们先把煤转化为CO和H2,再将它们转化为甲醇,某实验人员在一定温度下2L的密闭容器中,充入一定量的H2和CO,发生反应:2H2(g)+CO(g) CH3OH(g),测定的部分实验数据如下:
CH3OH(g),测定的部分实验数据如下:
(1)在500s内用H2表示的化学反应速率是________________ 。
(2)在1000s内用CO表示的化学反应速率是________________ ,1000s时CO的转化率是________ 。
(3)在500s时生成的甲醇的浓度是________
 CH3OH(g),测定的部分实验数据如下:
CH3OH(g),测定的部分实验数据如下:| t/s | 0 | 500 | 1 000 |
| c(H2)/ mol.L-1 | 5.00 | 3.52 | 2.48 |
| c(CO)/ mol.L-1 | 2.50 |
(2)在1000s内用CO表示的化学反应速率是
(3)在500s时生成的甲醇的浓度是
您最近一年使用:0次
2019-11-04更新
|
833次组卷
|
9卷引用:内蒙古自治区呼伦贝尔市鄂温克旗第三中学2020-2021学年高二上学期期中考试化学试题
内蒙古自治区呼伦贝尔市鄂温克旗第三中学2020-2021学年高二上学期期中考试化学试题(已下线)同步君 人教版 选修4 第2章 第1节 化学反应速率高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第一节 化学反应速率 化学反应速率(已下线)2018年9月8日 《每日一题》人教必修4-周末培优陕西省黄陵中学2019-2020学年高二上学期期中考试化学试题步步为赢 高二化学寒假作业:作业二 化学反应速率及其影响因素河南省驻马店市正阳县高级中学2019-2020学年高二上学期第二次月考化学试题课后-6.2.1 化学反应的速率-人教2019必修第二册(已下线)2.1.1 化学反应速率——同步学习必备知识
名校
5 . 在2 L密闭容器中进行反应:aX(s)+bY(g) cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
已知2 min内v(Q)=0.075 mol·L-1·min-1,v(P)∶v(Y)=2∶5。
(1)试确定以下物质的相关量:起始时n(Y)=______ ,2min末时n(Q)=______ 。
(2)上述反应的化学方程式为_________
(3)用Y表示2 min内的反应速率为______ 。2min末,Q在混合气体的体积分数为_____
(4)在保持温度和容积不变的情况下,下列关于上述反应的叙述不 正确的是_____
a.2 min内用X表示的反应速率为0.05mol·L-1·min-1
b.向容器内充入稀有气体Ar(不参与反应),会导致体系压强增大,反应速率加快
c.随着反应的进行,混合气体的平均相对分子质量不再改变即说明反应已经达到平衡
d.随着反应的进行,混合气体的密度不再改变即说明反应已经达到平衡
e.随着反应的进行,混合气体的压强不再改变即说明反应已经达到平衡
 cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:| 物质 时间 | X | Y | P | Q |
| 起始/mol | 0.5 | 1.0 | 1.5 | |
| 2min末/mol | 0.7 | 2.7 | 0.8 | |
| 3min末/mol | 2.7 |
(1)试确定以下物质的相关量:起始时n(Y)=
(2)上述反应的化学方程式为
(3)用Y表示2 min内的反应速率为
(4)在保持温度和容积不变的情况下,下列关于上述反应的叙述
a.2 min内用X表示的反应速率为0.05mol·L-1·min-1
b.向容器内充入稀有气体Ar(不参与反应),会导致体系压强增大,反应速率加快
c.随着反应的进行,混合气体的平均相对分子质量不再改变即说明反应已经达到平衡
d.随着反应的进行,混合气体的密度不再改变即说明反应已经达到平衡
e.随着反应的进行,混合气体的压强不再改变即说明反应已经达到平衡
您最近一年使用:0次
2019-05-31更新
|
251次组卷
|
5卷引用:内蒙古呼伦贝尔市满洲里市第一中学2021-2022学年高一下学期期末考试化学试题
解题方法
6 . 现有反应:CO(g)+ H2O(g) CO2(g)+ H2(g) △H﹤0,在850℃时,平衡常数K=1。现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):
CO2(g)+ H2(g) △H﹤0,在850℃时,平衡常数K=1。现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):
(1)达平衡时,CO转化率为______ ;
(2)H2的体积分数为___ ;
(3)若温度仍为850℃,初始时CO浓度为2mol/L,H2O(g)为6mol/L,则平衡时CO转化率为_____ ;
 CO2(g)+ H2(g) △H﹤0,在850℃时,平衡常数K=1。现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):
CO2(g)+ H2(g) △H﹤0,在850℃时,平衡常数K=1。现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):(1)达平衡时,CO转化率为
(2)H2的体积分数为
(3)若温度仍为850℃,初始时CO浓度为2mol/L,H2O(g)为6mol/L,则平衡时CO转化率为
您最近一年使用:0次
2017-02-17更新
|
329次组卷
|
4卷引用:内蒙古呼伦贝尔市阿荣旗第一中学2020-2021学年高二上学期月考化学试题
2011·内蒙古呼伦贝尔·一模
7 . 某石油液化气由丙烷和丁烷组成,其质量分数分别为80%和20%。它们燃烧的热化学方程式分别为:
C3H8(g)+5O2(g)==3CO2(g)+4H2O(1) △H=-2 200kJ/mol
C4H10(g)+ O2(g)==4CO2(g)+5H2O(1) △H=-2 900 kJ/mol
O2(g)==4CO2(g)+5H2O(1) △H=-2 900 kJ/mol
有一质量为0.80kg、容积为4.0L的铝壶,将一壶20℃的水烧开需消耗液化石油气0.056kg,试计算该燃料的利用率。[已知水的比热为4.2kJ/(kg·℃),铝的比热为0.88kJ/(kg·℃)]
C3H8(g)+5O2(g)==3CO2(g)+4H2O(1) △H=-2 200kJ/mol
C4H10(g)+
 O2(g)==4CO2(g)+5H2O(1) △H=-2 900 kJ/mol
O2(g)==4CO2(g)+5H2O(1) △H=-2 900 kJ/mol有一质量为0.80kg、容积为4.0L的铝壶,将一壶20℃的水烧开需消耗液化石油气0.056kg,试计算该燃料的利用率。[已知水的比热为4.2kJ/(kg·℃),铝的比热为0.88kJ/(kg·℃)]
您最近一年使用:0次
11-12高一上·陕西·期中
8 . 在含有35.8g Na2CO3和NaHCO3混合物的溶液中加入200mL 某浓度的盐酸,恰好完全反应,生成8.96L CO2(标准状况)。问:
(1)原溶液中有__________ mol Na2CO3,__________ mol NaHCO3。
(2)盐酸的物质的量浓度_________ 。
(1)原溶液中有
(2)盐酸的物质的量浓度
您最近一年使用:0次



