解题方法
1 . 某化学兴趣小组欲选用下列装置和药品制取纯净的乙炔并进行有关乙炔性质的探究,试回答下列问题:_______________ 。
(2)制取乙炔时,打开分液漏斗的活塞,使水缓慢滴下的原因是________________ 。
(3)用电石制得的乙炔中常含有H2S等杂质,除去杂质应选用装置________ (填字母,下同),气体应从______ 端进。
(4)乙炔可以通过下列合成路线合成聚丙烯腈,聚丙烯腈可用于生产腈纶(人造羊毛)。
反应①:_________________ 。
反应②:_________________ 。
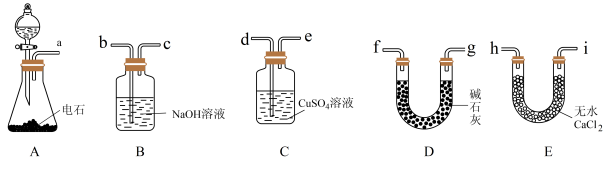
(2)制取乙炔时,打开分液漏斗的活塞,使水缓慢滴下的原因是
(3)用电石制得的乙炔中常含有H2S等杂质,除去杂质应选用装置
(4)乙炔可以通过下列合成路线合成聚丙烯腈,聚丙烯腈可用于生产腈纶(人造羊毛)。
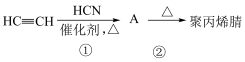
反应①:
反应②:
您最近一年使用:0次
2024-05-08更新
|
238次组卷
|
2卷引用:湖南省长沙市宁乡市第五高级中学2023-2024学年高二上学期期中考试化学试卷
2 . 废弃电脑的CPU中含有贵重金属Cu、Ag、Au,可回收利用,部分流程如下:

(1)铜元素在周期表中位于______ ,基态铜原子的核外电子排布式为______ 。
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
(3)用Zn粉还原 的化学反应方程式为
的化学反应方程式为______ ;
(4)试剂1为______ (填名称,下同),试剂2为______ ;
(5)加入过其铁粉的原因是______ ;
(6)滤渣2溶于试剂2的原因是______ ;(用离子反应方程式表示)
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为______  (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

(1)铜元素在周期表中位于
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
| A.NaOH溶液 | B.纯碱溶液 | C.稀硫酸 | D.酒精 |
(3)用Zn粉还原
 的化学反应方程式为
的化学反应方程式为(4)试剂1为
(5)加入过其铁粉的原因是
(6)滤渣2溶于试剂2的原因是
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为
 (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近一年使用:0次
解题方法
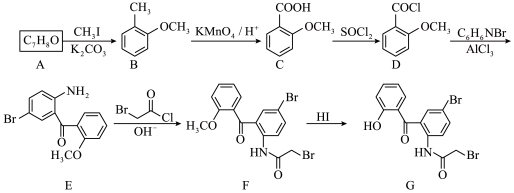
3 . 抗失眠药物的中间体G的合成路线如下:___________ ,其化学名称为___________ 。
(2)C中所含官能团名称为___________ 。
(3)C→D的反应类型为___________ 。
(4)D→E的反应方程式为___________ 。
(5)C的同分异构体之一X,符合条件:①含有苯环;②酸性条件下,水解产物的核磁共振氢谱都只有两个峰。则X的结构简式为___________ 。
(6)可用于鉴别F与G的常用化学试剂为___________ 。
(7)利用上图合成路线信息,以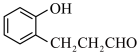 和
和 为原料,设计合成
为原料,设计合成 的路线
的路线___________ 。(无机试剂任选)。
已知: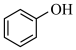

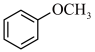 。
。
(2)C中所含官能团名称为
(3)C→D的反应类型为
(4)D→E的反应方程式为
(5)C的同分异构体之一X,符合条件:①含有苯环;②酸性条件下,水解产物的核磁共振氢谱都只有两个峰。则X的结构简式为
(6)可用于鉴别F与G的常用化学试剂为
(7)利用上图合成路线信息,以
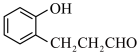 和
和 为原料,设计合成
为原料,设计合成 的路线
的路线
您最近一年使用:0次
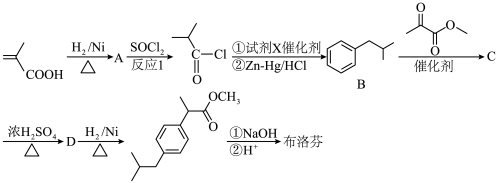
4 . 甲基丙烯酸是一种重要的有机化工原料,一种以甲基丙烯酸制备布洛芬的合成路线如下图所示:
(1)A的化学名称是___________ 。
(2)已知反应1会生成两种刺激性气味气体,写出反应1的化学方程式___________ 。
(3)B的分子式为___________ 。
(4)C→D的反应类型为___________ ,D中官能团的名称是___________ 。
(5)写出布洛芬的结构简式___________ (已知布洛芬的化学式为C13H18O2,不考虑立体异构)。
(6)具有两个取代基的B的芳香化合物同分异构体有___________ 种(不考虑立体异构,填标号)
a.6 b.9 c.12 d.15
其中核磁共振氢谱显示5组峰,且峰面积此为6:4:2:1:1的同分异构体的结构简式为___________ 。
(2)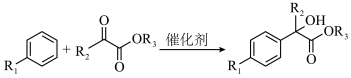
(1)A的化学名称是
(2)已知反应1会生成两种刺激性气味气体,写出反应1的化学方程式
(3)B的分子式为
(4)C→D的反应类型为
(5)写出布洛芬的结构简式
(6)具有两个取代基的B的芳香化合物同分异构体有
a.6 b.9 c.12 d.15
其中核磁共振氢谱显示5组峰,且峰面积此为6:4:2:1:1的同分异构体的结构简式为
您最近一年使用:0次
5 . 磷酸奥司他韦是临床常用的抗病毒药物,常用于治疗甲型和乙型流感。以下为其合成路线之一、______ 。
(2)A中含氧官能团的名称为______ 。
(3)E中碳原子的杂化方式有______ 种。
(4)A→B的化学方程式为______ 。
(5)X是B的同分异构体,符合下列条件的X有______ 种;
①含有六元碳环和“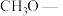 ”;②1molX与足量
”;②1molX与足量 溶液反应生成2mol
溶液反应生成2mol ,其中,核磁共振氢谱有5组峰的结构简式为
,其中,核磁共振氢谱有5组峰的结构简式为______ 。
(6)以上合成路线中反应用到了易爆物质 ,存在安全隐患,研究人员对合成方法进行了改进。改进后的方法需要经历中间物质Z(
,存在安全隐患,研究人员对合成方法进行了改进。改进后的方法需要经历中间物质Z(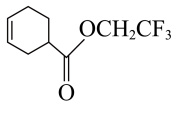 ),请选择1,3-丁二烯、丙烯醇(
),请选择1,3-丁二烯、丙烯醇(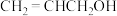 )和
)和 (无机试剂任选),设计合成物质Z的路线
(无机试剂任选),设计合成物质Z的路线______ 。

已知:①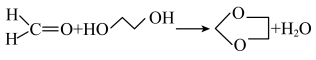
②
(2)A中含氧官能团的名称为
(3)E中碳原子的杂化方式有
(4)A→B的化学方程式为
(5)X是B的同分异构体,符合下列条件的X有
①含有六元碳环和“
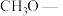 ”;②1molX与足量
”;②1molX与足量 溶液反应生成2mol
溶液反应生成2mol ,其中,核磁共振氢谱有5组峰的结构简式为
,其中,核磁共振氢谱有5组峰的结构简式为(6)以上合成路线中反应用到了易爆物质
 ,存在安全隐患,研究人员对合成方法进行了改进。改进后的方法需要经历中间物质Z(
,存在安全隐患,研究人员对合成方法进行了改进。改进后的方法需要经历中间物质Z( ),请选择1,3-丁二烯、丙烯醇(
),请选择1,3-丁二烯、丙烯醇(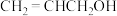 )和
)和 (无机试剂任选),设计合成物质Z的路线
(无机试剂任选),设计合成物质Z的路线
您最近一年使用:0次
解题方法
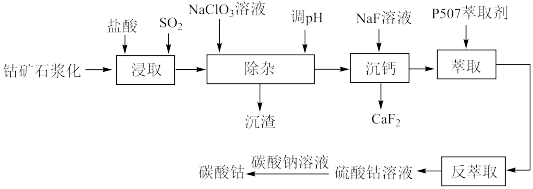
6 . 碳酸钴是一种无机化合物,其化学式为CoCO3。它是一种重要的钴盐,常用于电池、催化剂等领域。工业上以钴矿[主要成分是Co2O3]为原料制取碳酸钴的工艺流程如图: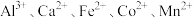 等阳离子
等阳离子
②25℃时,部分阳离子以氢氧化物形式沉淀时溶液的 见表:
见表:
③ 的
的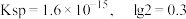
回答下列问题:
(1)Co原子的原子序数为27,其基态原子的价电子排布式为_______ 。
(2)浸取钴矿石前,需要浆化处理,原因是_______ 。
(3)除杂过程中,若加入过量 溶液会产生有毒气体
溶液会产生有毒气体 ,有人提出用压缩空气代替
,有人提出用压缩空气代替 溶液,则通入压缩空气后发生反应的离子方程式为
溶液,则通入压缩空气后发生反应的离子方程式为_______ ,调节 后,若溶液中
后,若溶液中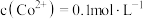 ,此时
,此时 的范围是
的范围是_______ 。
(4)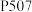 萃取剂
萃取剂 和
和 能发生反应:
能发生反应: 。萃取时,适当增大溶液
。萃取时,适当增大溶液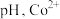 萃取率会增大,其原因是
萃取率会增大,其原因是_______ 。
(5)反萃取时需向萃取液中加入_______ (填写化学式),该工艺中设计萃取、反萃取的目的是_______ 。
(6)一种含 的氧化物晶胞结构如图所示,已知在该氧化物中
的氧化物晶胞结构如图所示,已知在该氧化物中 原子半径为
原子半径为 原子半径为
原子半径为 ,它们在晶体中是紧密接触的。用
,它们在晶体中是紧密接触的。用 表示阿伏加德罗常数的值,则该晶体密度为
表示阿伏加德罗常数的值,则该晶体密度为_______  (列出计算式即可)。
(列出计算式即可)。
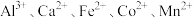 等阳离子
等阳离子②25℃时,部分阳离子以氢氧化物形式沉淀时溶液的
 见表:
见表:| 金属离子 |  |  |  |  |
沉淀完全的 | 8.3 | 2.8 | 4.7 | 9.8 |
 的
的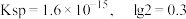
回答下列问题:
(1)Co原子的原子序数为27,其基态原子的价电子排布式为
(2)浸取钴矿石前,需要浆化处理,原因是
(3)除杂过程中,若加入过量
 溶液会产生有毒气体
溶液会产生有毒气体 ,有人提出用压缩空气代替
,有人提出用压缩空气代替 溶液,则通入压缩空气后发生反应的离子方程式为
溶液,则通入压缩空气后发生反应的离子方程式为 后,若溶液中
后,若溶液中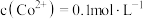 ,此时
,此时 的范围是
的范围是(4)
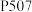 萃取剂
萃取剂 和
和 能发生反应:
能发生反应: 。萃取时,适当增大溶液
。萃取时,适当增大溶液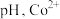 萃取率会增大,其原因是
萃取率会增大,其原因是(5)反萃取时需向萃取液中加入
(6)一种含
 的氧化物晶胞结构如图所示,已知在该氧化物中
的氧化物晶胞结构如图所示,已知在该氧化物中 原子半径为
原子半径为 原子半径为
原子半径为 ,它们在晶体中是紧密接触的。用
,它们在晶体中是紧密接触的。用 表示阿伏加德罗常数的值,则该晶体密度为
表示阿伏加德罗常数的值,则该晶体密度为 (列出计算式即可)。
(列出计算式即可)。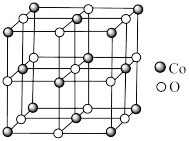
您最近一年使用:0次
名校
解题方法
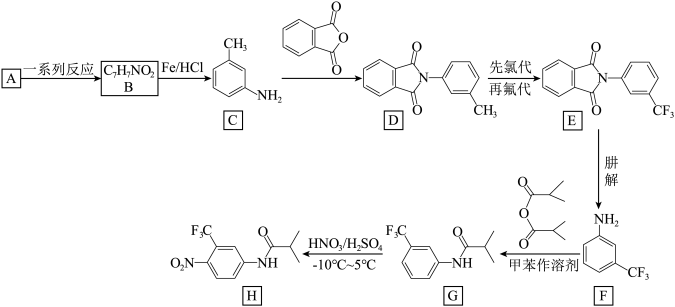
7 . 三氟苯胺类化合物广泛应用于新型医药、染料和农药的合成领域,以间三氟甲基苯胺为中间体合成一种抗肿瘤药物H的合成路线如下图所示:______ ,②化合物C中官能团的名称为______ ,③化合物H的分子式为______ 。
(2)F→G的反应类型是______ 。
(3)该流程中设计C→D的目的是______ 。
(4)G→H的反应方程式为______ 。
(5)化合物B的同分异构体中,符合下列条件的有______ 种;
①-NH2与苯环直接相连
②能与银氨溶液在加热条件下反应产生银镜
其中核磁共振氢谱图显示有4组峰,且峰面积比为1:2:2:2的结构简式为______ 。
(6)参照上述合成路线和信息,设计以苯和乙酸酐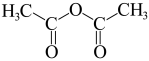 为原料,制备乙酰苯胺
为原料,制备乙酰苯胺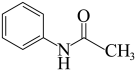 合成路线(其它试剂任选)
合成路线(其它试剂任选)______ 。
(2)F→G的反应类型是
(3)该流程中设计C→D的目的是
(4)G→H的反应方程式为
(5)化合物B的同分异构体中,符合下列条件的有
①-NH2与苯环直接相连
②能与银氨溶液在加热条件下反应产生银镜
其中核磁共振氢谱图显示有4组峰,且峰面积比为1:2:2:2的结构简式为
(6)参照上述合成路线和信息,设计以苯和乙酸酐
 为原料,制备乙酰苯胺
为原料,制备乙酰苯胺 合成路线(其它试剂任选)
合成路线(其它试剂任选)
您最近一年使用:0次
2024-04-16更新
|
647次组卷
|
4卷引用:广东省惠州市2023-2024学年高三上学期第三次调研化学试题
广东省惠州市2023-2024学年高三上学期第三次调研化学试题(已下线)押题卷02(15+4题型) -2024高考化学考点必杀300题(新高考通用)(已下线)压轴题14?有机合成与推断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)-2024年高考化学压轴题专项训练(新高考通用)云南省曲靖市第一中学2024届高三下学期第八次月考理综试题-高中化学
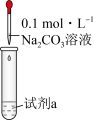
8 . 碳酸钠俗称纯碱,是一种重要的化工原料,在生活、生产和实验研究中均有广泛应用。某学习小组探究 溶液与盐溶液反应的产物,进行如下实验。
溶液与盐溶液反应的产物,进行如下实验。
(1)配制100mL 的
的 溶液。
溶液。
①配制溶液过程中用托盘天平称量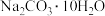 固体的质量为
固体的质量为_______ g。
②定容时,加蒸馏水不慎超过刻度线,处理的方法是_______ 。
(2)通过下列实验探究 溶液与盐溶液反应,记录实验现象如下表:
溶液与盐溶液反应,记录实验现象如下表:
为了探究白色沉淀的成分,设计了热分解实验,其装置如图所示:
①实验甲产生白色沉淀反应的离子方程式为_______ 。
②装置E的作用是_______ 。
③通过热分解实验可判断实验乙所得白色沉淀的成分为_______ (填化学式),实验乙反应的离子方程式为_______ 。
④实验丙所得白色沉淀的化学式可表示为 ,则
,则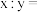
_______ 。
 溶液与盐溶液反应的产物,进行如下实验。
溶液与盐溶液反应的产物,进行如下实验。(1)配制100mL
 的
的 溶液。
溶液。①配制溶液过程中用托盘天平称量
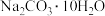 固体的质量为
固体的质量为②定容时,加蒸馏水不慎超过刻度线,处理的方法是
(2)通过下列实验探究
 溶液与盐溶液反应,记录实验现象如下表:
溶液与盐溶液反应,记录实验现象如下表:| 装置 | 实验 | 试剂a | 现象 |
| 甲 | 4mL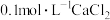 溶液 溶液 | 产生白色沉淀 |
| 乙 | 4mL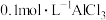 溶液 溶液 | 产生白色沉淀及大量气体 | |
| 丙 | 4mL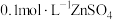 溶液 溶液 | 产生白色沉淀及大量气体 |

| 样品 | 加热前样品质量/g | 加热后样品质量/g | 装置C增重/g | 装置D增重/g |
| 实验乙样品 | 10.4 | 6.8 | 3.6 | 0 |
| 实验丙样品 | 22.4 | 16.2 | 1.8 | 4.4 |
②装置E的作用是
③通过热分解实验可判断实验乙所得白色沉淀的成分为
④实验丙所得白色沉淀的化学式可表示为
 ,则
,则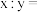
您最近一年使用:0次
9 . W、X、Y、Z、M、Q是原子序数依次增大的前四周期元素,其元素性质或原子结构如表所示。
(1)W、Z、Q的元素符号分别为_______ 、_______ 、_______ 。
(2)X的基态原子有_______ 种空间运动状态不同的电子,其中能量最高的电子所占据的原子轨道呈_______ 形。
(3)与Y处于同一周期的所有元素中,第一电离能比Y大的元素有_______ 种。[XW4]+的电子式为_______ 。
(4)M位于元素周期表的_______ 区,M3+简化的电子排布式为_______ 。
(5)Q在元素周期表中的位置为_______ ,其价层电子轨道表达式为_______ 。
(6)基态某原子的价层电子排布式为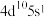 ,推断该元素位于
,推断该元素位于_______ 区。
(7)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 。
。 与
与 的离子半径大小关系为
的离子半径大小关系为
_______ (填“大于”、“小于”或“等于”) ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ 。
(8)下列各组多电子原子的能级能量比较不正确的是_______ (填序号)。
① ②
② ③
③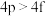 ④
④
| 元素 | 元素性质或原子结构 | ||||||||||||||||||
| W | 电子只有一种自旋取向 | ||||||||||||||||||
| X | 最外层电子排布式为nsnnpn+1 | ||||||||||||||||||
| Y | 非金属元素,且s能级上的电子总数与p能级上的电子总数相等 | ||||||||||||||||||
| Z |
| ||||||||||||||||||
| M | 前四周期元素中原子核外未成对电子数最多 | ||||||||||||||||||
| Q | 基态原子M能层全充满,N层没有成对电子 | ||||||||||||||||||
(2)X的基态原子有
(3)与Y处于同一周期的所有元素中,第一电离能比Y大的元素有
(4)M位于元素周期表的
(5)Q在元素周期表中的位置为
(6)基态某原子的价层电子排布式为
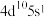 ,推断该元素位于
,推断该元素位于(7)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 。
。 与
与 的离子半径大小关系为
的离子半径大小关系为
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(8)下列各组多电子原子的能级能量比较不正确的是
①
 ②
② ③
③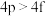 ④
④
您最近一年使用:0次
2024-04-09更新
|
99次组卷
|
2卷引用:江西省南昌市第十九中学2023-2024学年高二上学期期末考试化学试卷
名校
解题方法
10 . 已知五种前四周期的元素X、Y、Z、Q、T。其中,基态X原子的M层上有6种运动状态不同的电子;基态Y原子的简化电子排布式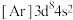 ,基态Z原子的L层的p能级有一个空轨道;基态Q原子的L层的p能级只有一对成对电子;基态T原子的M层上p轨道为半充满状态。根据题给信息,回答问题:
,基态Z原子的L层的p能级有一个空轨道;基态Q原子的L层的p能级只有一对成对电子;基态T原子的M层上p轨道为半充满状态。根据题给信息,回答问题:
(1)试推断这五种元素的符号:X:_____ ,Y:_____ ,Z:_____ ,Q:_____ ,T:_____ 。
(2)Y在元素周期表中的位置为_____________ 。
(3)基态Z原子的轨道表示式为_____________ 。
(4)对于T原子的p轨道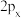 、
、 、
、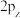 间的差异,下列说法错误的是
间的差异,下列说法错误的是____ (填字母)。
a.电子云形状相同 b.原子轨道的对称类型不同
c.电子的能量不同 d.电子云空间伸展方向不同
(5)Z元素的最高价氧化物对应水化物的电离方程式为______________ 。
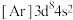 ,基态Z原子的L层的p能级有一个空轨道;基态Q原子的L层的p能级只有一对成对电子;基态T原子的M层上p轨道为半充满状态。根据题给信息,回答问题:
,基态Z原子的L层的p能级有一个空轨道;基态Q原子的L层的p能级只有一对成对电子;基态T原子的M层上p轨道为半充满状态。根据题给信息,回答问题:(1)试推断这五种元素的符号:X:
(2)Y在元素周期表中的位置为
(3)基态Z原子的轨道表示式为
(4)对于T原子的p轨道
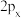 、
、 、
、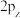 间的差异,下列说法错误的是
间的差异,下列说法错误的是a.电子云形状相同 b.原子轨道的对称类型不同
c.电子的能量不同 d.电子云空间伸展方向不同
(5)Z元素的最高价氧化物对应水化物的电离方程式为
您最近一年使用:0次
2024-04-09更新
|
59次组卷
|
2卷引用:名校期末好题汇编-原子结构与性质(非选择题)