解题方法
1 . 实验室用固体烧碱配制480mL0.1mol⋅L−1NaOH溶液。
(1)配制上述溶液时需称量NaOH固体的质量为__________ g(保留两位小数)
(2)配制过程中不需要使用下列仪器中的_______ (填仪器序号),其中还缺少的玻璃仪器是_________ 、___________ (填仪器名称)。_______ 。
A.用适量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量蒸馏水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加蒸馏水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻度线1~2cm处
(4)在容量瓶内确定溶液体积的过程中,当液面离容量瓶颈部的刻度线1~2cm时的做法是_______
(5)下列的实验操作可能导致配制的溶液浓度偏高的是(填序号)_______ 。
①称量NaOH固体时,砝码生锈
②移液时,未洗涤烧杯和玻璃棒
③定容时俯视容量瓶刻度线
④摇匀后液面低于刻度线,继续加水至刻度线
⑤容量瓶内有少量水
(1)配制上述溶液时需称量NaOH固体的质量为
(2)配制过程中不需要使用下列仪器中的
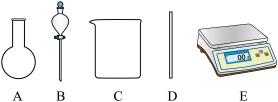
A.用适量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量蒸馏水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加蒸馏水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻度线1~2cm处
(4)在容量瓶内确定溶液体积的过程中,当液面离容量瓶颈部的刻度线1~2cm时的做法是
(5)下列的实验操作可能导致配制的溶液浓度偏高的是(填序号)
①称量NaOH固体时,砝码生锈
②移液时,未洗涤烧杯和玻璃棒
③定容时俯视容量瓶刻度线
④摇匀后液面低于刻度线,继续加水至刻度线
⑤容量瓶内有少量水
您最近一年使用:0次
解题方法
2 . 某学生欲用下列装置制取纯净FeCl3固体。其中A是Cl2的发生装置,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网,F为干燥的空广口瓶,烧杯G为尾气吸收装置。
(1)该装置中有一明显错误是____________ (填字母)。
(2)D中所装试剂为_____________ ,C装置的作用是___________________ 。
(3)A中发生反应的化学方程式是__________________ ,G中发生反应的离子方程式是________________ 。
(4)若用100mL 12mol/L盐酸与足量MnO2充分反应,生成的Cl2体积(标准状况)________________ (填“大于”“小于”或“等于”)6.72 L。
(5)用所制取的FeCl3固体制成Fe(OH)3胶体,区分胶体和溶液常用________ ,分离胶体和溶液常用的方法叫__________ 。

(1)该装置中有一明显错误是
(2)D中所装试剂为
(3)A中发生反应的化学方程式是
(4)若用100mL 12mol/L盐酸与足量MnO2充分反应,生成的Cl2体积(标准状况)
(5)用所制取的FeCl3固体制成Fe(OH)3胶体,区分胶体和溶液常用
您最近一年使用:0次
3 . Ⅰ.已知X、Y两种元素的原子序数之和等于41。X元素原子的4p能级上有3个电子,Y元素原子的最外层2p能级上有4个电子。请回答下列问题。
(1)X元素基态原子的电子排布式__________ ,该元素的符号是__________ 。
(2)Y元素原子的价层电子排布式为__________ ,该元素的名称是__________ 。
Ⅱ.有四种短周期元素,与其相关的结构、性质等信息如下表所述:
请根据表中信息回答不列问题:
(3)A元素基态原子的电子排布式为__________ 。
(4)B元素在元素周期表中的位置为__________ 。
(5)C基态原子的轨道表示式是__________ ,其原子核外有__________ 个未成对电子,能量最高的电子为轨道上的电子,其原子轨道呈__________ 形。
(6)D原子的电子排布式为__________ , 的结构示意图为
的结构示意图为__________ 。
(1)X元素基态原子的电子排布式
(2)Y元素原子的价层电子排布式为
Ⅱ.有四种短周期元素,与其相关的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物对应水化物具有两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最高的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(3)A元素基态原子的电子排布式为
(4)B元素在元素周期表中的位置为
(5)C基态原子的轨道表示式是
(6)D原子的电子排布式为
 的结构示意图为
的结构示意图为
您最近一年使用:0次
4 . (Ⅰ)已知A为常见的金属单质。B俗称磁性氯化铁。根据如图所示的关系:
B:_______ D:_______ 。
(2)写出③的离子方程式:_______ 。
(3)写出④的化学方程式:_______ 。
(4)写出⑤的化学方程式:_______ 。
(5)写出E→F的现象_______ 。
写出E→F的化学方程式_______ 。
(Ⅱ)某兴趣小组同学为探究黑木耳中的含铁量,进行如下实验。已知:
ⅰ.黑木耳富含蛋白质、糖类、卵磷脂、铁及一些还原性物质等。每100克黑木耳含铁高达185毫克。
ⅱ.紫色的 溶液在酸性条件下有强氧化性,其还原产物是无色的
溶液在酸性条件下有强氧化性,其还原产物是无色的 。
。
ⅲ. 与铁氰化钾(
与铁氰化钾(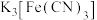 )溶液反应生成蓝色沉淀。
)溶液反应生成蓝色沉淀。
为确定黑木耳中含有铁元素,甲同学设计实验方案如图。_______ 。
(7)步骤④检验 所用试剂是
所用试剂是_______ 溶液。
(8)下列有关上述实验得出的结论正确的是_______ (填字母符号)。
a.黑木耳中一定含 和
和
b.滤液A中一定含 和
和
c.白色沉淀中一定含
为测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
(10)步骤⑦中观察到的实验现象是_______ ,反应的离子方程式是_______ 。

B:
(2)写出③的离子方程式:
(3)写出④的化学方程式:
(4)写出⑤的化学方程式:
(5)写出E→F的现象
写出E→F的化学方程式
(Ⅱ)某兴趣小组同学为探究黑木耳中的含铁量,进行如下实验。已知:
ⅰ.黑木耳富含蛋白质、糖类、卵磷脂、铁及一些还原性物质等。每100克黑木耳含铁高达185毫克。
ⅱ.紫色的
 溶液在酸性条件下有强氧化性,其还原产物是无色的
溶液在酸性条件下有强氧化性,其还原产物是无色的 。
。ⅲ.
 与铁氰化钾(
与铁氰化钾(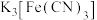 )溶液反应生成蓝色沉淀。
)溶液反应生成蓝色沉淀。为确定黑木耳中含有铁元素,甲同学设计实验方案如图。
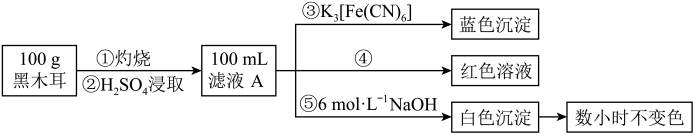
(7)步骤④检验
 所用试剂是
所用试剂是(8)下列有关上述实验得出的结论正确的是
a.黑木耳中一定含
 和
和
b.滤液A中一定含
 和
和
c.白色沉淀中一定含

为测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
| A.Na | B.Zn | C.Fe | D.Cu |
(10)步骤⑦中观察到的实验现象是
您最近一年使用:0次
解题方法
5 . 按要求填空
(1)实验室要配制240mL 0.1mol/L 溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、
溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、_______ 、_______
(2)用托盘天平称取碳酸钠固体,其质量为_______
(3)下列主要操作步骤的正确顺序是_______ (填序号)。
①称取一定质量的 ,放入烧杯中,用适量蒸馏水溶解;
,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度_______ (填“偏高”或“偏低”或“无影响”下同)。
定容前,容量瓶中有少量蒸馏水,结果所配溶液的物质的量浓度_______ 。定容时必须使溶液的凹液面与刻度相平,若仰视会使结果浓度_______ 。
(1)实验室要配制240mL 0.1mol/L
 溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、
溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、(2)用托盘天平称取碳酸钠固体,其质量为
(3)下列主要操作步骤的正确顺序是
①称取一定质量的
 ,放入烧杯中,用适量蒸馏水溶解;
,放入烧杯中,用适量蒸馏水溶解;②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度
定容前,容量瓶中有少量蒸馏水,结果所配溶液的物质的量浓度
您最近一年使用:0次
6 . 已知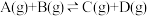 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的平衡常数表达式
___________ ,
___________ 0(填“<”、“>”或“=”);
(2)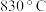 时,向一个
时,向一个 的密闭容器中充入
的密闭容器中充入 的A和
的A和 的B,若反应初始
的B,若反应初始 内A的平均反应速率
内A的平均反应速率 ,则
,则 时
时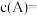
___________  ,C的物质的量为
,C的物质的量为___________  ;若反应一段时间后达到平衡,则A的转化率为
;若反应一段时间后达到平衡,则A的转化率为___________ ;如果这时向该密闭容器中再充入 氩气,平衡时A的转化率为
氩气,平衡时A的转化率为___________ 。
(3)判断该反应是否达到平衡的依据为___________ (填字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.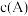 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等
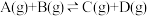 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式


(2)
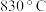 时,向一个
时,向一个 的密闭容器中充入
的密闭容器中充入 的A和
的A和 的B,若反应初始
的B,若反应初始 内A的平均反应速率
内A的平均反应速率 ,则
,则 时
时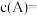
 ,C的物质的量为
,C的物质的量为 ;若反应一段时间后达到平衡,则A的转化率为
;若反应一段时间后达到平衡,则A的转化率为 氩气,平衡时A的转化率为
氩气,平衡时A的转化率为(3)判断该反应是否达到平衡的依据为
a.压强不随时间改变 b.气体的密度不随时间改变
c.
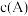 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等
您最近一年使用:0次
解题方法
7 . 用 盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。
盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。
(1)准确称取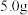 烧碱样品,所用主要仪器有托盘天平、砝码、药匙、
烧碱样品,所用主要仪器有托盘天平、砝码、药匙、___________ 。
(2)将样品配成 待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、
待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、___________ 。
(3)取 待测液,需要的仪器有
待测液,需要的仪器有___________ 、锥形瓶。
(4)酸碱中和滴定实验的操作步骤有:检查仪器、___________ 、加入反应液、调节起始读数、放出反应液、确定滴定终点、读取数据、重复上述实验步骤2次、处理数据。
(5)根据下表数据,计算被测烧碱溶液的浓度是___________ 。
(6)根据上述各数据,计算烧碱的纯度是___________ 。
(7)用蒸馏水洗涤完滴定管后,接着取标准液来滴定待测液,则导致计算出的待测液浓度___________ ;若滴定终点读取数据时俯视,则导致计算出的待测液浓度___________ (均填“偏大”“偏小”或“无影响”)。
 盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。
盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。(1)准确称取
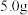 烧碱样品,所用主要仪器有托盘天平、砝码、药匙、
烧碱样品,所用主要仪器有托盘天平、砝码、药匙、(2)将样品配成
 待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、
待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、(3)取
 待测液,需要的仪器有
待测液,需要的仪器有(4)酸碱中和滴定实验的操作步骤有:检查仪器、
(5)根据下表数据,计算被测烧碱溶液的浓度是
| 滴定次数 | 待测溶液体积/ | 盐酸标准溶液体积/ | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
(6)根据上述各数据,计算烧碱的纯度是
(7)用蒸馏水洗涤完滴定管后,接着取标准液来滴定待测液,则导致计算出的待测液浓度
您最近一年使用:0次
名校
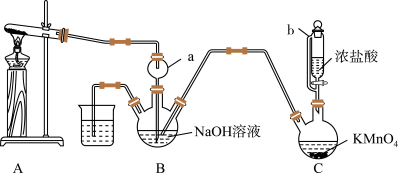
8 . 肼(N2H4)可作火箭发射的燃料。某实验兴趣小组利用氨气与次氯酸钠反应制备N2H4,并探究N2H4的性质,其制备装置如图所示。
(1)N2H4的电子式是_________________________________ 。
(2)仪器b的名称为_________________________ ,仪器a的作用是_________________________________ 。
(3)装置 中发生反应的化学方程式为
中发生反应的化学方程式为_________________________________ 。
(4)采用上述装置制备N2H4时产率较低,可能的原因是_________________________________ 。
(5)写出装置 中生成N2H4的化学方程式
中生成N2H4的化学方程式_________________________________ 。
(6)探究N2H4的性质。将制得的N2H4分离提纯后,进行如下实验。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
(7)肼是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg肼可除去水中溶解的O2的质量为_________________ kg。
(1)N2H4的电子式是
(2)仪器b的名称为
(3)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为(4)采用上述装置制备N2H4时产率较低,可能的原因是
(5)写出装置
 中生成N2H4的化学方程式
中生成N2H4的化学方程式(6)探究N2H4的性质。将制得的N2H4分离提纯后,进行如下实验。
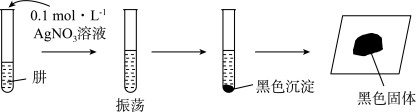
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
操作 | 现象 | 结论 |
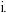 取少量黑色固体于试管中,加入足量 取少量黑色固体于试管中,加入足量 | 黑色固体部分溶解 | 黑色固体中有Ag2O |
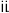 取少量黑色固体于试管中,加入足量稀硝酸,振荡 取少量黑色固体于试管中,加入足量稀硝酸,振荡 | 黑色固体是Ag和Ag2O,则肼具有的性质是碱性和 |
(7)肼是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg肼可除去水中溶解的O2的质量为
您最近一年使用:0次
2024-04-20更新
|
471次组卷
|
2卷引用:2024届天津市宁河区芦台第一中学高三下学期第三次模拟化学试题
9 . 已知: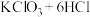 (浓)
(浓)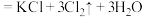 。某小组利用氯酸钾与
。某小组利用氯酸钾与 盐酸反应制氯气并进行氯气性质的研究,实验装置如图所示:
盐酸反应制氯气并进行氯气性质的研究,实验装置如图所示:
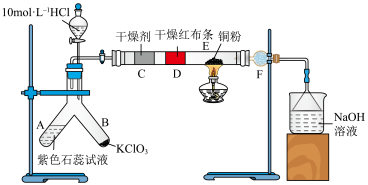
请回答:
(1)请你写出另一个不同的实验室制氯气原理:___________ (用化学方程式表示)。
(2)E中的实验现象是___________ 。
(3)根据“相关实验现象”就可以证明起漂白作用的不是氯气而是次氯酸,A中的现象是___________ ,D中的现象是___________ 。
(4)装置中 溶液的作用是
溶液的作用是___________ ,写出相应的离子方程式___________ 。
(5)反应后烧杯中的溶液也是84消毒液的主要成分 ,家用消毒液在使用过程中要注意不可与洁厕灵(主要成分为浓盐酸)混用,关于盐酸与次氯酸钠的反应,同学们持不同意见。
,家用消毒液在使用过程中要注意不可与洁厕灵(主要成分为浓盐酸)混用,关于盐酸与次氯酸钠的反应,同学们持不同意见。
①甲同学认为发生反应: ,该反应属于
,该反应属于___________ (填基本反应类型)。
②乙同学则认为二者发生氧化还原反应: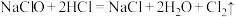 ,该反应中有
,该反应中有___________ (填百分数) 未发生氧化还原反应。
未发生氧化还原反应。
③丙同学通过实验证明乙同学的看法正确,过程如下:向盛有浓盐酸的试管中滴加 溶液后,观察到
溶液后,观察到___________ (填实验现象)。
(6)现要配制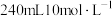 所需盐酸,请回答下列问题:
所需盐酸,请回答下列问题:
①所用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是___________ 。
②配制过程中有下列实验操作步骤,其正确的顺序为___________ 。
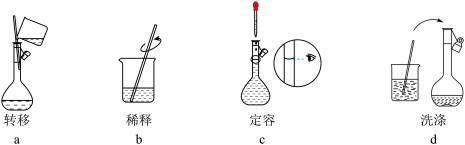
④下列操作会使配制结果偏高的是___________ 。
A.容量瓶洗净后未干燥直接用来配制溶液
B.图a操作中,玻璃棒位于刻度线以上
C.定容时俯视读数
D.用量筒量取浓盐酸配制所需盐酸时,量筒仰视读数
E.反复摇匀后发现液面低于刻度线,继续加水至刻度线
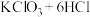 (浓)
(浓)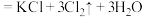 。某小组利用氯酸钾与
。某小组利用氯酸钾与 盐酸反应制氯气并进行氯气性质的研究,实验装置如图所示:
盐酸反应制氯气并进行氯气性质的研究,实验装置如图所示:
请回答:
(1)请你写出另一个不同的实验室制氯气原理:
(2)E中的实验现象是
(3)根据“相关实验现象”就可以证明起漂白作用的不是氯气而是次氯酸,A中的现象是
(4)装置中
 溶液的作用是
溶液的作用是(5)反应后烧杯中的溶液也是84消毒液的主要成分
 ,家用消毒液在使用过程中要注意不可与洁厕灵(主要成分为浓盐酸)混用,关于盐酸与次氯酸钠的反应,同学们持不同意见。
,家用消毒液在使用过程中要注意不可与洁厕灵(主要成分为浓盐酸)混用,关于盐酸与次氯酸钠的反应,同学们持不同意见。①甲同学认为发生反应:
 ,该反应属于
,该反应属于②乙同学则认为二者发生氧化还原反应:
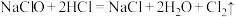 ,该反应中有
,该反应中有 未发生氧化还原反应。
未发生氧化还原反应。③丙同学通过实验证明乙同学的看法正确,过程如下:向盛有浓盐酸的试管中滴加
 溶液后,观察到
溶液后,观察到(6)现要配制
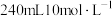 所需盐酸,请回答下列问题:
所需盐酸,请回答下列问题:①所用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是
②配制过程中有下列实验操作步骤,其正确的顺序为

④下列操作会使配制结果偏高的是
A.容量瓶洗净后未干燥直接用来配制溶液
B.图a操作中,玻璃棒位于刻度线以上
C.定容时俯视读数
D.用量筒量取浓盐酸配制所需盐酸时,量筒仰视读数
E.反复摇匀后发现液面低于刻度线,继续加水至刻度线
您最近一年使用:0次
10 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视⻆。铁元素的“价-类”二维图如图所示:

(1)C的化学式是___________ ,E→F反应的化学方程式是___________ ,反应过程的现象为___________ 。
(2)A在一定条件下可以和水蒸气发生反应,反应方程式是___________ 。
(3)维生素C可将H转化为G,维生素C具有___________ (填“酸性”、“氧化性”或“还原性”)。
(4)在指定条件下,下列铁及其化合物之间的转化不能实现的是___________ 。
A.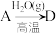 B.
B.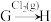 C.
C.
(5)某小组同学设计如下实验,研究亚铁盐与 溶液的反应。
溶液的反应。
试剂:酸化的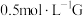 溶液,5%
溶液,5% 溶液
溶液
上述实验中 溶液与G溶液反应的离子方程式是
溶液与G溶液反应的离子方程式是___________ 。

(1)C的化学式是
(2)A在一定条件下可以和水蒸气发生反应,反应方程式是
(3)维生素C可将H转化为G,维生素C具有
(4)在指定条件下,下列铁及其化合物之间的转化不能实现的是
A.
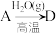 B.
B.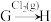 C.
C.
(5)某小组同学设计如下实验,研究亚铁盐与
 溶液的反应。
溶液的反应。试剂:酸化的
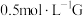 溶液,5%
溶液,5% 溶液
溶液| 操作 | 现象 |
取 酸化的G溶液于试管中,加入 酸化的G溶液于试管中,加入 5% 5% 溶液 溶液 | 溶液立即变为棕黄色,稍后,产生气泡。 |
向反应后的溶液中加入 溶液 溶液 | 溶液变红 |
 溶液与G溶液反应的离子方程式是
溶液与G溶液反应的离子方程式是
您最近一年使用:0次



