名校
解题方法
1 . “侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。模拟“侯氏制碱法”以粗盐水为原料制备纯碱的流程如图所示。
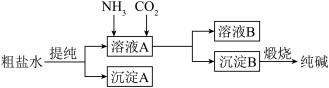
回答下列问题:
(1)粗盐水中含有 杂质,提纯过程应加试剂为
杂质,提纯过程应加试剂为___________ ;沉淀A___________ 电解质(填“是”或“不是”)。
(2)向溶液A中先通入___________ 至饱和(填“ ”或“
”或“ ”,下同),再向溶液中通入
”,下同),再向溶液中通入___________ ,此时观察到溶液中有晶体析出,该反应的化学方程式为___________ 。
(3)溶液B中主要溶质的电离方程式为___________ 。
(4)此流程中可以循环利用的物质是___________ 。

回答下列问题:
(1)粗盐水中含有
 杂质,提纯过程应加试剂为
杂质,提纯过程应加试剂为(2)向溶液A中先通入
 ”或“
”或“ ”,下同),再向溶液中通入
”,下同),再向溶液中通入(3)溶液B中主要溶质的电离方程式为
(4)此流程中可以循环利用的物质是
您最近一年使用:0次
2 . 某研究性学习小组利用下图装置制备漂白粉。

回答下列问题:
(1)若用二氧化锰和浓盐酸为原料制取氯气,则装置①应选用___________ (填“I”“Ⅱ”或“Ⅲ”),其反应的离子方程式为___________ 。
(2)装置②中饱和食盐水的作用是___________ ;装置④中的X试剂为___________ 。
(3)装置③中发生反应的化学方程式为___________ ;该反应是放热反应,反应温度较高时有副反应发生,为减少副反应发生可将装置③置于___________ (填“冷水浴”或“热水浴”)中进行反应。
(4)向装置①中加入200mL浓盐酸(密度为 、质量分数为36.5%)与
、质量分数为36.5%)与 反应,产生了5.6L的氯气(已换算成标准状况下的体积)。
反应,产生了5.6L的氯气(已换算成标准状况下的体积)。
①该浓盐酸的物质的量浓度为___________ 。
②被氧化的HCl的物质的量为___________ 。

回答下列问题:
(1)若用二氧化锰和浓盐酸为原料制取氯气,则装置①应选用
(2)装置②中饱和食盐水的作用是
(3)装置③中发生反应的化学方程式为
(4)向装置①中加入200mL浓盐酸(密度为
 、质量分数为36.5%)与
、质量分数为36.5%)与 反应,产生了5.6L的氯气(已换算成标准状况下的体积)。
反应,产生了5.6L的氯气(已换算成标准状况下的体积)。①该浓盐酸的物质的量浓度为
②被氧化的HCl的物质的量为
您最近一年使用:0次
名校
解题方法
3 . 下图中甲、乙、丙、丁是均含氯元素的常见物质,其中甲为单质,乙是“84”消毒液的有效成分,丙、丁为酸。

回答下列问题:
(1)甲、乙、丙、丁四种物质中能使湿润红色布条褪色的是___________ (填化学式)。
(2)下列关于四步反应的说法中错误的是___________(填标号)。
(3)甲在标准状况下的密度为___________ (保留三位有效数字)。
(4)某实验需用480mL 乙的消毒液,现用固体乙配制。
乙的消毒液,现用固体乙配制。
①需要用托盘天平称量固体乙的质量为___________ g(保留小数点后一位)。
②在配制过程中,除需要量筒、烧杯、玻璃棒、托盘天平外还必需的仪器有___________ 。
③某同学取10mL该消毒液,稀释10倍后用于环境消毒,稀释后溶液中阳离子的浓度为___________ 。

回答下列问题:
(1)甲、乙、丙、丁四种物质中能使湿润红色布条褪色的是
(2)下列关于四步反应的说法中错误的是___________(填标号)。
| A.均为氧化还原反应 | B.反应①为置换反应 |
| C.反应②为复分解反应 | D.反应③为分解反应 |
(4)某实验需用480mL
 乙的消毒液,现用固体乙配制。
乙的消毒液,现用固体乙配制。①需要用托盘天平称量固体乙的质量为
②在配制过程中,除需要量筒、烧杯、玻璃棒、托盘天平外还必需的仪器有
③某同学取10mL该消毒液,稀释10倍后用于环境消毒,稀释后溶液中阳离子的浓度为
您最近一年使用:0次
名校
解题方法
4 . 碳酸钠和碳酸氢钠是生活中常见的物质。
回答下列问题:
(1)向碳酸钠饱和溶液中通入 溶液变浑浊,反应的离子方程式为
溶液变浑浊,反应的离子方程式为___________ ;由此可知在相同温度下,碳酸钠的溶解度比碳酸氢钠的___________ (填“大”或“小”)。
(2)碳酸氢钠溶液与氢氧化钙溶液按溶质的物质的量之比为2∶1混合反应时,所得溶液中溶质为___________ (写化学式);检验所得溶液中溶质的阴离子的方法是___________ 。
(3)将27.4g 和
和 的混合物,加热到质量不再变化时,得残留固体21.2g.则原混合物中
的混合物,加热到质量不再变化时,得残留固体21.2g.则原混合物中 和
和 的质量之比为
的质量之比为___________ 。
(4)向碳酸钠溶液中逐滴滴入稀盐酸的微观示意图如下。由图可知向碳酸钠溶液中逐滴滴入稀盐酸时,实质是 依次与
依次与___________ 、___________ 发生反应(填微粒符号)。

回答下列问题:
(1)向碳酸钠饱和溶液中通入
 溶液变浑浊,反应的离子方程式为
溶液变浑浊,反应的离子方程式为(2)碳酸氢钠溶液与氢氧化钙溶液按溶质的物质的量之比为2∶1混合反应时,所得溶液中溶质为
(3)将27.4g
 和
和 的混合物,加热到质量不再变化时,得残留固体21.2g.则原混合物中
的混合物,加热到质量不再变化时,得残留固体21.2g.则原混合物中 和
和 的质量之比为
的质量之比为(4)向碳酸钠溶液中逐滴滴入稀盐酸的微观示意图如下。由图可知向碳酸钠溶液中逐滴滴入稀盐酸时,实质是
 依次与
依次与
您最近一年使用:0次
名校
解题方法
5 . 高锰酸钾是一种强氧化剂,具有很好的消炎、杀菌、抑菌的作用,因此临床上可以用于急性皮炎、湿疹、皮肤感染等疾病的治疗。
回答下列问题:
(1)某高锰酸钾外用片的部分使用说明及注意事项如下:
①高锰酸钾外用片可以治疗皮肤感染,是应用了高锰酸钾的___________ 性。
②高锰酸钾水溶液易变质的原因是___________ 。
③高锰酸钾外用片不可与碘化物接触或并用的原因是___________ 。
(2)将 溶液酸化可制得
溶液酸化可制得 ,同时生成
,同时生成 ,在此反应中氧化剂和还原剂的物质的量之比为
,在此反应中氧化剂和还原剂的物质的量之比为___________ ;当生成0.1mol还原产物时转移电子的数目为___________ 。
回答下列问题:
(1)某高锰酸钾外用片的部分使用说明及注意事项如下:
| 【注意事项】 1.本品仅供外用,切忌口服。 2.本品水溶液易变质,故使用前用温水配制,并立即使用。 【药品相互作用】 不可与碘化物、有机物接触或并用,尤其是晶体。 |
①高锰酸钾外用片可以治疗皮肤感染,是应用了高锰酸钾的
②高锰酸钾水溶液易变质的原因是
③高锰酸钾外用片不可与碘化物接触或并用的原因是
(2)将
 溶液酸化可制得
溶液酸化可制得 ,同时生成
,同时生成 ,在此反应中氧化剂和还原剂的物质的量之比为
,在此反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
名校
解题方法
6 . 离子反应是中学化学中重要的反应类型;离子方程式是用来表示离子反应的化学用语。
回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在___________(填标号)。
(2)从下列物质中选择合适反应物,按①~③的要求,各写出一个符合条件的离子方程式。
Na、Fe、 、
、 、HCl、
、HCl、 、NaOH、
、NaOH、 、
、 、
、
①只能表示一个具体的反应,不能代表同一类的离子反应:___________ 。
②不能表示为 的酸碱中和反应:
的酸碱中和反应:___________ 。
③难溶性的酸(碱或盐)不用画“↓”的离子反应:___________ 。
回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在___________(填标号)。
| A.单质 | B.化合物 | C.水 | D.电解质 |
Na、Fe、
 、
、 、HCl、
、HCl、 、NaOH、
、NaOH、 、
、 、
、
①只能表示一个具体的反应,不能代表同一类的离子反应:
②不能表示为
 的酸碱中和反应:
的酸碱中和反应:③难溶性的酸(碱或盐)不用画“↓”的离子反应:
您最近一年使用:0次
2022-12-17更新
|
190次组卷
|
2卷引用:山西省太原市外国语学校2021-2022学年高一上学期期中考试化学试题
名校
解题方法
7 . 下列有关物质鉴别的方法中错误的是
选项 | 物质 | 鉴别方法 |
A |
| 加入 |
B |
| 分别加入盐酸,观察是否有气泡 |
C |
| 分别加水溶解,观察溶液颜色 |
D | NaCl和 | 分别加入 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 关于容量瓶的使用及所配溶液的误差分析,下列描述正确的是
①容量瓶上标有温度、容积和刻度线
②若容量瓶中有少量蒸馏水,应烘干后使用
③配制好的溶液可用容量瓶长期贮存
④可用500mL容量瓶来配制250mL溶液
⑤未冷却到室温就将溶液转移到容量瓶并定容,使浓度偏高
⑥定容摇匀后,发现液面低于刻度线,又加水至凹液面与刻度线相切,使浓度偏低
①容量瓶上标有温度、容积和刻度线
②若容量瓶中有少量蒸馏水,应烘干后使用
③配制好的溶液可用容量瓶长期贮存
④可用500mL容量瓶来配制250mL溶液
⑤未冷却到室温就将溶液转移到容量瓶并定容,使浓度偏高
⑥定容摇匀后,发现液面低于刻度线,又加水至凹液面与刻度线相切,使浓度偏低
| A.①⑤⑥ | B.②③④ | C.③④⑤⑥ | D.①②③④⑤⑥ |
您最近一年使用:0次
9 . 下列有关含氯物质的叙述中错误的是
A. 具有氧化性,是一种新型的消毒剂 具有氧化性,是一种新型的消毒剂 |
| B.贮氯罐意外泄漏时,应沿逆风方向疏散群众 |
| C.新制氯水有氧化性,久置氯水无氧化性 |
D.漂白粉在空气中失效的原因是 与空气中的 与空气中的 和 和 发生反应 发生反应 |
您最近一年使用:0次
名校
10 . 按要求完成下列内容
(1)生产硫化钠大多采用无水芒硝(Na2SO4)-碳粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式:_______ 。
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2(已知HCN、HOCN中N元素的化合价相同)则反应的离子方程式:_______ 。
(3)FeO·Cr2O3+Na2CO3+NaNO3 Na2CrO4+Fe2O3+CO2+NaNO2;上述反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2;上述反应配平后FeO·Cr2O3与NaNO3的系数比为_______ 。该步骤不能使用陶瓷容器,原因是_______ 。
(4)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性,含VO2+、K+、SO 等。写出该反应的化学方程式:
等。写出该反应的化学方程式:_______ 。
(1)生产硫化钠大多采用无水芒硝(Na2SO4)-碳粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式:
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2(已知HCN、HOCN中N元素的化合价相同)则反应的离子方程式:
(3)FeO·Cr2O3+Na2CO3+NaNO3
 Na2CrO4+Fe2O3+CO2+NaNO2;上述反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2;上述反应配平后FeO·Cr2O3与NaNO3的系数比为(4)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性,含VO2+、K+、SO
 等。写出该反应的化学方程式:
等。写出该反应的化学方程式:
您最近一年使用:0次

 两种液体
两种液体 与
与 两种粉末
两种粉末 两种溶液
两种溶液 溶液,观察是否有沉淀
溶液,观察是否有沉淀

