1 . 分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机物有(不含立体异构)
| A.3种 | B.4种 | C.5种 | D.6种 |
您最近一年使用:0次
2023-07-10更新
|
1049次组卷
|
111卷引用:广西罗城仫佬族自治县高级中学2021-2022学年高二上学期开学检测化学试题
广西罗城仫佬族自治县高级中学2021-2022学年高二上学期开学检测化学试题广西河池市高级中学2021-2022学年高三上学期第三次月考化学试题宁夏平罗中学2020-2021学年高二上学期期末考试化学试题安徽省淮北市树人高级中学2020-2021学年高二下学期开学考试化学试题(已下线)3.4 羧酸 羧酸衍生物(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修3)(已下线)小题12 陌生有机化合物的组成、结构与性质 ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押全国卷理综第8题 有机化学基础(必考)-备战2021年高考化学临考题号押题(课标全国卷)河南省洛阳市2020-2021学年高一下学期期中考试化学试题新疆哈密第十五中学2020-2021学年高二下学期期中考试化学试题河南省安阳市洹北中学2020-2021学年高二下学期第一次月考化学试题(已下线)课时49 有机物同分异构体的判断-2022年高考化学一轮复习小题多维练(全国通用)河南省辉县市一中2020-2021学年高一下学期第二次阶段性考试化学试题黑龙江省大庆中学2022届高三上学期第一次月考化学试题上海市复旦大学附属中学青浦分校2022届高三化学测试(一)(已下线)专题28 甲烷、乙烯、苯、煤、石油、天然气的绿综合利用(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练黑龙江省实验中学2021-2022学年高三上学期第五次月考化学试题2015年全国普通高等学校招生统一考试化学(新课标II卷)2016届西藏拉萨中学高三上学期第二次月考化学试卷2016届福建省厦门市第六中学高三上学期期中测试化学试卷2016届湖南省郴州市高三第一次教学质量监测化学试卷2016届陕西省西安市长安区十中高三下学期第三次月考化学试卷2015-2016学年广东省深圳高中高二下期中化学试卷2015-2016学年青海师大附二中高二下期中化学试卷2015-2016学年江西省上饶市广丰一中高二下期中化学试卷2015-2016学年山西省太原五中高一下期末化学试卷2015-2016学年福建省师大附中高一下期末化学试卷2015-2016学年福建省福州一中高二下期末化学试卷2015-2016学年江西省丰城九中高二下学期期末考试化学试卷2015-2016学年黑龙江省哈尔滨六中高一下期末化学试卷2014-2015学年辽宁省锦州市高二下学期期末化学试卷2016-2017学年辽宁葫芦岛高级中学高二上期中化学卷2017届甘肃省定西市通渭县高三上学期期末化学试卷2017届广东省深圳市三校高三上学期第一次联考化学卷2017届上海市杨浦区高三上学期期末等级考质量调研(一模)化学试卷西藏自治区拉萨中学2016-2017学年高二第七次月考化学试题江西省南昌市八一中学、洪都中学、麻丘中学等七校2016-2017学年高一下学期期末考试化学试题河南省商丘市九校2016-2017学年高二下学期期末联考化学试题黑龙江省大庆中学2016-2017学年高二下学期期末考试化学试题辽宁省葫芦岛市第一高级中学2016-2017学年高二上学期期中考试化学试题黑龙江省大庆实验中学2018届高三上学期期中考试理科综合化学试题浙江省东阳中学2017-2018学年高二上学期期中考试化学试题内蒙古太仆寺旗宝昌一中2017-2018学年高二上学期期中考试化学试题2017-2018学年高一化学人教版必修2:第三章检测题云南省曲靖市2018届高三第一次复习统一检测理科综合化学试题河南省郑州市第一中学2018-2019学年高二上学期入学测试化学试题(已下线)解密15 乙醇、乙酸及基本营养物质——备战2018年高考化学之高频考点解密【全国百强校】重庆市西南大学附属中学校2018届高三第六次月考(3月)理科综合化学试题海南省儋州一中2018-2019学年高二下学期第一次月考化学试题湖南省邵阳市邵东县第一中学2018-2019学年高二(理)下学期第一次月考化学试题广东省深圳市科学高中2018-2019学年高二第二学期期中考试化学试题【校级联考】湖南省醴陵二中、醴陵四中2018-2019学年高二下学期期中联考化学试题山东省滨州市惠民县第二中学2018-2019学年高二5月份月考化学试题重庆市第三十中学2018-2019学年高二下学期期中考试化学试题江西省上饶市第二中学2018-2019学年高二下学期期中考试化学试题四川省遂宁市2018-2019学年高一下学期期末考试化学试题吉林省长春外国语学校2018-2019学年高一下学期期末考试(理)化学试题贵州省遵义航天高级中学2018届高三假期模拟考试理科综合化学试题上海市黄浦区晋元高级中学2018学年高二(下)期末等级考化学试题青海省海东市第二中学2019-2020学年高二上学期期中考试化学试题云南省景东彝族自治县第一中学2019-2020学年高二上学期第一次月考化学试题山西省朔州市怀仁县第一中学2018-2019学年高二下学期第二次月考化学试题湖南省株洲市2019-2020学年高二上学期期中考试化学试题江西省新余市第四中学2020届高三第八次训练理科综合化学试题辽宁省本溪高级中学2019-2020学年高二9月月考化学试题贵州省六盘水市红果镇育才中学2020届高三第五次月考理综化学试题上海市控江中学2016-2017学年高二下学期期中考试化学试题陕西省渭南市渭南中学2020届高三第二次模拟考试化学试题江西省南昌三中2020届高三考前第二次适应性检测理综化学试题内蒙古阿拉善盟2020届高三上学期月考化学试题河南省洛阳市宜阳一高2019-2020学年高一下学期入学考试(尖子班)化学试题安徽省芜湖市第一中学2020届高三5月模拟理综化学试题河北省张家口市尚义县第一中学2019-2020学年高二下学期期中考试化学试题宁夏海原县第一中学2019-2020学年高二下学期期末考试化学试题内蒙古集宁一中(西校区)2019-2020学年高二下学期期末考试化学试题黑龙江省大庆市第四中学2020届高三下学期第四次检测理综化学试题黑龙江省鸡西市鸡东县第二中学2019-2020学年高一下学期期末考试化学试题黑龙江省双鸭山市第一中学2020-2021学年高二上学期开学考试化学试题云南省昆明市官渡区第一中学2019-2020学年高二上学期期末考试化学试题山东省菏泽市单县第五中学2020-2021学年高二上学期开学考试化学试题甘肃省平凉市庄浪县第一中学2021届高三上学期第一次模拟化学试题高一必修第二册(人教2019版)第七章 有机化合物 素养检测陕西省西安市远东第一中学2018-2019学年高一下学期第二次月考化学试题福建省龙岩市武平县第一中学2020-2021学年高二上学期10月月考化学试题宁夏回族自治区银川市长庆高级中学2021届高三上学期第一次月考化学试题广西钦州市第四中学2020-2021学年高二10月月考化学试题广西桂林市逸仙中学2020-2021学年高二上学期期中考试化学(理)试题吉林省大安市第六中学2019-2020学年高二下学期期末考试化学(理)试题陕西省宝鸡市渭滨高中2021届高三上学期第一次月考化学试题甘肃省白银市第十中学2019-2020学年高二下学期第一次月考化学试题(已下线)【镇江新东方】高二上第二次月考辽宁省庄河市高级中学2016-2017学年高二下学期期中考试化学试题浙江省诸暨市2017-2018学年高二上学期期末考试化学试题 (已下线)押全国卷理综第8题 有机化学基础(选择题)-备战2022年高考化学临考题号押题(课标全国卷)江苏省海州高级中学2021-2022学年高二下学期期中考试化学试题湖北省部分市州2021-2022学年高一下学期7月联合期末调研考试化学试题内蒙古赤峰市2021-2022学年高二下学期期末考试化学试题(已下线)第17练 用有序思维突破同分异构体的书写及数目判断-2022年【暑假分层作业】高二化学(2023届一轮复习通用)辽宁省抚顺市六校协作体2021-2022学年高一下学期期末考试化学试题(已下线)第54练 羧酸与羧酸衍生物-2023年高考化学一轮复习小题多维练(全国通用)广东省江门市新会陈经纶中学2020-2021学年高二上学期期中考试化学(选择考)试题重庆市万州第二高级中学2022-2023学年高二上学期1月月考化学试题(已下线)专题31 同分异构体的书写及数目判断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题19 有机选择题题型分析黑龙江省齐齐哈尔市八校联考2022-2023学年高一下学期期末考试化学试题福建省福州第一中学2022-2023学年高二下学期期末考试化学试题2.4.1羧酸(课前)-鲁科版选择性必修3(已下线)考点32 共线共面 同分异构体(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)四川省双流中学2023-2024学年高二上学期10月月考化学试题章末知识整合23.4.1羧酸 随堂练习(已下线)专题04 认识有机化合物 乙烯与有机高分子材料-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
2 . 根据SO2通入不同溶液中的实验现象,所得结论不正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-07更新
|
1609次组卷
|
108卷引用:广西河池市高级中学2021-2022学年高三上学期第三次月考化学试题
广西河池市高级中学2021-2022学年高三上学期第三次月考化学试题吉林省长春市第二十九中学2021届高三上学期期末考试化学试题专题4 第一单元综合拔高练-高中化学苏教2019版必修第一册河北省深州市长江中学2020-2021学年高一下学期3月底月考化学试题新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题广东实验中学2020-201学年高一下学期期中考试化学(合格考)试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(A)试题(已下线)课时22 硫及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第11讲 硫及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第7周 晚练题-备战2022年高考化学周测与晚练(新高考专用)安徽省马鞍山市含山县第二中学2021-2022学年高三上学期第一次月考化学试题黑龙江省哈尔滨市第十九中学2021-2022学年高三上学期第一次月考化学试题云南省红河县第一中学2020-2021学年高一下学期期末考试化学试题广东省广州市广东实验中学2020-2021学年高一下学期期中考试(合格考)化学试题山东省淄博市淄川中学2016-2017学年高二下学期学分认定(期末)考试化学试题河北省安平中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)河北省涞水波峰中学2018届高三第一次调研考试化学试题江西省横峰中学、铅山一中、德兴一中2018届高三上学期第一次月考化学试题宁夏六盘山高级中学2018届高三上学期第一次月考化学试题山东省郓城实验中学2018届高三10月月考化学试题江西省铅山县第一中学2018届高三上学期第一次月考化学试题黑龙江省哈尔滨市第六中学2018届高三12月月考化学试题辽宁省大连渤海高级中学2018届高三上学期期末考试化学试题云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题内蒙古北方重工业集团有限公司第三中学2017-2018学年高一3月月考化学试题(已下线)《考前20天终极攻略》-5月21日 基础实验(已下线)《考前20天终极攻略》-5月26日 元素及其化合物(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密【全国市级联考】四川省广安市2017-2018学年高一下学期期末考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氧及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】【全国百强校】北京市中央民族大学附属中学(朝阳分校)2019届高三上学期10月月考化学试题【全国百强校】宁夏回族自治区育才中学2019届高三上学期月考(二)化学试题云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题【全国百强校】山东省济南市第一中学2019届高三上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第3讲 硫及其化合物 (教学案)【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期12月月考化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第1讲 碳、硅及无机非金属材料 (教学案)山东省德州市夏津县第一中学2019届高三上学期12月月考化学试题(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(教学案)(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(押题专练)(已下线)2019高考备考二轮复习精品资料-专题5 金属及其化合物(教学案)(已下线)2019年高考总复习巅峰冲刺-专题08 常见无机物及其应用应试策略河南省封丘县第一中学2018-2019学年高一下学期开学考试化学试题步步为赢 高二化学暑假作业:作业十三 化学实验综合内蒙古包头稀土高新区二中2020届高三10月月考理综化学试题四川省绵阳市南山中学2020届高三10月月考化学试题四川省成都石室中学2019-2020学年高二入学考试化学试题北京师范大学实验中学丰台学校2019-2020学年高三上学期期中考试化学试题2020届高三化学一轮复习 化学基础实验(选择题和大题训练)四川省成都市实验中学2020届高三上学期第十四次周考理科综合化学试题(已下线)专题01 硫及其化合物(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题广东省深圳中学2020年高中毕业班教学质量监测卷理科综合化学试题河北省衡水中学2020年高中毕业班教学质量监测卷理科综合化学试题辽宁省沈阳东北育才中学2020年高中毕业班教学质量监测卷理科综合化学试题山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题安徽省黄山市八校联盟2019-2020学年高一下学期期中联考化学试题(已下线)专题4.3 硫及其化合物(练)——2020年高考化学一轮复习讲练测(已下线)专题4.3 硫及其化合物(讲)——2020年高考化学一轮复习讲练测云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第二次综合测试化学试题黑龙江省大庆市第十中学2019-2020学年高二下学期期末考试化学试题四川省泸县第二中学2019-2020学年高一下学期期末模拟考试化学试题苏教版(2020)高一必修第一册专题4 总结检测(已下线)第15讲 硫及其化合物(精讲)——2021年高考化学一轮复习讲练测安徽省阜阳市阜南实验中学2020届高三下学期4月月考化学试题山东省济南市章丘区第四中学2021届高三上学期第一次教学质量检测(8月)化学试题黑龙江省哈尔滨市第三中学校2020-2021学年高三上学期第一次验收考试化学试题湖北省宜昌市葛洲坝中学2021届高三9月月考化学试题陕西省西安中学2018-2019学年高一下学期期末考试化学题湖南省邵阳市邵东县创新实验学校2021届高三上学期第一次月考化学试题(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(精练)-2021年高考化学一轮复习讲练测福建省莆田第二十五中学2021届高三上学期期中考试化学试题江西省鹰潭市2019-2020年度高一下学期期末检测化学试题辽宁沈阳市第二十八中学2020--2021学年高一上学期期末考试化学试题重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)北京市顺义牛栏山第一中学2021-2022学年高一下学期居家学习成果展示化学测试题北京师范大学附属中学2021-2022学年高一下学期期中考试化学试题(已下线)第11讲 硫及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)甘肃省武威第十八中学2022-2023学年高三上学期第一次诊断化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期第一次验收考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期9月月考化学试题辽宁省本溪满族自治县高级中学2021-2022学年高一下学期开学考试化学试题(已下线)化学(北京A卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)题型48 SO2的制备与性质探究北京市顺义区第一中学2022-2023学年高一下学期3月月考化学试题宁夏银川市第二中学2022-2023学年高一下学期第一次月考化学试题山东省济宁市曲阜孔子高级中学2022-2023学年高一下学期4月月考化学试题黑龙江省齐齐哈尔市第八中学校2022-2023学年高一下学期3月月考化学试题广东省开平市忠源纪念中学2022-2023学年高一下学期4月期中考试化学试题广东省东莞市东华高级中学2022-2023学年高一下学期3月月考化学试题广东省深圳聚龙科学中学2022-2023学年高一下学期第一次段考(学业水平)化学试题(已下线)第3讲 硫及其重要化合物北京市第二中学2022-2023学年高一下学期期末考试化学试题黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题江苏省南菁高级中学2023-2024学年高一上学期9月阶段性检测化学(创优班)试题北京师范大学第二附属中学2023-2024学年高一下学期3月化学测试题陕西省咸阳市三原县北城中学2023-2024学年高一下学期第一次月考化学试题(已下线)专题01 硫、氮及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
3 . 下列由废铜屑制取 的实验原理与装置能达到实验目的的是
的实验原理与装置能达到实验目的的是

 的实验原理与装置能达到实验目的的是
的实验原理与装置能达到实验目的的是
| A.用装置甲除去废铜屑表面的油脂 |
| B.用装置乙溶解废铜屑 |
C.用装置丙过滤得到 溶液 溶液 |
D.用装置丁蒸干溶液获得 |
您最近一年使用:0次
2023-05-29更新
|
1122次组卷
|
28卷引用:广西河池市高级中学2021-2022学年高三上学期第二次月考化学试题
广西河池市高级中学2021-2022学年高三上学期第二次月考化学试题2021年新高考江苏化学高考真题江苏省沭阳县修远中学2022届高三上学期第一次阶段考试化学试题(已下线)2020年天津卷化学高考真题变式题1-12(已下线)秘籍04 实验仪器使用与基本操作-备战2022年高考化学抢分秘籍(全国通用)(已下线)押江苏卷第3题 化学实验基础知识和技能 -备战2022年高考化学临考题号押题(江苏卷)(已下线)专题11 基本实验专练北京市和平街第一中学2021-2022学年高三下学期保温化学试题江苏省常熟市2021-2022学年高二下学期期中考试化学试题(已下线)易错点32 物质的分离、提纯与检验-备战2023年高考化学考试易错题福建省厦门集美中学2022-2023学年高三上学期期中考试化学试题天津市第一中学2022-2023学年高三上学期第二次月考化学试题天津市咸水沽第一中学2022-2023学年高三上学期线上期末考试化学试题天津市第十四中学2022-2023学年高三上学期期末考试化学试题(已下线)专题23 化学实验基础性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型166 物质制备中涉及的仪器选择与使用(已下线)专题13 化学实验基础(已下线)专题13 化学实验基础广东省华南师范大学附属中学2023届高三下学期第三次模拟考试化学试题(已下线)考点12 金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省广州市白云中学2023-2024学年高三上学期期中考试化学试题江苏省扬州大学附属中学2023-2024学年高二上学期12月月考化学试题福建省漳州市华安县第一中学2023-2024学年高三上学期12月月考化学试题黑龙江省齐齐哈尔市第八中学校2024届高三1月大联考考后强化卷化学试题2024届四川省成都市成华区某校高三上学期一诊模拟考试理综试题湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题(已下线)热点07 常见化学实验仪器与基本操作
名校
4 . 已知①②两种物质的结构简式如图所示,下列说法正确的是
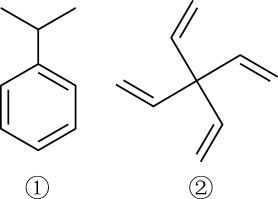

| A.①②两种物质的分子式均为C9H11 |
| B.②的一氯代物只有2种 |
| C.①和②分子中所有碳原子均可处于同一平面上 |
| D.①和②都能使Br2的CCl4溶液或酸性KMnO4溶液褪色 |
您最近一年使用:0次
2022-12-18更新
|
265次组卷
|
4卷引用:广西河池市2021届高三上学期期末教学质量检测理科综合化学试题
广西河池市2021届高三上学期期末教学质量检测理科综合化学试题(已下线)难点1 有机物分子中的共线共面问题-2021年高考化学【热点·重点·难点】专练(山东专用)广西百色民族高级中学2021-2022学年高二上学期9月月考化学试题湖北省襄阳市第一中学2022-2023学年高二上学期1月期末考试化学试题
名校
解题方法
5 . 可逆反应 在不同条件下的反应速率如下,其中反应速率最快的是
在不同条件下的反应速率如下,其中反应速率最快的是
 在不同条件下的反应速率如下,其中反应速率最快的是
在不同条件下的反应速率如下,其中反应速率最快的是A.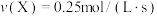 | B.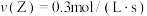 |
C. | D.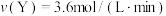 |
您最近一年使用:0次
2022-12-05更新
|
551次组卷
|
27卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
广西河池市2020-2021学年高二上学期期末教学质量检测化学试题广西来宾市2020-2021学年高二上学期期末教学质量检测化学试题河北省衡水市第十四中学2020-2021学年高二下学期摸底考试化学试题辽宁省阜新市第二高级中学2020-2021学年高二下学期第一次月考化学试题湖北省黄冈市麻城市麻城二中2020-2021学年高一下学期期中考试化学试题吉林省“BEST合作体”2020-2021学年高一下学期期中化学试题河南省周口市中英文学校2020-2021学年高一下学期期中考试化学试题四川省雅安中学2020-2021学年高一下学期期中考试化学试题湖北省华中师范大学潜江附属中学2020-2021学年高一下学期5月月考化学试题江苏省宿迁市2020-2021学年高一下学期期末考试化学试题吉林省长春市2020-2021学年高一下学期期末联考化学试题贵州省平塘民族中学2021-2022学年高二上学期第一次月考化学试题江苏省苏州市相城区陆慕高级中学2021-2022学年高二上学期第一次月考化学试题新疆生产建设兵团第二师八一中学2021-2022学年高二上学期期中考试化学试题陕西省神木中学2021-2022学年高二上学期第一次月考化学试题黑龙江省齐齐哈尔市恒昌中学校2021-2022学年高一下学期期中考试化学试题黑龙江省大庆市大庆中学2021-2022学年高一下学期期中考试化学试题辽宁省营口市普通高中2021-2022学年高一下学期期末化学试题吉林省长春市农安县2021-2022学年高一下学期期末考试化学试题河北省元氏县第四中学2022-2023学年高二上学期开学考试化学试卷河南省南乐县第一高级中学2022-2023学年高二上学期第二次月考化学试题河北省邯郸市大名县第一中学2022-2023学年高一下学期3月月考化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高一下学期5月期中考试化学试题江苏省常熟中学2023-2024学年高二上学期10月阶段性学业水平调研化学试题江苏省苏州市常熟中学2023-2024学年高二上学期10月月考化学试题湖南省邵东市第三中学2022-2023学年高一下学期期末考试化学试题(已下线)重难点01 化学反应速率的计算及平衡图像分析-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
名校
解题方法
6 . 已知 某烃M完全燃烧可得到
某烃M完全燃烧可得到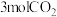 ;在一定条件下,
;在一定条件下,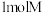 能与
能与 完全加成生成化合物N。下列说法正确的是
完全加成生成化合物N。下列说法正确的是
 某烃M完全燃烧可得到
某烃M完全燃烧可得到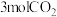 ;在一定条件下,
;在一定条件下,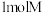 能与
能与 完全加成生成化合物N。下列说法正确的是
完全加成生成化合物N。下列说法正确的是| A.烃M为2-甲基丙烯 |
B.实验室制取烃M的化学方程式为 |
| C.化合物N可发生聚合反应 |
D.化合物N上的氢原子可被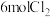 完全取代 完全取代 |
您最近一年使用:0次
2022-04-29更新
|
261次组卷
|
7卷引用:广西罗城仫佬族自治县高级中学2021-2022学年高二上学期开学检测化学试题
广西罗城仫佬族自治县高级中学2021-2022学年高二上学期开学检测化学试题陕西省西安市长安区第一中学2020-2021学年高二上学期期末考试化学(理)试题(已下线)专题一 脂肪烃-2020-2021学年高二《新题速递·化学》(人教版选修5)3月刊 (同步课堂必刷题)(已下线)第2章 烃(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修3)湖北省部分示范高中六校联考2021-2022学年高二下学期期中考试化学试题广东省深圳市光明区高级中学2021-2022学年高二下学期期中考试化学试题黑龙江省绥化市绥棱县第一中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
7 . 一种以辉铜矿(主要成分为Cu2S,含少量SiO2)为原料制备硝酸铜晶体的工艺流程如图所示:

(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:___________ 。
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减少,有研究指出CuCl2是该反应的催化剂,该过程的反应原理可用化学方程式表示为:①Cu2S+2CuCl2=4CuCl+S; ②___________
(3)向滤液M中加入(或通入)___________ (填字母), 所得物质可循环利用。
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(4)“保温除铁”过程中,加入CuO的目的是___________ ;向浓缩池中加入适量HNO3的作用是___________ ;操作1是___________ 。

(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减少,有研究指出CuCl2是该反应的催化剂,该过程的反应原理可用化学方程式表示为:①Cu2S+2CuCl2=4CuCl+S; ②
(3)向滤液M中加入(或通入)
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(4)“保温除铁”过程中,加入CuO的目的是
您最近一年使用:0次
名校
解题方法
8 . 以芳香族化合物A和化合物D为原料制备化合物M的合成路线如下:
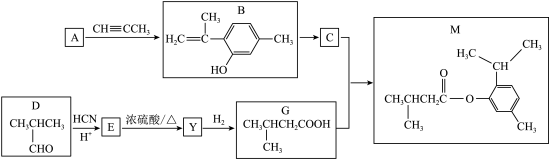
已知:① A→B符合原子经济学原理;
②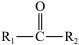

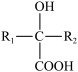 (R1、 R2表示氯原子或烃基)。
(R1、 R2表示氯原子或烃基)。
回答下列问题:
(1)D的化学名称为___________ ;
(2)B→C、 E →Y的反应类型分别为__________ 、___________ 。
(3)A的结构简式为___________ 。
(4)C与G生成M的化学方程式为___________ 。
(5)同时满足下列条件的B的同分异构体有___________ 种(不考虑立体异构),其中核磁共振氢谱图显示有五种不同化学环境的氢,且峰面积比为6:2:2:1:1的结构简式为___________ ;
①苯环上连有两个取代基
②能发生银镜反应
(6)设计由乙烯制备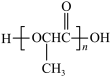 的合成路线 (无机试剂任选)。
的合成路线 (无机试剂任选)。___________

已知:① A→B符合原子经济学原理;
②


 (R1、 R2表示氯原子或烃基)。
(R1、 R2表示氯原子或烃基)。回答下列问题:
(1)D的化学名称为
(2)B→C、 E →Y的反应类型分别为
(3)A的结构简式为
(4)C与G生成M的化学方程式为
(5)同时满足下列条件的B的同分异构体有
①苯环上连有两个取代基
②能发生银镜反应
(6)设计由乙烯制备
 的合成路线 (无机试剂任选)。
的合成路线 (无机试剂任选)。
您最近一年使用:0次
2022-03-03更新
|
156次组卷
|
4卷引用:广西河池市高级中学2021-2022学年高三上学期第二次月考化学试题
名校
解题方法
9 . 钛(Ti)及其化合物的应用研究是目前前沿科学之一,请回答下列问题;
(1)基态钛原子的电子排布式为___________ ,核外电子占据的轨道数为___________ 。
(2)与钛位于同一周期且基态原子不成对电子与钛相同的元素,第一电离能由大到小的顺序为___________ (用元素符号填空)。
(3)TiCl4常温下为无色液体,熔点250K,沸点409K,则TiCl4属于___________ 晶体。 TiCl4在水中或空气中极易水解,露置于空气中形成白色烟雾,烟雾中的固体成分可用TiO2·nH2O表示,请写出TiCl4在空气中产生烟雾的化学方程式:___________ 。
(4)TiO2作光催化剂可将甲醛、苯等有害气体转化为CO2和H2O。
①上述含碳原子的分子中,碳原子的杂化方式为sp2的是___________ (填名称)
②下列各组微粒互为等电子体的是___________ (填字母标号)。
A. H2O与SO2 B. CO2与N2O C. CH2O与BF3 D. C6H6与B3N3H6
(5)金红石(TiO2)的晶胞结构如图所示,设NA为阿伏加德罗常数的值,则该晶体的密度为___________ g·cm-3(用含相关字母和符号的代数式表示)。

(1)基态钛原子的电子排布式为
(2)与钛位于同一周期且基态原子不成对电子与钛相同的元素,第一电离能由大到小的顺序为
(3)TiCl4常温下为无色液体,熔点250K,沸点409K,则TiCl4属于
(4)TiO2作光催化剂可将甲醛、苯等有害气体转化为CO2和H2O。
①上述含碳原子的分子中,碳原子的杂化方式为sp2的是
②下列各组微粒互为等电子体的是
A. H2O与SO2 B. CO2与N2O C. CH2O与BF3 D. C6H6与B3N3H6
(5)金红石(TiO2)的晶胞结构如图所示,设NA为阿伏加德罗常数的值,则该晶体的密度为

您最近一年使用:0次
名校
解题方法
10 . H2S广泛存在于废水及天然气等燃气中,除去H2S是利国利民之举。回答下列问题;
(1)已知; H2(g)+Cl2(g) 2HCl(g) ΔH1
2HCl(g) ΔH1
H2(g)+S(s) H2S(g) ΔH2
H2S(g) ΔH2
HCl(g) HCl(aq) ΔH3
HCl(aq) ΔH3
H2S(g) H2S(aq) ΔH4
H2S(aq) ΔH4
用氯气除去废水中H2S的热化学方程式为___________ (反应热用ΔH1、ΔH2、ΔH3和ΔH4表示)。
(2)H2S可用于高效制取氢气,发生的反应为2H2S(g) 2H2(g)+S2(g) ΔH
2H2(g)+S2(g) ΔH
在两个恒容密闭容器中充入H2S(如上表),容器I、II中H2S的平衡转化率如图a所示;
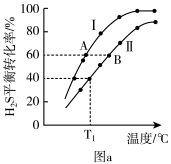
①该反应的ΔH___________ 0(填“> ”或“<”);
②在T1°C,容器II的体积为6L,该反应20s后达到平衡,则0~20s内容器II中生成S2(g)的反应速率为___________ mol·L-1·min-1;
(3)现改变条件进行(2)中反应;开始时,将lmol H2S与8mol Ne(g)混合于恒压(总压为p kPa)密闭容器中反应,测得平衡时H2S的平衡转化率为α,则S2(g)的平衡分压为___________ (分压=总压×体积分数)。
(4)H2S燃料电池应用前景非常广阔,该电池示意图如图b所示,
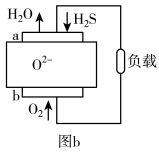
①电极b是___________ 极(填“正”或“负”);
②电极a的反应式为___________ 。
(1)已知; H2(g)+Cl2(g)
 2HCl(g) ΔH1
2HCl(g) ΔH1H2(g)+S(s)
 H2S(g) ΔH2
H2S(g) ΔH2HCl(g)
 HCl(aq) ΔH3
HCl(aq) ΔH3H2S(g)
 H2S(aq) ΔH4
H2S(aq) ΔH4用氯气除去废水中H2S的热化学方程式为
(2)H2S可用于高效制取氢气,发生的反应为2H2S(g)
 2H2(g)+S2(g) ΔH
2H2(g)+S2(g) ΔH| 容器编号 | 起始物质的量/mol | ||
| H2S | H2 | S2 | |
| I | 0.1 | 0 | 0 |
| II | 0.1 | 0 | 0 |

①该反应的ΔH
②在T1°C,容器II的体积为6L,该反应20s后达到平衡,则0~20s内容器II中生成S2(g)的反应速率为
(3)现改变条件进行(2)中反应;开始时,将lmol H2S与8mol Ne(g)混合于恒压(总压为p kPa)密闭容器中反应,测得平衡时H2S的平衡转化率为α,则S2(g)的平衡分压为
(4)H2S燃料电池应用前景非常广阔,该电池示意图如图b所示,

①电极b是
②电极a的反应式为
您最近一年使用:0次



