1 . 亚硫酸钠( )是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究
)是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究 的性质,进行了如下实验。
的性质,进行了如下实验。
【性质预测】
(1) 中硫元素的化合价是
中硫元素的化合价是_______ 价,属于S元素的中间价态,既具有氧化性,又具有还原性。
【实验验证】
资料:酸性条件下, 被还原为
被还原为 。
。
【分析解释】
(2)实验i中,反应的离子方程式是_______ 。
【继续探究】
(3)甲同学认为实验ii的现象不能直接得出“ 具有氧化性”。
具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设a:酸性溶液中的 具有氧化性,可产生S;
具有氧化性,可产生S;
假设b:空气中存在 ,在酸性条件下,由于
,在酸性条件下,由于_______ (用离子方程式表示),可产生S;
假设c:酸性溶液中的 具有氧化性,可产生S。
具有氧化性,可产生S。
②设计实验iii证实了假设a和b不是产生S的主要原因。
实验iii:向 溶液中加入
溶液中加入_______ (填试剂名称),产生有臭鸡蛋气味的气体,溶液未变浑浊。
(4)结合实验ii和iii,用离子方程式解释实验ii中产生淡黄色浑浊的原因:_______ 。
 )是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究
)是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究 的性质,进行了如下实验。
的性质,进行了如下实验。【性质预测】
(1)
 中硫元素的化合价是
中硫元素的化合价是【实验验证】
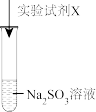 | 实验序号 | 实验试剂X | 实验现象 |
| i |  溶液、稀硫酸 溶液、稀硫酸 | 紫色褪去 | |
| ii |  溶液、稀硫酸 溶液、稀硫酸 | 加入 溶液,无明显现象;再加入稀硫酸,产生淡黄色浑浊 溶液,无明显现象;再加入稀硫酸,产生淡黄色浑浊 |
资料:酸性条件下,
 被还原为
被还原为 。
。【分析解释】
(2)实验i中,反应的离子方程式是
【继续探究】
(3)甲同学认为实验ii的现象不能直接得出“
 具有氧化性”。
具有氧化性”。①对淡黄色浑浊产生的原因作出如下假设:
假设a:酸性溶液中的
 具有氧化性,可产生S;
具有氧化性,可产生S;假设b:空气中存在
 ,在酸性条件下,由于
,在酸性条件下,由于假设c:酸性溶液中的
 具有氧化性,可产生S。
具有氧化性,可产生S。②设计实验iii证实了假设a和b不是产生S的主要原因。
实验iii:向
 溶液中加入
溶液中加入(4)结合实验ii和iii,用离子方程式解释实验ii中产生淡黄色浑浊的原因:
您最近一年使用:0次
名校
解题方法
2 . 某研究小组欲探究 能否与
能否与 溶液反应。
溶液反应。
【查阅资料】
i. 具有较强的还原性,
具有较强的还原性, 具有较强的氧化性。
具有较强的氧化性。
ii. 遇
遇 可生成
可生成 ,
, 溶液呈血红色,可用于
溶液呈血红色,可用于 的检验。
的检验。
【提出猜想】
(1)小组同学经过讨论后,认为 溶液可以与
溶液可以与 溶液反应,请从化合价的角度加以解释:
溶液反应,请从化合价的角度加以解释:___________ 。
【设计实验】
(2)实验I:在试管中加入 溶液和
溶液和 溶液,再加入
溶液,再加入 溶液,发现溶液
溶液,发现溶液_____ ,小组同学认为 和
和 溶液反应生成了
溶液反应生成了 。
。
(3)甲同学注意到盛放 溶液的试剂瓶中有空气,因此不同意该结论,他的理由是
溶液的试剂瓶中有空气,因此不同意该结论,他的理由是______ 。
重新设计实验:
实验II:在试管中加入 溶液,然后加入
溶液,然后加入 溶液,发现溶液无明显变化,再加入
溶液,发现溶液无明显变化,再加入 溶液,发现溶液变红。
溶液,发现溶液变红。
【获得结论】
(4)过氧化氢___________ (填“能”或者“不能”)氧化 。
。
【发现异常】
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将 氧化为
氧化为 。乙同学设计实验III并证实了该资料中的说法。
。乙同学设计实验III并证实了该资料中的说法。
(5)补全实验III的方案:在试管中加入 溶液,加入
溶液,加入 溶液,再加入
溶液,再加入___________ ,产生___________ 。
【总结反思】
(6)小组同学经过讨论后,提出了 的检验方法:取待测液于试管中,
的检验方法:取待测液于试管中,___________ ,证明待测液含有 。
。
(7)从上述实验中可以得出结论,在物质性质的检验中,应注意___________ (至少写出两条)对实验结果的影响。
 能否与
能否与 溶液反应。
溶液反应。【查阅资料】
i.
 具有较强的还原性,
具有较强的还原性, 具有较强的氧化性。
具有较强的氧化性。ii.
 遇
遇 可生成
可生成 ,
, 溶液呈血红色,可用于
溶液呈血红色,可用于 的检验。
的检验。【提出猜想】
(1)小组同学经过讨论后,认为
 溶液可以与
溶液可以与 溶液反应,请从化合价的角度加以解释:
溶液反应,请从化合价的角度加以解释:【设计实验】
(2)实验I:在试管中加入
 溶液和
溶液和 溶液,再加入
溶液,再加入 溶液,发现溶液
溶液,发现溶液 和
和 溶液反应生成了
溶液反应生成了 。
。(3)甲同学注意到盛放
 溶液的试剂瓶中有空气,因此不同意该结论,他的理由是
溶液的试剂瓶中有空气,因此不同意该结论,他的理由是重新设计实验:
实验II:在试管中加入
 溶液,然后加入
溶液,然后加入 溶液,发现溶液无明显变化,再加入
溶液,发现溶液无明显变化,再加入 溶液,发现溶液变红。
溶液,发现溶液变红。【获得结论】
(4)过氧化氢
 。
。【发现异常】
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将
 氧化为
氧化为 。乙同学设计实验III并证实了该资料中的说法。
。乙同学设计实验III并证实了该资料中的说法。(5)补全实验III的方案:在试管中加入
 溶液,加入
溶液,加入 溶液,再加入
溶液,再加入【总结反思】
(6)小组同学经过讨论后,提出了
 的检验方法:取待测液于试管中,
的检验方法:取待测液于试管中, 。
。(7)从上述实验中可以得出结论,在物质性质的检验中,应注意
您最近一年使用:0次
2021-11-07更新
|
1003次组卷
|
4卷引用:河南省安阳市第一中学2022-2023学年高一上学期12月月考化学试题
3 . 亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。某化学兴趣小组设计实验制备NaNO2并探究其性质。
查阅资料信息:①2NO+Na2O2 =2NaNO2;2NO2 +Na2O2=2NaNO3.
②酸性KMnO4溶液可将低价氮的氧化物或酸根离子氧化为 。
。
(1)NaNO2的制备(夹持装置和加热装置均已略,已检查装置气密性)。
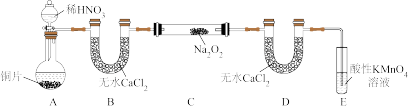
①若没有装置B,则装置C中Na2O2与水发生反应:_______ (填化学方程式)。
②制得的NaNO2固体中混有的杂质主要为NaNO3,改进措施是在装置A、B间添加_______ ,提高NaNO2的纯度。
③装置E中发生的主要反应的离子方程式为_______ 。
(2)验证亚硝酸钠与70%硫酸反应的气体产物为NO和NO2的混合气体。
已知:FeSO4溶液可吸收NO;NO2的沸点为21° C ,熔点为-11° C 。
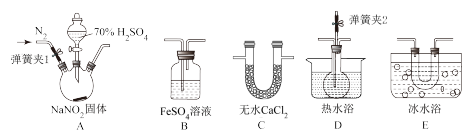
①为了检验装置A中生成的气体产物,装置的连接顺序是A→_______ 。(按气流方向从左到右)
②反应前应打开弹簧夹1, 先通入一段时间氮气,目的是_______ 。
③再关闭弹簧夹1,打开分液漏斗活塞,滴入70%硫酸后,装置A中产生红棕色气体。
设计实验检验装置A中产生的气体含有NO的操作及现象:_______ 。
(3)查阅资料知:酸性条件下NaNO2具有氧化性。利用所供试剂,设计实验方案验证此信息:_______ (供选用的试剂有NaNO2溶液、FeSO4溶液、稀硫酸、KSCN溶液)
(4)测定某亚硝酸钠样品的纯度。
设该样品的杂质均不与酸性KMnO4溶液反应,可用酸性KMnO4溶液测定NaNO2的含量。称取2.0 g亚硝酸钠样品溶于水配成250 mL溶液,取出25. 00 mL溶液于锥形瓶中,再用0. 1000 mol· L-1的酸性KMnO4标准溶液进行滴定,消耗酸性KMnO4标准溶液的体积如表:
该亚硝酸钠样品中NaNO2的质量分数为_______ 。
查阅资料信息:①2NO+Na2O2 =2NaNO2;2NO2 +Na2O2=2NaNO3.
②酸性KMnO4溶液可将低价氮的氧化物或酸根离子氧化为
 。
。(1)NaNO2的制备(夹持装置和加热装置均已略,已检查装置气密性)。

①若没有装置B,则装置C中Na2O2与水发生反应:
②制得的NaNO2固体中混有的杂质主要为NaNO3,改进措施是在装置A、B间添加
③装置E中发生的主要反应的离子方程式为
(2)验证亚硝酸钠与70%硫酸反应的气体产物为NO和NO2的混合气体。
已知:FeSO4溶液可吸收NO;NO2的沸点为21° C ,熔点为-11° C 。

①为了检验装置A中生成的气体产物,装置的连接顺序是A→
②反应前应打开弹簧夹1, 先通入一段时间氮气,目的是
③再关闭弹簧夹1,打开分液漏斗活塞,滴入70%硫酸后,装置A中产生红棕色气体。
设计实验检验装置A中产生的气体含有NO的操作及现象:
(3)查阅资料知:酸性条件下NaNO2具有氧化性。利用所供试剂,设计实验方案验证此信息:
(4)测定某亚硝酸钠样品的纯度。
设该样品的杂质均不与酸性KMnO4溶液反应,可用酸性KMnO4溶液测定NaNO2的含量。称取2.0 g亚硝酸钠样品溶于水配成250 mL溶液,取出25. 00 mL溶液于锥形瓶中,再用0. 1000 mol· L-1的酸性KMnO4标准溶液进行滴定,消耗酸性KMnO4标准溶液的体积如表:
| 实验组 | 第一组 | 第二组 | 第三组 | 第四组 |
| 消耗酸性KMnO4标准溶液的体积/mL | 9.97 | 10.02 | 12. 01 | 10. 01 |
您最近一年使用:0次
2022-05-27更新
|
396次组卷
|
5卷引用:河南省2022届高三下学期仿真模拟大联考理科综合化学试题
河南省2022届高三下学期仿真模拟大联考理科综合化学试题河北省秦皇岛市2022届高三三模化学试题(已下线)专题16 化学实验综合题-2022年高考真题模拟题分项汇编(已下线)新疆博乐高级中学2022届高三第一次诊断性测试理科综合化学试卷广东省部分学校2022届高三下学期高考冲刺化学试题
名校
解题方法
4 . 山大附中化学实验兴趣小组制备高铁酸钾(K2FeO4)并探究其性质和纯度分析。
资料:K2FeO4为紫色固体,微溶于KOH溶液,热稳定性差,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
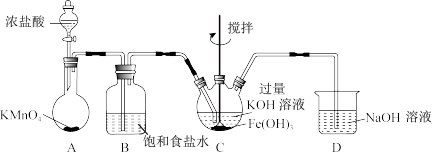
①A为氯气发生装置。A中反应离子方程式是___________ 。
②仪器C的名称为___________ 。反应时C的控温20~25℃,温度不能高于25℃的主要原因___________ 。C中得到紫色固体和溶液。写出C中反应生成K2FeO4的化学方程式___________ 。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2,为证明是否K2FeO4氧化了Cl﹣而产生Cl2,设计以下方案:
i.由方案1中溶液变红可知a中含有___________ 离子,但该离子的产生不能判断一定K2FeO4将Cl﹣氧化,还可能由___________ 产生(用离子方程式表示)。
ii.方案Ⅱ可证明K2FeO4氧化了Cl﹣。用KOH溶液洗涤的目的是___________ 。
②根据K2FeO4的制备实验得出:氧化性Cl2___________ FeO (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是___________ 。
(3)K2FeO4的纯度分析
将1.32 g样品与过量的的KI溶液 (硫酸酸化)充分反应(杂质不参与反应)后配成100 mL溶液,每次取10.00 mL用0.1000 mol·L-1的Na2S2O3标准溶液滴定,三次滴定消耗Na2S2O3标准溶液体积平均为19.20 mL,则原样品中高铁酸钾的质量分数为___________ 。已知:I2+2Na2S2O3=2NaI+ Na2S4O6
资料:K2FeO4为紫色固体,微溶于KOH溶液,热稳定性差,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置。A中反应离子方程式是
②仪器C的名称为
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2,为证明是否K2FeO4氧化了Cl﹣而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b,取少量b,滴加盐酸,有Cl2产生。 |
ii.方案Ⅱ可证明K2FeO4氧化了Cl﹣。用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是(3)K2FeO4的纯度分析
将1.32 g样品与过量的的KI溶液 (硫酸酸化)充分反应(杂质不参与反应)后配成100 mL溶液,每次取10.00 mL用0.1000 mol·L-1的Na2S2O3标准溶液滴定,三次滴定消耗Na2S2O3标准溶液体积平均为19.20 mL,则原样品中高铁酸钾的质量分数为
您最近一年使用:0次
2021-12-04更新
|
163次组卷
|
2卷引用:河南省示范性高中2021-2022学年高三上学期阶段性调研联考二化学试题
名校
5 . 有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中位于第_______ 周期第_______ 族。
(2)用电子式表示B与C形成化合物的过程:_______ 。
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是_______ (填化学式)。
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
a.其单质在常温下呈固态
b. 既有氧化性又有还原性
既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为
d.非金属性比Cl元素的强
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,且其水溶液显碱性 |
| B | 单质在焰色试验中显黄色 |
| C | 单质是淡黄绿色气体,可用于自来水消毒 |
| D | -2价阴离子的电子层结构与Ar原子相同 |
(1)A在周期表中位于第
(2)用电子式表示B与C形成化合物的过程:
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.
 既有氧化性又有还原性
既有氧化性又有还原性c.最高价氧化物对应的水化物的化学式为

d.非金属性比Cl元素的强
您最近一年使用:0次
6 . 双氧水和含氯消毒剂是生活中常用的消毒剂,了解物质的性质是科学合理使用化学品的基础和前提。请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质:
①从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明H2O2具有还原性的实验是_______ (填序号),写出该过程的离子方程式_______ 。
(2)“84”消毒液的(有效成分为NaClO)不能与洁厕灵(主要成分为盐酸)混用的原因_______ (用离子方程式解释其原理)。
(3)二氧化氯(ClO2)是广谱性具有强氧化性的高效低毒的消毒剂。
①用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,该过程的化学方程式为_______ 。
②ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的_______ 倍。
(1)某同学设计如下实验研究H2O2的性质:
| 序号 | 实验 | 实验现象 |
| i | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
②能证明H2O2具有还原性的实验是
(2)“84”消毒液的(有效成分为NaClO)不能与洁厕灵(主要成分为盐酸)混用的原因
(3)二氧化氯(ClO2)是广谱性具有强氧化性的高效低毒的消毒剂。
①用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,该过程的化学方程式为
②ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的
您最近一年使用:0次
名校
解题方法
7 . 瑞典化学家舍勒是最早发现氯气的人,他在研究软锰矿矿石(主要成分是二氧化锰)时,把浓盐酸和软锰矿矿石混合加热,意外地得到了氯气。至今,实验室中还用这种方法制取氯气,装置如图所示,化学反应方程式为: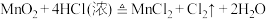
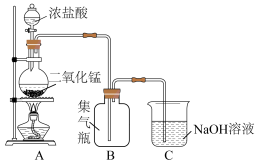
回答下列问题:
(1)实验室制取 的反应中,浓盐酸表现
的反应中,浓盐酸表现_________ (填“氧化性”、“还原性”或“酸性”)。
(2)请用单线桥表示该反应中电子转移的方向和数目_________ 。
(3)标况下,若生成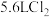 ,则转移电子的数目为
,则转移电子的数目为_________ 。
(4)装置C可吸收多余的 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式_________ 。所用 溶液一般为
溶液一般为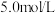 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、_________ 。
(5) 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是_________ 。
(6)装置C中也可能生成 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式_________ 。
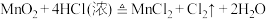

回答下列问题:
(1)实验室制取
 的反应中,浓盐酸表现
的反应中,浓盐酸表现(2)请用单线桥表示该反应中电子转移的方向和数目
(3)标况下,若生成
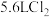 ,则转移电子的数目为
,则转移电子的数目为(4)装置C可吸收多余的
 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式 溶液一般为
溶液一般为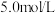 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、(5)
 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是(6)装置C中也可能生成
 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式
您最近一年使用:0次
解题方法
8 . 氯气是一种重要的化工产品和基础原料,实验室制备氯气装置如下,请回答:

(1)装置A中的化学方程式为_______ 。在该反应中浓盐酸表现的性质是_______ (填字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)装置B的作用是_______ 。
(3)氯气能将 氧化为I2,因氯气有毒常用H2O2替代,H2O2氧化
氧化为I2,因氯气有毒常用H2O2替代,H2O2氧化 的离子方程式是
的离子方程式是_______ 。
(4)有同学认为H2O2既有氧化性又有还原性,理论依据是_______ (从氧元素价态回答),选择合适的试剂设计实验,可以验证H2O2的还原性,提供试剂:0.1mol/LKMnO4(H+)溶液、0.1mol/LKI溶液、淀粉溶液、10% H2O2溶液、0.1mol/LFeCl3溶液。请写出H2O2只做还原剂的离子方程式_______ ,该反应中能够证明H2O2被氧化的实验现象是_______ 。

(1)装置A中的化学方程式为
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)装置B的作用是
(3)氯气能将
 氧化为I2,因氯气有毒常用H2O2替代,H2O2氧化
氧化为I2,因氯气有毒常用H2O2替代,H2O2氧化 的离子方程式是
的离子方程式是(4)有同学认为H2O2既有氧化性又有还原性,理论依据是
您最近一年使用:0次
解题方法
9 . 利用下图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:
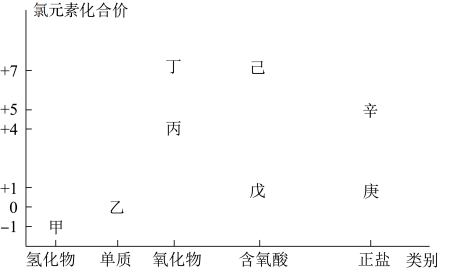
(1)丁属于___________ (“酸性”或“碱性”)氧化物;
(2)图中甲、乙、丙、戊中,属于电解质的是___________ (填化学式);根据氯元素的化合价判断,乙物质___________ ;
A. 只有氧化性 B. 只有还原性 C. 既有氧化性又有还原性
(3)电解甲溶液制备己的化学反应为: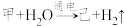 (未配平),则配平后参与反应的甲与H2O的物质的量之比是
(未配平),则配平后参与反应的甲与H2O的物质的量之比是___________ ;
(4)庚是漂白粉的有效成分,用乙制取庚的化学方程式为___________ ;
(5)已知己是最强的无机酸,写出己的电离方程式___________ 。

(1)丁属于
(2)图中甲、乙、丙、戊中,属于电解质的是
A. 只有氧化性 B. 只有还原性 C. 既有氧化性又有还原性
(3)电解甲溶液制备己的化学反应为:
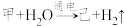 (未配平),则配平后参与反应的甲与H2O的物质的量之比是
(未配平),则配平后参与反应的甲与H2O的物质的量之比是(4)庚是漂白粉的有效成分,用乙制取庚的化学方程式为
(5)已知己是最强的无机酸,写出己的电离方程式
您最近一年使用:0次
2021-11-17更新
|
1156次组卷
|
4卷引用:河南省洛阳市第二中学2022-2023学年高一上学期期末达标考试化学试题
10 . 一氧化二氯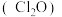 为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:
为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:
实验室制备原理: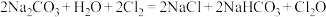 。
。
现用如图所示装置设计实验制备少量 。
。

(1)仪器组装完成、加药品前应进行的实验操作为_______ 。
(2)装置A中发生反应的化学方程式为_______ ,其中浓盐酸表现出来的性质_______ 。
①酸性②氧化性③还原性
(3)装置B中盛放的试剂是_______ 溶液。
(4)E装置中冰水混合物的作用_______ 。
(5)反应结束后,请设计简单实验证明装置C中的残留固体中含有NaCl_______ 。
 为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:
为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:| 物理性质 | 化学性质 |
常温下, 是棕黄色有刺激性气味的气体; 是棕黄色有刺激性气味的气体;熔点:-120.6℃;沸点2.0℃ |  热稳定性差,常温下即可分解; 热稳定性差,常温下即可分解;易溶于水,同时反应生成次氯酸。 |
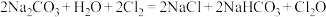 。
。现用如图所示装置设计实验制备少量
 。
。
(1)仪器组装完成、加药品前应进行的实验操作为
(2)装置A中发生反应的化学方程式为
①酸性②氧化性③还原性
(3)装置B中盛放的试剂是
(4)E装置中冰水混合物的作用
(5)反应结束后,请设计简单实验证明装置C中的残留固体中含有NaCl
您最近一年使用:0次
2021-11-17更新
|
265次组卷
|
5卷引用:河南省商丘市2022-2023学年高一上学期期中考试化学试题



