解题方法
1 . 完成下列问题
(1)已知反应:① 时,
时,
②稀溶液中, (1)
(1) 
下列结论中正确的是___________(填字母)。
(2)用如图所示装置进行中和反应反应热测定实验,请回答下列问题:
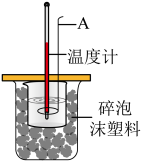
①中和反应反应热测定实验中,每得到一组数据,至少需要测量___________ 次温度。
②取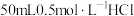 溶液与
溶液与 溶液在小烧杯中进行中和反应,通过实验并计算可得生成
溶液在小烧杯中进行中和反应,通过实验并计算可得生成 放出热量
放出热量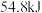 ,上述实验数值与
,上述实验数值与 有偏差,产生此偏差的原因可能是
有偏差,产生此偏差的原因可能是___________ (填字母)。
a.实验装置保温、隔热效果差
b.用温度计测定 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度
c.一次性把 溶液倒入盛有
溶液倒入盛有 溶液的小烧杯中
溶液的小烧杯中
③仪器A的使用过程中操作为___________ 。
④现将一定量的稀 溶液、稀
溶液、稀 溶液、稀氨水分别和
溶液、稀氨水分别和 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为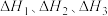 ,则
,则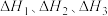 的大小关系为
的大小关系为___________ 。
⑤若用 溶液与
溶液与 锌粉在量热计中充分反应。测得反应前温度为
锌粉在量热计中充分反应。测得反应前温度为 ,反应后最高温度为
,反应后最高温度为 。(已知:反应前后,溶液的比热容均近似为
。(已知:反应前后,溶液的比热容均近似为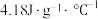 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:反应
,忽略溶液体积、质量变化和金属吸收的热量。请计算:反应 的
的
___________ 。
(1)已知反应:①
 时,
时,
②稀溶液中,
 (1)
(1) 
下列结论中正确的是___________(填字母)。
A.碳的燃烧热等于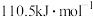 |
B.反应①的反应热为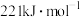 |
C.稀硫酸与稀 溶液反应的中和反应反应热为 溶液反应的中和反应反应热为 |
D.含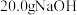 的稀溶液与稀盐酸完全中和,放出 的稀溶液与稀盐酸完全中和,放出 的热量 的热量 |
(2)用如图所示装置进行中和反应反应热测定实验,请回答下列问题:

①中和反应反应热测定实验中,每得到一组数据,至少需要测量
②取
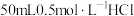 溶液与
溶液与 溶液在小烧杯中进行中和反应,通过实验并计算可得生成
溶液在小烧杯中进行中和反应,通过实验并计算可得生成 放出热量
放出热量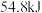 ,上述实验数值与
,上述实验数值与 有偏差,产生此偏差的原因可能是
有偏差,产生此偏差的原因可能是a.实验装置保温、隔热效果差
b.用温度计测定
 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度c.一次性把
 溶液倒入盛有
溶液倒入盛有 溶液的小烧杯中
溶液的小烧杯中③仪器A的使用过程中操作为
④现将一定量的稀
 溶液、稀
溶液、稀 溶液、稀氨水分别和
溶液、稀氨水分别和 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为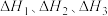 ,则
,则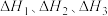 的大小关系为
的大小关系为⑤若用
 溶液与
溶液与 锌粉在量热计中充分反应。测得反应前温度为
锌粉在量热计中充分反应。测得反应前温度为 ,反应后最高温度为
,反应后最高温度为 。(已知:反应前后,溶液的比热容均近似为
。(已知:反应前后,溶液的比热容均近似为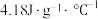 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:反应
,忽略溶液体积、质量变化和金属吸收的热量。请计算:反应 的
的
您最近一年使用:0次
解题方法
2 . 在一定温度下,向容积不等的恒温恒容密闭容器中分别加入足量活性炭和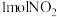 气体,发生反应
气体,发生反应 ,反应相同时间,测得各容器中
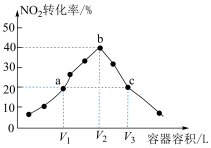
,反应相同时间,测得各容器中 的转化率与容器容积的关系如图所示。下列说法错误的是
的转化率与容器容积的关系如图所示。下列说法错误的是
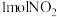 气体,发生反应
气体,发生反应 ,反应相同时间,测得各容器中
,反应相同时间,测得各容器中 的转化率与容器容积的关系如图所示。下列说法错误的是
的转化率与容器容积的关系如图所示。下列说法错误的是
| A.b、c两点均为平衡状态 |
B.a点所示条件下一定满足 |
C.向b点体系中充入一定量 ,平衡正移, ,平衡正移, 体积分数增大 体积分数增大 |
D.对c点容器加压,缩小容器容积,此时Q(浓度商)、 大小关系无法确定 大小关系无法确定 |
您最近一年使用:0次
解题方法
3 . 为减少 对环境造成的影响,可采用“
对环境造成的影响,可采用“ 催化加经制甲醇”方法将其资源化利用。该反应体系中涉及以下两个反应:
催化加经制甲醇”方法将其资源化利用。该反应体系中涉及以下两个反应:
I.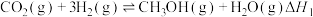
Ⅱ.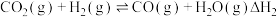
回答下列问题:
(1)反应Ⅰ、Ⅱ的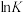 (
( 代表化学平衡常数)随
代表化学平衡常数)随 (温度的倒数)的变化如图所示。
(温度的倒数)的变化如图所示。
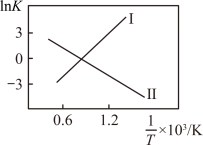

___________ 0(填“>”、“<”或“=”);升高温度,反应 的化学平衡常数
的化学平衡常数___________ (填“增大”、“减小”或“不变”)。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________(填字母)。
(3)恒压下将 和
和 按体积比
按体积比 混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内
混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内 的选择性和产率随温度的变化如图。
的选择性和产率随温度的变化如图。
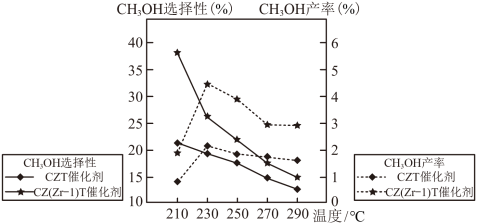
其中: 的选择性
的选择性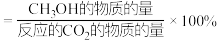
①在上述条件下合成甲醇的工业条件是___________ (填字母)。
A. B.
B. C.催化CZT D.催化剂
C.催化CZT D.催化剂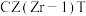
②在 以上,升高温度
以上,升高温度 的转化率增大,但甲醇的产率降低,原因是
的转化率增大,但甲醇的产率降低,原因是___________ 。
(4)恒温恒压密闭容器中,加入 和
和 ,只发生反应I和反应Ⅱ,初始压强为
,只发生反应I和反应Ⅱ,初始压强为 ,在
,在 发生反应,反应达平衡时,
发生反应,反应达平衡时, 的转化率为
的转化率为 ,容器体积减小
,容器体积减小 。则反应Ⅱ的平衡常数
。则反应Ⅱ的平衡常数
___________ (保留两位有效数字)。
 对环境造成的影响,可采用“
对环境造成的影响,可采用“ 催化加经制甲醇”方法将其资源化利用。该反应体系中涉及以下两个反应:
催化加经制甲醇”方法将其资源化利用。该反应体系中涉及以下两个反应:I.
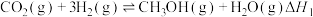
Ⅱ.
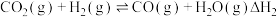
回答下列问题:
(1)反应Ⅰ、Ⅱ的
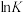 (
( 代表化学平衡常数)随
代表化学平衡常数)随 (温度的倒数)的变化如图所示。
(温度的倒数)的变化如图所示。

 的化学平衡常数
的化学平衡常数(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________(填字母)。
A.增大 的浓度,反应Ⅰ的平衡向正反应方向移动 的浓度,反应Ⅰ的平衡向正反应方向移动 |
| B.降低温度,反应Ⅰ和Ⅱ的正、逆反应速率都减小 |
| C.恒温恒容下充入氦气,反应Ⅰ的平衡向正反应方向移动 |
| D.增大压强,反应I和Ⅱ重新达到平衡的时间不同 |
(3)恒压下将
 和
和 按体积比
按体积比 混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内
混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内 的选择性和产率随温度的变化如图。
的选择性和产率随温度的变化如图。
其中:
 的选择性
的选择性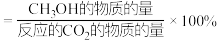
①在上述条件下合成甲醇的工业条件是
A.
 B.
B. C.催化CZT D.催化剂
C.催化CZT D.催化剂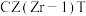
②在
 以上,升高温度
以上,升高温度 的转化率增大,但甲醇的产率降低,原因是
的转化率增大,但甲醇的产率降低,原因是(4)恒温恒压密闭容器中,加入
 和
和 ,只发生反应I和反应Ⅱ,初始压强为
,只发生反应I和反应Ⅱ,初始压强为 ,在
,在 发生反应,反应达平衡时,
发生反应,反应达平衡时, 的转化率为
的转化率为 ,容器体积减小
,容器体积减小 。则反应Ⅱ的平衡常数
。则反应Ⅱ的平衡常数
您最近一年使用:0次
解题方法
4 . 将浓度均为 的
的 、
、 、
、 、
、 溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。
溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。
资料:该“碘钟实验”的总反应为 。反应分A、B两步进行。
。反应分A、B两步进行。
反应A: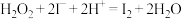 ;
;
反应B:……
(1)反应B的离子方程式是___________ 。
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向酸化的 溶液中加入
溶液中加入 溶液和试剂X,溶液变为蓝色。
溶液和试剂X,溶液变为蓝色。
b.再向得到的蓝色溶液中加入 溶液,溶液的蓝色褪去。
溶液,溶液的蓝色褪去。
试剂X是___________ 。
(3)为探究溶液变蓝快慢的影响因素,进行实验Ⅱ、实验Ⅲ(溶液浓度均为 )
)
溶液从混合时的无色变为蓝色的时间:实验Ⅱ是 ,实验Ⅲ是
,实验Ⅲ是 。
。
①实验Ⅲ中x、y、z,所对应的数值分别是___________ 、___________ 、___________ 。
②对比实验Ⅱ、实验Ⅲ,可得出的实验结论是___________ 。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验IV。(溶液浓度均为 )
)
实验过程中,溶液始终无明显颜色变化。
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验IV未产生颜色变化的原因:___________ 。
 的
的 、
、 、
、 、
、 溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。
溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。资料:该“碘钟实验”的总反应为
 。反应分A、B两步进行。
。反应分A、B两步进行。反应A:
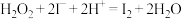 ;
;反应B:……
(1)反应B的离子方程式是
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向酸化的
 溶液中加入
溶液中加入 溶液和试剂X,溶液变为蓝色。
溶液和试剂X,溶液变为蓝色。b.再向得到的蓝色溶液中加入
 溶液,溶液的蓝色褪去。
溶液,溶液的蓝色褪去。试剂X是
(3)为探究溶液变蓝快慢的影响因素,进行实验Ⅱ、实验Ⅲ(溶液浓度均为
 )
)| 用量/mL 实验序号 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 | KI溶液 (含淀粉) |  |
| 实验Ⅱ | 5 | 4 | 8 | 3 | 0 |
| 实验Ⅲ | 5 | 2 |  |  |  |
 ,实验Ⅲ是
,实验Ⅲ是 。
。①实验Ⅲ中x、y、z,所对应的数值分别是
②对比实验Ⅱ、实验Ⅲ,可得出的实验结论是
(4)为探究其他因素对该“碘钟实验”的影响,进行实验IV。(溶液浓度均为
 )
)| 用量/mL 实验序号 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 | KI溶液(含淀粉) |  |
| 实脸IV | 4 | 4 | 9 | 3 | 0 |
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验IV未产生颜色变化的原因:
您最近一年使用:0次
5 . 根据所给信息及要求填空。
(1) 时,四种弱电解质的电离平衡常数如表:
时,四种弱电解质的电离平衡常数如表:
①常温下, 的
的 溶液加水稀释过程,下列说法错误的是
溶液加水稀释过程,下列说法错误的是___________ (填字母)。
a. 增大 b.
增大 b. 增大
增大
c. 的电离程度增大 d.
的电离程度增大 d. 增大
增大
②下列反应不能发生的是___________ (填字母)。
A.
B.
C.
D.
(2)常温下,有 相同、体积相同的醋酸溶液和盐酸溶液,现采取以下措施:
相同、体积相同的醋酸溶液和盐酸溶液,现采取以下措施:
①分别加适量醋酸钠晶体后,忽略溶液体积的变化,则醋酸溶液中
___________ (填“增大”、“减小”或“不变”,下同),盐酸溶液中
___________ 。
②分别加等浓度的 溶液至恰好中和,所需
溶液至恰好中和,所需 溶液的体积:醋酸溶液
溶液的体积:醋酸溶液___________ (填“>”、“=”或“<”)盐酸溶液。
(1)
 时,四种弱电解质的电离平衡常数如表:
时,四种弱电解质的电离平衡常数如表:| 化学式 |  |  |  |  |
| 电离平衡常数 | 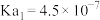 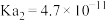 |  |  |  |
 的
的 溶液加水稀释过程,下列说法错误的是
溶液加水稀释过程,下列说法错误的是a.
 增大 b.
增大 b. 增大
增大c.
 的电离程度增大 d.
的电离程度增大 d. 增大
增大②下列反应不能发生的是
A.

B.

C.

D.

(2)常温下,有
 相同、体积相同的醋酸溶液和盐酸溶液,现采取以下措施:
相同、体积相同的醋酸溶液和盐酸溶液,现采取以下措施:①分别加适量醋酸钠晶体后,忽略溶液体积的变化,则醋酸溶液中


②分别加等浓度的
 溶液至恰好中和,所需
溶液至恰好中和,所需 溶液的体积:醋酸溶液
溶液的体积:醋酸溶液
您最近一年使用:0次
解题方法
6 . 已知: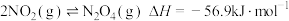 ,反应速率表达式为
,反应速率表达式为
 是反应速率常数,只与温度有关)。下列说法正确的是
是反应速率常数,只与温度有关)。下列说法正确的是
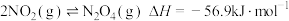 ,反应速率表达式为
,反应速率表达式为
 是反应速率常数,只与温度有关)。下列说法正确的是
是反应速率常数,只与温度有关)。下列说法正确的是| A.达到平衡后,充入NO2,v正增大,v逆减小 |
| B.达到平衡后,加入催化剂,v正和v逆都增大 |
| C.达到平衡后,升高温度,k正增大、k逆减小 |
| D.若恒温恒压条件下充入NO,则平衡不移动 |
您最近一年使用:0次
7 . 下列事实中,不能用勒夏特列原理解释的是
| A.酯和热氢氧化钠溶液混合,一段时间后酯层消失 |
| B.在配制硫酸亚铁溶液时往往要加入一定量的铁粉 |
| C.实验室用排饱和食盐水的方法收集氯气 |
D.用钠与氯化钾共融的方法制备气态钾: |
您最近一年使用:0次
8 . 在 溶液中存在:
溶液中存在: ,下列有关叙述错误的是
,下列有关叙述错误的是
 溶液中存在:
溶液中存在: ,下列有关叙述错误的是
,下列有关叙述错误的是A.加入少量冰醋酸,电离平衡向正向移动,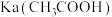 保持不变 保持不变 |
B.加入少量 固体,溶液中 固体,溶液中 浓度减小 浓度减小 |
| C.升高温度,醋酸的电离程度增大 |
D.加入少量 固体, 固体, 减小 减小 |
您最近一年使用:0次
解题方法
9 . 下列说法正确的是
A.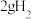 完全燃烧生成液态水,放热 完全燃烧生成液态水,放热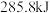 ,则表示氢气燃烧热的热化学方程式为 ,则表示氢气燃烧热的热化学方程式为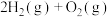  |
B.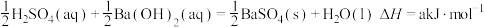 (a>-57.3) (a>-57.3) |
C.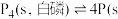 ,红磷) ,红磷)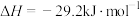 ,常温下,红磷比白磷稳定 ,常温下,红磷比白磷稳定 |
D.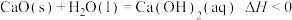 ,理论上可利用该反应设计成原电池 ,理论上可利用该反应设计成原电池 |
您最近一年使用:0次
10 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.25g质量分数为46%的乙醇水溶液中含有的氢原子数为 |
B.将22.4L(标准状况)Cl2通入足量水中,转移的电子数为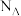 |
C.1molH2和1molO2在一定条件下完全反应,转移的电子数为 |
D.64gSO2和32gO2混合,反应一段时间后总原子数为 |
您最近一年使用:0次



