解题方法
1 . C40H10呈现出深碗状几何形状,高温条件下,C40H10可以由C40H20分子经过连续5步反应生成。回答下列问题:
(1)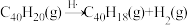 反应机理和能量变化如下:
反应机理和能量变化如下:
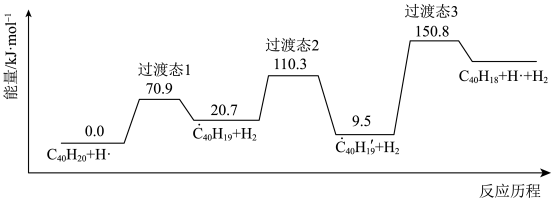
图示历程包含___________ 个基元反应,其中速率最快的是第___________ 个。
(2)已知:ⅰC40H20(g) C40H18(g)+H2(g) ΔH=+128kJ·mol−1
C40H18(g)+H2(g) ΔH=+128kJ·mol−1
ⅱC40H18(g) C40H16(g)+H2(g) ΔH=+128kJ·mol−1
C40H16(g)+H2(g) ΔH=+128kJ·mol−1
则C40H20(g) C40H16(g)+2H2(g) ΔH=
C40H16(g)+2H2(g) ΔH=___________ kJ·mol−1。
(3)某温度下,在恒容密闭容器中加入一定量的C40H20(g),假定体系内只有反应C40H20(g) C40H18(g)+H2(g)发生,能表明该反应达到平衡状态的是
C40H18(g)+H2(g)发生,能表明该反应达到平衡状态的是___________ (填标号)。
a.混合气体密度不变
b.混合气体的平均相对分子质量不变
c.气体的总物质的量不再改变
d.容器中C40H20、C40H18、H2物质的量之比为1∶1∶1
(4)在一密闭容器中进行反应:C40H12(g) C40H10(g)+H2(g) ΔH>0。
C40H10(g)+H2(g) ΔH>0。
①下列措施既能提高反应物的平衡转化率,又能增大生成C40H10的反应速率的是___________ (填标号)。
a.升高温度 b.增大压强 c.加入催化剂
②在某温度、100kPa下,向反应器中充入1mol气态C40H12,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入___________ mol水蒸气作为稀释气。
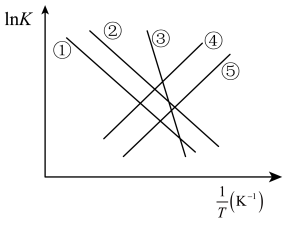
(5)在本反应体系中,存在上面(2)问中的ⅰ、ⅱ等反应,这些反应的平衡常数用K表示,已知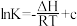 (R为理想气体常数,c为截距)。如图中能正确表示这两个反应的lnK与温度倒数(
(R为理想气体常数,c为截距)。如图中能正确表示这两个反应的lnK与温度倒数( )的关系的两条线是
)的关系的两条线是___________ (填标号),你选择这两条线的理由是___________ 。
(1)
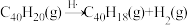 反应机理和能量变化如下:
反应机理和能量变化如下:
图示历程包含
(2)已知:ⅰC40H20(g)
 C40H18(g)+H2(g) ΔH=+128kJ·mol−1
C40H18(g)+H2(g) ΔH=+128kJ·mol−1ⅱC40H18(g)
 C40H16(g)+H2(g) ΔH=+128kJ·mol−1
C40H16(g)+H2(g) ΔH=+128kJ·mol−1则C40H20(g)
 C40H16(g)+2H2(g) ΔH=
C40H16(g)+2H2(g) ΔH=(3)某温度下,在恒容密闭容器中加入一定量的C40H20(g),假定体系内只有反应C40H20(g)
 C40H18(g)+H2(g)发生,能表明该反应达到平衡状态的是
C40H18(g)+H2(g)发生,能表明该反应达到平衡状态的是a.混合气体密度不变
b.混合气体的平均相对分子质量不变
c.气体的总物质的量不再改变
d.容器中C40H20、C40H18、H2物质的量之比为1∶1∶1
(4)在一密闭容器中进行反应:C40H12(g)
 C40H10(g)+H2(g) ΔH>0。
C40H10(g)+H2(g) ΔH>0。①下列措施既能提高反应物的平衡转化率,又能增大生成C40H10的反应速率的是
a.升高温度 b.增大压强 c.加入催化剂
②在某温度、100kPa下,向反应器中充入1mol气态C40H12,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入
(5)在本反应体系中,存在上面(2)问中的ⅰ、ⅱ等反应,这些反应的平衡常数用K表示,已知
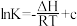 (R为理想气体常数,c为截距)。如图中能正确表示这两个反应的lnK与温度倒数(
(R为理想气体常数,c为截距)。如图中能正确表示这两个反应的lnK与温度倒数( )的关系的两条线是
)的关系的两条线是
您最近一年使用:0次
解题方法
2 . Ce2(CO3)3可用于催化剂载体及功能材料的制备。天然独居石中铈(Ce)主要以CePO4形式存在,还含有SiO2、Al2O3、Fe2O3、CaF2等物质。以独居石为原料制备Ce2(CO3)3·8H2O的工艺流程如图所示:
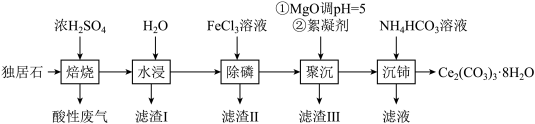
| A.“焙烧”时,酸性废气含HF、SO2 |
| B.“水浸”后,滤渣Ⅰ的成分是SiO2 |
| C.“除磷”时,离子反应为Fe3++H3PO4=FePO4↓+3H+ |
| D.“沉铈”后,滤液中大量存在的阴离子只有Cl- |
您最近一年使用:0次
解题方法
3 . 硫酸镍一般用于电镀、催化剂制备和医药制造等领域。电镀污泥中主要含有Cr2O3、CuO、NiO、Al2O3、Fe2O3和SiO2等物质。一种从电镀污泥制备回收金属铜和制备硫酸镍晶体的工艺流程如图1,回答下列问题:
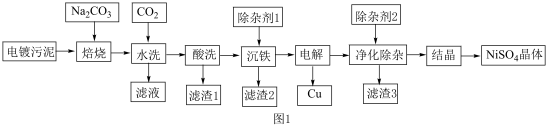
已知:①“焙烧”时Cr2O3和Al2O3分别转化为Na2CrO4、NaAlO2
②Na2CrO4溶液中存在平衡: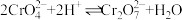
(1)“焙烧”时,Cr2O3参与反应的化学方程式为___________ 。
(2)提高“酸洗”的速率的措施为___________ 、___________ (写出两种措施)。
(3)“酸洗”后,滤渣1的化学式为___________ 。
(4)“滤液”主要成分是含有少量重金属阳离子的Na2CrO4溶液,除杂装置如图2所示
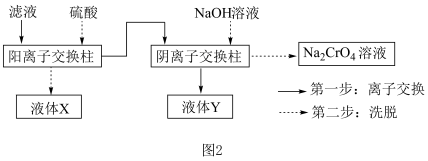
已知:图中离子交换柱原理为HR+M+ MR+H+;2ROH+CrO
MR+H+;2ROH+CrO
 R2CrO4+2OH-
R2CrO4+2OH-
则液体X的溶质主要是___________ (填化学式),液体Y是___________ (填名称)。
(5)为确定硫酸镍晶体中含有的结晶水,称取纯化后的硫酸镍晶体5.26g,加热至完全失去结晶水,固体减重2.16g,则该晶体的化学式为___________ 。

已知:①“焙烧”时Cr2O3和Al2O3分别转化为Na2CrO4、NaAlO2
②Na2CrO4溶液中存在平衡:
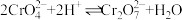
(1)“焙烧”时,Cr2O3参与反应的化学方程式为
(2)提高“酸洗”的速率的措施为
(3)“酸洗”后,滤渣1的化学式为
(4)“滤液”主要成分是含有少量重金属阳离子的Na2CrO4溶液,除杂装置如图2所示

已知:图中离子交换柱原理为HR+M+
 MR+H+;2ROH+CrO
MR+H+;2ROH+CrO
 R2CrO4+2OH-
R2CrO4+2OH-则液体X的溶质主要是
(5)为确定硫酸镍晶体中含有的结晶水,称取纯化后的硫酸镍晶体5.26g,加热至完全失去结晶水,固体减重2.16g,则该晶体的化学式为
您最近一年使用:0次
解题方法
4 . 某实验小组利用如图所示装置制备SO2,并验证其部分性质。
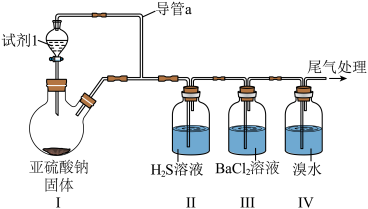
回答下列问题:
(1)盛装试剂1的仪器名称为___________ 。试剂1最好选择___________ (填标号)。
a.50%硝酸 b.30%盐酸 c.70%硫酸
(2)导管a的作用为___________ 。
(3)实验过程中,装置Ⅱ中的实验现象为___________ 。
(4)实验过程中,某同学预测装置Ⅲ中不会产生白色沉淀,随着实验的进行,装置Ⅲ中产生了少量白色沉淀,产生该白色沉淀的可能原因为___________ 。
(5)该实验小组的甲、乙两位同学为了进一步探究SO2的漂白性,按如图装置继续进行实验并记录相关实验现象。
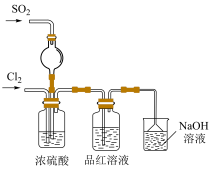
①装置中浓硫酸的作用为___________ 。
②根据表中实验现象做出合理解释。

回答下列问题:
(1)盛装试剂1的仪器名称为
a.50%硝酸 b.30%盐酸 c.70%硫酸
(2)导管a的作用为
(3)实验过程中,装置Ⅱ中的实验现象为
(4)实验过程中,某同学预测装置Ⅲ中不会产生白色沉淀,随着实验的进行,装置Ⅲ中产生了少量白色沉淀,产生该白色沉淀的可能原因为
(5)该实验小组的甲、乙两位同学为了进一步探究SO2的漂白性,按如图装置继续进行实验并记录相关实验现象。

①装置中浓硫酸的作用为
②根据表中实验现象做出合理解释。
| 组别 | 实验现象 | 合理解释 |
| 甲 | 品红溶液几乎不褪色 | 反应的离子方程式为 |
| 乙 | 品红溶液随时间的推移变得越来越浅 | 原因可能是 |
您最近一年使用:0次
5 . 实验室中下列有关试剂的保存方法错误的是
| A.浓硝酸应密封保存在铁制容器中 |
| B.少量的钠保存在煤油中 |
| C.NaOH溶液保存在具有橡胶塞的玻璃试剂瓶中 |
| D.液溴存放在棕色试剂瓶中并加水封 |
您最近一年使用:0次
解题方法
6 . 下列有关离子检验涉及的反应表达错误的是
| A.Fe2+:K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓ |
B.Fe3+:Fe3++3SCN- Fe(SCN)3 Fe(SCN)3 |
C.NH :NH :NH +OH-=NH3·H2O +OH-=NH3·H2O |
D.SO :Ba2++SO :Ba2++SO =BaSO4↓ =BaSO4↓ |
您最近一年使用:0次
解题方法
7 . 下列反应的离子方程式正确的是
| A.碘化亚铁溶液与等物质的量的氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
B.用稀硝酸除去试管内壁银镜:3Ag+4H++NO =3Ag++NO↑+2H2O =3Ag++NO↑+2H2O |
C.用醋酸和淀粉-KI溶液检验加碘盐中的IO :IO :IO +5I-+6H+=3I2+3H2O +5I-+6H+=3I2+3H2O |
D.向硫化钠溶液通入足量二氧化硫:S2-+2SO2+2H2O=H2S+2HSO |
您最近一年使用:0次
解题方法
8 . 碳是构成地球生命的重要元素。下列说法正确的是
| A.自然界中不存在游离态的碳 |
| B.碳的化合物数量众多分布极广 |
| C.向空气中排放二氧化碳会形成酸雨 |
| D.碳酸盐的沉积会增加自然界中CO2含量 |
您最近一年使用:0次
9 . 根据下列实验操作和现象,得出的结论合理且正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用洁净铂丝蘸取溶液进行焰色试验 | 火焰呈黄色 | 原溶液中有Na+,无K+ |
| B | 将碳酸钠与盐酸反应产生的气体通入盛有硅酸钠溶液的烧杯中 | 烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
| C | 某溶液中加入Ba(NO3)2溶液,再加足量盐酸 | 先生成白色沉淀,加盐酸后白色沉淀不消失 | 原溶液中有SO |
| D | 将Fe(NO3)2样品溶于稀硫酸后滴加KSCN溶液 | 溶液变红 | 不能确定Fe(NO3)2原样品是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 氮、磷元素的单质和它们的化合物用途广泛,与生产、生活有密切关系。
请回答下列问题。
(1)下列属于氮的固定的是___________ 。
a.工业上N2和H2合成NH3 b.NH3催化氧化生成NO
c.N2和O2放电条件下生成NO d.NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为___________ 。
(3)实验室中向浓氨水中加CaO固体可以快速制备氨气,请解释其反应原理___________ 。
(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途___________ 。
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0gNaOH最多可中和100mL1mol·L−1H3PO2溶液,则NaH2PO2是___________ (填“正盐”或“酸式盐”)。
②已知常温下酸性:H3PO3>CH3COOH>H2PO ,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为___________ 。
请回答下列问题。
(1)下列属于氮的固定的是
a.工业上N2和H2合成NH3 b.NH3催化氧化生成NO
c.N2和O2放电条件下生成NO d.NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为
(3)实验室中向浓氨水中加CaO固体可以快速制备氨气,请解释其反应原理
(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0gNaOH最多可中和100mL1mol·L−1H3PO2溶液,则NaH2PO2是
②已知常温下酸性:H3PO3>CH3COOH>H2PO
 ,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
您最近一年使用:0次



