名校
解题方法
1 . 可用CO2催化加氢合成CH3OH,主要反应的热化学方程式如下:
反应Ⅰ: ΔH1
ΔH1
反应Ⅱ: ΔH2=+41.0kJ/mol
ΔH2=+41.0kJ/mol
(1)已知几种化学键的键能如表所示,根据键能估算反应Ⅰ的ΔH1=___________ 。
(2)向某一密闭容器中充入1molCO2和3molH2发生反应Ⅰ,下列能说明反应Ⅰ在恒温恒压条件下达到平衡的是___________(填序号)。
(3)向恒压(3.0MPa)密闭装置中通入1molCO2和2molH2,在不同催化剂下测定甲醇的平均生成速率随温度的变化曲线,如图所示。
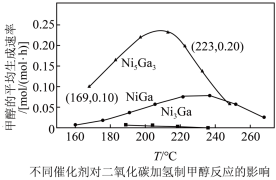
①最佳催化剂及最佳反应温度是___________ 。
②甲醇的平均生成速率呈先增大后减小的抛物线趋势,请解释后减小的原因:___________ 。
③二氧化碳加氢制甲醇的速率方程可表示为v=k·pm(CO2)·pn(H2),其中k为速率常数,各物质起始分压的指数为各物质的反应级数。实验结果表明,速率常数与反应级数均受反应温度的影响。使用Ni5Ga3催化剂时,反应温度由169℃升高到223℃,若CO2反应级数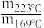 =2,H2反应级数不变,则速率常数之比
=2,H2反应级数不变,则速率常数之比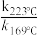 =
=___________ 。
(4)某温度时,向压强为5.0MPa的恒压装置中加入1molCO2(g)和3molH2(g)反应并达到平衡状态,CO2平衡转化率为40%,甲醇选择性为50%,则甲醇的平衡分压为___________ (结果保留2位有效数字)。已知:甲醇选择性x(CH3OH)%= 。
。
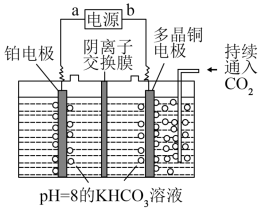
(5)如图所示的电解装置可实现低电位下高效催化CO2制取甲烷,温度控制在10℃左右,持续通入二氧化碳,电解过程中阴极区KHCO3物质的量基本不变。阴极反应为___________ 。
反应Ⅰ:
 ΔH1
ΔH1反应Ⅱ:
 ΔH2=+41.0kJ/mol
ΔH2=+41.0kJ/mol(1)已知几种化学键的键能如表所示,根据键能估算反应Ⅰ的ΔH1=
| 化学键 | H-H | C-O | C-H | H-O | C=O |
| E(kJ/mol) | 436 | 351 | 406 | 465 | 800 |
| A.容器内混合气体的密度不再改变 |
| B.容器内混合气体的压强不再改变 |
| C.反应物转化率的比值不再改变 |
| D.v正(CO2)=3v逆(H2O) |

①最佳催化剂及最佳反应温度是
②甲醇的平均生成速率呈先增大后减小的抛物线趋势,请解释后减小的原因:
③二氧化碳加氢制甲醇的速率方程可表示为v=k·pm(CO2)·pn(H2),其中k为速率常数,各物质起始分压的指数为各物质的反应级数。实验结果表明,速率常数与反应级数均受反应温度的影响。使用Ni5Ga3催化剂时,反应温度由169℃升高到223℃,若CO2反应级数
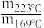 =2,H2反应级数不变,则速率常数之比
=2,H2反应级数不变,则速率常数之比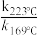 =
=(4)某温度时,向压强为5.0MPa的恒压装置中加入1molCO2(g)和3molH2(g)反应并达到平衡状态,CO2平衡转化率为40%,甲醇选择性为50%,则甲醇的平衡分压为
 。
。(5)如图所示的电解装置可实现低电位下高效催化CO2制取甲烷,温度控制在10℃左右,持续通入二氧化碳,电解过程中阴极区KHCO3物质的量基本不变。阴极反应为

您最近一年使用:0次
2024-01-23更新
|
310次组卷
|
3卷引用:重庆市巴蜀中学校2023-2024学年高三上学期11月期中化学试题
2 . 清华大学开发出一种锂离子电池,在室温条件下可进行循环充放电,实现对磁性的可逆调控,如图电池一极为纳米Fe2O3,另一极为金属锂和石墨的复合材料,电解质只传导锂离子。下列说法错误的是
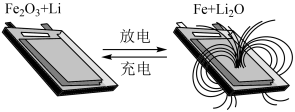

| A.该电池不能使用氯化锂水溶液作为电解质 |
| B.充电时,Fe2O3连接电源的正极,发生氧化反应 |
| C.该电池正极的电极反应式为Fe2O3+6Li++6e-=3Li2O+2Fe |
| D.放电时,电池逐渐远离磁铁 |
您最近一年使用:0次
2024-01-16更新
|
534次组卷
|
5卷引用:重庆市巴蜀中学校2023-2024学年高三上学期11月期中化学试题
重庆市巴蜀中学校2023-2024学年高三上学期11月期中化学试题重庆市巴蜀中学校2023-2024学年高三上学期11月期中化学试题重庆市巴蜀中学2024届高三上学期高考适应性月考卷(四)化学试题(已下线)寒假收官卷02-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)(已下线)专题07 原电池-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)
名校
解题方法
3 . 物质的性质决定了其用途,下列关于物质性质及其用途错误的是
| A.SO2可以使某些色素褪色:用作漂白剂 |
| B.硝酸有腐蚀性:用于刻蚀玻璃 |
| C.H2O2有氧化性:用作消毒剂 |
| D.金属钠有良好的导热性:用作导热介质 |
您最近一年使用:0次
2024-01-10更新
|
239次组卷
|
4卷引用:重庆市巴蜀中学校2023-2024学年高三上学期11月期中化学试题
名校
4 . 一氧化二氯(Cl2O)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,浓度过高时会发生爆炸,42℃以 上易分解。某化学兴趣小组设计如图装置以制备Cl2O(支撑及夹持装置已省略)。
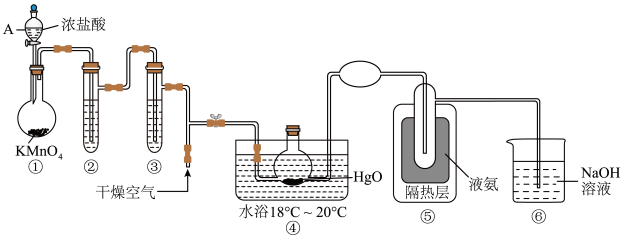
已知:Cl2O的部分性质如表:
请回答下列问题。
(1)装置①中仪器A的名称为___________ 。
(2)装置②的作用是___________ ,装置③中盛有的试剂是___________ 。
(3)通入干燥空气的主要目的是___________ 。
(4)装置④中采用18°C~ 20℃水浴的原因之一是:如温度低,反应速率慢,另一个可能的原因是___________ 。
(5)Cl2O是市场上一种比较理想的饮用水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,则ClO2的消毒效率(以单位质量得到的电子数表示)是等质量的Cl2O的___________ 倍(结果保留一位小数)
(6)据文献报道,Cl2O的另一种制备方法是利用Cl2与适量潮湿的Na2CO3反应来制得,同时产生氯化钠和碳酸氢钠两种盐,写出该反应的化学方程式__________ 。

已知:Cl2O的部分性质如表:
| 熔点 | 沸点 | 制备方法 |
| 120.69℃ | 3.8℃ | 2HgO+2Cl2=Cl2O+HgCl2·HgO(反应放热) |
(1)装置①中仪器A的名称为
(2)装置②的作用是
(3)通入干燥空气的主要目的是
(4)装置④中采用18°C~ 20℃水浴的原因之一是:如温度低,反应速率慢,另一个可能的原因是
(5)Cl2O是市场上一种比较理想的饮用水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,则ClO2的消毒效率(以单位质量得到的电子数表示)是等质量的Cl2O的
(6)据文献报道,Cl2O的另一种制备方法是利用Cl2与适量潮湿的Na2CO3反应来制得,同时产生氯化钠和碳酸氢钠两种盐,写出该反应的化学方程式
您最近一年使用:0次
5 . “价类二维图”是学习元素及其化合物知识的重要模型。氯元素的“价类二维图*如图所示,下列说法错误的是
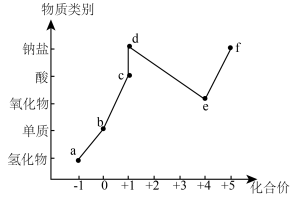

| A.物质a可由H2与b发生爆炸得到 |
| B.物质c具有漂白性,能使湿润的有色布条褪色 |
| C.物质e分子式为ClO2,是一种新型自来水消毒剂 |
| D.物质f中的阴离子可以用稀硝酸和硝酸银溶液来检验 |
您最近一年使用:0次
名校
6 . 下列离子方程式书写正确的是
| A.Cl2与水反应:Cl2 +H2O= 2H+ +Cl- +ClO- |
| B.石灰石与醋酸反应:CaCO3+2H+ =Ca2+ +H2O+CO2↑ |
| C.过氧化钠溶于水:Na2O2 +H2O=2OH-+O2↑ |
D.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO 刚好沉淀完全:H+ + SO 刚好沉淀完全:H+ + SO + Ba2++OH- =H2O+BaSO4↓ + Ba2++OH- =H2O+BaSO4↓ |
您最近一年使用:0次
名校
7 . 水合氧化铁[ FeO(OH)]是一种重要的化工原料,用作磁性材料、颜料铁黄等。一种以硫铁矿烧渣(含Fe、FeO、SiO2和少量CuO)为原料生产FeO(OH)的工艺流程如下:

已知:SiO2难溶于水和硫酸
回答下列问题:
(1)FeO(OH)中Fe元素的化合价为___________ 。
(2)“酸浸”时FeO与硫酸发生反应的离子方程式为___________ 。
(3)“除杂”时滤渣②的成分为___________ ;“沉淀”时___________ (填“能”或“不能")用NaOH溶液代替氨水。
(4)某研究小组进行过滤步骤实验,所需要用到的玻璃仪器除烧杯外,还需要___________ 。
(5)“加热氧化”时Fe(OH)2发生的化学方程式为___________ 。
(6)“过滤"后需洗涤FeO(OH)沉淀,请设计实验检验FeO(OH)沉淀是否洗涤干净___________ 。
(7)测定产品的纯度:准确称取FeO(OH)样品10 g,完全溶解于稀硫酸中,用过量的NaOH溶液沉淀其中的铁元素,得到沉淀质量为11g。该样品纯度为___________ (保留3位有效数字)

已知:SiO2难溶于水和硫酸
回答下列问题:
(1)FeO(OH)中Fe元素的化合价为
(2)“酸浸”时FeO与硫酸发生反应的离子方程式为
(3)“除杂”时滤渣②的成分为
(4)某研究小组进行过滤步骤实验,所需要用到的玻璃仪器除烧杯外,还需要
(5)“加热氧化”时Fe(OH)2发生的化学方程式为
(6)“过滤"后需洗涤FeO(OH)沉淀,请设计实验检验FeO(OH)沉淀是否洗涤干净
(7)测定产品的纯度:准确称取FeO(OH)样品10 g,完全溶解于稀硫酸中,用过量的NaOH溶液沉淀其中的铁元素,得到沉淀质量为11g。该样品纯度为
您最近一年使用:0次
名校
8 . 有下列物质:①Ba(OH)2固体;②熔融的KHSO4;③浓HNO3;④稀硫酸;⑤CO2;⑥铜;⑦氨水;⑧蔗糖晶体;⑨NaHCO3固体,⑩纯醋酸(CH3COOH)。
(1)上述状态 下的物质可导电的是___________ (填序号,下同);属于电解质的是___________ 。
(2)写出②的电离方程式:___________ 。
(3)写出向①的水溶液中通入少量⑤的离子方程式:___________ 。
(4)写出⑦和⑨反应的离子方程式:___________ 。
(5)向①溶液中滴加⑨溶液,当Ba2+恰好沉淀完全时,溶液显___________ (填“酸”碱”或“中”)性。
(6)如图所示为实验室制备氢氧化铁胶体的装置,请回答下列问题:
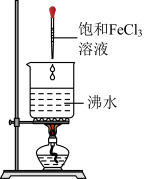
①证明已经制得Fe(OH)3胶体的实验现象是___________ ;
②Fe(OH)3胶体提纯的方法是___________ (填名称),请写出制备Fe(OH)3胶体的离子方程式:___________ 。
(1)上述状态 下的物质可导电的是
(2)写出②的电离方程式:
(3)写出向①的水溶液中通入少量⑤的离子方程式:
(4)写出⑦和⑨反应的离子方程式:
(5)向①溶液中滴加⑨溶液,当Ba2+恰好沉淀完全时,溶液显
(6)如图所示为实验室制备氢氧化铁胶体的装置,请回答下列问题:

①证明已经制得Fe(OH)3胶体的实验现象是
②Fe(OH)3胶体提纯的方法是
您最近一年使用:0次
名校
9 . 某实验研究小组对工业废水中所含离子成分进行了探究。已知该废水中仅含K+、Mg2+、Ba2+、Ag+、Cl-、HCO 、NO
、NO 、SO
、SO 中的几种离子,且每种离子数目相等。实验步骤如下:
中的几种离子,且每种离子数目相等。实验步骤如下:
Ⅰ.取废水少许加入足量盐酸,无白色沉淀析出,但生成能使澄清石灰水变浑浊的无色无味气体。
Ⅱ.向I中所得的溶液中加入BaCl2溶液或AgNO3溶液都有白色沉淀生成。
下列说法错误的是
 、NO
、NO 、SO
、SO 中的几种离子,且每种离子数目相等。实验步骤如下:
中的几种离子,且每种离子数目相等。实验步骤如下:Ⅰ.取废水少许加入足量盐酸,无白色沉淀析出,但生成能使澄清石灰水变浑浊的无色无味气体。
Ⅱ.向I中所得的溶液中加入BaCl2溶液或AgNO3溶液都有白色沉淀生成。
下列说法错误的是
A.由实验可知,该废液中一定含有HCO ,一定不含Ag+ ,一定不含Ag+ |
B.该废液中一定含有K+、Mg2+、 HCO 、SO 、SO |
C.无法确定溶液中是否含有Cl-、NO |
D.实验Ⅰ中加入BaCl2生成白色沉淀的离子方程式为Ba2++ SO =BaSO4↓ =BaSO4↓ |
您最近一年使用:0次
名校
10 . 化学是一门以实验为基础的学科。下列实验方案能够达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A |  | 通过焰色反应确认溶液中是否含有K+ |
| B | 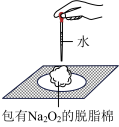 | 验证Na2O2与水反应放热 |
| C | 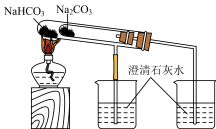 | 比较碳酸钠和碳酸氢钠的热稳定性 |
| D | 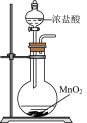 | 实验室用该装置制取Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



