名校
解题方法
1 . 一种新型锌-乙炔电池的结构如图所示,工作时,该电池左右室中KOH的质量均保持不变。下列有关说法错误的是
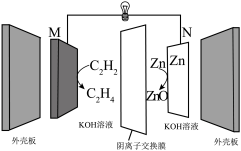

| A.M极为电源正极 |
| B.左室溶液pH增大,右室溶液pH减小 |
| C.N极的电极反应式为Zn - 2e- + 2OH- = ZnO + H2O |
| D.每转移4 mole-,左室中溶液质量减少68 g |
您最近一年使用:0次
名校
2 . 设NA为阿伏加德罗常数的值。下列叙述正确的是
A.1LpH均为2的硫酸和醋酸溶液,氢离子数均为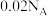 |
| B.60 g二氧化硅晶体中含有NA个SiO2分子 |
C.1mol 中含有 中含有 键的数目为5NA 键的数目为5NA |
| D.由1 mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO−数目等于NA |
您最近一年使用:0次
名校
解题方法
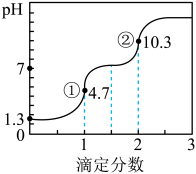
3 . 滴定分数是指滴定过程中标准溶液与待测溶液中溶质的物质的量之比。25℃时,用(0.1 NaOH溶液滴定 0.1
NaOH溶液滴定 0.1 H2C2O4溶液所得滴定曲线如图所示。已知
H2C2O4溶液所得滴定曲线如图所示。已知 下列说法正确的是
下列说法正确的是
 NaOH溶液滴定 0.1
NaOH溶液滴定 0.1 H2C2O4溶液所得滴定曲线如图所示。已知
H2C2O4溶液所得滴定曲线如图所示。已知 下列说法正确的是
下列说法正确的是
A.25℃ 时H2C2O4的电离常数:  |
B.点②所示溶液中:c(H+)+ c(Na+)= c(OH-)+c(HC2O )+c(C2O )+c(C2O ) ) |
C.滴定分数为0.5对应曲线上的点的溶液中:2c(H+)+c(H2C2O4)=2c(OH-)+3c(C2O )+c(HC2O )+c(HC2O ) ) |
D.点①所示溶液中:c(Na+)>c(HC2O )>c(H2C2O4)>c(C2O )>c(H2C2O4)>c(C2O )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
您最近一年使用:0次
名校
4 . 纳米二氧化钛催化剂可用于工业上合成甲醇: ,按投料比
,按投料比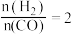 将
将 与
与 充入
充入 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是

 ,按投料比
,按投料比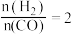 将
将 与
与 充入
充入 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
A. , ,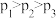 |
B.达到平衡后,再按照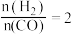 加入气体,平衡后 加入气体,平衡后 的体积分数增大 的体积分数增大 |
| C.M点平衡后,恒温恒容下,向容器中再加入2molCH3OH、3molCO,则平衡不移动 |
D. 、 、 压强下,Q点对应的 压强下,Q点对应的 |
您最近一年使用:0次
名校
解题方法
5 . 奥培米芬是一种雌激素受体调节剂,其合成中间体的结构简式如图所示:
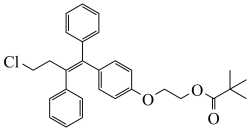
关于该中间体,下列说法正确的是

关于该中间体,下列说法正确的是
| A.含有三种官能团 |
| B.能发生消去反应、水解反应、加成反应、氧化反应 |
| C.所有碳原子可能共平面 |
| D.苯环上的一氯代物有5种结构 |
您最近一年使用:0次
名校
6 . 下列说法不正确的是
A.0.1 的CH3COONa溶液加水稀释 的CH3COONa溶液加水稀释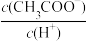 的比值逐渐减小 的比值逐渐减小 |
| B.常温下,pH和为14的盐酸与氨水等体积混合后,溶液的pH>7 |
| C.对MgCl2∙6H2O的固体加热灼烧,最后可得MgO固体 |
| D.Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-36,向10mL0.1mol∙L-1 的MgCl2溶液中滴加20mL0.1mol∙L-1 的NaOH溶液,取澄清溶液滴加两滴0.1mol∙L-1 的FeCl3 溶液,没有浑浊出现 |
您最近一年使用:0次
名校
7 . 铋酸钠( NaBiO3 )常用作分析试剂、氧化剂等,某同学在实验室用氯气氧化Bi(OH)3制取NaBiO3,并进行相关实验。已知NaBiO3固体不溶于冷水,能与沸水或酸溶液反应产生O2,在酸性条件下能将Mn2+氧化为MnO ;Bi(OH)3为白色难溶于水的固体。各实验装置如图所示:
;Bi(OH)3为白色难溶于水的固体。各实验装置如图所示:
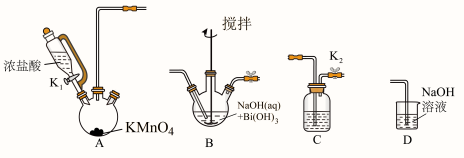
请回答下列问题:
(1)装置的连接顺序是___________→___________→ ___________→ ___________(填字母)。___________
(2)C中装有的试剂是___________ ,若没有装置C,可能产生的影响是___________ 。
(3)反应开始时,打开K1和K2,B中Cl2发生的反应有;Cl2+2NaOH=NaClO+NaCl+H2O,___________ (填化学方程式)。
(4)反应结束后,为从装置B中获得尽可能多的产品,需要进行的操作是___________ 、过滤、冷水洗涤、干燥。
(5)取上述NaBiO3产品w g,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用c mol·L-1的H2C2O4标准溶液滴定生成的 MnO ,消耗V mL标准溶液。
,消耗V mL标准溶液。
①滴定终点判断___________ ,如果装H2C2O4标准溶液的滴定管滴定前有气泡、滴定后没有气泡,则会导致测定结果___________ (填偏大或偏小)。
②不能用c mol·L-1的H2C2O4标准溶液直接滴定NaBiO3的原因是___________ 。
③该产品的纯度为___________ (用含w 、c、V的代数式表示)。
(6)取少量B中反应后的悬浊液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2。该实验不能证明一定是NaBiO3氧化了Cl-,理由是___________ 用离子方程式说明。
 ;Bi(OH)3为白色难溶于水的固体。各实验装置如图所示:
;Bi(OH)3为白色难溶于水的固体。各实验装置如图所示:
请回答下列问题:
(1)装置的连接顺序是___________→___________→ ___________→ ___________(填字母)。
(2)C中装有的试剂是
(3)反应开始时,打开K1和K2,B中Cl2发生的反应有;Cl2+2NaOH=NaClO+NaCl+H2O,
(4)反应结束后,为从装置B中获得尽可能多的产品,需要进行的操作是
(5)取上述NaBiO3产品w g,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用c mol·L-1的H2C2O4标准溶液滴定生成的 MnO
 ,消耗V mL标准溶液。
,消耗V mL标准溶液。①滴定终点判断
②不能用c mol·L-1的H2C2O4标准溶液直接滴定NaBiO3的原因是
③该产品的纯度为
(6)取少量B中反应后的悬浊液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2。该实验不能证明一定是NaBiO3氧化了Cl-,理由是
您最近一年使用:0次
名校
8 . 下列由实验操作及现象所得结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向1 mL 0.1 mol·L−1硝酸银溶液中,加入2 mL等浓度NaCl溶液,出现白色沉淀,再加入几滴等浓度的Na2S溶液,有黑色沉淀生成 | 溶解度AgCl>Ag2S |
| B | 适量溴乙烷与氢氧化钠的乙醇溶液共热反应,将产生的气体通入酸性高锰酸钾溶液,溶液紫红色褪去 | 证明有乙烯生成 |
| C | 某溶液中加盐酸,产生使品红溶液褪色的无色有刺激味气体 | 原溶液中一定存在SO |
| D | 对有酚酞的碳酸钠溶液加热,溶液颜色变浅 | 说明水解平衡逆向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . X、Y、Z、W 是原子序数依次增大的四种短周期元素。基态X、Z原子的电子均填充了3个能级,且均有2个未成对电子,W的核外电子数是X原子最外层电子数的3倍。下列说法正确的是
| A.与Y同周期且第一电离能比Y小的元素有四种 |
| B.元素X的氢化物的沸点一定比元素Y的氢化物低 |
| C.Z与W形成WZ,属于离子晶体可作耐高温材料 |
| D.简单离子半径:r(W)>r(Z)>r(Y) |
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式书写正确的是
A.泡沫灭火器反应原理:Al3++3HCO =3CO2↑+Al(OH)3↓ =3CO2↑+Al(OH)3↓ |
B.CuO溶于 溶液: 溶液: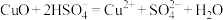 |
C.已知:酸性H2CO3>HClO> HCO ,则有ClO-+CO2+H2O=HClO+CO ,则有ClO-+CO2+H2O=HClO+CO |
D.向 溶液中通入 溶液中通入 : : |
您最近一年使用:0次



