名校
解题方法
1 . CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式分别为
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3kJ•mol-1,
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ•mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ•mol-1
(1)在深海中存在一种甲烷细菌,它们依靠甲烷与O2在酶的催化作用下产生的能量存活,在甲烷细菌使1mol甲烷转化为CO2气体与气态水的过程中,放出的能量___________ (填“>”“<”或“=”)890.3kJ。
(2)C(s)与H2(g)很难发生反应,所以C(s)+2H2(g)=CH4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H2(g)=CH4(g)的反应热ΔH =___________ 。
(3)甲烷与CO2可用于生产合成气,其成分是一氧化碳和氢气: 1gCH4完全反应可释放15.46kJ的热量。则:
①热化学方程式为___________
②若将物质的量均为1mol的CH4与CO2充入2L的恒容密闭容器中,体系放出的热量随着时间的变化曲线如下图所示,则CH4的转化率为___________ ;反应开始到此时用时5min,则CO2的反应速率为 ___________

(4)CH4、H2、CO等都是优质的能源物质,可以设计成燃料电池。下图是用于驱动潜艇的液氨-液氧燃料电池示意图。

①此原电池的负极是___________ (填“电极1”或“电极2”),电池工作一段时间后,电解质溶液的pH___________ (填“增大”或“减小”或“不变”)
②电极1的电极反应为___________ 。
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3kJ•mol-1,
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ•mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ•mol-1
(1)在深海中存在一种甲烷细菌,它们依靠甲烷与O2在酶的催化作用下产生的能量存活,在甲烷细菌使1mol甲烷转化为CO2气体与气态水的过程中,放出的能量
(2)C(s)与H2(g)很难发生反应,所以C(s)+2H2(g)=CH4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H2(g)=CH4(g)的反应热ΔH =
(3)甲烷与CO2可用于生产合成气,其成分是一氧化碳和氢气: 1gCH4完全反应可释放15.46kJ的热量。则:
①热化学方程式为
②若将物质的量均为1mol的CH4与CO2充入2L的恒容密闭容器中,体系放出的热量随着时间的变化曲线如下图所示,则CH4的转化率为

(4)CH4、H2、CO等都是优质的能源物质,可以设计成燃料电池。下图是用于驱动潜艇的液氨-液氧燃料电池示意图。

①此原电池的负极是
②电极1的电极反应为
您最近一年使用:0次
名校
解题方法
2 . 高铁酸钾(K2FeO4)是一种环保、高效饮水处理剂,利用铁屑制备的简略流程如图所示:

请回答下列问题:
(1)反应Ⅰ的生成物中可能含有的金属阳离子是___________ (用离子符号表示),如何检验该离子___________ 。
(2)操作A和操作B相同,其操作名称是___________ ;由操作B判断该生产条件下物质的溶解性:Na2FeO4___________ K2FeO4 (填“>”或“<”)。
(3)溶液C可与氯气反应制取漂白液,其离子方程式为___________ 。
(4)当生产过程中制得2mol的K2FeO4时,反应Ⅱ中转移的电子数为___________ 。
(5)反应Ⅱ中用到NaOH,若某同学做实验时要用到200mL 0.1mol/L NaOH溶液,现进行配制,则:
①配制该浓度的溶液需用托盘天平称量NaOH固体的质量为___________ g;
②配制过程中,下列操作导致所配溶液浓度偏大的是___________ (填标号)。
a.转移溶液时有少许液体溅出
b.溶解后,将溶液直接转移到容量瓶中
c.定容时俯视刻度线
d.定容摇匀后,发现液面下降,继续加水至刻度线

请回答下列问题:
(1)反应Ⅰ的生成物中可能含有的金属阳离子是
(2)操作A和操作B相同,其操作名称是
(3)溶液C可与氯气反应制取漂白液,其离子方程式为
(4)当生产过程中制得2mol的K2FeO4时,反应Ⅱ中转移的电子数为
(5)反应Ⅱ中用到NaOH,若某同学做实验时要用到200mL 0.1mol/L NaOH溶液,现进行配制,则:
①配制该浓度的溶液需用托盘天平称量NaOH固体的质量为
②配制过程中,下列操作导致所配溶液浓度偏大的是
a.转移溶液时有少许液体溅出
b.溶解后,将溶液直接转移到容量瓶中
c.定容时俯视刻度线
d.定容摇匀后,发现液面下降,继续加水至刻度线
您最近一年使用:0次
名校
解题方法
3 . 亚硝酸钙[ ]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
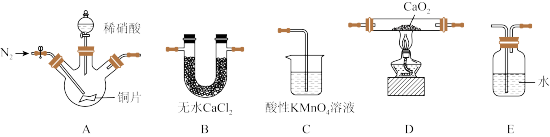
已知:①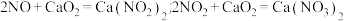
②酸性条件下, 能与
能与 溶液反应生成
溶液反应生成 和
和 。
。
请回答下列问题:
(1)上述装置按气流方向连接的顺序为___________ (填字母)。
(2)检查装置的气密性,装入药品,实验开始前通入一段时间 ,然后关闭弹簧夹,再滴加稀硝酸,通入
,然后关闭弹簧夹,再滴加稀硝酸,通入 的作用是
的作用是___________ 。
(3)A装置中反应的化学方程式为___________ 。
(4)B装置的作用是___________ ;E装置的作用是___________ 。
(5)C装置中反应的离子方程式为___________ 。
(6)工业上可用石灰乳和硝酸工业的尾气(含 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 ,反应原理为:
,反应原理为: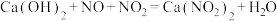 。若
。若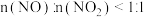 ,则会导致
,则会导致___________ 。
 ]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。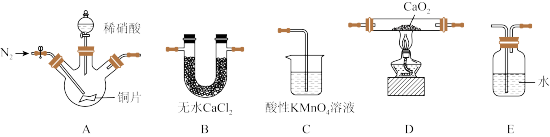
已知:①
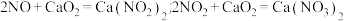
②酸性条件下,
 能与
能与 溶液反应生成
溶液反应生成 和
和 。
。请回答下列问题:
(1)上述装置按气流方向连接的顺序为
(2)检查装置的气密性,装入药品,实验开始前通入一段时间
 ,然后关闭弹簧夹,再滴加稀硝酸,通入
,然后关闭弹簧夹,再滴加稀硝酸,通入 的作用是
的作用是(3)A装置中反应的化学方程式为
(4)B装置的作用是
(5)C装置中反应的离子方程式为
(6)工业上可用石灰乳和硝酸工业的尾气(含
 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 ,反应原理为:
,反应原理为: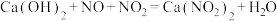 。若
。若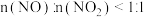 ,则会导致
,则会导致
您最近一年使用:0次
名校
解题方法
4 . I.化学研究的物质多种多样,按要求回答下列问题:
(1)过二硫酸钠( )可以看成过氧化氢的衍生物,
)可以看成过氧化氢的衍生物, 分子中的两个H原子被磺酸基(
分子中的两个H原子被磺酸基(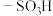 )替换后即为过二硫酸。
)替换后即为过二硫酸。
① 中硫元素的化合价为
中硫元素的化合价为___________ 。
②写出 的电子式
的电子式___________ 。
(2)硫代硫酸钠( )又名大苏打,造纸工业用作纸浆漂白后的除氯剂。
)又名大苏打,造纸工业用作纸浆漂白后的除氯剂。
① 在中性与碱性溶液中很稳定,遇酸则迅速反应。
在中性与碱性溶液中很稳定,遇酸则迅速反应。 溶液中加入稀硫酸时反应的离子方程式为
溶液中加入稀硫酸时反应的离子方程式为 ___________ 。
② 常用于防毒面具中吸收
常用于防毒面具中吸收 。若2 mol
。若2 mol  完全反应,失去16 mol电子,则其水溶液吸收
完全反应,失去16 mol电子,则其水溶液吸收 的离子方程式为
的离子方程式为___________ 。
II.自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。已知:ClO2是极易溶于水的气体,具有强氧化性,可以杀菌消毒。
用如图装置探究ClO2性质,回答下列问题:
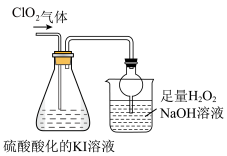
(3)锥形瓶内ClO2进气导管不伸入液面以下,原因是___________ 。烧杯内液体用于吸收尾气,若反应的氧化产物是一种单质,且还原剂与氧化剂的物质的量之比是1: 2,则还原产物是___________ (填化学式)。
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。若ClO2的还原产物为Cl-,则ClO2的有效氯含量为___________ 。(保留2位小数)
(1)过二硫酸钠(
 )可以看成过氧化氢的衍生物,
)可以看成过氧化氢的衍生物, 分子中的两个H原子被磺酸基(
分子中的两个H原子被磺酸基(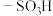 )替换后即为过二硫酸。
)替换后即为过二硫酸。①
 中硫元素的化合价为
中硫元素的化合价为②写出
 的电子式
的电子式(2)硫代硫酸钠(
 )又名大苏打,造纸工业用作纸浆漂白后的除氯剂。
)又名大苏打,造纸工业用作纸浆漂白后的除氯剂。①
 在中性与碱性溶液中很稳定,遇酸则迅速反应。
在中性与碱性溶液中很稳定,遇酸则迅速反应。 溶液中加入稀硫酸时反应的离子方程式为
溶液中加入稀硫酸时反应的离子方程式为 ②
 常用于防毒面具中吸收
常用于防毒面具中吸收 。若2 mol
。若2 mol  完全反应,失去16 mol电子,则其水溶液吸收
完全反应,失去16 mol电子,则其水溶液吸收 的离子方程式为
的离子方程式为II.自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。已知:ClO2是极易溶于水的气体,具有强氧化性,可以杀菌消毒。
用如图装置探究ClO2性质,回答下列问题:

(3)锥形瓶内ClO2进气导管不伸入液面以下,原因是
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。若ClO2的还原产物为Cl-,则ClO2的有效氯含量为
您最近一年使用:0次
名校
5 . 将2 mol X和2 mol Y充入2 L密闭容器中发生如下反应:X(g)+3Y(g) = 2Z(g)+aQ(g),经过2 min后,生成0.8 mol Z,Q的浓度为0.4 mol·L-1,下列叙述错误的是
| A.a的值为2 | B.反应速率v(Y)=0.3 mol·(L·min)-1 |
| C.X的转化率为20% | D.2 min后,X的浓度为0.2 mol·L-1 |
您最近一年使用:0次
名校
解题方法
6 . 一种高性价比的液流电池,其工作原理为在充放电过程中,在液泵推动下,电解液[KOH、K2Zn(OH)4]不断流动,发生以下反应:Zn+2NiOOH+2H2O+2OH- Zn(OH)
Zn(OH) +2Ni(OH)2,
+2Ni(OH)2,

下列说法错误的是
 Zn(OH)
Zn(OH) +2Ni(OH)2,
+2Ni(OH)2,
下列说法错误的是
| A.放电时,电极B发生还原反应 |
| B.储液罐中KOH浓度减小时,OH-移向电极A |
| C.充电时,电极B的电极反应式: OH- + Ni(OH)2 - e- = NiOOH + H2O |
| D.放电时,电子由电极A经电解质溶液转移至电极B |
您最近一年使用:0次
7 . 纳米级 Fe3O4可用于以太阳能为热源分解水制 H2,过程如图所示,下列说法中不正确的是


| A.Fe3O4、FeO 两者都是以太阳能为热源分解水制 H2过程中的催化剂 |
B.过程 I 的反应:2Fe3O4 6FeO+O2↑ 6FeO+O2↑ |
C.过程 I、Ⅱ的总反应:2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
| D.整个过程实现了太阳能向化学能的转化 |
您最近一年使用:0次
名校
8 . 用所给试剂与图示装置能够制取相应气体的是(夹持仪器略)


| A | B | C | D | |
| X 中试剂 | 浓盐酸 | 浓硝酸 | 双氧水 | 浓氨水 |
| Y 中试剂 | MnO2 | Cu | MnO2 | CaO |
| 气体 | Cl2 | NO2 | O2 | NH3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 下列是对某气体或溶液中离子进行检测的方法和结论,其中正确的是
| A.将某气体通入品红溶液,若品红溶液褪色,则气体中一定含有SO2 |
B.取样,先加入盐酸酸化,无现象,再加入 BaCl2溶液,若产生白色沉淀,则溶液中含 |
| C.取样,加入氯水,再加入KSCN溶液,若出现红色,则溶液中含有Fe2+ |
| D.取样,加入适量盐酸酸化,再加入 AgNO3溶液,若产生白色沉淀,则含 Cl- |
您最近一年使用:0次
名校
解题方法
10 . 下图为 分子在催化剂的作用下发生的一系列转化示意图:
分子在催化剂的作用下发生的一系列转化示意图:

下列叙述错误的是
 分子在催化剂的作用下发生的一系列转化示意图:
分子在催化剂的作用下发生的一系列转化示意图:
下列叙述错误的是
A.反应①属于氮的固定;反应②可用于工业上合成 |
| B.在催化剂a、b的作用下,降低反应活化能,改变反应的热效应 |
C. 与 与 反应生成 反应生成 的原子利用率为100% 的原子利用率为100% |
| D.在反应①和反应②中,均有极性共价键形成,并且反应①中的氮原子发生了还原反应,而反应②中的氮原子发生了氧化反应 |
您最近一年使用:0次



