名校
解题方法
1 . 用 催化还原
催化还原 可以消除氮氧化物的污染。已知:
可以消除氮氧化物的污染。已知:
①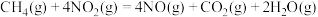

②

下列说法错误的是
 催化还原
催化还原 可以消除氮氧化物的污染。已知:
可以消除氮氧化物的污染。已知:①
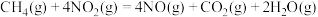

②


下列说法错误的是
| A.反应①②中,相同物质的量的甲烷发生反应,转移的电子数相同。 |
B.若用标准状况下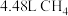 还原 还原 生成 生成 、 、 和 和 ,则放出的热量为 ,则放出的热量为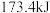 。 。 |
C.由反应①可知:  。 。 |
D.已知 的燃烧热为 的燃烧热为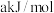 ,由 ,由 组成的混合物 组成的混合物 ,完全燃烧并恢复到常温时放出的热量为 ,完全燃烧并恢复到常温时放出的热量为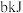 ,则 ,则 的燃烧热为 的燃烧热为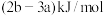 。 。 |
您最近一年使用:0次
2024-05-21更新
|
234次组卷
|
4卷引用: 重庆市第一中学校2022-2023学年高一下学期期中考试化学试题
名校
解题方法
2 . 甲醇制丙烯的反应为:
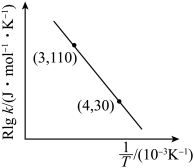
 ,已知:速率常数k与反应温度T、活化能
,已知:速率常数k与反应温度T、活化能 之间满足关系:
之间满足关系: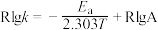 (R和A为常数)。下列说法错误的是
(R和A为常数)。下列说法错误的是

 ,已知:速率常数k与反应温度T、活化能
,已知:速率常数k与反应温度T、活化能 之间满足关系:
之间满足关系: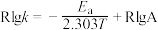 (R和A为常数)。下列说法错误的是
(R和A为常数)。下列说法错误的是
A.加催化剂不能减小 |
| B.升温能改变该反应的速率常数k |
C.已知 、 、 的燃烧热可以计算该反应的 的燃烧热可以计算该反应的 |
D.若实验得出Rlgk和 的关系如图,可计算该反应的活化能 的关系如图,可计算该反应的活化能 为 为 |
您最近一年使用:0次
2024-01-21更新
|
165次组卷
|
5卷引用:重庆市南开中学校2023-2024学年高三上学期10月月考化学试题
重庆市南开中学校2023-2024学年高三上学期10月月考化学试题重庆市2024届高三上学期第二次质量检测化学试题黑龙江省大庆实验中学实验三部2023-2024学年高三上学期阶段考试(二)化学试题河南省南阳市第一中学校2023-2024学年高二下学期开学考试化学试题 (已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
解题方法
3 . 亚硝酸钙 是白色粉末、易潮解、易溶于水,在钢筋混凝土工程中,常用作水泥硬化促进剂和防冻阻锈剂。实验用
是白色粉末、易潮解、易溶于水,在钢筋混凝土工程中,常用作水泥硬化促进剂和防冻阻锈剂。实验用 与
与 制备亚硝酸钙装置如图所示(夹持装置已略去)。
制备亚硝酸钙装置如图所示(夹持装置已略去)。
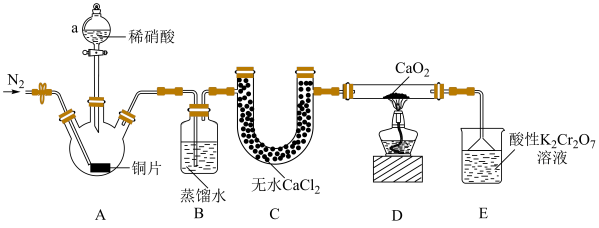
回答下列问题:
(1)盛装稀硝酸的仪器 名称为
名称为________ 。
(2)加入稀硝酸之前需通入一段时间 ,其目的是
,其目的是________ 。
(3)装置A中反应的化学方程式为________ 。
(4)上述装置有一处明显不足,会导致亚硝酸钙产率降低,改进的方法是________ 。
(5)此法制得的亚硝酸钙中常含有硝酸钙杂质,现用如下方法测定产品中硝酸钙的含量。
实验原理:



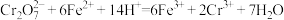
实验步骤:
Ⅰ.称量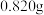 产品溶于水,加入足量的硫酸钠固体,充分搅拌后过滤;
产品溶于水,加入足量的硫酸钠固体,充分搅拌后过滤;
Ⅱ.将滤液配制成 溶液,取
溶液,取 溶液于锥形瓶中,加入足量
溶液于锥形瓶中,加入足量 饱和溶液,煮沸
饱和溶液,煮沸 ,冷却;
,冷却;
Ⅲ.再向锥形瓶中加入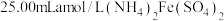 溶液和适量硫酸;
溶液和适量硫酸;
Ⅳ.加入4滴指示剂,用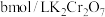 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 。
。
①步骤Ⅳ中盛装 标准溶液的仪器名称是
标准溶液的仪器名称是________ 。
②所得产品中硝酸钙的质量分数为________
③下列操作会导致硝酸钙的质量分数测定结果偏高的是________ 。
A.盛装 标准液前未用
标准液前未用 标准液润洗滴定管
标准液润洗滴定管
B.滴定时振荡太剧烈,使锥形瓶中液体溅出
C.达到滴定终点时,仰视读数
 是白色粉末、易潮解、易溶于水,在钢筋混凝土工程中,常用作水泥硬化促进剂和防冻阻锈剂。实验用
是白色粉末、易潮解、易溶于水,在钢筋混凝土工程中,常用作水泥硬化促进剂和防冻阻锈剂。实验用 与
与 制备亚硝酸钙装置如图所示(夹持装置已略去)。
制备亚硝酸钙装置如图所示(夹持装置已略去)。
回答下列问题:
(1)盛装稀硝酸的仪器
 名称为
名称为(2)加入稀硝酸之前需通入一段时间
 ,其目的是
,其目的是(3)装置A中反应的化学方程式为
(4)上述装置有一处明显不足,会导致亚硝酸钙产率降低,改进的方法是
(5)此法制得的亚硝酸钙中常含有硝酸钙杂质,现用如下方法测定产品中硝酸钙的含量。
实验原理:



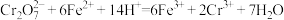
实验步骤:
Ⅰ.称量
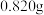 产品溶于水,加入足量的硫酸钠固体,充分搅拌后过滤;
产品溶于水,加入足量的硫酸钠固体,充分搅拌后过滤;Ⅱ.将滤液配制成
 溶液,取
溶液,取 溶液于锥形瓶中,加入足量
溶液于锥形瓶中,加入足量 饱和溶液,煮沸
饱和溶液,煮沸 ,冷却;
,冷却;Ⅲ.再向锥形瓶中加入
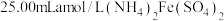 溶液和适量硫酸;
溶液和适量硫酸;Ⅳ.加入4滴指示剂,用
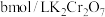 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 。
。①步骤Ⅳ中盛装
 标准溶液的仪器名称是
标准溶液的仪器名称是②所得产品中硝酸钙的质量分数为
③下列操作会导致硝酸钙的质量分数测定结果偏高的是
A.盛装
 标准液前未用
标准液前未用 标准液润洗滴定管
标准液润洗滴定管B.滴定时振荡太剧烈,使锥形瓶中液体溅出
C.达到滴定终点时,仰视读数
您最近一年使用:0次
名校
解题方法
4 . 向一恒容密闭容器中加入 A和一定量的B,发生反应:
A和一定量的B,发生反应: 。A的平衡转化率
。A的平衡转化率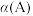 按不同投料比
按不同投料比 [
[  ]随温度的变化曲线如图所示。下列说法错误的是
]随温度的变化曲线如图所示。下列说法错误的是
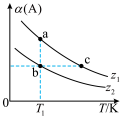
 A和一定量的B,发生反应:
A和一定量的B,发生反应: 。A的平衡转化率
。A的平衡转化率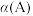 按不同投料比
按不同投料比 [
[  ]随温度的变化曲线如图所示。下列说法错误的是
]随温度的变化曲线如图所示。下列说法错误的是
A.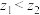 | B. 温度下,B的平衡转化率:a点 温度下,B的平衡转化率:a点 点 点 |
C.反应速率: | D.点a、b、c对应的平衡常数: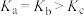 |
您最近一年使用:0次
名校
解题方法
5 . 高分子M广泛用于牙膏等口腔护理产品,合成路线如下图:
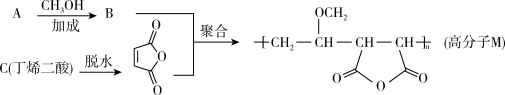
下列说法正确的是

下列说法正确的是
| A.物质A是乙烯 | B.丁烯二酸分子中最多有12个原子共面 |
| C.合成M的聚合反应是缩聚反应 | D. D在一定条件下最多能与 D在一定条件下最多能与  加成 加成 |
您最近一年使用:0次
名校
解题方法
6 . 主要成分为 的工业废气的回收利用有重要意义。
的工业废气的回收利用有重要意义。
Ⅰ.克劳斯工艺
(1)将占 总量约
总量约___________ 的 燃烧,产生的
燃烧,产生的 与其余
与其余 混合后反应回收单质硫
混合后反应回收单质硫 (x为2~8)。
(x为2~8)。
Ⅱ.湿法脱硫
(2)当废气中硫化氢浓度较低时常用纯碱溶液进行吸收,已知 、
、 的电离平衡常数如下表所示:
的电离平衡常数如下表所示:
纯碱溶液吸收少量 的离子方程式为
的离子方程式为___________ 。
Ⅲ.热解 制
制
一种热解 的方法是将
的方法是将 、
、 按一定比例混合,并用Ar稀释,通入管式气体反应器热解(一边进料,另一边出料),反应分两步进行:
按一定比例混合,并用Ar稀释,通入管式气体反应器热解(一边进料,另一边出料),反应分两步进行:
第一步
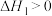
第二步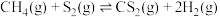

常压,不同温度下反应相同时间后,测得生成的 、
、 和
和 体积分数如图(a):
体积分数如图(a):
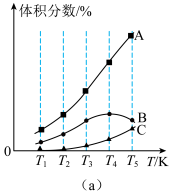
(3)A、B、C三条曲线中表示 的是
的是______ 。
(4)判断下列说法不正确的是___________(填序号)。
(5) 温度下,在恒压密闭容器中按
温度下,在恒压密闭容器中按 充入混合气体发生上述第一步反应,测得平衡时
充入混合气体发生上述第一步反应,测得平衡时 、
、 的体积分数相等。若起始压强为
的体积分数相等。若起始压强为 ,则
,则 温度下,
温度下, 平衡转化率为
平衡转化率为___________ ,平衡常数
___________ 。
(6)回收的硫单质可以用于制钠—硫电池。一种室温钠—硫电池的结构如图(b)所示,电解质为含 的离子液体。工作时,电池总反应为
的离子液体。工作时,电池总反应为 。
。

①放电时正极的电极反应为___________ 。
②若放电过程中硫电极只检测到 、
、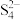 的生成,当硫单质反应16g,电路中转移
的生成,当硫单质反应16g,电路中转移 电子时,生成的
电子时,生成的 、
、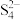 的个数比是
的个数比是______ 。
 的工业废气的回收利用有重要意义。
的工业废气的回收利用有重要意义。Ⅰ.克劳斯工艺
(1)将占
 总量约
总量约 燃烧,产生的
燃烧,产生的 与其余
与其余 混合后反应回收单质硫
混合后反应回收单质硫 (x为2~8)。
(x为2~8)。Ⅱ.湿法脱硫
(2)当废气中硫化氢浓度较低时常用纯碱溶液进行吸收,已知
 、
、 的电离平衡常数如下表所示:
的电离平衡常数如下表所示:| 电离平衡常数 |  |  |
 |  | 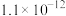 |
 | 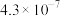 | 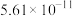 |
 的离子方程式为
的离子方程式为Ⅲ.热解
 制
制
一种热解
 的方法是将
的方法是将 、
、 按一定比例混合,并用Ar稀释,通入管式气体反应器热解(一边进料,另一边出料),反应分两步进行:
按一定比例混合,并用Ar稀释,通入管式气体反应器热解(一边进料,另一边出料),反应分两步进行:第一步

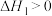
第二步
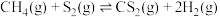

常压,不同温度下反应相同时间后,测得生成的
 、
、 和
和 体积分数如图(a):
体积分数如图(a):
(3)A、B、C三条曲线中表示
 的是
的是(4)判断下列说法不正确的是___________(填序号)。
| A.上述两个反应都能在高温条件下自发进行 |
| B.适当的高温有利于增大反应速率和反应物转化率 |
C. ,增大 ,增大 的投料量, 的投料量, 的转化率一定增大 的转化率一定增大 |
D.恒温恒压下,增加Ar的体积分数, 的浓度升高 的浓度升高 |
(5)
 温度下,在恒压密闭容器中按
温度下,在恒压密闭容器中按 充入混合气体发生上述第一步反应,测得平衡时
充入混合气体发生上述第一步反应,测得平衡时 、
、 的体积分数相等。若起始压强为
的体积分数相等。若起始压强为 ,则
,则 温度下,
温度下, 平衡转化率为
平衡转化率为
(6)回收的硫单质可以用于制钠—硫电池。一种室温钠—硫电池的结构如图(b)所示,电解质为含
 的离子液体。工作时,电池总反应为
的离子液体。工作时,电池总反应为 。
。
①放电时正极的电极反应为
②若放电过程中硫电极只检测到
 、
、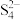 的生成,当硫单质反应16g,电路中转移
的生成,当硫单质反应16g,电路中转移 电子时,生成的
电子时,生成的 、
、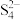 的个数比是
的个数比是
您最近一年使用:0次
名校
解题方法
7 . 以红土镍矿(含Ni、Co、Fe、Al、Si等元素的氧化物)为原料制备硫酸镍的工艺受到越来越多的关注,其流程如下:
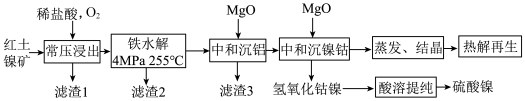
已知:①氢氧化物
②氢氧化铁在高温下不稳定,200℃左右会分解为 。
。
③ 的摩尔质量
的摩尔质量 。
。
回答下列问题:
(1)为提高浸出效率,可以采取___________ 措施(写出两条)。
(2)“铁水解”过程能实现金属的选择性浸出,写出该过程的化学方程式:___________ 。
(3)常温下,若浸取液中各离子浓度均为 ,为保证去除效率,沉铝时应控制溶液的pH为
,为保证去除效率,沉铝时应控制溶液的pH为___________ 。(当溶液中某离子浓度 时,可认为该离子沉淀完全)
时,可认为该离子沉淀完全)
(4)通过“中和沉钴镍”后,进一步酸溶、提纯可得到硫酸镍。由1kg红土镍矿经工艺处理后镍的浸取率约为95%,再经后续一系列处理可得到37.44g的硫酸镍,原红土镍矿中镍元素的质量分数为___________ %(结果保留两位有效数字)。
(5)“热解再生”可产生的两种物质是___________ 。(填化学式)
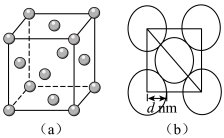
(6)金属镍的晶胞结构如图(a)所示,晶胞中镍原子可看作刚性圆球,位于面对角线上的镍原子彼此相切如图(b)所示。晶胞中,每个Ni原子周围紧邻的Ni原子数为___________ ;若Ni的原子半径为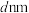 ,晶胞中Ni原子空间利用率的计算表达式为
,晶胞中Ni原子空间利用率的计算表达式为___________ (空间利用率 )。
)。

已知:①氢氧化物

| 氢氧化物 |  |  |  |  |
 |  | 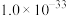 | 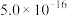 |  |
 。
。③
 的摩尔质量
的摩尔质量 。
。回答下列问题:
(1)为提高浸出效率,可以采取
(2)“铁水解”过程能实现金属的选择性浸出,写出该过程的化学方程式:
(3)常温下,若浸取液中各离子浓度均为
 ,为保证去除效率,沉铝时应控制溶液的pH为
,为保证去除效率,沉铝时应控制溶液的pH为 时,可认为该离子沉淀完全)
时,可认为该离子沉淀完全)(4)通过“中和沉钴镍”后,进一步酸溶、提纯可得到硫酸镍。由1kg红土镍矿经工艺处理后镍的浸取率约为95%,再经后续一系列处理可得到37.44g的硫酸镍,原红土镍矿中镍元素的质量分数为
(5)“热解再生”可产生的两种物质是
(6)金属镍的晶胞结构如图(a)所示,晶胞中镍原子可看作刚性圆球,位于面对角线上的镍原子彼此相切如图(b)所示。晶胞中,每个Ni原子周围紧邻的Ni原子数为
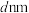 ,晶胞中Ni原子空间利用率的计算表达式为
,晶胞中Ni原子空间利用率的计算表达式为 )。
)。
您最近一年使用:0次
名校
8 . 标准状态下,下列微粒气态时的相对能量如下表:
依据表中数据,下列说法正确的是
| 物质(g) | O | H | 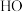 |  |  |  |  |  |
能量 | 249 | 218 | 39 | 0 | 0 | 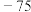 |  | 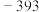 |
A. 的燃烧热 的燃烧热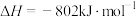 |
B.反应: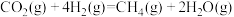 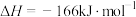 |
C. 的键能为 的键能为 |
D.已知: 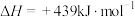 ,则 ,则 的键能是 的键能是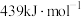 |
您最近一年使用:0次
名校
9 . 下列说法正确的是
A.  的醋酸溶液稀释至 的醋酸溶液稀释至 ,稀释后溶液的 ,稀释后溶液的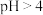 |
B.弱电解质 的稀溶液在加水稀释的过程中, 的稀溶液在加水稀释的过程中,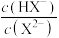 逐渐增大 逐渐增大 |
C. 溶液中的粒子浓度关系: 溶液中的粒子浓度关系: |
D.反应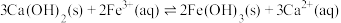 的平衡常数 的平衡常数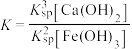 |
您最近一年使用:0次
名校
解题方法
10 . Al元素可以形成多种类型的物质。例如AlCr2晶体具有体心四方结构,如图(a)所示;AlN晶胞结构如图(b)所示;气态AlCl3通常以二聚体Al2Cl6形式存在,其空间结构如图(c)所示。下列说法正确的是
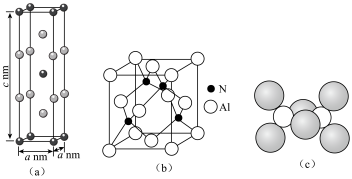

A.基态铬原子的核外电子排布式为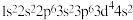 |
B.AlCr2晶体的密度为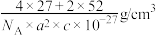 |
| C.AlN中各原子均未达到8电子稳定结构 |
D.二聚体Al2Cl6中Al的轨道杂化类型为 |
您最近一年使用:0次



