1 . 某烃与H2反应后能生成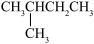 ,则该烃不可能是
,则该烃不可能是
A.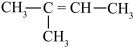 | B.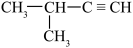 |
C.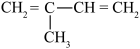 | D.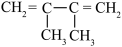 |
您最近一年使用:0次
2024-04-27更新
|
301次组卷
|
10卷引用:四川省华蓥中学2022-2023学年高一下学期5月月考化学试题
四川省华蓥中学2022-2023学年高一下学期5月月考化学试题北京市第三十五中学2022-2023学年高二下学期期中考试化学试题北京市西城区2021-2022学年高二下学期期末化学试题北京师范大学第二附属中学2023-2024学年高二下学期期中考试化学试题名校期中好题汇编-烃(选择题)2.2.1 烯烃 随堂练习(已下线)清单05 烃(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)北京市宣武外国语实验学校2023-2024学年高二下学期期中考试化学试题北京市铁路第二中学2023-2024学年高二下学期期中考试化学试题北京市顺义区第一中学2023-2024学年高二下学期期中考试化学试题
2 . 25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)HCOOH、H2CO3、HCN的酸性由强到弱的顺序为___________ 。
(2)向Na2CO3溶液中加入足量HCN,反应的离子方程式为___________ 。
(3)写出HCOONa溶液中的电荷守恒式___________ 。
(4)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.00mol/L的NaOH标准溶液滴定:
①用NaOH固体配置100mL,1.00mol/L的NaOH溶液,需要用到的仪器除托盘天平,药匙,烧杯,玻璃棒,胶头滴管,还必须要___________ 。
②实验过程中,将25.00mLHCOOH放入锥形瓶,滴入酚酞2-3滴;NaOH溶液应装___________ 入(填“酸式滴定管”或“碱式滴定管”);滴定过程中,眼睛应注视___________ 。
③连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为___________ mL。
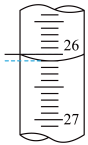
④某学生根据3次实验分别记录有关数据如下表:
依据上表数据计算该HCOOH溶液的物质的量浓度为___________ mol/L(计算结果保留到小数点后两位)。
⑤下列操作中可能使所测HCOOH溶液的浓度数值偏低的是___________ (填字母)。
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
| 化学式 | HCOOH | H2CO3 | HCN |
| 电离平衡常数 | 1.5×10-4 | Ka1=4.2×10-7 Ka2=4.9×10-11 | 3.0×10-8 |
(1)HCOOH、H2CO3、HCN的酸性由强到弱的顺序为
(2)向Na2CO3溶液中加入足量HCN,反应的离子方程式为
(3)写出HCOONa溶液中的电荷守恒式
(4)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.00mol/L的NaOH标准溶液滴定:
①用NaOH固体配置100mL,1.00mol/L的NaOH溶液,需要用到的仪器除托盘天平,药匙,烧杯,玻璃棒,胶头滴管,还必须要
②实验过程中,将25.00mLHCOOH放入锥形瓶,滴入酚酞2-3滴;NaOH溶液应装
③连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为

④某学生根据3次实验分别记录有关数据如下表:
| 实验序号 | 待测HCOOH溶液体积/mL | 1.00mol/LNaOH的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液的体积 | ||
| 1 | 25.00 | 0.00 | 12.49 | V1 |
| 2 | 25.00 | 0.56 | 14.56 | V2 |
| 3 | 25.00 | 0.22 | 12.73 | V3 |
⑤下列操作中可能使所测HCOOH溶液的浓度数值偏低的是
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
您最近一年使用:0次
解题方法
3 . 广安代市镇火力发电厂需要燃烧大量的煤,产生大量CO2和SO2等,并留下大量煤渣,对环境有较大影响。其中一种不能继续燃烧的煤渣成分俗名叫“铁甲石”,主要成分为:Al2O3(15%~24%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)、FeO(0.9%~2.0%)、CuO(8.5%~11.0%)以及其他不溶性杂质,铁甲石中的氧化铝难溶于酸,可以通过煅烧改变铁甲石结构,使其溶于酸。铁甲石经过下列化工工艺,可以制取无水CuCl2。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
(1)第一次过滤的滤渣为___________ 。
(2)加H2O2后发生反应的离子方程式为___________ 。
(3)调节溶液pH需要控制的范围是___________ ,“调节溶液pH”的过程中除添加试剂,还需借助于___________ 测定溶液pH值。
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
(5)从滤液2中得到无水CuCl2的操作为___________ 。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| 开始沉淀pH | 5.8 | 5.8 | 2.0 | 4.0 |
| 沉淀完成pH | 7.5 | 8.3 | 3.1 | 5.4 |
(1)第一次过滤的滤渣为
(2)加H2O2后发生反应的离子方程式为
(3)调节溶液pH需要控制的范围是
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
| A.氢氧化钠 | B.氨水 | C.CuO | D.AlCl3 |
(5)从滤液2中得到无水CuCl2的操作为
您最近一年使用:0次
4 . 认真观察下列装置,回答下列问题:
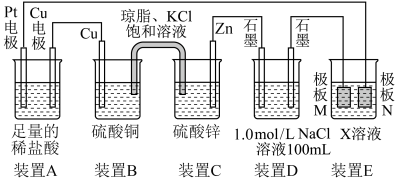
(1)C装置中,Zn电极叫___________ (填“正极”或“负极”);电极方程式为___________ ;盐桥中K+的移动方向___________ (填“向左”、“向右”或“不移动”)。
(2)电池工作初期,A装置中总反应的离子方程式为___________ 。
(3)若装置E中的目的是在Cu材料上镀Ag,则X溶液中的溶质为___________ ,极板M的材料为___________ 。
(4)当装置A中Cu电极质量改变12.8g时,则装置D中产生的气体体积为___________ L(标准状况下)。

(1)C装置中,Zn电极叫
(2)电池工作初期,A装置中总反应的离子方程式为
(3)若装置E中的目的是在Cu材料上镀Ag,则X溶液中的溶质为
(4)当装置A中Cu电极质量改变12.8g时,则装置D中产生的气体体积为
您最近一年使用:0次
5 . 已知NO2(g)+CO(g) NO(g)+CO2(g) ΔH=-230kJ/mol,下图是恒容密闭容器中,该反应CO和NO的浓度随时间变化的示意图。根据图意回答下列问题:
NO(g)+CO2(g) ΔH=-230kJ/mol,下图是恒容密闭容器中,该反应CO和NO的浓度随时间变化的示意图。根据图意回答下列问题:
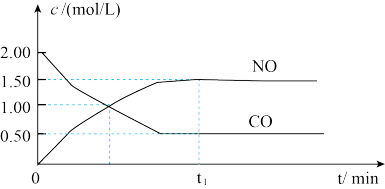
(1)该反应是___________ 反应(填“放热”或“吸热”)。
(2)从反应开始到平衡,用NO2浓度变化表示平均反应速率v(NO2)=___________ 。
(3)此温度下,该反应的平衡常数表达式K=___________ ;温度降低,K___________ (填“变大”、“变小”或“不变”)。
(4)下列条件或者现象能判断该反应一定达到平衡状态的是___________(填下列字母)。
(5)已知:
①CO(g)+ O2(g)=CO2(g) ΔH=−283.0kJ·mol−1
O2(g)=CO2(g) ΔH=−283.0kJ·mol−1
②S(s)+O2(g)=SO2(g) ΔH=−296.0kJ·mol−1
处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为固态单质S。此反应的热化学方程式是___________ 。
 NO(g)+CO2(g) ΔH=-230kJ/mol,下图是恒容密闭容器中,该反应CO和NO的浓度随时间变化的示意图。根据图意回答下列问题:
NO(g)+CO2(g) ΔH=-230kJ/mol,下图是恒容密闭容器中,该反应CO和NO的浓度随时间变化的示意图。根据图意回答下列问题:
(1)该反应是
(2)从反应开始到平衡,用NO2浓度变化表示平均反应速率v(NO2)=
(3)此温度下,该反应的平衡常数表达式K=
(4)下列条件或者现象能判断该反应一定达到平衡状态的是___________(填下列字母)。
| A.容器内颜色不再改变 | B.当c(NO)=c(CO2)时 |
| C.混合气体平均摩尔质量不再改变 | D.容器内压强不再改变 |
(5)已知:
①CO(g)+
 O2(g)=CO2(g) ΔH=−283.0kJ·mol−1
O2(g)=CO2(g) ΔH=−283.0kJ·mol−1②S(s)+O2(g)=SO2(g) ΔH=−296.0kJ·mol−1
处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为固态单质S。此反应的热化学方程式是
您最近一年使用:0次
6 . 下表中的实验操作不能达到实验目的或不能得出相应结论的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 配制FeCl3溶液时,加入少量稀盐酸 | 抑制Fe3+的水解 |
| B | 将醋酸溶液加入碳酸钙固体中有二氧化碳生成 | 醋酸酸性大于碳酸 |
| C | 向盛有5mL0.1mol/LNaOH溶液的试管中滴加2滴0.1mol/LMgCl2溶液,有白色沉淀生成,再滴加0.1mol/LFeCl3溶液,产生红褐色沉淀生成 | 常温下,Ksp(Mg(OH)2)>Ksp(Fe(OH)3) |
| D | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 广安最近严查酒驾,一种酸性燃料电池酒精检测仪如下图所示,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是
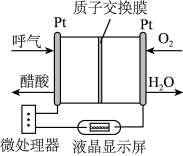

| A.电子由呼气所在的铂电极流出 |
| B.微处理器可以通过检测电流大小而计算出被测气体中酒精的含量 |
| C.该电池的负极反应式为:CH3CH2OH+H2O-4e-=CH3COOH+4H+ |
| D.O2所在的铂电极为电源负极 |
您最近一年使用:0次
8 . 在HF H++F-的电离平衡中,要使平衡右移且氢离子浓度减小,应采取的措施为
H++F-的电离平衡中,要使平衡右移且氢离子浓度减小,应采取的措施为
 H++F-的电离平衡中,要使平衡右移且氢离子浓度减小,应采取的措施为
H++F-的电离平衡中,要使平衡右移且氢离子浓度减小,应采取的措施为| A.升高温度 | B.加NaF固体 | C.加HF | D.加NaCl溶液 |
您最近一年使用:0次
解题方法
9 . 量程为50.00mL的酸式滴定管,滴定前凹液面停留在20.00mL,若把里面的液体全部放完,放出液体的体积
| A.大于30.00mL | B.小于30.00mL | C.等于20.00mL | D.等于30.00mL |
您最近一年使用:0次
解题方法
10 . 对于可逆反应2A(s)+B(g) C(g)+3D(g),下列措施一定可以增加该反应化学反应速率的是
C(g)+3D(g),下列措施一定可以增加该反应化学反应速率的是
 C(g)+3D(g),下列措施一定可以增加该反应化学反应速率的是
C(g)+3D(g),下列措施一定可以增加该反应化学反应速率的是| A.降低温度 | B.升高温度 | C.增加A的量 | D.及时移走产物D |
您最近一年使用:0次



