解题方法
1 . 氮、硫、碳的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系: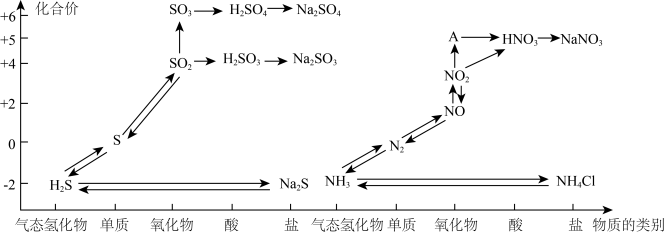
(1)根据A对应的化合价和物质类别,A为___________ (写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的化合物有____________ 。
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择________ ,反应的离子方程式为______________ 。
(3)某同学设计了如图所示的套管实验装置(部分装置未画出)来制备SO2并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4。回答下列问题:

①写出制取SO2的化学方程式:_______________ 。
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为_____ 。
A. 品红溶液 B. 酸性高锰酸钾溶液 C. 双氧水(H2O2)
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学反应方程式_______ 。
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2吸收Br2反应的化学方程式为____________ 。

(1)根据A对应的化合价和物质类别,A为
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(3)某同学设计了如图所示的套管实验装置(部分装置未画出)来制备SO2并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4。回答下列问题:

①写出制取SO2的化学方程式:
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为
A. 品红溶液 B. 酸性高锰酸钾溶液 C. 双氧水(H2O2)
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学反应方程式
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2吸收Br2反应的化学方程式为
您最近一年使用:0次
2020-05-29更新
|
732次组卷
|
2卷引用:第五章 化工生产中的重要非金属元素 单元测试
名校
2 . 某实验小组为探究酸性条件下碘化钾与过氧化氧反应的化学反应速率,进行了以下实验探究。
(1)实验一:向硫酸酸化的过氧化氢溶液中加入碘化钾、淀粉和硫代硫酸钠( )的混合溶液,一段时间后溶液变蓝。该小组查阅资料知体系中存在下列两个主要反应:
)的混合溶液,一段时间后溶液变蓝。该小组查阅资料知体系中存在下列两个主要反应:
反应ⅰ: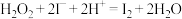 ;
;
反应ⅱ: 。
。
为了证实上述反应过程,进行下列实验(所用试剂浓度均为 )
)
实验二:向酸化的 溶液中加入淀粉KI溶液,溶液几秒后变为蓝色。再向已经变蓝的溶液中加入
溶液中加入淀粉KI溶液,溶液几秒后变为蓝色。再向已经变蓝的溶液中加入 溶液,溶液立即褪色。
溶液,溶液立即褪色。
根据此现象可知反应ⅰ的速率_______ 反应ⅱ的速率(填“大于”、“小于”或“等于”),解释实验一中溶液混合一段时间后才变蓝的原因是_______ 。
(2)为了探究 对反应速率的影响,设计两组对比实验,按下表中的试剂用量将其迅速混合观察现象。(各实验均在室温条件下进行)
对反应速率的影响,设计两组对比实验,按下表中的试剂用量将其迅速混合观察现象。(各实验均在室温条件下进行)
①V1=_______ ,V2=_______ 。
②对比实验I和实验II,
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)利用实验I的数据,计算反应ⅱ在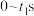 的化学反应速率
的化学反应速率
_______  ;反应ⅰ在
;反应ⅰ在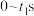 的化学反应速率
的化学反应速率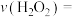
_______ 
(1)实验一:向硫酸酸化的过氧化氢溶液中加入碘化钾、淀粉和硫代硫酸钠(
 )的混合溶液,一段时间后溶液变蓝。该小组查阅资料知体系中存在下列两个主要反应:
)的混合溶液,一段时间后溶液变蓝。该小组查阅资料知体系中存在下列两个主要反应:反应ⅰ:
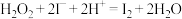 ;
;反应ⅱ:
 。
。为了证实上述反应过程,进行下列实验(所用试剂浓度均为
 )
)实验二:向酸化的
 溶液中加入淀粉KI溶液,溶液几秒后变为蓝色。再向已经变蓝的溶液中加入
溶液中加入淀粉KI溶液,溶液几秒后变为蓝色。再向已经变蓝的溶液中加入 溶液,溶液立即褪色。
溶液,溶液立即褪色。根据此现象可知反应ⅰ的速率
(2)为了探究
 对反应速率的影响,设计两组对比实验,按下表中的试剂用量将其迅速混合观察现象。(各实验均在室温条件下进行)
对反应速率的影响,设计两组对比实验,按下表中的试剂用量将其迅速混合观察现象。(各实验均在室温条件下进行)| 实验编号 | 试剂体积/mL | 溶液开始变蓝的时间/s | ||||
  |   |   |  KI(含淀粉) |  | ||
| I | 40 | 40 | 20 | 40 | 20 |  |
| II | V1 | 20 | 20 | 40 | V2 |  |
②对比实验I和实验II,

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)利用实验I的数据,计算反应ⅱ在
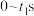 的化学反应速率
的化学反应速率
 ;反应ⅰ在
;反应ⅰ在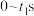 的化学反应速率
的化学反应速率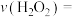

您最近一年使用:0次
2022-07-14更新
|
1321次组卷
|
5卷引用:第六章 化学反应与能量【单元测试B卷】
2023高一·全国·专题练习
解题方法
3 . 某实验小组利用压强传感器,数据采集器和计算机等数字化实验设备组成数据采集系统,探究外界条件对双氧水分解速率的影响。实验装置(下图)和所完成实验编号如下。请回答下列问题。
资料显示:通常情况下, 较稳定,不易分解。
较稳定,不易分解。
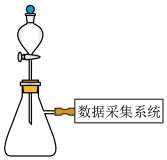
实验药品: ,热水、冰水。
,热水、冰水。
(1)用化学方程式表示实验原理_______ 。
(2)编号①和②的实验目的是_______ 。
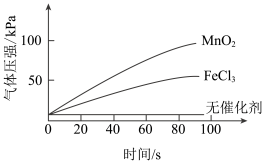
(3)编号③④⑤探究的是不同催化剂条件下双氧水的分解速率,实验结果如图所示。说明图中曲线的含义_______ 。结合实验条件,分析三条曲线的区别_______ 。
(4)模仿上述设计,完成“温度对化学反应速率的影响”的实验方案设计。
资料显示:通常情况下,
 较稳定,不易分解。
较稳定,不易分解。
实验药品:
 ,热水、冰水。
,热水、冰水。| 实验编号 | 实验药品 | 催化剂 |
| ① | 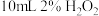 溶液 溶液 | 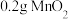 |
| ② | 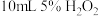 溶液 溶液 | 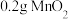 |
| ③ | 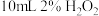 溶液 溶液 | 无催化剂 |
| ④ | 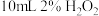 溶液 溶液 | 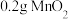 |
| ⑤ | 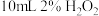 溶液 溶液 | 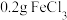 |
(2)编号①和②的实验目的是
(3)编号③④⑤探究的是不同催化剂条件下双氧水的分解速率,实验结果如图所示。说明图中曲线的含义

(4)模仿上述设计,完成“温度对化学反应速率的影响”的实验方案设计。
| 实验编号 | 实验药品 | 反应条件 |
您最近一年使用:0次
名校
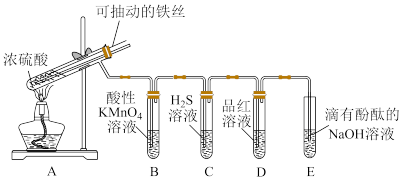
4 . 实验室为探究铁与足量浓硫酸的反应,并验证 的性质,设计如图所示装置进行实验,下列说法错误的是
的性质,设计如图所示装置进行实验,下列说法错误的是
 的性质,设计如图所示装置进行实验,下列说法错误的是
的性质,设计如图所示装置进行实验,下列说法错误的是
A.实验结束后,可取A中试管内的溶液稀释后滴加KSCN溶液检验是否有 |
B.B中溶液紫色褪去,C中生成淡黄色沉淀,均体现了 的还原性 的还原性 |
C.D中品红溶液褪色,体现了 的漂白性 的漂白性 |
D.E中溶液红色变浅,体现了 酸性氧化物的性质 酸性氧化物的性质 |
您最近一年使用:0次
2022-07-14更新
|
1882次组卷
|
5卷引用:第五章 化工生产中的重要非金属元素【单元测试B卷】
5 . 某学习小组设计的蔗糖水解反应如图所示(夹持装置省略)。下列说法错误的是( )
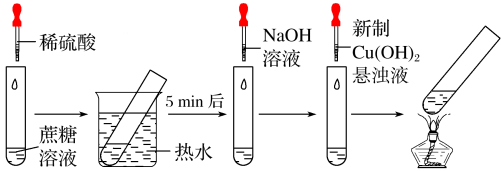

| A.稀硫酸和热水浴都能加快蔗糖水解速率 |
| B.滴加NaOH溶液的目的是调溶液的pH至碱性 |
| C.加热至沸腾后试管内生成黑色沉淀 |
| D.实验现象证明蔗糖水解有还原性物质生成 |
您最近一年使用:0次
2020-06-01更新
|
651次组卷
|
16卷引用:第四章 生物大分子(B卷)
(已下线)第四章 生物大分子(B卷)四川省宜宾市普通高中2020届高三高考适应性考试(三诊)理综-化学试题四川省攀枝花市第十五中学校2019-2020学年高二期末模拟考试化学试卷湖南省长沙县第九中学2019-2020学年高二下学期期末检测化学试题(已下线)4.2 糖类(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版选修5)江西省抚州市南城一中2020-2021学年高二下学期期中联考化学试题(已下线)考向31 生命中的的基础化学物质 有机合成高分子-备战2022年高考化学一轮复习考点微专题专题6 生命活动的物质基础——糖类、油脂、蛋白质 第一单元 糖类和油脂 第1课时 糖类第四章 本章复习提升山东省菏泽市单县第二中学2021-2022学年高二下学期四月月考化学试题(已下线)易错点30 大分子和高分子-备战2023年高考化学考试易错题(已下线)第一部分 二轮专题突破 专题19 有机选择题题型分析(已下线)第九章 有机化学基础 必做实验提升(七) 有机化合物中常见官能团的检验6.1.1糖类 课后黑龙江省双鸭山市第一中学2022-2023学年高二下学期期末考试化学试题河南省焦作市博爱县第一中学2022-2023学年高三下学期5月月考化学试题
名校
解题方法
6 . 某小组同学欲研究SO2及Na2S2O3的性质。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是_______ 。
(2)利用下图所示的装置研究SO2的性质:(熔点:SO2-76.1℃,SO316.8℃;沸点:SO2-10℃,SO345℃)

①装置I模拟工业生产中SO2催化氧化的反应,其化学方程式是_______ 。
②甲同学按I、II、III、IV的顺序连接装置,装置II的作用是_______ ;装置III中溶液逐渐褪色,生成Mn2+,则该反应的离子方程式是_______ 。
③乙同学按I、II、IV的顺序连接装置,若装置IV中有40mL2.5mol•L-1NaOH溶液,反应后增重4.8g,则装置IV中发生总反应的化学方程式_______ 。
(3)已知Na2S2O3溶液与Cl2反应时,1molNa2S2O3转移8mol电子。该反应的离子方程式是_______ 。甲同学设计如下实验流程探究Na2S2O3的化学性质。
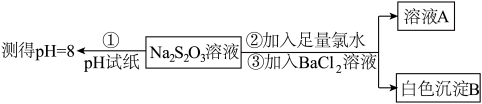
(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和_______ 性。
(Ⅱ)加入BaCl2溶液生成白色沉淀B的离子方程式是_______ 。
(Ⅲ)乙同学认为应将上述流程中②③所加试剂顺序颠倒,你认为甲、乙两同学的设计更合理的是_______ (填“甲”或“乙”),理由是_______ 。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、X、Na2SO3、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |

①装置I模拟工业生产中SO2催化氧化的反应,其化学方程式是
②甲同学按I、II、III、IV的顺序连接装置,装置II的作用是
③乙同学按I、II、IV的顺序连接装置,若装置IV中有40mL2.5mol•L-1NaOH溶液,反应后增重4.8g,则装置IV中发生总反应的化学方程式
(3)已知Na2S2O3溶液与Cl2反应时,1molNa2S2O3转移8mol电子。该反应的离子方程式是

(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和
(Ⅱ)加入BaCl2溶液生成白色沉淀B的离子方程式是
(Ⅲ)乙同学认为应将上述流程中②③所加试剂顺序颠倒,你认为甲、乙两同学的设计更合理的是
您最近一年使用:0次
2023-03-18更新
|
1125次组卷
|
3卷引用:第五章 化工生产中的重要非金属元素 单元测试
名校
解题方法
7 . 某化学学习小组设计实验制取氨气并探究氨气的有关性质:
(1)已知NH3难溶于有机溶剂CCl4,该小组成员设计实验制备氨气并探究氨气的还原性及产物 ,提供实验装置如图:______
②根据上述提供的装置正确的连接顺序为______ (用各接口序号表示)
③该装置在设计上有一定的缺陷,你对该装置的改进措施是___________ 。
(2)利用改进后的装置进行实验,观察到CuO全部变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式______
(3)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。请你设计一个简单的实验检验该红色物质中是否含有Cu2O___________ 。(已知:Cu2O+2H+=Cu+Cu2+ +H2O)
(4)按下图装置进行NH3性质实验。___________ ,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是___________ 。
(1)已知NH3难溶于有机溶剂CCl4,该小组成员设计实验制备氨气并探究
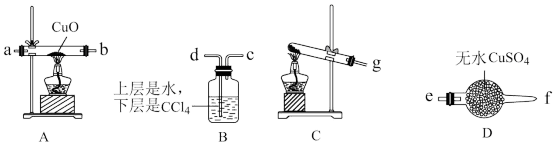
②根据上述提供的装置正确的连接顺序为
③该装置在设计上有一定的缺陷,你对该装置的改进措施是
(2)利用改进后的装置进行实验,观察到CuO全部变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式
(3)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。请你设计一个简单的实验检验该红色物质中是否含有Cu2O
(4)按下图装置进行NH3性质实验。
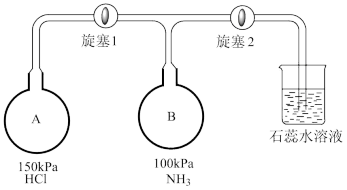
②再打开旋塞2,B瓶中的现象是
您最近一年使用:0次
2021-11-23更新
|
1495次组卷
|
13卷引用:第五章 化工生产中的重要非金属元素【单元测试A卷】
(已下线)第五章 化工生产中的重要非金属元素【单元测试A卷】第五章 化工生产中的重要非金属元素(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)山西省大同市2023-2024学年高一下学期3月月考化学试题陕西省安康市高新中学2023-2024学年高一下学期3月月考化学试题江西省宜春市丰城市第九中学2023-2024学年高一下学期期中考试化学试题安徽省太和中学2023-2024学年高一下学期4月期中考试化学试题黑龙江省绥化市绥棱县第一中学2023-2024学年高一下学期4月月考化学试题(已下线)清单02 氮及其化合物的性质 无机非金属材料(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)浙江省绍兴市诸暨中学2021-2022学年高一上学期期中考试(实验班)化学试题(已下线)5.2.2 氨和铵盐-2021-2022学年高一化学课后培优练(人教版2019必修第二册)(已下线)第04练 常见气体的制备与性质实验-2022年【暑假分层作业】高一化学(人教版2019必修第二册)湖北省竹山县第二中学2021-2022学年高一下学期第一次月考化学试题新疆乌鲁木齐市第十二中学2023-2024学年高三上学期12月月考 化学试卷
名校
解题方法
8 . 新冠肺炎疫情防控,消毒用品必不可少。试回答下列问题:
(1)过氧乙酸(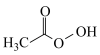 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有___________ ,分子中 键和
键和 键的个数比为
键的个数比为___________ 。
(2)生活中常用的手消毒凝胶,其主要有效成分是三氮羟基二苯醚和乙醇,其中三氯羟基二苯醚是一种广谱抗菌剂,高效、安全。三氯羟基二苯醚的结构简式如图所示。

①组成三氯羟基二苯醚的四种元素H、C、O、Cl的电负性从大到小的顺序为___________ ;基态氯原子的价电子排布图为___________ ,最高能级的原子轨道电子云轮廓图形状为___________ 。
②三氯羟基二苯醚的熔点:55~57℃,沸点:120℃,常态为白色或灰白色晶状粉末,稍有酚臭味,不溶于水,易溶于碱液和有机溶剂,三氯羟基二苯醚属于___________ 晶体。
③乙醇与甲醚 的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是
的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是___________ 。
(3)Na、K等活泼金属在 中燃烧得到的
中燃烧得到的 、
、 具有强氧化性,也常做消毒剂。已知
具有强氧化性,也常做消毒剂。已知 的晶胞如图所示:
的晶胞如图所示:
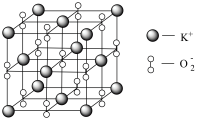
设阿伏加德罗常数的值为 ,晶胞的参数为a nm。晶胞的密度为
,晶胞的参数为a nm。晶胞的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
(1)过氧乙酸(
 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有 键和
键和 键的个数比为
键的个数比为(2)生活中常用的手消毒凝胶,其主要有效成分是三氮羟基二苯醚和乙醇,其中三氯羟基二苯醚是一种广谱抗菌剂,高效、安全。三氯羟基二苯醚的结构简式如图所示。

①组成三氯羟基二苯醚的四种元素H、C、O、Cl的电负性从大到小的顺序为
②三氯羟基二苯醚的熔点:55~57℃,沸点:120℃,常态为白色或灰白色晶状粉末,稍有酚臭味,不溶于水,易溶于碱液和有机溶剂,三氯羟基二苯醚属于
③乙醇与甲醚
 的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是
的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是(3)Na、K等活泼金属在
 中燃烧得到的
中燃烧得到的 、
、 具有强氧化性,也常做消毒剂。已知
具有强氧化性,也常做消毒剂。已知 的晶胞如图所示:
的晶胞如图所示:
设阿伏加德罗常数的值为
 ,晶胞的参数为a nm。晶胞的密度为
,晶胞的参数为a nm。晶胞的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
9 . 下列对试验现象的解释或结论均正确的是
| 实验操作 | 实验现象 | 解释与结论 | |
| A | 向鸡蛋清溶液中加入饱和 溶液 溶液 | 有白色沉淀产生 | 蛋白质发生了变性 |
| B | 室温下,向苯酚钠溶液中通入 | 出现白色浑浊 |  结合质子的能力比 结合质子的能力比 强 强 |
| C | 向苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 苯和溴水发生取代反应,使溴水褪色 |
| D | 向蔗糖中加入浓硫酸 | 蔗糖变黑,体积膨胀,放热并放出刺激性气味气体 | 浓硫酸具有脱水性和强氧化性,反应中生成C、 和 和 等 等 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 下列说法不正确旳是
| A.浓硫酸和浓硝酸都具有强氧化性,都能把HCl气体氧化 |
| B.浓硝酸在光照条件下颜色变黄,说明浓硝酸不稳定 |
| C.同温同压下,两份相同质量的锌粉,分别与足量的稀硫酸和浓硫酸反应,产生气体的体积相同 |
| D.将SO2气体通入BaCl2溶液中至饱和未见沉淀生成,继续通入NH3则有沉淀生成 |
您最近一年使用:0次
2023-03-27更新
|
714次组卷
|
2卷引用:第五章 化工生产中的重要非金属元素 单元测试



