1 . 向 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②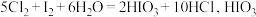 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是

 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②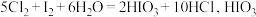 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是
A.还原性: |
B.b点溶液中 |
C.a点时已通入标准状况下氯气的总体积为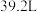 |
D.c点溶液中阴离子的个数为 |
您最近一年使用:0次
2023-12-01更新
|
896次组卷
|
4卷引用:陕西省西安市西北工业大学附属中学2023-2024学年高一上学期第二次月考化学试题
名校
解题方法
2 . 二氟草酸硼酸锂(LiBF2C2O4)热稳定性好,在较宽的温度范围内具有良好的离子电导率,对水分不敏感,被认为是最有希望取代六氟磷酸锂的电解质锂盐。由锂精矿(主要成分有LiAlSi2O6还含有少量Fe2+等离子)制备LiBF2C2O4的工艺如下。
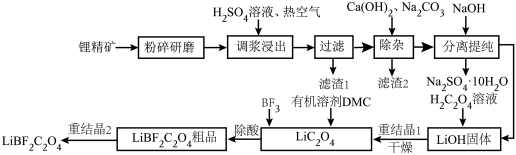
回答下列问题:
(1)调浆浸出时通入热空气的作用是___________ (用离子方程式表示)。
(2)锂精矿中所有的Al元素和Si元素以某种铝硅酸盐从滤渣1中分离,该铝硅酸盐的化学式为___________ ,滤渣2的主要成分是CaCO3和___________ (填化学式)。
(3)分离提纯的步骤,将滤液蒸发浓缩,加入NaOH后,冷却到-5~-15℃分离出Na2SO4·10H2O。再将分离后的母液___________ 、___________ (填简要操作),得到LiOH固体。
(4)在较短的反应时间内,BF3和Li2C2O4反应时的比例对产物组成的影响如下表所示。
①一般认为BF3和Li2C2O4反应分两步进行:
第一步:Li2C2O4+BF3=LiBF2C2O4+LiFEa1
第二步:___________ Ea2
请补齐第二步反应,并判断两步反应的活化能Ea1___________ (填“>”或“<”)Ea2。
②为避免药品浪费,反应的最佳比例n(BF3):n(Li2C2O4)=___________ 。
(5)BF3和环境中微量的水反应会生成酸性物质,影响产品的纯度和性质,用Li2CO3比用LiOH除酸更好的原因是___________ 。
(6)LiBF2C2O4的阴离子含五元环状结构,且B最外层为8e-构型,请你补全LiBF2C2O4的结构式:_____ 。
Li+[ _____ ]。

回答下列问题:
(1)调浆浸出时通入热空气的作用是
(2)锂精矿中所有的Al元素和Si元素以某种铝硅酸盐从滤渣1中分离,该铝硅酸盐的化学式为
(3)分离提纯的步骤,将滤液蒸发浓缩,加入NaOH后,冷却到-5~-15℃分离出Na2SO4·10H2O。再将分离后的母液
(4)在较短的反应时间内,BF3和Li2C2O4反应时的比例对产物组成的影响如下表所示。
| n(BF3):n(Li2C2O4) | 产物组成 |
| 0.5 1.0 1.5 2.0 2.5 | LiBF2C2O4、LiBF4、Li2C2O4 LiBF2C2O4、LiBF4、Li2C2O4 LiBF2C2O4、LiBF4、Li2C2O4 LiBF2C2O4、LiBF4 LiBF2C2O4、LiBF4 |
第一步:Li2C2O4+BF3=LiBF2C2O4+LiFEa1
第二步:
请补齐第二步反应,并判断两步反应的活化能Ea1
②为避免药品浪费,反应的最佳比例n(BF3):n(Li2C2O4)=
(5)BF3和环境中微量的水反应会生成酸性物质,影响产品的纯度和性质,用Li2CO3比用LiOH除酸更好的原因是
(6)LiBF2C2O4的阴离子含五元环状结构,且B最外层为8e-构型,请你补全LiBF2C2O4的结构式:
Li+[ _____ ]。
您最近一年使用:0次
2023-05-17更新
|
594次组卷
|
3卷引用:陕西省西安市西北工业大学附属中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
3 . 将Cl2通入含a mol NaOH的溶液中,反应会放热,温度升高后发生反应: 3Cl2+6NaOH = 5NaCl+NaClO3+3H2O。当NaOH完全反应时,下列说法正确的是
| A.反应中作氧化剂的Cl2有0.25a mol |
B.若反应后溶液中 =2,则 =2,则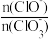 =5 =5 |
C.NaClO与NaClO3的物质的量之和可能为 a mol a mol |
D.反应中转移电子的物质的量可能为 a mol a mol |
您最近一年使用:0次
2023-05-16更新
|
931次组卷
|
3卷引用:陕西省西安铁一中滨河高级中学2023-2024学年高一上学期期中考试化学试题
解题方法
4 . 将一定量铁粉和铜粉混合均匀后分为四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成 的体积和剩余金属的质量如表所示(设
的体积和剩余金属的质量如表所示(设 的还原产物只有
的还原产物只有 ):
):
下列说法错误的是
 的体积和剩余金属的质量如表所示(设
的体积和剩余金属的质量如表所示(设 的还原产物只有
的还原产物只有 ):
):| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
稀硝酸的体积/ | 50 | 100 | 150 | 175 |
| 剩余金属的质量/g | 9.0 | 4.8 | 0 | 0 |
 的体积(标准状况)/ 的体积(标准状况)/ | 1120 | 2240 | 3360 | V |
A.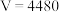 |
B.每等份混合物的质量为 |
C.稀硝酸的物质的量的浓度为 |
D.实验Ⅰ中发生反应的化学方程式为 |
您最近一年使用:0次
2023-04-27更新
|
743次组卷
|
2卷引用:陕西省商洛市2022-2023学年高一下学期7月期末考试化学试题
5 . 下列实验能得出相关结论的是
| 实验操作 | 实验结论 | |
| A | 向NaHA溶液中滴加紫色石蕊溶液,溶液变为蓝色 | Kw>Ka1(H2A)·Ka2(H2A) |
| B | 常温下将铝片投入浓硝酸中,无明显现象 | 铝与浓硝酸不反应 |
| C | 向10mL0.1mol·L-1FeCl3溶液中加入5mL0.1mol·L-1KSCN溶液,溶液显红色,再滴加少量1mol·L-1KSCN溶液,红色加深 | Fe3+和SCN-的反应是可逆反应 |
| D | 向FeCl2溶液中滴加少量的酸性KMnO4溶液,KMnO4溶液褪色 | 氧化性: >Cl2 >Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 甲溶液是Na2CO3和NaOH[c(NaOH)=0.5mol•L-1]的混合溶液,乙溶液是NH4Cl和HCl的混合溶液,已知乙溶液中c(NH )=0.40mol•L-1。取5份体积均为100mL的甲溶液,向其中缓慢加入不同体积的乙溶液,微热并充分反应后,测得各组产生的气体体积如表所示:
)=0.40mol•L-1。取5份体积均为100mL的甲溶液,向其中缓慢加入不同体积的乙溶液,微热并充分反应后,测得各组产生的气体体积如表所示:
已知:①NH +OH-
+OH- NH3↑+H2O;
NH3↑+H2O;
②假设生成的气体全部逸出;
③不考虑溶液混合时体积的变化和微热时盐酸的挥发;
④忽略水的电离及与水发生的反应,气体均换算成标准状况下。
回答下列问题:
(1)甲溶液中所含的金属阳离子共有____ 种;在100mL0.5mol•L-1的NaOH溶液中,n(NaOH)=____ mol。
(2)在实验I中:
①反应后所得的溶液中溶质有____ (填化学式)。
②生成的气体为____ (填“CO2”、“NH3”或“CO2和NH3”)。
(3)在反应II中,无气体生成的原因为____ (用简要的文字解释)。
(4)在实验IV中:
①生成气体的离子方程式为_____ 。
②当反应结束后,c(Cl-)=____ mol•L-1。
(5)由上述实验可得出,50mL乙溶液中所含的阳离子总数为____ NA(不考虑NH 时与水的反应及水电离出的H+)。
时与水的反应及水电离出的H+)。
 )=0.40mol•L-1。取5份体积均为100mL的甲溶液,向其中缓慢加入不同体积的乙溶液,微热并充分反应后,测得各组产生的气体体积如表所示:
)=0.40mol•L-1。取5份体积均为100mL的甲溶液,向其中缓慢加入不同体积的乙溶液,微热并充分反应后,测得各组产生的气体体积如表所示:| 实验序号 | I | II | III | IV | V |
| 乙溶液体积/mL | 50 | 100 | 150 | 200 | 250 |
| 气体体积/mL | 224 | 0 | 448 | 1120 | 1120 |
已知:①NH
 +OH-
+OH- NH3↑+H2O;
NH3↑+H2O;②假设生成的气体全部逸出;
③不考虑溶液混合时体积的变化和微热时盐酸的挥发;
④忽略水的电离及与水发生的反应,气体均换算成标准状况下。
回答下列问题:
(1)甲溶液中所含的金属阳离子共有
(2)在实验I中:
①反应后所得的溶液中溶质有
②生成的气体为
(3)在反应II中,无气体生成的原因为
(4)在实验IV中:
①生成气体的离子方程式为
②当反应结束后,c(Cl-)=
(5)由上述实验可得出,50mL乙溶液中所含的阳离子总数为
 时与水的反应及水电离出的H+)。
时与水的反应及水电离出的H+)。
您最近一年使用:0次
2022-12-08更新
|
294次组卷
|
2卷引用:陕西省咸阳市高新一中2022-2023学年高一上学期第三次质量检测化学试题
名校
7 . 将一定质量的Mg和Al的混合物投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是
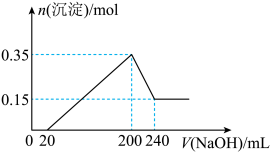

| A.Mg和Al的质量比为3:4 |
| B.生成的H2的体积为10.08 L |
| C.NaOH溶液的物质的量浓度为5 mol/L |
| D.硫酸的物质的量浓度为0.5 mol/L |
您最近一年使用:0次
2022-11-29更新
|
985次组卷
|
2卷引用:陕西省西安市第七十五中学2022-2023学年高一上学期期末结业化学试题
名校
解题方法
8 . 白磷(P4)有毒,实验时若皮肤接触到白磷,应立即用稀CuSO4溶液清洗,发生两个反应:
反应①为P4和CuSO4反应的主要生成物为Cu、H3PO4和H2SO4;
反应②为11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4。
下列说法正确的是
反应①为P4和CuSO4反应的主要生成物为Cu、H3PO4和H2SO4;
反应②为11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4。
下列说法正确的是
| A.在反应①和②中,P4只作还原剂 |
| B.反应①中氧化产物与还原产物的个数之比为5∶2 |
| C.皮肤接触到白磷,用稀CuSO4溶液清洗后,应再使用NaOH溶液清洗 |
| D.若P4反应完全且转化为H3PO4的转化率是80%,理论上反应①和②消耗P4的个数之比为14∶11 |
您最近一年使用:0次
2022-11-09更新
|
1308次组卷
|
4卷引用:陕西省西安市西北工业大学附属中学2023-2024学年高一上学期第二次月考化学试题
名校
解题方法
9 . 已知:将Cl2通入适量NaOH溶液中,反应会放热,当温度升高后会发生如下反应:3Cl2+6NaOH=5NaCl+NaClO3+3H2O。则Cl2通入NaOH溶液的产物中可能有NaCl、NaClO、NaClO3中的两种或三种,且 的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
 的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是| A.与碱的反应中,Cl2既是氧化剂又是还原剂 |
| B.参加反应的Cl2物质的量为0.5a mol |
C.若某温度下,反应后 =6,则溶液中 =6,则溶液中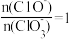 |
D.改变温度,反应中转移电子的物质的量可能为 mol mol |
您最近一年使用:0次
2022-10-24更新
|
2075次组卷
|
12卷引用:陕西省榆林中学2022-2023学年高一上学期期末考试化学试题
陕西省榆林中学2022-2023学年高一上学期期末考试化学试题陕西省安康市2022-2023学年高一下学期开学摸底考试化学试题江苏省无锡市锡山高级中学2021-2022学年高一上学期期中考试化学试题山东省实验中学2022-2023学年高一上学期11月期中考试化学试题甘肃省酒泉市玉门油田第一中学2022-2023学年高一上学期期中考试化学(A卷)试题北京市第八中学2022-2023学年高一上学期12月月考化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试(选考)化学试题江苏省苏州中学2022-2023学年高一下学期开学考试化学试题辽宁省沈阳市五校协作体2022-2023学年高一上学期期末考试化学试题 山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题(已下线)专题03 氧化还原反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
名校
解题方法
10 . 回答下列问题:
(1)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是__ 。
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1mol/L,c(Fe3+)=0.3mol/L,c(SO )=0.6mol/L,则c(K+)为
)=0.6mol/L,则c(K+)为___ 。
(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为__ 。
(4)某状况下aL氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成bmL氨水溶液,所得溶液的密度为ρg/mL,则该氨水的物质的量浓度可表示为___ mol/L;氨水的质量分数为___ 。
(1)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1mol/L,c(Fe3+)=0.3mol/L,c(SO
 )=0.6mol/L,则c(K+)为
)=0.6mol/L,则c(K+)为(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为
(4)某状况下aL氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成bmL氨水溶液,所得溶液的密度为ρg/mL,则该氨水的物质的量浓度可表示为
您最近一年使用:0次



