1 . 下列图示装置不能达到实验目的的是
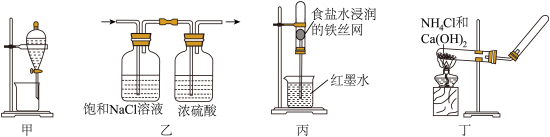

| A.装置甲用CCl4萃取溴水中的Br2 | B.装置乙除去Cl2中的HCl并干燥 |
| C.装置丙验证铁的吸氧腐蚀 | D.装置丁实验室制备少量NH3 |
您最近一年使用:0次
2022-10-17更新
|
9546次组卷
|
9卷引用:2022年河北省高考真题化学试题
2022年河北省高考真题化学试题(已下线)专题11 化学实验基础-2022年高考真题模拟题分项汇编(已下线)2022年河北省高考真题变式题(1-9)北京市第二中学2022-2023学年高三下学期2月开学测试化学试题(已下线)专题13 化学实验基础(已下线)专题13 化学实验基础北京市第二中学2023-2024学年高三下学期开学考化学试卷山东省菏泽市郓城县第一中学(英华校区)2023-2024学年高三上学期9月第一次月考化学试题(已下线)第08练 实验仪器的选用与基本操作 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
2 . 下列有关实验装置进行的相应实验,能达到实验目的的是
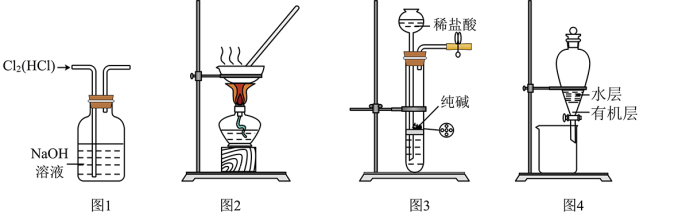

A.用图 所示装置除去 所示装置除去 中含有的少量 中含有的少量 |
B.用图 所示装置蒸干 所示装置蒸干 饱和溶液制备 饱和溶液制备 晶体 晶体 |
C.用图 所示装置制取少量纯净的 所示装置制取少量纯净的 气体 气体 |
D.用图 所示装置分离 所示装置分离 萃取碘水后已分层的有机层和水层 萃取碘水后已分层的有机层和水层 |
您最近一年使用:0次
2022-12-09更新
|
2082次组卷
|
50卷引用:2012年普通高等学校招生全国统一考试化学(江苏卷)
2012年普通高等学校招生全国统一考试化学(江苏卷)(已下线)2013届安徽省阜阳一中高三上学期第二次模化学试卷(已下线)2014届高考化学二轮复习 专题12化学实验基础练习卷(已下线)2014高考化学名师选择题专练 实验基础练习卷(已下线)2014年高中化学二轮创新训练上 专题12化学实验基础练习卷(已下线)2014年高考化学苏教版总复习 10-2 物质的检验、分离和提纯练习卷(已下线)2014届浙江省温州中学高三上学期期末理综化学试卷(已下线)2013-2014贵州省遵义四中高三第五次月考理综化学试卷(已下线)2015届江西省信丰中学高三上学期第一次月考化学试卷2015届江苏省盐城市时杨中学高三第二次调研考试化学试卷2016届湖北省荆州中学高三上学期第一次质检化学试卷2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷2016届河南省宜阳县实验学校高三第二次月考化学试卷2016届浙江省杭州高级中学高三上学期月考(三)化学试卷2016届浙江临海台州中学高三上学期第三次统练化学试卷2016届福建省闽粤联合体高三上学期第三次联考化学试卷2016届浙江省临海市台州中学高三上学期第三次统考化学试卷2016届湖北省荆州市公安一中高三上学期12月月考化学试卷2017届广西陆川中学高三上9月月考化学试卷2017届湖南省长沙市长郡中学高三上月考二化学试卷河南省郑州市外国语学校2018届高三上学期第一次月考化学试题新疆石河子第二中学2018届高三上学期第一次月考化学试题河北省邯郸市永年区第二中学2019届高三上学期9月月考化学试题(已下线)2018年11月7日——《每日一题》高考一轮复习 化学实验基本操作(已下线)上海市奉贤区2013年高考二模化学试题海南省海南枫叶国际学校2021-2022学年高三上学期第三次月考(1月)化学试题(已下线)专题11 化学实验基础(测)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)2013-2014浙江省宁波效实中学高二下学期期末考试化学试卷2014-2015广西桂林市第十八中学高二下学期期中考试化学试卷2014-2015学年江西省南昌市二中高二下学期期末化学试卷2015-2016学年湖南省怀化市高一上学期期末化学试卷2015-2016学年吉林松原油田高中高一下期初考试化学试卷2015-2016学年广西桂林十八中高一下开学测化学试卷2015-2016学年贵州省遵义航天中学高一下3月月考化学卷2015-2016学年吉林省松原市油田高中高二下期中化学试卷2016年山东省普通高中学业水平化学模拟试卷(4)山西省忻州市第一中学2016-2017学年高一必修一:第1章从实验学化学同步练习化学试题广西桂林市2017-2018学年高二上学期期末考试化学试题山东省泰安市2017-2018学年高一上学期期末考试化学试题湖北省襄阳市第四中学2017-2018学年高一3月月考化学试题江苏省泰州中学2017-2018学年高二下学期学业水平测试模拟(三)(必修)化学试题山东省泰安市宁阳一中2018-2019学年高一上学期阶段性考试二(12月)化学试题江苏省苏州市震泽中学2019-2020学年高一上学期第二次月考化学试题江苏省苏州市2019~2020学年第一学期期末高一学业质量阳光指标调研化学试题甘肃省张掖市高台县第一中学2018—2019学年高二下学期期中考试化学试题山东省潍坊市2019-2020学年高一下学期3月阶段监测化学试题山东省泰安第一中学2019-2020学年高一下学期期中考试化学试题陕西省延安市第一中学2019-2020学年高一下学期期中考试化学试题山东省泰安市宁阳一中2020-2021学年高一下学期第一次考试化学试题海南省海口市第一中学2023-2024学年高二上学期第一次月考化学试题
3 . 利用下列装置(夹持装置略)进行实验,能达到实验目的的是
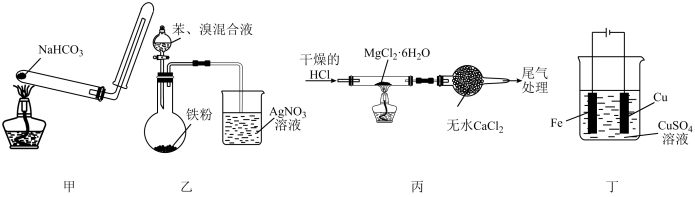
| A.用甲装置制备并收集CO2 |
| B.用乙装置制备溴苯并验证有HBr产生 |
| C.用丙装置制备无水MgCl2 |
| D.用丁装置在铁上镀铜 |
您最近一年使用:0次
2020-07-11更新
|
11990次组卷
|
57卷引用:2020年山东省高考化学试卷(新高考)
2020年山东省高考化学试卷(新高考)(已下线)专题11 化学实验基础-2020年高考真题和模拟题化学分项汇编广东省仲元中学、中山一中等七校联合体2021届高三上学期第一次联考化学试题(已下线)小题必刷13 镁及其化合物——2021年高考化学一轮复习小题必刷(通用版)河南省三门峡市第一高级中学2021届高三8月开学考试化学试题山东省临沂市莒南第二中学2021届高三10月月考化学试题山东省青岛市第十七中学2021届高三上学期10月阶段性检测化学试题河北省武安市第三中学2021届高三上学期期中考试化学试题福建省福州市第一中学2021届高三上学期开学质检化学试题湖南省邵东县第一中学2021届高三上学期第三次月考化学试题陕西省西安中学2021届高三上学期第四次月考化学试题(已下线)热点4 化学实验的装置与操作分析-2021年高考化学专练【热点·重点·难点】(已下线)热点6 化学实验方案的设计与评价-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)专题10 化学实验基础——备战2021年高考化学纠错笔记(已下线)重点6 制备型实验综合题-2021年高考化学专练【热点·重点·难点】(已下线)重点1 仪器组合型实验方案的设计与评价-2021年高考化学【热点·重点·难点】专练(新高考)广东省华南师范大学附属中学2021届高三综合测试(三)化学试题(已下线)小题06 装置型实验选择题(侧重物质的制备、分离提纯) ——备战2021年高考化学经典小题考前必刷(全国通用)上海市七宝中学2021届高三下学期3月摸底考试化学试题上海市复旦大学附属中学2021届高三下学期模拟(一)化学试题(已下线)2021年高考化学押题预测卷(江苏卷)(02)(含考试版、答题卡、参考答案、全解全析)(已下线)押山东卷第05题 实验装置的评价-备战2021年高考化学临考题号押题(山东卷)(已下线)考点29 化学实验基础-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点28 化学实验仪器与基本操作-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题11 化学实验基础-备战2022年高考化学真题及地市好题专项集训【山东专用】吉林省长春市北师大附属学校2021-2022学年高三上学期期初考试化学试题黑龙江省大庆中学2022届高三上学期第一次月考化学试题江西省宜春市丰城市第九中学2021-2022学年高三上学期第三次月考化学试题河北省实验中学2021届高三上学期第一次月考化学试题(已下线)考向35 实验的方案设计与评价-备战2022年高考化学一轮复习考点微专题(已下线)专题05 化学基础实验—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)卷13 化学基础实验(检验、鉴别、分离、提纯)-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押新高考卷05题 化学实验基础-备战2022年高考化学临考题号押题(新高考通版)(已下线)2020年山东卷化学高考真题变式题1-10(已下线)考点49 化学实验基础-备战2023年高考化学一轮复习考点帮(全国通用)陕西省安康中学2023届高三第一次检测性考试化学试题广东省惠州市惠阳高级中学实验学校2021-2022学年高三上学期月考化学试题河南省洛阳市第一高级中学2022~2023学年高三上学期9月月考化学试题(已下线)微专题44 以气体制备为主体的实验-备战2023年高考化学一轮复习考点微专题上海市控江中学2022-2023学年高三上学期第一次月考化学试题上海市宝山区行知中学2022-2023学年高三上学期期中测试化学试题(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)北京市朝阳区2023届高三下学期三模化学试题(已下线)专题13 化学实验基础(已下线)第二章 单元测试卷河南省南阳市第一中学校2023-2024学年高三上学期第二次月考化学试题重庆市巴蜀中学校2023-2024学年高三上学期9月月考化学试题重庆市巴蜀中学校2024届高三上学期适应性月考卷(二)化学试题北京市第一六一中学2021-2022学年高三上学期期中考试化学试题河南省焦作第一中学2023-2024学年高三上学期10月模拟化学测试 四川省攀枝花市第十五中学校2023-2024学年高三上学期第3次统一考试理科综合-高中化学黑龙江省哈尔滨市师大附中2020-2021学年高二上学期期末考试化学试题吉林省长春外国语学校2020-2021学年高二下学期第二次月考化学试题黑龙江省大庆实验中学2020-2021学年高二下学期期末化学试题河北省张家口市第一中学2020-2021学年高二上学期10月月考(衔接班)化学 试题陕西省西北农林科技大学附属中学2021-2022学年高二上学期期末考试化学试题湖南省株洲市第一中学2022-2023学年高二上学期期中考试化学试题
真题
4 . 下列设计的实验方案能达到实验目的的是( )
| A.制备Al(OH)3悬浊液:向1mol·L-1AlCl3溶液中加过量的6mol·L-1NaOH溶液 |
| B.提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和碳酸钠溶液,振荡后静置分液,并除去有机相的水 |
| C.检验溶液中是否含有Fe3+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象 |
| D.探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
您最近一年使用:0次
2019-01-30更新
|
1221次组卷
|
3卷引用:2015年全国普通高等学校招生统一考试理科综合能力测试化学(江苏卷)
2015年全国普通高等学校招生统一考试理科综合能力测试化学(江苏卷)江苏省南通市启东市吕四中学2020届高三第一次质量检测化学试题(已下线)小题必刷27 化学反应速率、图像及其影响因素——2021年高考化学一轮复习小题必刷(通用版本)
5 . 根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是
A.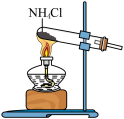 制取氨气 制取氨气 | B. 制取碳酸氢钠 制取碳酸氢钠 |
C.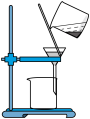 分离碳酸氢钠 分离碳酸氢钠 | D. 干燥碳酸氢钠 干燥碳酸氢钠 |
您最近一年使用:0次
2019-01-30更新
|
6986次组卷
|
117卷引用:2016年全国普通高等学校招生统一考试化学(江苏卷精编版)
2016年全国普通高等学校招生统一考试化学(江苏卷精编版)2016年全国普通高等学校招生统一考试化学(江苏卷参考版)2017届江西省九江第一中学高三7月暑期阶段性测试化学试题2017届河北沧州市第一中学高三上学期第一次月考化学试题2017届湖北省荆州中学高三上学期8月摸底化学试卷2017届甘肃省兰州一中高三上学期9月月考化学试卷2017届吉林省实验中学高三上第二次模拟化学试卷2017届广西桂林十八中高三上10月月考化学试卷2017届江苏省徐州、宿迁、连云港、淮安四市高三11月模拟化学卷2017届江苏省丹阳高级中学高三下学期期初考试化学试卷2017届山东省师大附中高三第三次模拟考试化学试卷2016-2017学年上海市青浦区高三上学期期终学业质量调研测试化学试卷福建省莆田第一中学2017届高三考前模拟(最后一卷)化学试题河南省郑州市外国语学校2018届高三上学期第一次月考化学试题河北省衡水中学2018届高三上学期一轮复习周测化学试题河北省鸡泽县第一中学2018届高三上学期第一次月考化学试题贵州省遵义航天高级中学2018届高三第二次模拟(10月)理科综合化学试题甘肃省白银市会宁县第一中学2018届高三上学期第二次月考理科综合化学试题河南省信阳市普通高中2018届高三第一次教学质量检测化学试题全国衡水金卷2018届高三大联考化学试题内蒙古巴彦淖尔市第一中学2018届高三上学期期中考试理科综合化学试题湖北省荆州中学2018届高三上学期第三次双周考(11月)化学试卷辽宁省沈阳市省实验中学2018届高三10月月考化学试题辽宁省师范大学附属中学2018届高三上学期期中考试化学试题福建省诗山县2018届高三上学期期中化学试题江西省上高二中2018届高三上学期第三次月考化学试题辽宁师大附中2017-2018学年第一学期期中考试高三化学试卷安徽省黄山市2018届高三一模检测化学试题(已下线)【艺体生百日捷进提升系列-技能方法】专题3.10 氮族方面试题的解题方法与技巧(已下线)解密05 金属及其化合物(教师版)——备战2018年高考化学之高频考点解密2018-2019学年 钠及其化合物 专项训练题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第1讲 钠及其氧化物【教学案】【全国百强校】四川省成都市石室中学2019届高三上学期入学考试化学试题山东省德州市夏津县一中2019届高三上学期第一次月考化学试题湖北省公安县车胤中学2019届高三上学期9月月考化学试题【全国百强校】福建省莆田市第一中学2019届高三上学期第一次月考化学试题【全国百强校】江西省新余市第四中学2019届高三上学期10月月考化学试题安徽省白泽湖中学2017届高三上学期期中考试化学试题【全国百强校】吉林省实验中学2019届高三上学期期中考试化学试题【校级联考】福建省福州八县一中2019届高三上学期期中考试化学试题天津市滨海新区大港油田一中2019届高三上学期期中考试化学试题【全国百强校】北京市师范大学附属中学2019届高三上学期期中考试化学试题1【全国百强校】北京市师范大学附属中学2019届高三上学期期中考试化学试题2【全国百强校】山西省晋中市平遥县平遥中学2019届高三上学期12月月考化学试题(已下线)解密17 物质的检验分离与提纯(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考二轮复习精品资料-专题5 金属及其化合物(教学案)甘肃省武威第一中学2019届高三上学期期末考试化学试题山东省泰安市第一中学2020届高三10月月考化学试题山东省泰安市宁阳县第一中学2020届高三上学期第二次段考化学试题四川省乐山市外国语学校2020届高三9月月考化学试题福建省漳州市华安一中、龙海二中2020届高三上学期第一次联考化学试题2020届高三化学二轮冲刺新题专练——气体制取流程的规范操作2广东省潮州市高级中学2020届高三下学期第一次网上模拟测试理科综合化学试题天津市滨海新区塘沽第十三中学2020届高三下学期第一次统测化学试题湖南长沙长郡中学2020届高三2月份网络教学质量监测卷理综化学试题河北省石家庄市第二中学2020届高中毕业班四月份教学质量监测卷理科综合化学部分安徽省合肥市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题黑龙江省哈尔滨师范大学青冈实验中学校2020届高三上学期开学考试(8月)化学试题河南省郑州市第一中学2020届高三12月联考化学试题上海市建平中学2021届高三上学期9月月考化学试题安徽省肥东县高级中学2021届高三上学期第二次月考化学试题(已下线)安徽省芜湖市2019届高三上学期期末考试理综化学试题福建省福州市福清西山学校高中部2020届高三上学期期中考试化学试题辽宁省葫芦岛第八高级中学2021届高三上学期10月月考化学试题江苏省徐州市沛县2021届高三上学期第一次学情调研化学试题宁夏固原市五原中学补习部2021届高三上学期期中考试化学试题湖北省利川市第五中学2021届高三上学期期中考试化学试题黑龙江省哈尔滨工业大学附属中学2021届高三上学期期中考试化学试题福建省长泰县第一中学2021届高三上学期11月考试化学试题新疆维吾尔自治区呼图壁县第一中学2021届高三上学期11月月考化学试题贵州省贵阳市清镇养正学校2021届高三上学期第二次月考化学试题吉林省辉南县第六中学2022届高三上学期第一次月考化学试题河北省邢台市2022届高三9月第二次联合考试化学试题(已下线)第1周 晚练题-备战2022年高考化学周测与晚练(新高考专用)辽宁省营口市第二高级中学2021-2022学年高三上学期第一次月考化学试题山东省济南市商河县第三中学2022届高三10月月考化学试题湖北省竹溪县第一高级中学2022届高三上学期第二次月考化学试题(已下线)专题05 化学基础实验—2022年高考化学二轮复习讲练测(全国版)-测试(已下线)第07讲 钠及其重要化合物(练)-2023年高考化学一轮复习讲练测(全国通用)四川省成都市第七中学2023届高三上学期零诊模拟考试化学试题河南省濮阳市南乐县第一高级中学2022-2023学年高三上学期7月月考化学试题天津市五校2022-2023学年高三上学期期中联考化学试题甘肃省兰州第一中学2022-2023学年高三上学期期中考试化学试题广东省广州市广东实验中学2023届高三上学期第二次阶段考试化学试题西藏林芝市第二高级中学2021-2022学年高三上学期第二次月考理综化学试题上海市青浦区2017年高考化学一模试卷北京市平谷区2022-2023学年高三下学期质量监控(零模)化学试题(已下线)第1讲 钠及其重要化合物河北省保定市河北安国中学等4校2022-2023学年高三上学期11月期中化学试题四川省南充市白塔中学2023-2024学年高三上学期第五次考试理科综合试题2015-2016学年湖北省武汉市新洲一中、黄陂一中高二下期末化学试卷2015-2016学年山东省济宁市高一下期末化学试卷2016-2017学年湖北省宜昌一中高二上开学测化学试卷黑龙江省哈尔滨市第六中学2016-2017学年高二下学期期末考试化学试题山西省原平市范亭中学2016-2017学年高一下学期期末考试化学试题浙江省金华一中2017-2018学年度高一上学期第二次段考试化学试题广西桂林市第十八中学2017-2018学年高一下学期开学考试化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第1讲 钠及化合物 (教学案)【全国百强校】陕西省西安市长安区第一中学2018-2019学年高一上学期期末考试化学试题步步为赢 高二化学暑假作业:作业四 金属及其化合物四川省成都外国语学校2018-2019学年高二5月月考化学试题黑龙江省大庆市铁人中学2018-2019学年高二下学期期末考试化学试题步步为赢 高一化学寒假作业:作业十一 阶段检测(三)内蒙古包头市包钢第四中学2018-2019学年高二下学期期末考试化学试题吉林省延边市长白山第一高级中学2019-2020学年高一下学期验收考试化学试题新疆乌鲁木齐市第四中学2019-2020学年高二下学期期末考试化学试题黑龙江省鹤岗市第一中学2019-2020学年高二下学期期末考试化学试题新疆实验中学2019-2020学年高一上学期期中考试化学试题(已下线)2.1.2钠的几种化合物(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)陕西省西安市长安区第一中学2019-2020学年高一上学期期末考试化学试题专题3 第二单元综合拔高练-高中化学苏教2019版必修第一册(已下线)【绍兴新东方】绍兴高中化学00014(已下线)易错专题14 侯氏制碱法生产纯碱-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)江苏省扬州市2021-2022学年高二下学期期初调研测试化学(选修)试题广东省大联考2021-2022学年高一下学期期中检测化学试题湖北省十堰市联合体2022-2023学年高一上学期10月期中联考化学试题安徽省淮北市第一中学2023-2024学年高一下学期3月月考化学试题
真题
名校
6 . 下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
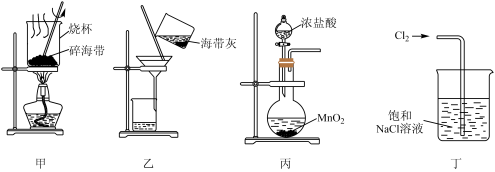

| A.用装置甲灼烧碎海带 |
| B.用装置乙过滤海带灰的浸泡液 |
| C.用装置丙制备用于氧化浸泡液中I−的Cl2 |
| D.用装置丁吸收氧化浸泡液中I−后的Cl2尾气 |
您最近一年使用:0次
2018-06-10更新
|
11754次组卷
|
84卷引用:2018年全国普通高等学校招生统一考试化学(江苏卷)
2018年全国普通高等学校招生统一考试化学(江苏卷)(已下线)2018年高考题及模拟题汇编 专题11 化学实验基础江苏省盐城市田家炳中学2019届高三上学期开学考试化学试题陕西省城固县第一中学2019届高三上学期第一次月考化学试题辽宁省沈阳市东北育才学校2019届高三上学期第一次模拟考试化学试题甘肃省师范大学附属中学2019届高三上学期第一次月考化学试题辽宁省葫芦岛协作校2019届高三上学期第一次月考化学试题甘肃省武威市第二中学2019届高三上学期第二次(10月)月考化学试题【全国百强校】甘肃省平凉市静宁县第一中学2019届高三上学期第三次模拟考试化学试题江苏师范大学附属实验学校2019届高三上学期10月学情调研化学试题河南省郑州市实验中学2019届高三上学期期中考试化学试题【全国百强校】山东省山东师范大学附属中学2019届高三上学期第五次模拟考试化学试题【市级联考】陕西省榆林市2019届高三下学期高考模拟第三次测试理科综合化学试题四川省武胜县烈面中学校2018届高三9月入学考试化学试题湖北省利川市第三中学2019届高三一模化学试题(已下线)专题10.2 物质的分离、提纯、检验与鉴别(练)-《2020年高考一轮复习讲练测》(已下线)专题10.2 物质的分离、提纯、检验与鉴别(讲)-《2020年高考一轮复习讲练测》河南省南阳市2020届高三上学期期中质量评估化学试题(已下线)考点20 化学基础实验——《备战2020年高考精选考点专项突破题集》福建省莆田第二十五中学2020届高三上学期期末考试化学试题2020届人教版高中化学高三专题基础复习专题1《从实验学化学》测试卷上海市宝山区2020届高三上学期第一次模拟考试(等级考)化学试题新疆阿克苏市阿瓦提四中2020届高三上学期第二次月考化学试题(已下线)专题3.6 金属材料和无机非金属材料 海水的开发利用 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》江苏省南通市启东市吕四中学2020届高三第一次质量检测化学试题(已下线)第02讲 物质的分离和提纯(精讲)——2021年高考化学一轮复习讲练测四川省成都市龙泉中学2021届高三上学期开学考试化学试题(已下线)第6单元 常见的非金属元素(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)小题必刷18 氯及其化合物——2021年高考化学一轮复习小题必刷(通用版)江苏省扬州市江都区大桥高级中学2021届高三上学期期初调研化学试题山东师范大学附属中学2021届高三上学期期中考试(11月)化学试题山西省实验中学2019届高三上学期第四次月考化学试题江苏省泰州中学2021届高三上学期第二次月考化学试题云南省普洱市景东县第一中学2021届高三上学期期末考试化学试题(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)内蒙古包头市2022届高三上学期起点调研考试化学试题(已下线)课时52 物质的分离、提纯和检验-2022年高考化学一轮复习小题多维练(全国通用)重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题福建省厦门市湖滨中学2021-2022学年高三上学期期中考试化学试题山东省济南市莱芜第一中学2021-2022学年高三上学期期中考试化学试题湖南省浏阳市第一中学2022届高三下学期期中考试化学试题新疆叶城县第八中学2021-2022学年高三上学期第二次月考化学试题贵州省贵阳市2022-2023学年高三上学期10月质量监测化学试题湖南省长沙市同升湖实验学校2022-2023学年高三上学期第三次月考化学试题第四章 非金属及其化合物 第19讲 卤素的性质及提取(已下线)题型46 从海水中提取氯、溴、碘河南省焦作第一中学2023-2024学年高三上学期9月化学模拟测试 【全国百强校】山西省临汾第一中学2017-2018学年高二下学期期末考试化学试题黑龙江省青冈县一中2017-2018学年高一下学期期末考试化学试题江西省南昌三中2019届高二下期末考试 化学【全国百强校】黑龙江省哈尔滨市第三中学2017-2018学年高二下学期期末考试化学试题湖北省汉川市第二中学2017-2018学年高一下学期期末考试化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高二上学期9月模块诊断化学试题云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题山西省长治二中2018-2019学年高一下学期第一次月考化学试题吉林省长春汽车经济开发区第三中学2018-2019学年高一下学期4月月考化学试题(已下线)2019年5月20日 《每日一题》 必修2 海带提碘步步为赢 高一化学暑假作业:作业十六 开发利用金属矿物和海水资源【全国百强校】吉林省延边第二中学2018-2019学年高二下学期第二次月考化学试题黑龙江省大庆市第四中学2018-2019学年高一下学期第三次月考化学试题江西省宜春市万载中学2019-2020学年高二上学期期中考试化学试题(衔接班)广东省2020年普通高中学业水平考试化学合格性考试模拟试题(五)四川省广安市邻水县四川省邻水中学2019-2020学年高一下学期期中考试化学试题鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律微项目 海带提碘与海水提溴高一必修第二册(人教2019版)第八章 化学与可持续发展 素养检测高一必修第一册(苏教2019版)专题3 C 高考挑战区 过模拟 2年模拟精编精练高一必修第一册(苏教2019)专题3 第三单元 海洋化学资源的综合利用3江苏省邗江中学2020-2021学年高一上学期期中考试化学试题专题3 第三单元综合拔高练-高中化学苏教2019版必修第一册(人教版2019)必修第二册 第八章 化学与可持续发展 第一节 自然资源的开发利用吉林省通化县综合高级中学2020-2021学年高一下学期期末考试化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题湖北省武汉市蔡甸区实验高级中学2020-2021学年高二上学期10月联合考试化学试题福建省厦门市翔安第一中学2021-2022学年高一下学期第一次月考(3月)化学试题云南省昭通市永善、绥江县2021-2022学年高一上学期期末考试化学试题山东省菏泽市单县第五中学2021-2022学年高一下学期第一次段考化学(A)试题四川省广安市育才学校2022-2023学年高一上学期9月月考化学试题江苏省扬州中学2022-2023学年高一上学期期中检测化学试题广东省揭阳市惠来县第一中学2022-2023学年高二上学期期中考试化学试题广东省广州市越秀区2023-2024学年高二上学期开学考试化学试题
真题
7 . NH3及其盐都是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为_____ 。
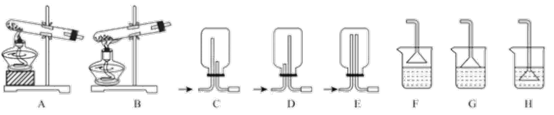
(2)按下图装置进行NH3性质实验。
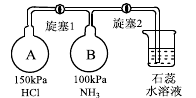
①先打开旋塞1,B瓶中的现象是_______ ,原因是__________ ,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是_________________ 。
(3)设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限制试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可控制温度)
①实验目的:探究______ 对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中V(溶液)表示所配制溶液的体积)。_________________
③按实验序号I所拟数据进行实验,若读取的待测物理量的数值为Y,则NH4Cl水解反应得平衡转化率
为_____ (只列出算式,忽略水自身电离的影响)。
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为

(2)按下图装置进行NH3性质实验。

①先打开旋塞1,B瓶中的现象是
②再打开旋塞2,B瓶中的现象是
(3)设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限制试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可控制温度)
①实验目的:探究
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中V(溶液)表示所配制溶液的体积)。
| 物理量 实验序号 | V(溶液)/mL | …… | |||
| 1 | 100 | ||||
| 2 | 100 |
③按实验序号I所拟数据进行实验,若读取的待测物理量的数值为Y,则NH4Cl水解反应得平衡转化率
为
您最近一年使用:0次
2016-12-09更新
|
2441次组卷
|
3卷引用:2015年全国普通高等学校招生统一考试化学(广东卷)
8 . 磷酸氢二铵[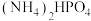 ]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备
]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备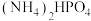 ,装置如图所示(夹持和搅拌装置已省略)。
,装置如图所示(夹持和搅拌装置已省略)。

回答问题:
(1)实验室用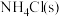 和
和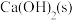 制备氨气的化学方程式为
制备氨气的化学方程式为_______ 。
(2)现有浓 质量分数为85%,密度为1.7g/mL。若实验需100mL1.7mol/L的
质量分数为85%,密度为1.7g/mL。若实验需100mL1.7mol/L的 溶液,则需浓
溶液,则需浓
_______ mL(保留一位小数)。
(3)装置中活塞 的作用为
的作用为_______ 。实验过程中,当出现_______ 现象时,应及时关闭 ,打开
,打开 。
。
(4)当溶液pH为8.0~9.0时,停止通 ,即可制得
,即可制得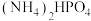 溶液。若继续通入
溶液。若继续通入 ,当
,当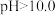 时,溶液中
时,溶液中 、
、_______ 和_______ (填离子符号)浓度明显增加。
(5)若本实验不选用pH传感器,还可选用_______ 作指示剂,当溶液颜色由_______ 变为_______ 时,停止通 。
。
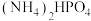 ]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备
]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备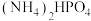 ,装置如图所示(夹持和搅拌装置已省略)。
,装置如图所示(夹持和搅拌装置已省略)。
回答问题:
(1)实验室用
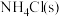 和
和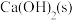 制备氨气的化学方程式为
制备氨气的化学方程式为(2)现有浓
 质量分数为85%,密度为1.7g/mL。若实验需100mL1.7mol/L的
质量分数为85%,密度为1.7g/mL。若实验需100mL1.7mol/L的 溶液,则需浓
溶液,则需浓
(3)装置中活塞
 的作用为
的作用为 ,打开
,打开 。
。(4)当溶液pH为8.0~9.0时,停止通
 ,即可制得
,即可制得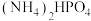 溶液。若继续通入
溶液。若继续通入 ,当
,当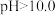 时,溶液中
时,溶液中 、
、(5)若本实验不选用pH传感器,还可选用
 。
。
您最近一年使用:0次
2022-07-04更新
|
7996次组卷
|
21卷引用:2022年海南省高考真题化学试题
2022年海南省高考真题化学试题(已下线)专题16 化学实验综合题-2022年高考真题模拟题分项汇编(已下线)2022年海南省高考真题变式题15-19(已下线)考点51 物质的制备-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第14讲 氮及其化合物(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第12讲 氮及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第27讲 物质的制备与性质实验(练)-2023年高考化学一轮复习讲练测(新教材新高考)福建省厦门集美中学2022-2023学年高三上学期10月月考化学试题(已下线)易错点11 氮元素及其化合物-备战2023年高考化学考试易错题(已下线)专题27 物质制备类综合性实验题(学生版)-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)回归教材重难点11 熟记“五气体”制备实验、“两定量”测定实验-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)第13讲氮及其化合物(已下线)考点16 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型一 实验简答题答题规范-备战2024年高考化学答题技巧与模板构建(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
9 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确 的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 探究 和浓 和浓 反应后溶液呈绿色的原因 反应后溶液呈绿色的原因 | 将 通入下列溶液至饱和: 通入下列溶液至饱和:①浓  ②  和HNO3,混合溶液 和HNO3,混合溶液 | ①无色变黄色 ②蓝色变绿色 |  和浓 和浓 反应后溶液呈绿色的主要原因是溶有 反应后溶液呈绿色的主要原因是溶有 |
| B | 比较 与 与 结合 结合 的能力 的能力 | 向等物质的量浓度的 和 和 混合溶液中滴加几滴 混合溶液中滴加几滴 溶液,振荡 溶液,振荡 | 溶液颜色无明显变化 | 结合 的能力: 的能力: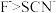 |
| C | 比较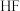 与 与 的酸性 的酸性 | 分别测定等物质的量浓度的 与 与 溶液的 溶液的 | 前者 小 小 | 酸性: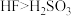 |
| D | 探究温度对反应速率的影响 | 等体积、等物质的量浓度的 与 与 溶液在不同温度下反应 溶液在不同温度下反应 | 温度高的溶液中先出现浑浊 | 温度升高,该反应速率加快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-02更新
|
2859次组卷
|
5卷引用:2024年浙江高考真题化学(1月)
2024年浙江高考真题化学(1月)(已下线)通关练03 常考化学实验基础知识-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)选择题11-16浙江省余姚中学2023-2024学年高二下学期3月质量检测化学试题山东省青岛一中2023-2024学年高二下学期第二次月考化学试卷
真题
10 . TiO2既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料。
(1)实验室利用反应TiO2(s)+CCl4(g) TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下:
TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下:

有关物质性质如下表
仪器A的名称是________ ,装置E中的试剂是_____________ 。反应开始前依次进行如下操作:组装仪器、____________ 、加装药品、通N2一段时间后点燃酒精灯。反应结束后的操作包括:①停止通N2②熄灭酒精灯 ③冷却至室温。正确的顺序为_________ (填序号)。欲分离D中的液态混合物,所采用操作的名称是________________ 。
(2)工业上由钛铁矿(FeTiO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
酸溶 FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+ TiOSO4(aq)+ 2H2O(l)
水解 TiOSO4(aq)+ 2H2O(l) H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq)
简要工艺流程如下:

①试剂A为___ 。钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品TiO2收率降低,原因是________ 。
②取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是_______ 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是_________ (填化学式)。
(1)实验室利用反应TiO2(s)+CCl4(g)
 TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下:
TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下:
有关物质性质如下表
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
(2)工业上由钛铁矿(FeTiO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
酸溶 FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+ TiOSO4(aq)+ 2H2O(l)
水解 TiOSO4(aq)+ 2H2O(l)
 H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq)简要工艺流程如下:

①试剂A为
②取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是
您最近一年使用:0次
2019-01-30更新
|
1708次组卷
|
4卷引用:2013年全国普通高等学校招生统一考试理科综合能力测试化学(山东卷)
2013年全国普通高等学校招生统一考试理科综合能力测试化学(山东卷)(已下线)2014届高考化学二轮复习四川配套训练 第13讲实验方案的设计练习卷2015届河南省陕州中学高三下学期第一次月考理科综合化学试卷(已下线)第29讲 化学实验方案的设计与评价-2021年高考化学一轮复习名师精讲练



