名校
1 . 由于大苏打在空气中放置易变质失效,因此在进行定量实验前,往往需要对溶液浓度进行标定。探究小组查阅资料后决定利用重铬酸钾( )对配制的0.1000mol/L
)对配制的0.1000mol/L 溶液进行重新标定,具体实验过程如下:
溶液进行重新标定,具体实验过程如下:
①取0.0190mol/L重铬酸钾标准溶液20.00mL,硫酸酸化后加入过量的KI溶液,发生反应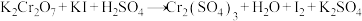 (未配平)
(未配平)
②向上述溶液中滴加样品 溶液,发生反应
溶液,发生反应 。直到恰好完全反应时,停止滴加,记录加入
。直到恰好完全反应时,停止滴加,记录加入 溶液的体积。平行实验3次,消耗的
溶液的体积。平行实验3次,消耗的 溶液的平均体积为24.80mL
溶液的平均体积为24.80mL
(1)配平步骤①中的化学方程式_______ 。
(2)步骤②可以加入少量_______ 作为恰好完全反应的指示剂。当恰好完全反应时,溶液的颜色变化是_______ 。
(3)经过标定,样品溶液的实际浓度是_______ 。(保留3位有效数字)
 )对配制的0.1000mol/L
)对配制的0.1000mol/L 溶液进行重新标定,具体实验过程如下:
溶液进行重新标定,具体实验过程如下:①取0.0190mol/L重铬酸钾标准溶液20.00mL,硫酸酸化后加入过量的KI溶液,发生反应
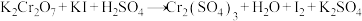 (未配平)
(未配平)②向上述溶液中滴加样品
 溶液,发生反应
溶液,发生反应 。直到恰好完全反应时,停止滴加,记录加入
。直到恰好完全反应时,停止滴加,记录加入 溶液的体积。平行实验3次,消耗的
溶液的体积。平行实验3次,消耗的 溶液的平均体积为24.80mL
溶液的平均体积为24.80mL(1)配平步骤①中的化学方程式
(2)步骤②可以加入少量
(3)经过标定,样品溶液的实际浓度是
您最近一年使用:0次
解题方法
2 . 某变质小苏打样品中含Na2CO3,取m克样品用如图装置测定Na2CO3含量,下列说法不正确的是
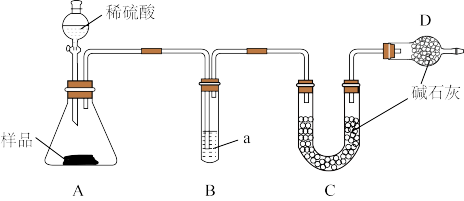

| A.装置B所装试剂a是浓硫酸,其作用是干燥CO2 |
| B.装置D的作用是防止空气中的H2O、CO₂进入装置C |
| C.反应后称量装置C的质量为n克,用数据m、n可求得Na2CO3含量 |
| D.上述装置的不足之处是没有在A装置前接一个赶气装置 |
您最近一年使用:0次
名校
解题方法
3 . 金属钛在航天、医疗等领域有着广泛的应用。工业上用钛铁矿(主要成分为FeTiO3,含有Fe2O3、CaO、SiO2等杂质)为原料制备金属钛的工艺流程如下:
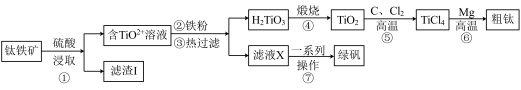
已知:FeTiO3中Fe为+2价;高温下钛易与N2、H2反应。
(1)提高①中浸取反应速率可采取的措施有___________ (答两条)。
(2)“滤渣I”的主要成分为___________ 。
(3)钛铁矿与硫酸发生非氧化还原反应,生成TiOSO4,试写出该反应的化学方程式________ 。
(4)⑥中镁与TiCl4高温下反应制备粗钛时需加保护气,下列可作为保护气的是________ (填标号)。
a.H2 b.Ar c.Cl2 d.N2
(5)⑦中经过“一系列操作”可获得副产品绿矾( ),其过程包括
),其过程包括_____ 、洗涤、干燥。
(6)绿矾易被氧化而变质。现取在空气中放置一段时间的某绿矾样品,请选择合适的试剂,设计实验方案,证明该样品被部分氧化:___________ 。

已知:FeTiO3中Fe为+2价;高温下钛易与N2、H2反应。
(1)提高①中浸取反应速率可采取的措施有
(2)“滤渣I”的主要成分为
(3)钛铁矿与硫酸发生非氧化还原反应,生成TiOSO4,试写出该反应的化学方程式
(4)⑥中镁与TiCl4高温下反应制备粗钛时需加保护气,下列可作为保护气的是
a.H2 b.Ar c.Cl2 d.N2
(5)⑦中经过“一系列操作”可获得副产品绿矾(
 ),其过程包括
),其过程包括(6)绿矾易被氧化而变质。现取在空气中放置一段时间的某绿矾样品,请选择合适的试剂,设计实验方案,证明该样品被部分氧化:
您最近一年使用:0次
名校
解题方法
4 . 氢氧化钠固体在空气中具有较强吸湿性,还易吸收空气中二氧化碳变质,需要密封保存
(1)氢氧化钠电离方程式___________ ;
(2)氢氧化钠电离产生的正负离子质子数之比为___________ ,电子数之比为___________ ;
(3)溶质质量分数为28%的氢氧化钠溶液中,钠离子和水分子物质的量之比为___________ ,钠离子氧原子质量之比为___________ 。(不考虑水分子的电离)
现实验室要配制0.3mol/L的氢氧化钠溶液100mL,某同学认为可以采用如下的两种方法:
方法一:用较浓的氢氧化钠溶液加水稀释
(4)可以取用6molL的氢氧化钠溶液___________ mL(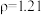 g/mL)和蒸馏水
g/mL)和蒸馏水___________ mL进行混合(答案保留一位小数)(已知0.3mol/L的氢氧化钠溶液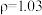 g/mL)
g/mL)
方法二:用氢氧化钠固体配制
(5)该溶液的配制过程如下
a.通过计算,用烧杯在电子天平上准确称取氢氧化钠固体___________ g;
b.在烧杯中加入适量的蒸馏水溶解氢氧化钠,然后转移至仪器A内;
c.通过玻璃棒将溶液转移至仪器A中,洗涤有关仪器,并将洗涤液转移至所配制的溶液中;
d.轻轻哹动仪器A后,___________ (填具体操作)、上下摇匀;
(6)方法二的过程中,涉及的定量仪器有___________ (填写具体名称)
(7)下列操作中能使所配制的溶液浓度偏大的是___________ (每步不受影响)
①在溶解过程中,有少量溶液溅出容器
②在溶解并转移溶液后,没有对有关仪器洗涤而直接进行定容
③在定容过程中,视线高于刻度线
④在摇匀后,发现容器中的液面低于刻度线,再滴加蒸馏水至刻度线
(8)某同学取20mL所配制的氢氧化钠溶液与标准浓度的盐酸进行中和反应,根据消耗的盐酸的体积计算,发现氢氧化钠浓度偏小,若配制的各步骤操作正确,则对于所取的样品,影响因素可能是下列中的___________ (各种影响因素单独发生)
①称好的NaOH固体吸收了空气中少量的水
②NaOH固体混有少量的氯化钠
③NaOH固体吸收了空气中少量的
④NaOH固体中混有少量的氢氧化钾
你对③④做出判断的依据是
③___________ 。
④___________ 。
有一瓶NaOH固体样品由于放置时间较长,某同学怀疑其由于吸收空气中 而发生部分变质。为证明此推测,进行如下实验。
而发生部分变质。为证明此推测,进行如下实验。
称取2.000g样品,配制成250mL待测液。量取20.00mL待测液,当慢慢滴0.1000mol/L的硫酸溶液18.60mL时测得溶液正好显中性。根据实验数据可知:
(9)待测溶液中氢氧化钠的浓度为___________ mol/L:(四位小数)
(10)样品中NaOH的质量百分数为___________ 。(四位小数)
(1)氢氧化钠电离方程式
(2)氢氧化钠电离产生的正负离子质子数之比为
(3)溶质质量分数为28%的氢氧化钠溶液中,钠离子和水分子物质的量之比为
现实验室要配制0.3mol/L的氢氧化钠溶液100mL,某同学认为可以采用如下的两种方法:
方法一:用较浓的氢氧化钠溶液加水稀释
(4)可以取用6molL的氢氧化钠溶液
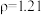 g/mL)和蒸馏水
g/mL)和蒸馏水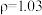 g/mL)
g/mL) 方法二:用氢氧化钠固体配制
(5)该溶液的配制过程如下
a.通过计算,用烧杯在电子天平上准确称取氢氧化钠固体
b.在烧杯中加入适量的蒸馏水溶解氢氧化钠,然后转移至仪器A内;
c.通过玻璃棒将溶液转移至仪器A中,洗涤有关仪器,并将洗涤液转移至所配制的溶液中;
d.轻轻哹动仪器A后,
(6)方法二的过程中,涉及的定量仪器有
(7)下列操作中能使所配制的溶液浓度偏大的是
①在溶解过程中,有少量溶液溅出容器
②在溶解并转移溶液后,没有对有关仪器洗涤而直接进行定容
③在定容过程中,视线高于刻度线
④在摇匀后,发现容器中的液面低于刻度线,再滴加蒸馏水至刻度线
(8)某同学取20mL所配制的氢氧化钠溶液与标准浓度的盐酸进行中和反应,根据消耗的盐酸的体积计算,发现氢氧化钠浓度偏小,若配制的各步骤操作正确,则对于所取的样品,影响因素可能是下列中的
①称好的NaOH固体吸收了空气中少量的水
②NaOH固体混有少量的氯化钠
③NaOH固体吸收了空气中少量的

④NaOH固体中混有少量的氢氧化钾
你对③④做出判断的依据是
③
④
有一瓶NaOH固体样品由于放置时间较长,某同学怀疑其由于吸收空气中
 而发生部分变质。为证明此推测,进行如下实验。
而发生部分变质。为证明此推测,进行如下实验。称取2.000g样品,配制成250mL待测液。量取20.00mL待测液,当慢慢滴0.1000mol/L的硫酸溶液18.60mL时测得溶液正好显中性。根据实验数据可知:
(9)待测溶液中氢氧化钠的浓度为
(10)样品中NaOH的质量百分数为
您最近一年使用:0次
21-22高一·全国·假期作业
5 . Na2O2是一种重要化工原料,工业上可以用来漂白纺织类物品、麦秆、纤维等。回答下列问题:
(1)Na2O2中氧元素化合价为_______ ,写出过氧化钠与水反应的化学方程式_______ 。
(2)过氧化钠若长期保存不当,容易生成_______ (填化学式),证明过氧化钠变质情况的一种实验方案如下。
(3)过氧化钠还可以作为潜艇工作人员的供氧剂,某工作人员携带10kg的过氧化钠固体进入潜艇,相当于携带标况下_______ m3空气(只需列出计算表达式,已知氧气占空气体积分数约为20%,空气的密度为1.293g/cm3)。
(1)Na2O2中氧元素化合价为
(2)过氧化钠若长期保存不当,容易生成
| 操作 | 现象 | 结论 |
| 取少量样品于试管中,加水溶解,加入 | 有白色沉淀生成 | |
| 另取少量样品于试管中,再加入适量的水,用带火星的木条靠近管口 | 带火星的木条复燃 |
(3)过氧化钠还可以作为潜艇工作人员的供氧剂,某工作人员携带10kg的过氧化钠固体进入潜艇,相当于携带标况下
您最近一年使用:0次
名校
解题方法
6 . 根据实验目的,下列实验操作及现象、结论都正确的是
| 选项 | 实验目的 | 实验操作及现象 | 结论 |
| A | 探究浓硫酸的性质 | 浓硫酸滴入蔗糖中,将产生的气体通入澄清石灰水中,蔗糖变黑、体积膨胀,石灰水变浑浊 | 浓硫酸具有脱水性和强氧化性 |
| B | 检验硫代硫酸钠氧化变质可能混有的 | 取少量样品溶于水,先加入过量稀盐酸,再滴加 溶液,若有沉淀生成 溶液,若有沉淀生成 | 可能混有 |
| C | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,产生无色气体 | 乙醇中含有水 |
| D | 利用乙醇与钠的反应,探究乙醇的结构 | 在0.01 mol金属钠与过量的 反应,收集到标准状况下的气体112 mL 反应,收集到标准状况下的气体112 mL | 乙醇分子中有1个氢原子与氧原子相连,其余的氢原子与碳原子相连 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 .  俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
 俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是| 选项 | 实验目的 | 实验操作或现象 | 相关离子方程式 |
| A | 制备 | 实验室用 通入 通入 和 和 的混合溶液中来制备 的混合溶液中来制备 | 4SO2+2S2-+CO =3S2O =3S2O +CO2 +CO2 |
| B | 检验硫代硫酸钠氧化变质可能混有的 | 取少量样品溶于水,先加入过量稀盐酸,再滴加 溶液,有沉淀生成 溶液,有沉淀生成 | SO +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C | 探究温度对硫代硫酸钠与硫酸反应速率的影响 | 分别将两种反应溶液先混合,再水浴加热至反应要求温度,测得该温度下的反应速率 | 2S2O +2H+=S↓+SO +2H+=S↓+SO +2H2O +2H2O |
| D | 用过量硫代硫酸钠除去水中溶解的氯气 | 黄绿色褪去 | S2O +4Cl2+5H2O=2SO +4Cl2+5H2O=2SO +8Cl-+10H+ +8Cl-+10H+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-11更新
|
2445次组卷
|
7卷引用:湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题
湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题(已下线)素养卷09 微型原理验证方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题04 离子反应湖南省部分学校2022-2023学年高三下学期开学考试化学试题湖南省衡阳市第八中学2023-2024学年高三上学期开学(暑假检测)化学试题江苏省靖江高级中学、华罗庚中学2023-2024学年高三上学期第一次阶段考试化学试题江西省新余市第一中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
8 . 根据实验目的,下列实验操作及现象、结论都正确的是
| 选项 | 实验目的 | 实验操作及现象 | 结论 |
| A | 探究浓硫酸的性质 | 浓硫酸滴入蔗糖中,将产生的气体通入澄清石灰水中,蔗糖变黑、体积膨胀,石灰水变浑浊 | 浓硫酸具有脱水性和强氧化性 |
| B | 检验硫代硫酸钠氧化变质可能混有的 | 取少量样品溶于水,先加入过量稀盐酸,再滴加 溶液,若有沉淀生成 溶液,若有沉淀生成 | 可能混有 |
| C | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,产生无色气体 | 乙醇中含有水 |
| D | 利用乙醇与钠的反应,探究乙醇的结构 | 在0.01 mol金属钠与过量的 反应,收集到标准状况下的气体112 mL 反应,收集到标准状况下的气体112 mL | 乙醇分子中有1个氢原子与氧原子相连,其余的氢原子与碳原子相连 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的试剂。
I.欲使用0.30mol/L的 溶液950mL,现拟用36.5%(
溶液950mL,现拟用36.5%(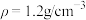 )的浓盐酸来配制,请回答下列问题:
)的浓盐酸来配制,请回答下列问题:
(1)配制溶液所用36.5%的盐酸的体积为_______ 。
(2)该实验需要使用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管、_______ 。
(3)下列操作会使所配溶液浓度小于0.30mol/L的是:_______ 。(填对应的序号)
a、容量瓶用蒸馏水洗净后没有烘干,瓶内有少量残留的蒸馏水;
b、在操作中没有用蒸馏水洗涤烧杯和玻璃棒;
c、定容时视线俯视刻度线;
d、定容时加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水定容到刻度线;
e、将配制好的溶液转入试剂瓶的过程中不慎洒出了少许溶液;
f、用量筒量取浓盐酸时视线仰视刻度线。
II.酸碱中和滴定
(4)某学生用盐酸标准液测定氢氧化钠待测液时,选择酚酞作指示剂。达到滴定终点的现象是_______ 。滴定时不必用到的仪器是_______ 。
A.酸式滴定管 B.容量瓶 C.锥形瓶 D.铁架台
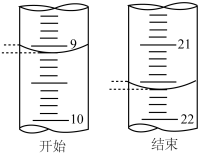
(5)若滴定开始和结束时,酸式滴定管中的液面如图所示,此时消耗盐酸的体积为_______ mL。已知用 的盐酸标定25mL的氢氧化钠溶液,则测得
的盐酸标定25mL的氢氧化钠溶液,则测得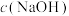 为
为_______  。
。
III.为了测定摩尔盐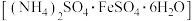 产品的纯度,称取ag样品溶于水,配制成500mL溶液,用浓度为
产品的纯度,称取ag样品溶于水,配制成500mL溶液,用浓度为 的酸性
的酸性 溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
(6)滴定过程中发生反应的离子方程式为_______ 。
(7)通过实验数据计算该产品的纯度:_______ (用含字母a、c的式子表示,用M表示摩尔盐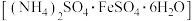 的摩尔质量)。上表第一次实验中记录的数据明显大于后两次,其原因可能是
的摩尔质量)。上表第一次实验中记录的数据明显大于后两次,其原因可能是_______ 。
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
I.欲使用0.30mol/L的
 溶液950mL,现拟用36.5%(
溶液950mL,现拟用36.5%(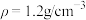 )的浓盐酸来配制,请回答下列问题:
)的浓盐酸来配制,请回答下列问题:(1)配制溶液所用36.5%的盐酸的体积为
(2)该实验需要使用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管、
(3)下列操作会使所配溶液浓度小于0.30mol/L的是:
a、容量瓶用蒸馏水洗净后没有烘干,瓶内有少量残留的蒸馏水;
b、在操作中没有用蒸馏水洗涤烧杯和玻璃棒;
c、定容时视线俯视刻度线;
d、定容时加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水定容到刻度线;
e、将配制好的溶液转入试剂瓶的过程中不慎洒出了少许溶液;
f、用量筒量取浓盐酸时视线仰视刻度线。
II.酸碱中和滴定
(4)某学生用盐酸标准液测定氢氧化钠待测液时,选择酚酞作指示剂。达到滴定终点的现象是
A.酸式滴定管 B.容量瓶 C.锥形瓶 D.铁架台
(5)若滴定开始和结束时,酸式滴定管中的液面如图所示,此时消耗盐酸的体积为
 的盐酸标定25mL的氢氧化钠溶液,则测得
的盐酸标定25mL的氢氧化钠溶液,则测得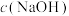 为
为 。
。
III.为了测定摩尔盐
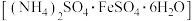 产品的纯度,称取ag样品溶于水,配制成500mL溶液,用浓度为
产品的纯度,称取ag样品溶于水,配制成500mL溶液,用浓度为 的酸性
的酸性 溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
(7)通过实验数据计算该产品的纯度:
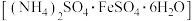 的摩尔质量)。上表第一次实验中记录的数据明显大于后两次,其原因可能是
的摩尔质量)。上表第一次实验中记录的数据明显大于后两次,其原因可能是A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
您最近一年使用:0次
10 . 氯气(Cl2)是一种能溶于水的有毒气体,它能与水发生反应生成盐酸(HCl)和次氯酸(HClO),次氯酸(HClO) 具有漂白性,能使品红等有色物质褪色。
(1)向含有酚酞的NaOH溶液中逐滴滴入饱和氯水(氯气的水溶液),发现溶液会由红色褪成无色,请根据以上信息猜想溶液变成无色的两个可能原因(用简要文字说明);
①___________ ;
②___________ 。
(2)请设计一个简单的实验,验证(1) 中猜想:___________ 。
(3)工业制取漂白粉的原理为2Cl2+2Ca (OH)2 =CaCl2+Ca (C1O)2+2H2O, 漂白粉的有效成分是次氯酸钙Ca (ClO)2 ,它能与酸发生复分解反应生成HClO。在空气中容易吸收水和CO2发生反应:Ca (ClO) 2+CO2+H2O=CaCO3 ↓+2HClO, HClO是一种酸性比盐酸弱的酸,不稳定、易分解。
①HClO在常温下分解,发生反应:2HClO=2HCl+O2↑。某瓶HClO溶液放置一段时间后,溶液的pH会___________ (填 “增大”或“减小”或“不变”)。
②实验室有一包长时间放置的漂白粉,某同学设计了下列实验探究该漂白粉是否变质。
[提出问题]长时间放置的漂白粉是否变质?
[作出猜想]猜想1:该漂白粉未未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为___________ ;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3。
[实验探究]
[反思评价]I.有同学认为无需进行操作步骤②,只需在步骤①反应后的溶液中滴加适量品红,观察品红是否褪色即可,理由是___________ (用化学方程式表示)。
II.漂白粉在保存时一定要注意___________ 。
(1)向含有酚酞的NaOH溶液中逐滴滴入饱和氯水(氯气的水溶液),发现溶液会由红色褪成无色,请根据以上信息猜想溶液变成无色的两个可能原因(用简要文字说明);
①
②
(2)请设计一个简单的实验,验证(1) 中猜想:
(3)工业制取漂白粉的原理为2Cl2+2Ca (OH)2 =CaCl2+Ca (C1O)2+2H2O, 漂白粉的有效成分是次氯酸钙Ca (ClO)2 ,它能与酸发生复分解反应生成HClO。在空气中容易吸收水和CO2发生反应:Ca (ClO) 2+CO2+H2O=CaCO3 ↓+2HClO, HClO是一种酸性比盐酸弱的酸,不稳定、易分解。
①HClO在常温下分解,发生反应:2HClO=2HCl+O2↑。某瓶HClO溶液放置一段时间后,溶液的pH会
②实验室有一包长时间放置的漂白粉,某同学设计了下列实验探究该漂白粉是否变质。
[提出问题]长时间放置的漂白粉是否变质?
[作出猜想]猜想1:该漂白粉未未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3。
[实验探究]
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入适量 | 有气体产生,气体使石灰水变浑浊。 | 猜想2成立 |
| ②把少量样品加入水中,通入足量的CO2气体后,再滴入适量的品红溶液 |
II.漂白粉在保存时一定要注意
您最近一年使用:0次



