1 . NA表示阿伏加 德罗常数的值。下列叙述正确的是( )
| A.在0.1mol·L-1的Na2CO3溶液中,阴离子总数一定大于0.1NA |
| B.常温常压下,由32gO2与O3组成的混合气体中含有的分子总数小于NA |
| C.36.0gCaO2与足量水完全反应,转移的电子数为NA |
| D.1molCH4与1molCl2混合,充分反应后,生成气体分子数为NA |
您最近一年使用:0次
2020-06-28更新
|
194次组卷
|
2卷引用:2024届四川省雅安市神州天立学校高三下学期高考冲刺考试理科综合试题-高中化学
2 . 设NA为阿伏加 德罗常数值。下列说法正确的是
A.12g  的原子核内中子数为6NA 的原子核内中子数为6NA |
| B.9.0g葡萄糖和蔗糖的混合物中含碳原子的数目为0.3NA |
| C.25℃时,1L pH=2的H2C2O4溶液中含H+的数目为0.02NA |
| D.标准状况下,2.24L CO2与足量Na2O2反应转移的电子数为0.1NA |
您最近一年使用:0次
2020-01-08更新
|
526次组卷
|
2卷引用:2019年四川省绵阳市高三第二次诊断性考试理综化学试题
3 . 在aLAl2(SO4)3和(NH4)2SO4的混合物溶液中加入b molBaCl2,恰好使溶液中的 离子完全沉淀;如加入足量强碱并加热可得到cmolNH3气,则原溶液中的Al3+离子浓度(mol/L)为( )
离子完全沉淀;如加入足量强碱并加热可得到cmolNH3气,则原溶液中的Al3+离子浓度(mol/L)为( )
 离子完全沉淀;如加入足量强碱并加热可得到cmolNH3气,则原溶液中的Al3+离子浓度(mol/L)为( )
离子完全沉淀;如加入足量强碱并加热可得到cmolNH3气,则原溶液中的Al3+离子浓度(mol/L)为( )A.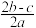 | B.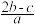 | C.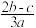 | D.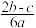 |
您最近一年使用:0次
2019-01-30更新
|
1463次组卷
|
40卷引用:2014届四川省成都市高三第二次诊断考试理综化学试卷
(已下线)2014届四川省成都市高三第二次诊断考试理综化学试卷2008年普通高等学校招生统一考试理综试题化学部分(四川卷)2016届四川省雅安市天全中学高三9月月考化学试卷上海市吴淞中学2018届高三上学期第一次调研考试化学试题河南省辉县市第一高级中学2019届高三上学期第二次月考化学试题四川省成都外国语学校2021-2022学年高一上学期期中化学试题(已下线)09-10学年河北省衡水中学高一年级下学期期末考试化学试卷(已下线)2011-2012学年黑龙江哈尔滨市第六中学高二下学期期末考试化学卷(已下线)2012届福建省福州市高三第一学期期末质量检查考试化学试卷(已下线)2014高考名师推荐化学CB计算法2014-2015黑龙江省绥化市三校高一上学期期末联考化学试卷2016届宁夏回族自治区银川一中高三上学期第一次月考化学试卷12016届宁夏回族自治区银川一中高三上学期第一次月考化学试卷22016届吉林省汪清县第六中学高三9月月考化学试卷2016届湖北省枣阳市白水高级中学高三上学期第一次月考化学试卷2015-2016学年湖北省襄阳一中高一上学期期中测试化学试卷2016届吉林省吉林大学附属中学高三上第一次摸底考试化学试卷2015-2016学年江西省上高二中高一上期末化学试卷2015-2016学年湖南省长沙市望城一中高二下期末理科化学试卷2016-2017学年河北省武邑中学高一上期中化学卷黑龙江省大庆中学2016-2017学年高二下学期期末考试化学试题甘肃省武威市第六中学2018届高三第一次阶段性过关考试化学试题(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第4讲 守恒思想在化学中的应用——守恒法解题技巧【教学案】安徽省阜阳三中2017-2018学年高一上学期第二次调研考试化学试题【全国百强校】宁夏回族自治区六盘山高级中学2018届高三上学期第一次月考化学试题新疆自治区北京大学附属中学新疆分校2019届高三上学期10月月考化学试题【全国百强校】安徽省师范大学附属中学2018-2019学年高一上学期期中考试化学试题【全国百强校】甘肃省兰州市第一中学2018-2019学年高一上学期12月月考化学试题宁夏青铜峡市高级中学2020届高三上学期第一次月考化学试题甘肃省武威第十八中学2020届高三上学期第一次诊断考试化学试题2019年湖南省怀化市高三化上学期期末考试化学试题2020届高三化学二轮复习——常见的化学计算方法练习【精编25题】广东省云浮市郁南县蔡朝焜纪念中学2021届高三9月月考化学试题江苏省邗江中学2020-2021学年高一上学期期中考试化学试题陕西省榆林市子洲中学2021届高三上学期第一次月考化学试题新疆乌鲁木齐市第八中学2019-2020学年高一上学期第二次月考化学试题辽宁省辽河油田第一高级中学2020-2021学年高一上学期期末考试化学试题(A部)上海市行知中学2022-2023学年高一上学期期中考试化学试题第5课时 物质的量在化学反应中的应用江苏省南通中学2023-2024学年高一上学期期中考试化学试题
解题方法
4 . 某工厂将制革工业污泥中的铬元素以难溶物CrOH(H2O)5SO4的形式回收,工艺流程如下,其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
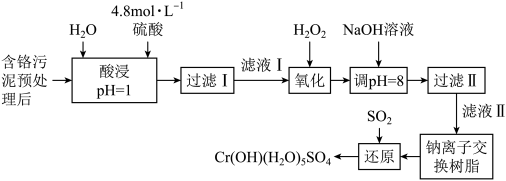
回答下列问题:
(1)4.8 mol/L的硫酸溶液密度为1.27g/cm3,该溶液中硫酸的质量分数是_______ 。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:______ 。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
①Cr (OH)3溶解于NaOH溶液时反应的离子方程式是___________ 。
②加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。滤液Ⅱ中阳离子主要有______ ;但溶液的pH不能超过8,其理由是______________________________ 。
(4)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是_____________ 。
(5)写出上述流程中用SO2进行还原时发生反应的化学方程式:_______________ 。

回答下列问题:
(1)4.8 mol/L的硫酸溶液密度为1.27g/cm3,该溶液中硫酸的质量分数是
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | — | — | — |
| 沉淀完全时的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
②加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。滤液Ⅱ中阳离子主要有
(4)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是
(5)写出上述流程中用SO2进行还原时发生反应的化学方程式:
您最近一年使用:0次
2018-05-05更新
|
498次组卷
|
2卷引用:【全国市级联考】四川省攀枝花市2018届高三第三次统考理科综合化学试题
名校
5 . 用下列装置进行的实验, 能达到相应实验目的的是
A. 配制一定浓度的硫酸溶液 配制一定浓度的硫酸溶液 | B.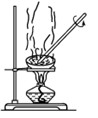 分离溶解在CCl4中的I2 分离溶解在CCl4中的I2 |
C. 制备和收集少量NH3 制备和收集少量NH3 | D.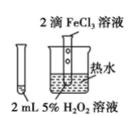 验证FeCl3 对 H2O2分解有催化作用 验证FeCl3 对 H2O2分解有催化作用 |
您最近一年使用:0次
2017-03-31更新
|
894次组卷
|
5卷引用:2017届四川省宜宾市高三第二次诊断理科综合能力测试化学试卷
2017届四川省宜宾市高三第二次诊断理科综合能力测试化学试卷江西省宜丰中学2019届高三上学期第三次月考理科综合化学试题江苏省沭阳县修远中学2018-2019学年高一下学期第二次月考(实验班)化学试题(已下线)江苏省沭阳县修远中学2018-2019学年高一下学期第二次月考化学试题广东省佛山市第一中学2021-2022学年高三上学期12月模拟考试化学试题
解题方法
6 . 硫代硫酸钠(Na2S2O3)商品名“海波”,俗名“大苏打”,分析化学上常用于滴定实验。某化学兴趣小组在实验室制备硫代硫酸钠晶体并探究其化学性质
已知:Na2SO3 + S = Na2S2O3
I.制备Na2S2O3
(1)如图,组装好仪器,检验完气密性(气密性良好),各装置试剂均装入后的下一步操作是______
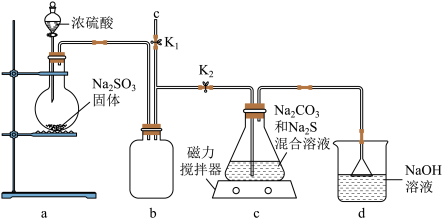
(2)反应开始后,C中发生了多个化学反应。写出其中任意一个非氧化还原反应的方程式_____________
(3)装置c中反应结束后, 先关闭分液漏斗旋塞,在e处连 接盛NaOH溶液的注射器,再关闭K2打开K1,其目的是______ 。待c中溶液冷却后,倒入蒸发皿,通过加热蒸发、冷却结晶和干燥等操作获得Na2S2O3·5H2O晶体。
Ⅱ.探究Na2S2O3的部分化学性质
【提出假设】
假设一:Na2S2O3与Na2SO4结构相似,化学性质也应该相似,因此室温时Na2S2O3溶液pH=7。
假设二:从S元素的化合价推测Na2S2O3具有较强的还原性。
(4)【验证假设】配制适量Na2S2O3溶液,进行如下实验(请填空)
【实验结论】_____________
Ⅲ:用Na2S2O3的溶液测定溶液中ClO2的物质的量浓度,可进行以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知:I2+2S2O =2I-+S4O
=2I-+S4O )
)
(5)根据上述步骤计算出原ClO2溶液的物质的量浓度为_______ mol·L-1(用含字母的代数式表示)
已知:Na2SO3 + S = Na2S2O3
I.制备Na2S2O3
(1)如图,组装好仪器,检验完气密性(气密性良好),各装置试剂均装入后的下一步操作是

(2)反应开始后,C中发生了多个化学反应。写出其中任意一个非氧化还原反应的方程式
(3)装置c中反应结束后, 先关闭分液漏斗旋塞,在e处连 接盛NaOH溶液的注射器,再关闭K2打开K1,其目的是
Ⅱ.探究Na2S2O3的部分化学性质
【提出假设】
假设一:Na2S2O3与Na2SO4结构相似,化学性质也应该相似,因此室温时Na2S2O3溶液pH=7。
假设二:从S元素的化合价推测Na2S2O3具有较强的还原性。
(4)【验证假设】配制适量Na2S2O3溶液,进行如下实验(请填空)
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| 假设一 | 溶液pH=8 | ||
| 假设二 | 向溴水中滴入适量Na2S2O3溶液 | 溴水褪色 |
Ⅲ:用Na2S2O3的溶液测定溶液中ClO2的物质的量浓度,可进行以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知:I2+2S2O
 =2I-+S4O
=2I-+S4O )
)(5)根据上述步骤计算出原ClO2溶液的物质的量浓度为
您最近一年使用:0次
2010·四川成都·一模
7 . 用NA表示阿伏加德罗常数的值。下列叙述错误的是
| A.标准状况下,1.12 LHCHO所含的原子总数是0.2NA |
| B.标准状况下,11.2LC2H2和N2的混合气分子中叁键数目为0.5NA |
C.常温常压下,4.6g Na在O2中燃烧消耗O2的分子数为0.1 NA   |
| D.25℃时, pH=1的CH3COOH溶液中的H+数为0.1 NA |
您最近一年使用:0次



