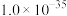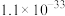1 . As(0)、As(Ⅲ)和As(V)分别表示砷单质、三价砷和五价砷的化合物。硫酸厂产生的酸性废水中含有超标的H3AsO3,需处理达标后才能排放。目前含砷废水的处理常用石灰中和-PFS、氧化吸附、纳米级零价铁等方法。
(1)石灰中和-PFS法,处理过程如下:
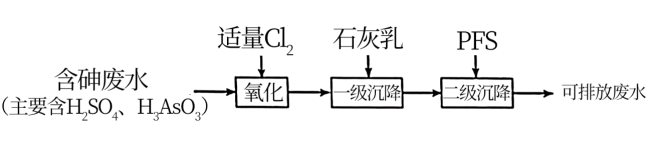
含砷废水经氧化后,加入石灰乳,在相同时间内,废水中沉降的固体、砷的去除率与溶液pH的关系如图1所示。H3AsO3水溶液中含砷微粒的物质的量分布分数与pH的关系如图2所示。已知此温度下,Ca(H2AsO4)2溶于水,Ksp(FeAsO4)=5.7×10-21,Ksp[Ca3(AsO4)2] =6.8×10-19,Ksp(CaHAsO4)=8.4×10-4,。
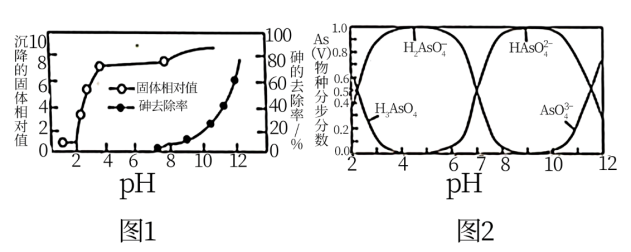
①一级沉降时,当pH=2,废水中开始产生沉淀,该沉淀主要成分的化学式为___________ 。pH调节到8时,开始产生Ca3(AsO4)2沉淀,原因是___________ 。
②二级沉降中,保持溶液pH在8-10之间。加入PFS(聚合硫酸铁,[(Fe2(OH)2n(SO4)3-n]m)形成的Fe(OH)3胶体粒子与含砷微粒反应可提高砷的去除率,其主要反应的离子方程式为___________ 。
(2)氧化吸附法:新生态MnO2悬浊液具有较强的氧化性,能将As(Ⅲ)氧化为As(V),也具有较强的吸附性,能吸附水体中的H+而带正电荷。所带正电荷越多,吸附含砷微粒的能力越强。pH不同时,新生态MnO2悬浊液对砷去除率如图所示。
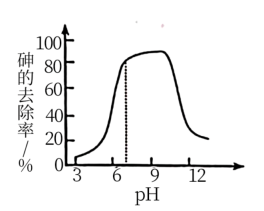
①加入新生态MnO2悬浊液使废水中H3AsO3转化为H3AsO4反应的离子方程式为___________ 。
②pH从3增大到7的过程中,随着pH增大,砷的去除率上升。其原因是___________ 。
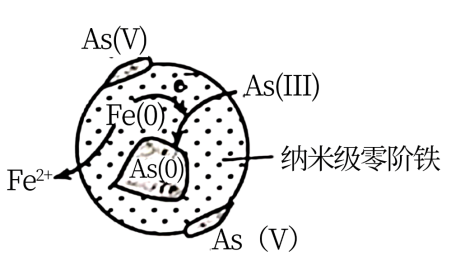
(3)纳米级零价铁法:纳米级零价铁具有强吸附性和还原性,可直接处理有氧条件下含As(Ⅰ)较多的废水。处理后在纳米级零价铁表面有大量的As(0),外围有大量的As(V)。产生As(0)的原理如图所示。请描述产生As(0)、As(V)的过程:___________ 。
(1)石灰中和-PFS法,处理过程如下:

含砷废水经氧化后,加入石灰乳,在相同时间内,废水中沉降的固体、砷的去除率与溶液pH的关系如图1所示。H3AsO3水溶液中含砷微粒的物质的量分布分数与pH的关系如图2所示。已知此温度下,Ca(H2AsO4)2溶于水,Ksp(FeAsO4)=5.7×10-21,Ksp[Ca3(AsO4)2] =6.8×10-19,Ksp(CaHAsO4)=8.4×10-4,。

①一级沉降时,当pH=2,废水中开始产生沉淀,该沉淀主要成分的化学式为
②二级沉降中,保持溶液pH在8-10之间。加入PFS(聚合硫酸铁,[(Fe2(OH)2n(SO4)3-n]m)形成的Fe(OH)3胶体粒子与含砷微粒反应可提高砷的去除率,其主要反应的离子方程式为
(2)氧化吸附法:新生态MnO2悬浊液具有较强的氧化性,能将As(Ⅲ)氧化为As(V),也具有较强的吸附性,能吸附水体中的H+而带正电荷。所带正电荷越多,吸附含砷微粒的能力越强。pH不同时,新生态MnO2悬浊液对砷去除率如图所示。

①加入新生态MnO2悬浊液使废水中H3AsO3转化为H3AsO4反应的离子方程式为
②pH从3增大到7的过程中,随着pH增大,砷的去除率上升。其原因是
(3)纳米级零价铁法:纳米级零价铁具有强吸附性和还原性,可直接处理有氧条件下含As(Ⅰ)较多的废水。处理后在纳米级零价铁表面有大量的As(0),外围有大量的As(V)。产生As(0)的原理如图所示。请描述产生As(0)、As(V)的过程:

您最近一年使用:0次
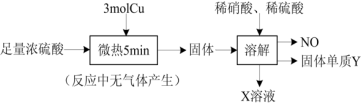
2 . 实验室中利用洁净的铜片和浓硫酸进行如图实验,经检测所得固体中含有 和白色物质X,下列说法正确的是
和白色物质X,下列说法正确的是
 和白色物质X,下列说法正确的是
和白色物质X,下列说法正确的是
A.白色物质X为 ,体现了浓硫酸具有吸水性 ,体现了浓硫酸具有吸水性 |
| B.NO和Y均为还原产物 |
| C.3mol Cu参与反应,转移了6mol电子 |
| D.若稀硫酸足量,在溶解的环节中至少需要0.8mol的稀硝酸 |
您最近一年使用:0次
2022-12-03更新
|
1010次组卷
|
3卷引用: 山东省济宁市兖州区2022-2023学年高三上学期期中考试化学试题
名校
3 . 以炼铁厂锌灰(主要成分为ZnO,含少量的CuO、SiO2、Fe2O3)为原料制备ZnO的流程如图所示。下列说法正确的是
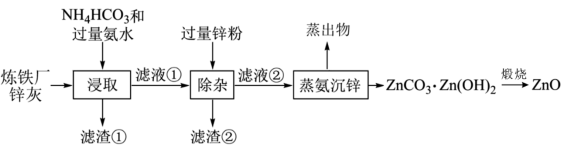
| A.H-N-H键角:[Cu(NH3)4]2+<NH3 |
| B.“滤渣②”的主要成分为Fe、Cu和Zn |
| C.所含金属元素的质量“滤液①”<“滤液②” |
| D.“煅烧”时需要在隔绝空气条件下进行 |
您最近一年使用:0次
2024-03-22更新
|
465次组卷
|
2卷引用:2024届福建省龙岩市高三下学期3月份质量检测一模化学试题
名校
解题方法
4 . 钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪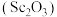 的一种流程如下:
的一种流程如下:
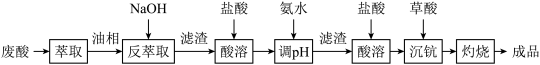
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是_______________________ 。
(2)常温下,先加入氨水调节 ,过滤,滤渣主要成分是
,过滤,滤渣主要成分是__________ ;再向滤液加入氨水调节 ,滤液中
,滤液中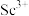 的浓度为
的浓度为__________ 。
{已知: 、
、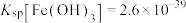 、
、 }
}
(3)用草酸“沉钪”,写出“沉钪”得到草酸钪的离子方程式:___________________________ 。
(4)草酸钪“灼烧”氧化的化学方程式为________________________________________________ 。
(5)废酸中含钪量为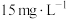 ,VL废酸最多可提取
,VL废酸最多可提取 的质量为
的质量为__________ 。
(6)镧与Sc同族位于第六周期,一种镧、锑形成的配合物结构如图所示:
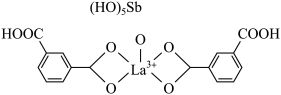
该结构中,中心离子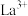 配位数为
配位数为__________ 。
(7)某铁、镧、锑的合金晶胞如图1,铁原子位于锑原子构成的正八面体的体心,晶胞的六个表面结构都如图2:
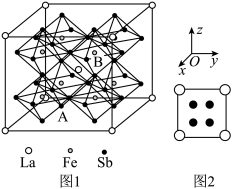
①若图中A点锑原子的坐标为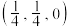 ,则B点铁原子的坐标为
,则B点铁原子的坐标为__________ 。
②若该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Sb原子与Sb原子的最近距离为
,则Sb原子与Sb原子的最近距离为__________ cm。
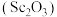 的一种流程如下:
的一种流程如下:
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是
(2)常温下,先加入氨水调节
 ,过滤,滤渣主要成分是
,过滤,滤渣主要成分是 ,滤液中
,滤液中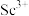 的浓度为
的浓度为{已知:
 、
、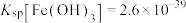 、
、 }
}(3)用草酸“沉钪”,写出“沉钪”得到草酸钪的离子方程式:
(4)草酸钪“灼烧”氧化的化学方程式为
(5)废酸中含钪量为
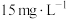 ,VL废酸最多可提取
,VL废酸最多可提取 的质量为
的质量为(6)镧与Sc同族位于第六周期,一种镧、锑形成的配合物结构如图所示:

该结构中,中心离子
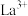 配位数为
配位数为(7)某铁、镧、锑的合金晶胞如图1,铁原子位于锑原子构成的正八面体的体心,晶胞的六个表面结构都如图2:

①若图中A点锑原子的坐标为
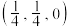 ,则B点铁原子的坐标为
,则B点铁原子的坐标为②若该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Sb原子与Sb原子的最近距离为
,则Sb原子与Sb原子的最近距离为
您最近一年使用:0次
2023-02-06更新
|
585次组卷
|
3卷引用:湖南师范大学附属中学2022-2023学年高三上学期月考卷(六)化学试题
解题方法
5 . 化合物X由三种元素组成,某学习小组按如下流程进行实验:
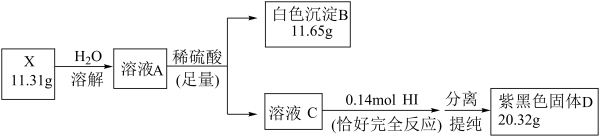
其中,溶液C含有一种摩尔质量为 的含氧弱酸,其物质的量为
的含氧弱酸,其物质的量为 。
。
(1)X的组成元素是_______ ,X的化学式是_______ 。
(2)写出溶液A与足量稀硫酸反应的化学方程式_______ 。
(3)写出生成紫黑色固体D的离子方程式_______ 。
(4)请设计实验检验溶液C中的一种阴离子_______ 。

其中,溶液C含有一种摩尔质量为
 的含氧弱酸,其物质的量为
的含氧弱酸,其物质的量为 。
。(1)X的组成元素是
(2)写出溶液A与足量稀硫酸反应的化学方程式
(3)写出生成紫黑色固体D的离子方程式
(4)请设计实验检验溶液C中的一种阴离子
您最近一年使用:0次
名校
解题方法
6 . 镓是优良的半导体材料。氮化镓是制作发光二极管的新材料,用于雷达、卫星通信设备等。某工厂利用铝土矿(主要成分为 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
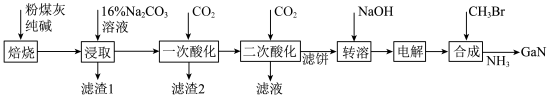
已知:①镓性质与铝相似,金属活动性介于锌和铁之间。
②当溶液中可溶组分浓度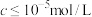 时,可认为已除尽。
时,可认为已除尽。
③金属离子氢氧化物的溶度积(25℃)
④ 、
、 均为两性,
均为两性, 的酸性略强于
的酸性略强于 。
。
回答下列问题:
(1)写出元素镓在周期表中的位置______ ,其简化电子排布式为______ 。
(2)“焙烧”后所得产物主要有______ (写化学式)。
(3)“一次酸化”的目的是______ 。
(4)“二次酸化”中 与足量
与足量 发生反应的离子方程式为
发生反应的离子方程式为______ 。
(5)“电解”可得金属镓(铝不干扰镓盐的电解),写出阴极电极反应式______ 。
(6)“合成”得到的三甲基镓与氨反应得到氮化镓,写出此反应的化学方程式______ 。
(7)25℃时,已知: 可溶于氨水中,
可溶于氨水中,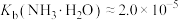 ,反应
,反应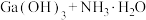
 的平衡常数
的平衡常数 ,计算反应
,计算反应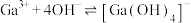 的平衡常数
的平衡常数
______ 。
 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
已知:①镓性质与铝相似,金属活动性介于锌和铁之间。
②当溶液中可溶组分浓度
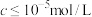 时,可认为已除尽。
时,可认为已除尽。③金属离子氢氧化物的溶度积(25℃)
|
|
| |
|
|
|
|
 、
、 均为两性,
均为两性, 的酸性略强于
的酸性略强于 。
。回答下列问题:
(1)写出元素镓在周期表中的位置
(2)“焙烧”后所得产物主要有
(3)“一次酸化”的目的是
(4)“二次酸化”中
 与足量
与足量 发生反应的离子方程式为
发生反应的离子方程式为(5)“电解”可得金属镓(铝不干扰镓盐的电解),写出阴极电极反应式
(6)“合成”得到的三甲基镓与氨反应得到氮化镓,写出此反应的化学方程式
(7)25℃时,已知:
 可溶于氨水中,
可溶于氨水中,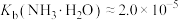 ,反应
,反应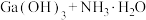
 的平衡常数
的平衡常数 ,计算反应
,计算反应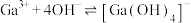 的平衡常数
的平衡常数
您最近一年使用:0次
名校
解题方法
7 . 常温下,向1L 1.0mol/L的NaClO溶液中缓慢通入SO2气体,使其充分吸收,溶液pH与通入SO2物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解)。下列说法错误的是
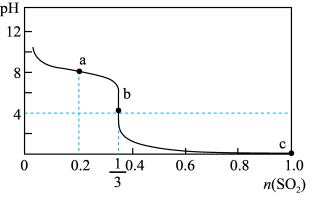

| A.常温下,HClO电离平衡常数的数量级为10﹣8 |
| B.a点溶液中存在 4c(Cl-)=c(HClO)+c(ClO-) |
C.b点溶液中存在c(Na+)>c(SO )>c(Cl-)>c(H+)>c(OH-) )>c(Cl-)>c(H+)>c(OH-) |
| D.c点溶液中c(H+)=2mol/L |
您最近一年使用:0次
2020-11-12更新
|
1729次组卷
|
5卷引用:湖北省武汉市华中师大第一附中高考化学押题试卷
8 . 电镀废水中含有的络合态镍(Ⅱ)和甘氨酸铬(Ⅲ)等重金属污染已成为世界性环境问题。常用的处理方法是臭氧法和纳米零价铁法。
I.臭氧法
(1)在废水中通入 ,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:
,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:
ⅰ.
ⅱ.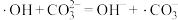
ⅲ.
①写出产生·OH的化学方程式:__________ 。
②加入一定量的 有利于提高氧化效果,原因是
有利于提高氧化效果,原因是____________ 。
Ⅱ.纳米零价铁法
(2)制备纳米零价铁。
将 和
和 溶液在乙醇和水的混合溶液中混合搅拌(
溶液在乙醇和水的混合溶液中混合搅拌( 氛围),充分反应得到纳米零价铁、
氛围),充分反应得到纳米零价铁、 、HCl、NaCl和
、HCl、NaCl和 。写出反应的化学方程式
。写出反应的化学方程式_______________ 。
(3)纳米零价铁处理甘氨酸铬。
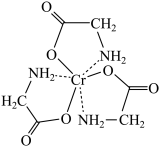
①甘氨酸铬(结构简式如图)分子中与铬配位的原子为_________ 。
②研究表明:纳米零价铁对有机物的降解通常是产生液相·OH对有机物官能团进行断键,使有机络合态Cr(Ⅲ)被释放到溶液中,同时氧化成无机Cr(Ⅵ)。纳米零价铁对甘氨酸铬的去除机理如图所示:
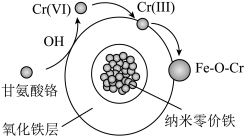
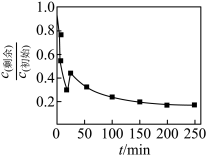
对初始铬浓度为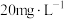 的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是
的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是____________ 。
I.臭氧法
(1)在废水中通入
 ,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:
,在紫外光(UV)照射下产生羟基自由基(·OH),氧化分解络合态Ni(Ⅱ)使镍离子游离到废水中,部分机理如下:ⅰ.

ⅱ.
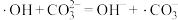
ⅲ.

①写出产生·OH的化学方程式:
②加入一定量的
 有利于提高氧化效果,原因是
有利于提高氧化效果,原因是Ⅱ.纳米零价铁法
(2)制备纳米零价铁。
将
 和
和 溶液在乙醇和水的混合溶液中混合搅拌(
溶液在乙醇和水的混合溶液中混合搅拌( 氛围),充分反应得到纳米零价铁、
氛围),充分反应得到纳米零价铁、 、HCl、NaCl和
、HCl、NaCl和 。写出反应的化学方程式
。写出反应的化学方程式(3)纳米零价铁处理甘氨酸铬。
①甘氨酸铬(结构简式如图)分子中与铬配位的原子为

②研究表明:纳米零价铁对有机物的降解通常是产生液相·OH对有机物官能团进行断键,使有机络合态Cr(Ⅲ)被释放到溶液中,同时氧化成无机Cr(Ⅵ)。纳米零价铁对甘氨酸铬的去除机理如图所示:

对初始铬浓度为
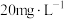 的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是
的甘氨酸铬去除率进行研究,总铬去除率随时间的变化如图所示,其可能的原因是
您最近一年使用:0次
23-24高一上·浙江·期末
9 . 将一定量的铁和铜组成的混合物加入稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加入3mol·L-1NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g。下列叙述不正确的是
| A.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100mL |
| B.当金属全部溶解时收集到NO气体的体积折算成标准状况为2.24L |
| C.参加反应的金属的总质量3.6g<m<9.6g |
| D.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.3mol |
您最近一年使用:0次
解题方法
10 . 化学正在走向精准。当代化学的三大支柱是:理论、实验和计算。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。______
Ⅱ.某硫铜矿的主要成分为 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):
步骤1:在1.00g试样中加入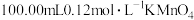 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。
步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用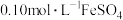 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数______ 。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为
 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。Ⅱ.某硫铜矿的主要成分为
 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):步骤1:在1.00g试样中加入
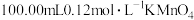 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用
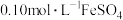 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数
您最近一年使用:0次